微波消解-电感耦合等离子体质谱法检测虾中铅含量
2016-05-24李倩云周国燕曹蕾
李倩云,周国燕,曹蕾
(上海理工大学 医疗器械与食品学院,上海,200092)
微波消解-电感耦合等离子体质谱法检测虾中铅含量
李倩云,周国燕*,曹蕾
(上海理工大学 医疗器械与食品学院,上海,200092)
摘要建立微波消解-电感耦合等离子体质谱法(inductively coupled plasma mass spectrometry,ICP-MS)测定虾中铅的方法。在单因素试验基础上,通过正交试验分析研究H2O2量、HNO3量、微波消解时间对虾中铅提取量的影响,优选虾中铅的提取条件。结果表明:在H2O2量为1.0 mL、HNO3量为5 mL、微波消解时间为13 min条件下,虾中铅含量可达到0.497 mg/kg。检测国家标准物质GBW10050(大虾)进行方法验证,结果与标准值一致。方法检出限为0.01 μg /kg,平行测定RSD(n=6)小于5%。该方法能够简单、快速、灵敏和准确地测定虾中的重金属铅元素。
关键词微波消解;电感耦合等离子体质谱法(ICP-MS);虾;铅
水生动物对重金属等微量元素具有较强的富集作用,虾贝类对重金属的富集能力明显高于鱼类,人类食用虾后, 虾体内如果富集重金属元素就会转移并蓄积于人体的不同组织器官中, 引起慢性损伤[1-2]。目前我国很多地区鱼类、贝类重金属铅、砷等含量都超标[3-4]。铅能损害动物及人体的血液系统、神经系统和肾脏等, 其中以对骨髓造血系统和神经系统的损害最为严重[5]。因此,研究快速、准确测定虾中铅含量的方法具有重要的意义。
电感耦合等离子体质谱法(inductively coupled plasma mass spectrometry,ICP-MS)具有检测限低、动态范围宽、干扰少、分析精度高、分析速度快、可进行多种元素同时测定等优势[6]。样品的前处理方法是虾中重金属含量准确测量的一个重要环节,它直接影响测定结果的准确性、平行性[7]。近年来,微波消解因其消解时间短、样品污染小、操作简便等特点,与电感耦合等离子体质谱仪配套,广泛应用于食品及包装材料中重金属等元素的检测[8-11]。消解体系有HNO3-HCl体系[12]、HNO3-HF体系[13]、HNO3-H2O2体系等,其中国内外最常用是HNO3-H2O2体系[14-15],本文即采用HNO3-H2O2体系进行消解。由于原料不同, 研究中前处理条件也不尽相同。本文采用正交试验设计对微波消解-电感耦合等离子体质谱法测定虾中铅含量的条件进行优化,确定微波消解-电感耦合等离子体质谱法测定虾中铅含量的最佳工艺参数。
1材料与方法
1.1材料与试剂
南美白对虾,上海东方国际水产中心;大虾标准物质GBW10050,国家标准物质中心;Pb标准储备液( 1 000 mg /L),国家标准物质中心; HNO3(优级纯)、H2O2(优级纯),国药集团化学试剂有限公司。
1.2仪器与设备
X series″型四级杆电感耦合等离子体质谱仪(配备同心雾化器和旋流雾室),美国Thermo Fisher公司;MARS-6 型微波加速反应系统,美国CEM 公司;超纯水( 18. 2 MΩ·cm,由Molecula 纯水仪制备),摩勒科学仪器有限公司。
1.3实验方法
1.3.1ICP-MS工作条件
测试方法为CCT(碰撞反应池)模式,射频功率为1 200 W,采样深度150 mm,样品气流0.86 L/min,辅助气流速0.8 L/min,冷却气流速13 L/min。
1.3.2流程
将样品虾去头、去壳,剔除虾线,取可食部分匀浆,用分析天平准确称取0.25 g放于消解罐中,加入5 mL HNO3,0.5 mL H2O2,加热进行预消解,然后采用一步升温法用微波消解仪进行消解,升温时间为20 min,保持15 min,最大功率1 000 W;消解完毕后冷却至室温,用超纯水定容至25 mL容量瓶,同时做样品空白溶液。所有容器使用前均以体积分数30% HNO3浸泡12 h后以超纯水反复冲洗。
1.3.3标准曲线的绘制
用体积分数5%的HNO3制备质量浓度分别为0,1.0,5.0,10.0,20.0 μg/L的铅标准溶液系列进行测定,结果在0~20 μg/L内工作曲线呈良好线性,回归方程为y=9 954.81x+796.81,R2=0.999 9。
1.3.4单因素试验设计
通过对HNO3、H2SO4、HCl的比较发现,HNO3提取效果最好[16],HCl和H2SO4容易引入氯离子和硫离子。虾中有机质含量较高,消解时会产生大量气体,为防止消解罐出现压力过大,根据仪器工程师建议选择试验条件为:H2O2体积0.5 mL、HNO3体积5 mL、微波消解温度180 ℃、微波消解时间15 min,在以上条件不变的情况下,进行单因素试验,参考各因素对虾中铅提取量的影响。
1.3.5正交试验设计
在单因素试验的基础上,选用L9(34)进行正交试验设计,每个试验重复3次。
1.4数据统计分析
数据统计方法,利用SPSS 17.0版软件进行单因素试验方差分析和正交试验方差分析。
2结果与分析
2.1单因素试验结果
2.1.1H2O2体积对虾中铅提取量的影响
由图1可知,H2O2体积对虾中铅的提取量有极显著影响(P<0.05),H2O2体积在0.5~1 mL内,虾中铅的提取量随着H2O2体积的增大而升高。

图1 过氧化氢体积对虾中铅提取量的影响Fig.1 Effects of H2O2 volume on concentration of Pb in shrimp
由图2可知,HNO3体积对虾中铅的提取量有极显著影响(P<0.05),HNO3量在4~6 mL内,虾中铅的提取量随着HNO3量的增大而升高,因为HNO3是一种强氧化剂,且所有金属的硝酸盐均为易溶盐,有利于有机物的消解;当HNO3量大于6 mL时,铅的提取量降低,这是由于消解完毕后酸剩余过多,从而影响或干扰铅含量的测定,因此选择HNO3量为6 mL左右最为合适。
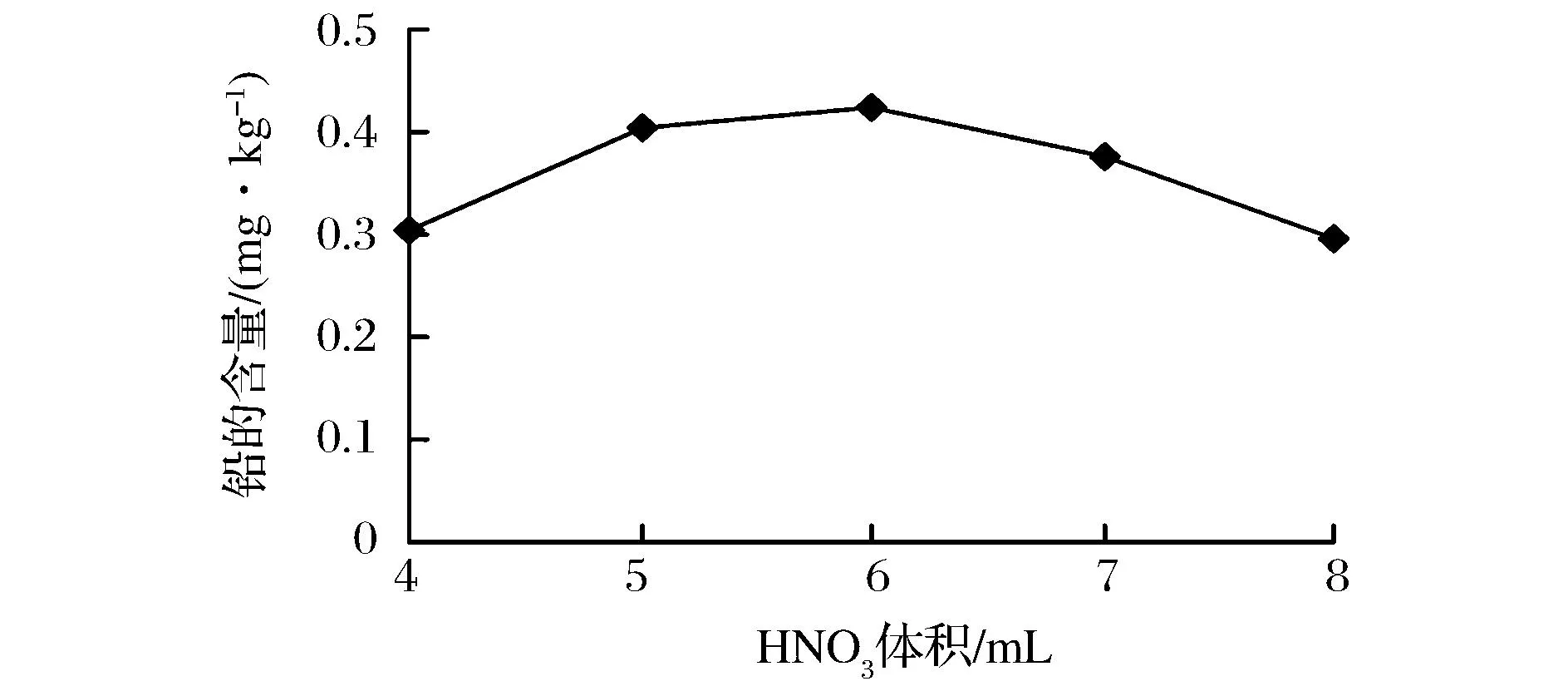
图2 硝酸体积对虾中铅提取量的影响Fig.2 Effects of HNO3 volume on concentration of Pb in shrimp
2.1.3微波消解温度对虾中铅提取量的影响
由图3可知,微波消解温度对虾中铅的提取量无显著影响(P>0.05),微波消解温度在160~180 ℃范围内,铅提取量随着微波消解温度的增加而升高,由于生物样品中不含难消解的物质,在180 ℃时已基本消化完全;微波消解温度大于180 ℃时,提取量下降,当微波消解温度过高时,可能会产生泻压导致内罐损坏,使内罐杯口变形。因此选择微波消解温度为180 ℃左右最合适。
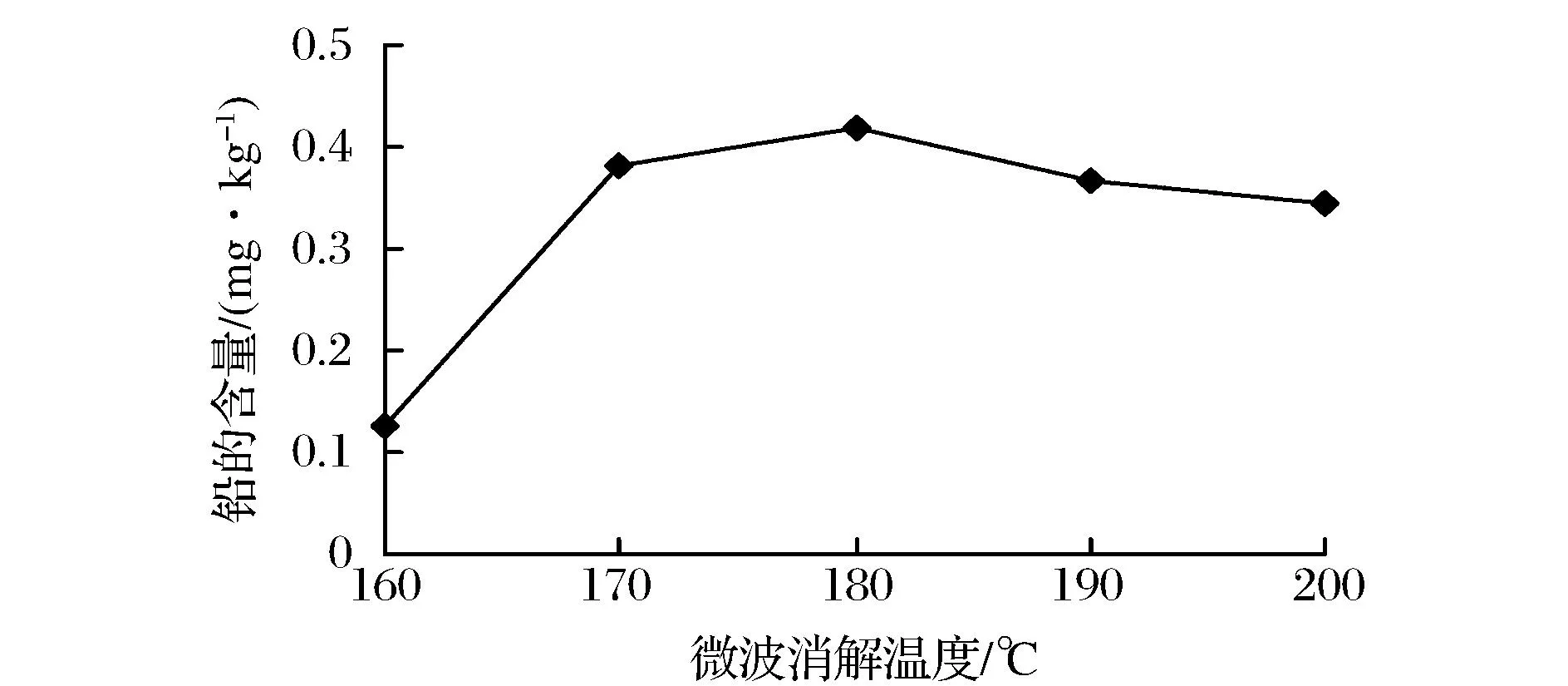
图3 微波消解温度对虾中铅提取量的影响Fig.3 Effects of microwave digestion temperature on concentration of Pb in shrimp
2.1.4微波消解时间对虾中铅提取量的影响
由图4可知,微波消解时间对虾中铅的提取量有极显著影响(P<0.05),微波消解时间在11~15 min内,随着微波消解时间增大,样品消化越来越完全,铅提取量越来越大,当微波消解时间达到15 min时铅含量最大;微波消解时间大于15 min时,铅提取量基本稳定不变,时间过长会导致内压过大,超出消解罐的承受能力,造成消解罐破裂,溶液溅失。因此选择微波消解时间为15 min左右最为合适。
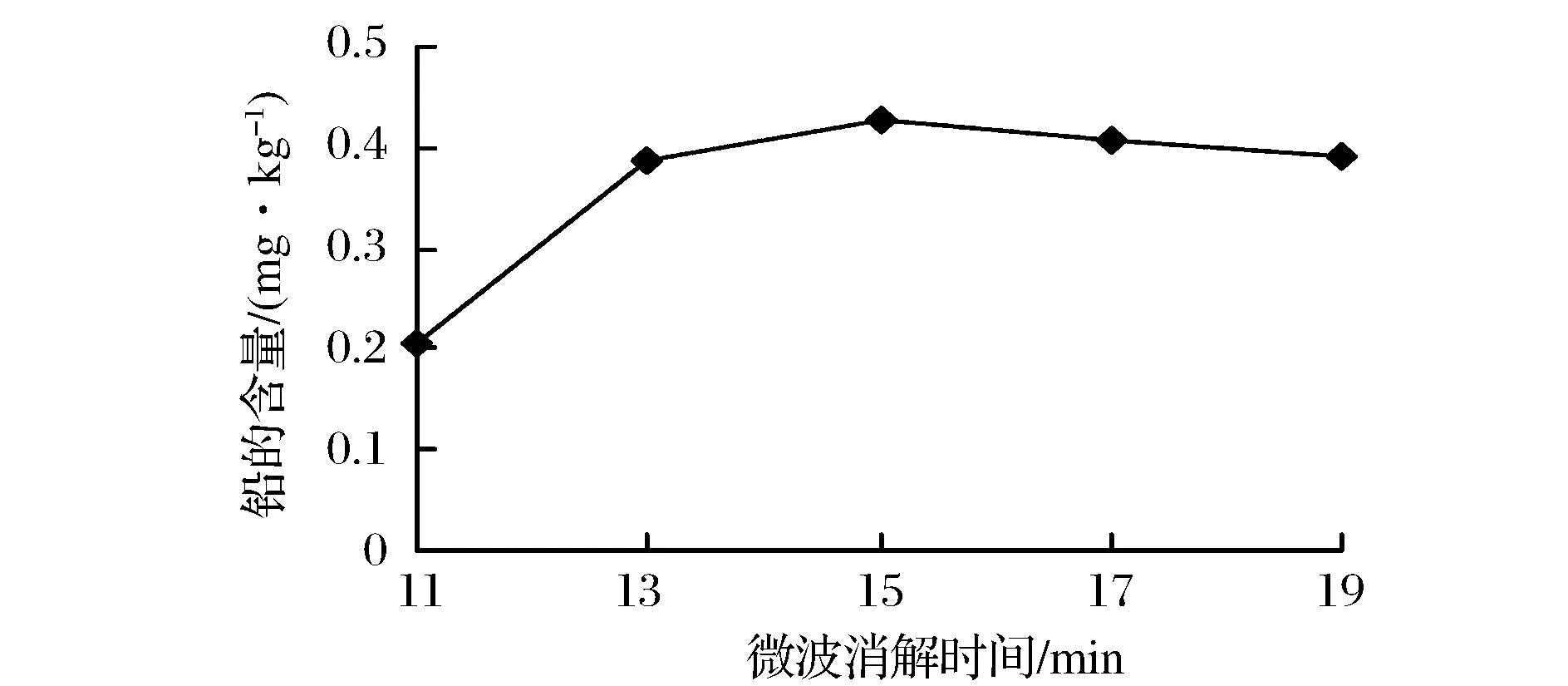
图4 微波消解时间对虾中铅提取量的影响Fig.4 Effects of microwave digestion time on concentration of Pb in shrimp
2.2微波消解条件的优化试验
2.2.1正交试验
根据单因素试验结果,选择对铅提取量有显著性影响的H2O2体积、HNO3体积、微波消解时间3个因素,采用L9(34)正交设计,因素水平见表1。
与对照组比较,BV模型组小鼠子宫组织中MMP-9蛋白表达量显著增加(P<0.01),不同剂量黄柏碱与加替沙星可减少小鼠子宫组织中MMP-9表达。黄柏碱(20、40 mg/kg)与加替沙星均可有效降低小鼠子宫组织中MMP-9表达量,与模型组比较差异显著(P<0.05、0.01)。结果见图2。

表1 正交试验因素水平表
2.2.2正交试验结果及分析
正交试验结果见表2,方差分析见表3。
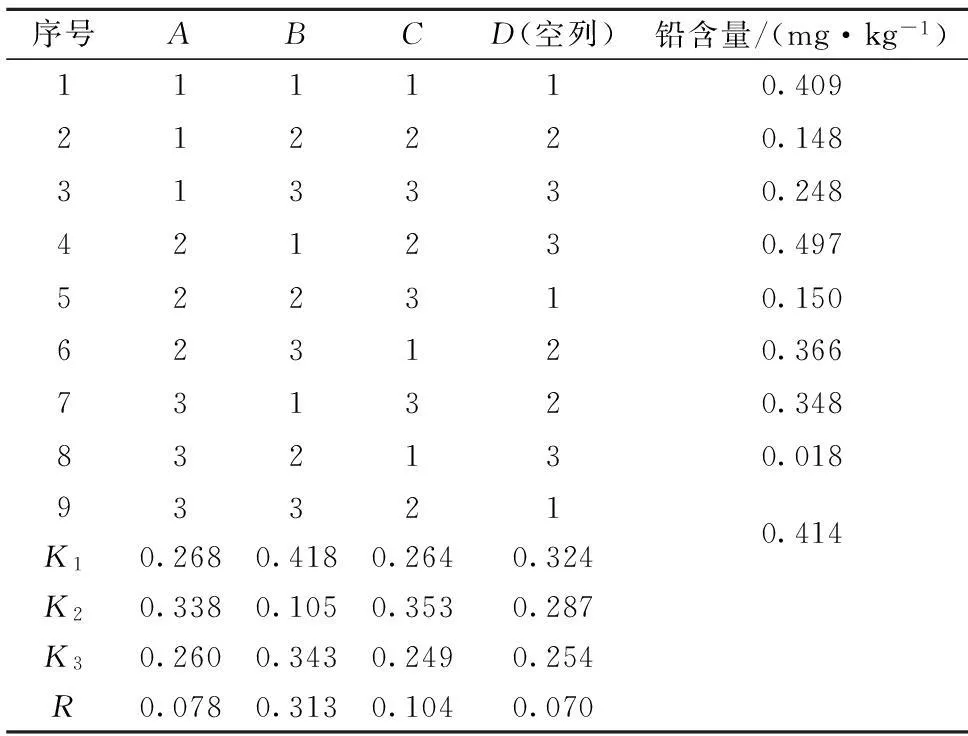
表2 正交试验结果及方差分析
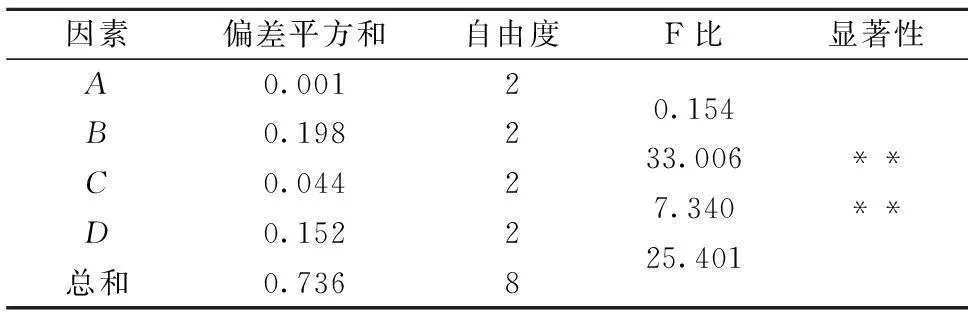
表3 正交试验方差分析
由表2可知,3 个因素对铅提取量的影响顺序为B>C>A,即HNO3体积>微波消解时间>H2O2体积,其中HNO3体积对铅提取量的影响最强。由表3可知,在0.05显著性水平上HNO3体积、微波消解时间对铅提取量的差异显著,H2O2体积对铅提取量的影响不显著。极差分析所得的最佳测定条件为A2B1C2,与试验最佳测定条件吻合,即H2O2体积1 mL、HNO3体积4 mL、微波消解时间13 min,铅含量为0.497 mg/kg,比单因素初始条件下铅含量0.413 mg/kg提高了20.3%。
2.2.3验证实验
按照最佳测定条件A2B1C2进行验证实验,取3个样本,平行测定3次虾样品中铅的含量,取平均值0.497 mg/kg,与正交表中的最大值一致。
2.3方法性能评价
2.3.1精密度、检出限
针对同种虾样品平行测定6 次,获得测定结果精密度RSD 为2.72%。在优化的实验条件下,取样品的试剂空白溶液,进行11 次平行测定,采用国际通用的IUPAC计算检出限,获得检出限为0.01 μg/kg,低于文献中[18]的0.06 μg/kg。
2.3.2加标回收率
取虾样品作为本底,平均测量值为0.497 mg/kg,铅元素加标量为0.25,0.5,1.0 mg/kg,测定加标回收率,回收率在98.2%~101.7%之间(表4)。
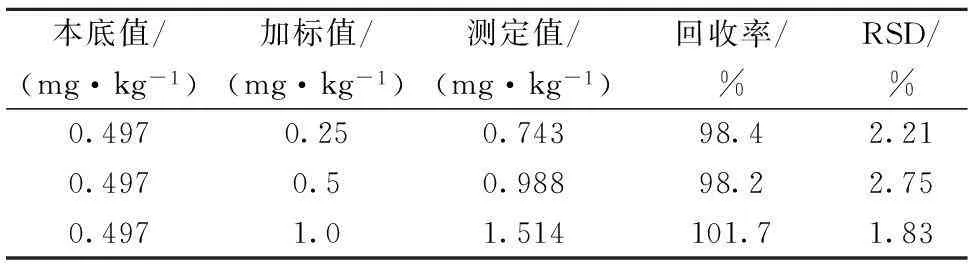
表4 虾中铅元素加标回收率(n=6)
2.3.3标准物质验证
大虾标准物质中铅元素的标准值为(0.2±0.05) mg/kg,平行测定3次,平均测量值为(0.23±0.02) mg/kg,在标准值范围之内。
3结论
为建立微波消解-电感耦合等离子体质谱法测定虾中铅的方法,在单因素试验基础上,通过正交试验进一步优化H2O2量、HNO3量、微波消解时间对虾中铅提取量的影响。结果表明,在H2O2量为1.0 mL、HNO3量为5.0 mL、微波消解时间为13 min条件下,所获得的虾中铅的提取量最高,达到0.497 mg/kg。经优化条件后,方法检出限在0.01 μg/kg,测定大虾标准参考物质的结果与标准值一致。优化后的微波消解法具有操作简便快速、污染损失少、灵敏度高、准确度好等优点。
参考文献
[1]AGAH H,LEERMAKERS M,ELSKENS M,et al . Accumulation of trace metals in the muscle and liver tissues of five fish species from the Persian Gulf[J].Environmental Monitoring and Assessment,2009,157(1-4):499-514.
[2]TURKMEN M, TURKMEN A,TEPE Y, et al. Determination of metals in fish species from Aegean and Mediterranean seas[J].Food Chemistry,2009,113(1):233-237.
[3]陈红红,毋福海,黄丽玫,等.广州市场食用鱼中5种重金属含量分析及评价[J].中国卫生检验杂志,2008,18(12):2 736-2 738.
[4]母清林,王晓华,佘运勇,等.浙江近岸海域贝类中重金属和贝毒污染状况研究[J].海洋科学,2013,37(1):87-91.
[5]胡晓锋.虾中重金属提取量的分析检测[J]. 咸宁学院学报,2011,31(6):74-75.
[6]黄亮亮,吴志强,李艳红,等.鱼体重金属检测方法的研究进展[J].安徽农业科学,2013,41(14):6 305-6 307,6 311.
[7]古小治,章钢娅,戴荣玲,等.密闭消解ICP-AES测定土壤及沉积物中主量和微量元素[J].分析试验室,2008,27(8):17-20.
[8]张江义,王小菊,李国敏. 微波消解-电感耦合等离子体质谱法同时测定食品中的主、微量元素[J]. 分析化学,2014,42(11):1 706-1 709.
[9]SUDEEPTA B, KRISHNA P, JAHIR H, et al. Heavy metals concentration in edible fishes from coastal region of Kalpakkam, southeastern part of India[J].Environmental Monitoring and Assessment,2012,184(8):5 097-5 104.
[10]JASMINA D, THORJORN L, ARMIN S, etal. Contents of cadmium, copper, mercury and lead in fish from the Neretva river (Bosnia and Herzegovina) determined by inductively coupled plasma mass spectrometry (ICP-MS)[J].Food Chemistry,2011,131(2):469-476.
[11]周谙非,杨彦丽. 微波消解ICP-MS同时测定色母粒中多种重金属元素[J]. 食品与发酵工业,2012,38(1):169-171.
[12]张静芬,邹小兵,季金苟,等.两种不同方法提取鲜橙皮中挥发油的比较研究[J]. 食品研究与开发,2012,33(5): 45-47.
[13]孙瑾,陈春英,李玉锋,等.超声波辅助溶剂萃取-电感耦合等离子体质谱法测定生物样品中的总汞和甲基汞[J]. 光谱学与光谱分析,2007,27(1): 173-176.
[14]MORGANA F, DAIANE P C Q, IVAN N B C, et al. A novel extraction-based procedure for the determination of trace elements in estuarine sediment samples by ICP-MS[J]. Microchemical Journal,2014,117(21):1-6.
[15]FERHAT M A,MEKLATI B Y,SMADJA J,et al. An improved microwave Clevenger apparatus for distillation of essential oils from orange peel[J]. Journal of Chromatography A,2006,1112(1): 121-126.
[16]汪慧,江涛,唐勇,等.稀酸浸提水产品中重金属铜、铅和镉[J].食品科学,2014,35(12):88-92.
[17]梁淑轩,王欣,吴虹,等.微波消解/ICP-MS测定水系沉积物中的9种重金属元素[J].光谱学与光谱分析,2012,32(3):809-812.
[18]郭雨时,焦阳,娄丽.ICP-MS同时测定水产品中的铅、镉、汞和砷[J].光谱试验室,2012,29(6):3 717-3 720.
Determination of lead in shrimps by microwave digestion and inductively coupled plasma mass spectrometry
LI Qian-yun, ZHOU Guo-yan*, CAO Lei
(University of Shanghai for Science and Technology College of Medical Equipment and Food, Shanghai 200092,China)
ABSTRACTA method was established for the analysis of Pb in shrimps by using microwave digestion and inductively coupled plasma mass spectrometry (ICP-MS). Based on the single-factor test analysis,the orthogonal array design methods were applied to analyze the influence of three factors (H2O2 volume, HNO3 volume and microwave digestion time) and their effect on the extraction of Pb. The experimental results showed that the contents of Pb reached at 0.497 mg/kg when H2O2 volume was 1.0 mL, HNO3 volume is 5.0 mL and microwave digestion time was 13 minutes and 46 seconds. Contents of Pb that was determined in GBW10050 (big shrimps) had the same results with standards values. Method limit of detection was 0.01 μg /kg,the RSD was less than 5%. These results showed that this is a simple, rapid, sensitive and accurate method for the determination of Pb in shrimps.
Key wordsmicrowave digestion; inductively coupled plasma mass spectrometry (ICP-MS); Pb; shrimps
收稿日期:2015-06-11,改回日期:2015-10-21
DOI:10.13995/j.cnki.11-1802/ts.201604035
第一作者:硕士研究生(周国燕副教授为通讯作者)。
