氮硫共掺杂SrSnO3的制备及光催化降解染料研究*
2016-05-17黄秋锋肖含兵张晓凤
黄秋锋,肖含兵,张晓凤,林 深
(福建师范大学 化学与化工学院, 福州 350007)
氮硫共掺杂SrSnO3的制备及光催化降解染料研究*
黄秋锋,肖含兵,张晓凤,林深
(福建师范大学 化学与化工学院, 福州 350007)
摘要:以氨气作为氮源,硫脲作为硫源,制备N/S共掺杂SrSnO3样品。通过X射线粉末衍射仪(XRD)和X射线光电子能谱(XPS)表征确定了N、S分别是以晶格取代和间隙掺杂的形式存在于样品中。紫外漫反射光谱(DRS)表明氮硫共掺杂的样品对可见光的吸收比单掺杂要强。以罗丹明B、亚甲基蓝、橙黄Ⅱ号作为模拟废水污染物并考察了样品在可见光下降解染料的活性。实验结果表明,在氮化时间为12 h,硫掺杂比为1∶1得到的N/S共掺杂SrSnO3的催化剂在可见光照射的条件下,一定浓度的罗丹明B溶液在6 h内被彻底降解至无色溶液,亚甲基蓝溶液的在3 h内,脱色率达到96%以上,偶氮类染料橙黄Ⅱ号在加入少量H2O2,3.5 h内降解率为93%。
关键词:SrSnO3;共掺杂;光催化;降解染料
0引言
印染废水是目前工业生产中危害较为严重的污染之一。随着我国纺织工业的发展,印染废水排放量逐年增加,占工业废水总排放量的10%以上[1]。印染废水具有成分复杂、水体颜色深、水质变化多样等特点,已成为危害最大的重要污染源,如何有效地对印染废水进行综合治理是一个急需解决的难题。近年来,多相光催化作为一项崭新的污染治理技术,因其光催化效率高,节约能源,可催化多种污染物,且具有无毒、反应条件温和、操作简便、可减少二次污染等特点而日益受到人们的关注。1972年,Fujishima和Honda研究了n型半导体TiO2电极上光电催化分解水的作用,以此为契机揭开了光催化研究的新纪元[2],但TiO2宽禁带宽度(Eg=3.2 eV),只对紫外光有响应,而紫外部分只占太阳光的5%左右,限制了其的应用。因此,近年来科学工作者为提高光催化剂在可见光下的催化活性进行大量的改性研究。
Zhu等[3]以蓝色发光的二极管作为光源,考察不同条件下F、N共掺杂的TiO2降解甲醛的实验,发现N,F共掺杂样品具有很好的降解活性。Daimei等[4]采用得到了C、N共掺杂TiO2光催化剂,认为C、N共掺杂样品比单独的N或者C掺杂具有更高的光催化活性,且合成过程中生成溶胶的温度对催化活性有很大的影响。Li等[5]采用sol-gel法结合蒸发自组装法(EISA)制备了N、S共掺杂的介孔型TiO2,研究结果表明,该共掺杂样品大大提高了催化剂在可见光下的性能,对甲基橙和罗丹明B都有很好的降解效果。Dong等[6]对C、N、S共掺杂TiO2的样品研究发现,共掺杂有效的提高了可见光下降解罗丹明B的催化能力,且三掺杂具有比单独掺杂具有更好的稳定性和更强的可见光吸收能力。由上述可知在通常情况下合适的多组分掺杂比单组分掺杂具有更好的光催化活性。
钙钛矿型的SrSnO3,具有导电率高,高温热稳定性好,目前已被广泛应用于光致发光材料[7],陶瓷材料[8]等作为光催化剂还具有一定的紫外光催化性能,在紫外光照射下具有光降解水的催化活性。但由于SrSnO3禁带宽度过宽(约为4.0 eV左右),限制了该化合物的可见光催化活性,目前对锡酸锶的光催化研究还仅局限于紫外光区域,尚未见到其可见光催化活性相关报道。
故本文拟通过氮硫共掺杂SrSnO3的方法,对价带进行调节和控制,从而缩小禁带宽度,提高可见光催化活性。通过相关的表征分析,探索非金属的掺杂机理、掺杂对能带结构的影响、光催化活性影响因素等,拟采用多种染料为目标降解物考察光催化剂的降解能力,为开发新型非TiO2基系列可见响应光催化剂提供更丰富的研究实例。
1实验
1.1试剂与仪器
1.1.1试剂
锡酸钠、硝酸锶、氢氧化钠、硫脲(SC(NH2)2)、盐酸、双氧水、罗丹明B、氨水、无水乙醇、硝酸镍、硝酸铁、硝酸镉均为分析纯,上海国药集团公司售,氩气为普通纯,福州城门电气厂售,采用一次蒸馏的普通蒸馏水为溶剂。
1.1.2仪器
样品的物相及晶型的确定用荷兰Philip X’pertpro粉末衍射仪(CuKα,λ=0.154178 nm)表征;样品的光吸收能力及能带结构采用美国PE Lampda 850型UV-Vis光谱仪表征;采用中国TU1810型紫外-可见分光光度计测试RhB溶液吸收光谱;样品表面的组分及化合物的价态形式由VG-Multilab2000 型X射线光电子能谱仪测试,以MgKα X射线为激发源,电子结合能用污染碳的C1s峰(284.6eV)校正; 染料溶液吸光度以22-PC型分光光度计(上海棱光科技有限公司)测得。
1.2氮硫共掺杂锡酸锶的制备
锡酸锶前驱体参照文献[7]合成:按物质的量比为1∶1称取锡酸钠、硝酸锶,各自溶解于15 mL的蒸馏水后,在磁力搅拌下将二者混合;将得到的白色沉淀物转移至水热反应釜中,在180 ℃下恒温18 h,反应完后自然冷却至室温,经过滤后用蒸馏水和无水乙醇各洗涤3遍,在70 ℃真空干燥后得到前驱体。
称取一定量锡酸锶前驱体于小瓷舟中(确保放置均匀),将小瓷舟放置于管式炉中,再将以氩气通入氨水得到的混合气体通入,在不同的温度下保持一段时间(通过控制时间来达到控制掺杂量),待自然冷却后取样,用蒸馏水和无水乙醇各洗涤3遍后干燥。
称取一定量的氮掺杂产物与硫脲按物质量比1∶1混合均匀后压片,在氩气保护下,300 ℃焙烧3 h使硫脲完全分解,自然降温后取出样品研成粉末,水洗至中性后干燥。
1.3光催化活性评价
光催化反应在间歇式的可见光反应器中进行,如图1所示。
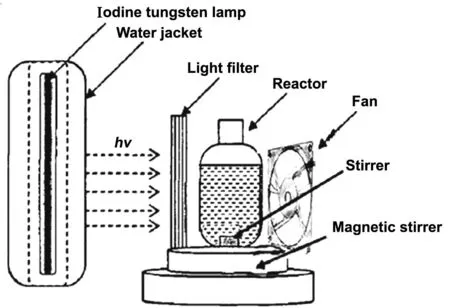
图1 光催化反应装置示意图
Fig 1 Schematic diagram of the photocatalytic reaction device
以500 W的卤钨灯(光强度约为50 mW/cm2)作为光源,经过隔热玻璃和光学滤片组合滤光后得到光波长为400~800 nm的可见光,同时在评价光催化活性过程中通入循环冷却水防止温度过高影响实验。反应溶液放置于普通的玻璃瓶中并在磁力搅拌下进行确保催化剂高度分散。取目标降解物50 mL,加入一定量催化剂,在避光条件下经吸附-脱附平衡后(约1 h),光照,每隔一段时间取样,高速离心分离(12 000 r/min),取上层清液用分光光度计在各染料最大吸收波长处测定吸光度,根据溶液的吸光度的变化计算残留率C/C0以评价催化剂的催化活性。
2结果与讨论
2.1XRD分析
图2为不同温度下NH3/Ar中热处理SrSnO3的XRD图。从图2可见,在400~600 ℃温度下焙烧SrSnO3,出现的3个最强衍射峰(分别为(200)、(312)、(220))与JCPDS标准卡片号为77-1798的钙钛矿型SrSnO3各衍射峰对比,两者基本一致且没有其它新相的生成。另外,随着温度升高,(200)晶面处的峰变尖锐,说明晶型进一步完善。而当温度上升到700 ℃时,出现了少量的锡单质衍射峰,这说明此时SrSnO3的晶型已经发生变化。通常而言,晶型的破坏会对催化剂的光催化活性产生不利的影响,实验中也恰恰验证了这一点。造成锡单质出现的原因,是因焙烧温度过高,SrSnO3中的锡被NH3分解出的氢气还原为金属锡单质。因此从分析结果可以得出氮掺杂的最佳温度为600 ℃,这不仅可以保持比较好的晶型,而且更有利于NH3的分解(适当地升高温度,NH3的分解速度越快越充分)。
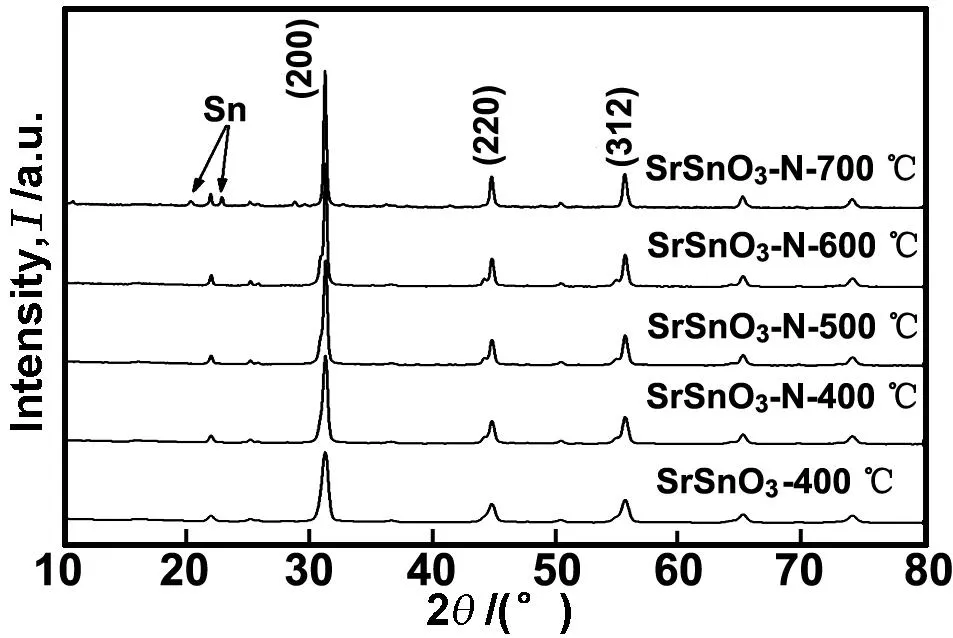
图2NH3/氩气气氛下不同温度焙烧后SrSnO3的XRD图(处理时间 12 h)
Fig 2 XRD patterns of nitrided samples with different temperature under NH3/Ar atmosphere (nitridation duration:12 h)
图3为在600 ℃下通入NH3/氩气混合气体经恒温不同时间后再进行硫掺杂得到的氮硫共掺杂的SrSnO3样品XRD图。从图3可以看出,氮硫共掺杂后样品各衍射峰与纯的SrSnO3(600 ℃焙烧)有着良好的匹配,对应值钙钛矿型的SrSnO3。通过对(200)晶面(图4)仔细观察对比发现硫氮共掺杂后衍射峰向小角度发生偏移,变化量比硫单掺杂大,晶格常数a从0.5234 nm增大到0.5378 nm。这是因为氮和硫的原子半径都比氧的原子半径大,当发生硫的间隙掺杂和氮晶格取代时会使得样品的晶格间距增大,根据布拉格定律
可以得知衍射角会向小角度移动。因此推断氮、硫进入了SrSnO3的体相当中。

图3不同氮化时间得到的氮硫共掺杂样XRD谱图(氮化时间分别为10,12和14 h)
Fig 3 XRD patterns of N,S-codoped samples with different time under NH3/Ar atmosphere (nitridation duration:10,12,14 h)

图4不同氮化时间得到的氮硫共掺杂样品(200)晶面处衍射峰的变化(2θ=26~36°)
Fig 4 Diffraction peak positions of the (200) plane in the range of N,S co-doped samples
2.2XPS分析
为了确定化合物中氮、硫价态及存在的形式,对其进行了XPS表征如图5所示。从图5可以看出,样品里面含有Sr、Sn、O、N、S、C元素的特征峰,说明样品已有硫元素和氮元素进入。碳元素的特征峰可以认为是测试仪器产生的污染峰[8]。

图5氮硫共掺杂样品的XPS谱图(氮化时间12 h,温度600 ℃)
Fig 5 XPS spectra of N,S co-doped SrSnO3sample (nitridation duration 12 h and calcined in the temperature of 600 ℃)
通过观察氮元素的窄区XPS图(图6(a)),发现氮的谱峰只有一个对称的特征峰位于电子结合能为397.65 eV处,同时没有杂峰或肩峰和其它的吸附氮峰存在。这是由于NH3在600 ℃下分解,形成的吸附氮经过高温焙烧已被除去。根据研究认为,电子结合能为397.65 eV可以归属于晶格取代氮[9]。说明采用NH3/氩气作为氮源能够对钙钛矿型的SrSnO3进行有效的氮掺杂,这一结果与其它学者在采用类似的方法进行氮掺杂得到N-TiO2光催化剂的实验结果相符[10]。
通过对硫元素的窄区XPS图(图6(b))观察,可以看出硫的特征峰位于电子结合161.9 eV处,略大于负二价的硫阴离子(S2-)的S2p特征峰161.8 eV[8,11]。这是因为在制备的过程中有惰性气体(氩气)的保护,可以有效防止硫阴离子与空气中的氧气接触而被氧化为正价的硫阳离子(S4+、S6+);又由于硫原子半径远比氧原子大得多,故认为不可能得到硫原子直接取代氧原子的化合物[8,10,13],该特征可以归属于间隙掺杂的硫阴离子(S2-)。结合前面XRD的分析,可认为硫是以间隙掺杂的形式存在,氮则是进入到晶格取代晶格中的氧位形成晶格取代氮。

图6 氮硫共掺杂SrSnO3的N1s和S2p XPS谱图
Fig 6 High-resolution XPS spectra of N1s and S2p of N,S co-doped sample
2.3DRS分析
图7为SrSnO3在600 ℃下氮化不同时间,然后与硫脲按物质量比为1∶1混合后焙烧300 ℃所得氮硫共掺杂SrSnO3的DRS图。如图7所示,未经过掺杂的SrSnO3的光吸收区域位于350 nm之前的紫外光区,在可见光区并没有光吸收。而随着氮化时间的增加,样品的吸收边逐渐向可见光区域红移,当氮化时间为10 h,吸收边红移到400 nm左右,经光催化活性测试发现其光催化活性并不高,这是因为氮化时间不足时,不利于氮进入到样品当中,而未能有效地改变样品的能带结构,对可见光吸收不足而导致可见光催化活性低。当氮化时间为12 h后得到的氮硫共掺杂SrSnO3样品的光吸收边扩展到了约480 nm处,根据公式[8]
该样品的带隙由原来3.54 eV减小到了2.61 eV,相比硫单掺杂的样品带隙更窄,此时具有最好的光催化活性。这是因为S2p,N2p轨道与O2p轨道混合杂化成新的轨道,使样品价带上方宽化而向上移动,使得带隙宽度减小,所以可见光吸收能力增强,可见光催化活性增强。当通入NH3/氩气时间继续增加到14 h后,光吸收边进一步扩展到550 nm左右,这是因为随着掺杂比的增加可见光吸收能力也随之增强。

图7不同氮化时间得到的氮硫共掺杂样DRS谱图(氮化时间分别为10,12,14 h)
Fig 7 DRS patterns of N,S co-doped samples with different time under NH3/Ar atmosphere (nitridation duration:10,12,14 h)
2.4光催化活性评价
2.4.1光催化降解罗丹明B
以1.0×10-5RhB为模拟污染物(催化剂浓度为1 g/L),在可见光下照射一段时间的光催化活性如图8所示。

图8氮硫共掺杂SrSnO3的光催化降解罗丹明B活性图
Fig 8 Photocatalytic degradation of RhB in the presence of undoped and N,S co-doped SrSnO3
纯SrSnO3的样品在可见光下基本没有光催化活性, 而硫氮掺杂的样品在可见光下降解罗丹明B都具有一定的催化活性。当氮化12 h后再进行硫掺杂的样品具有最佳的光催化活性。该催化剂在可见光照6 h后可将染料彻底降解至无色溶液,且通过对罗丹明B溶液进行紫外-可见分光光度分析(见图9),发现降解过程染料的生色基团、共轭体系、苯环结构已被彻底破坏。与硫单掺杂样品相比,单掺杂样品对罗丹明B溶液彻底降解需要12 h以上,而氮硫共掺杂样品只需6 h,说明氮硫共掺杂能够有效地提高催化剂对染料的彻底降解能力。当通入NH3/氩气时间增加到14 h后,并不利于共掺杂样品光催化活性的提高,可能是因为过量的掺杂会导致新空穴-电子复合中心的形成,阻碍光生载流子传到光催化剂的表面,产生活性分子的量下降最终导致光催化活性下降[14-15]。
2.4.2光催化降解亚甲基蓝和橙黄Ⅱ号
在实际的印染废水中通常是由多种染料混合而成,为了进一步测试氮硫共掺杂SrSnO3样品是否对其它染料也有同样的光催化效果,现以阳离子型染料亚甲基蓝(MB) 、偶氮染料橙黄Ⅱ号(Or Ⅱ)为模拟污染物并考察它们在可见光照射下的光催化活性。
如图9所示,亚甲基蓝的各吸收峰经过3 h的可见光催化反应后已基本消失,其中位于665 nm处的吸收峰强度随着反应时间的增加逐渐减弱,同时观察到溶液的颜色逐渐变浅,这意味着染料的大共轭体系被破坏,而同样苯环的吸收峰(288 nm)和同环双烯的吸收峰(242 nm)也出现不同程度的减弱,这说明在降解的过程中苯环结构和同环双烯结构也发生断裂,吸收峰下降。实验中也观察到溶液的颜色从蓝色逐渐褪色直至无色,3 h内溶液的脱色率达到96%以上,在不加入光催化剂的条件下亚甲基蓝的自行褪色<6%。
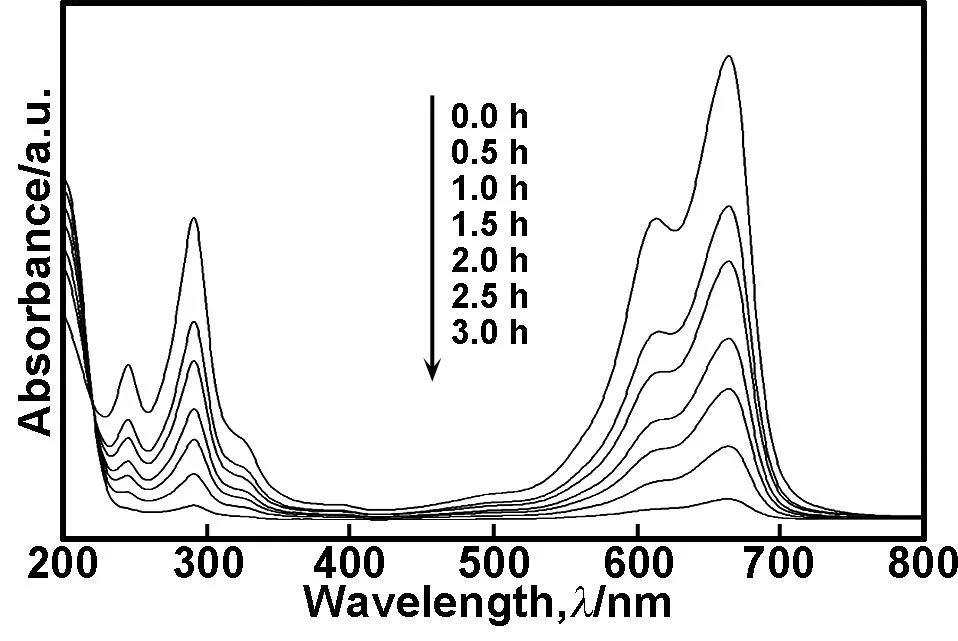
图9光催化过程中MB溶液UV-Vis光谱变化图(MB初始浓度1.0×10-5,催化剂浓度 1 g/L)
Fig 9 UV-Vis spectra changes of 1.0×10-5MB during visible-light photocatalysis in presence of 1 g/L N/S co-doped SrSnO3catalys

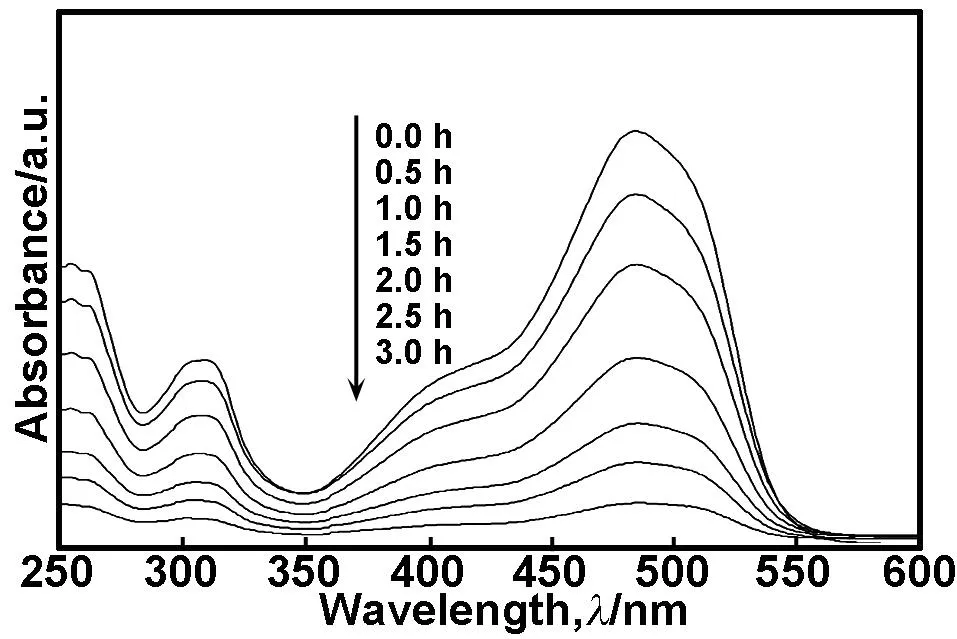
图10光催化过程中Or Ⅱ溶液UV-Vis光谱变化图(Or Ⅱ初始浓度为1.0×10-5,催化剂浓度为1 g/L,助催化剂为20 mmol/L的H2O2)
Fig 10 UV-Vis spectra changes of 1.0×10-5Or Ⅱ in presence of 1 g/L N/S co-doped SrSnO3catalys and 20 mmol/L H2O2co-catalyst
3结论
将非金属的掺杂改性研究应用于SrSnO3,制备出了氮硫共掺杂的SrSnO3。实验结果表明,氮、硫分别是以晶格取代和间隙掺杂的形式存在于样品中,且氮硫共掺杂的样品对可见光的吸收比单掺杂要强。对其可见光催化性能进行了研究,发现其对罗丹明B、亚甲基蓝和橙黄Ⅱ号表现出良好的降解能力和适用性,获得了一些有意义和有价值的结果。
参考文献:
[1]Wang Shaowen, Chen Sheng, Sun Dezhi. Advances in the treatment of printing and dyeing wastewater by physical and chemical processes[J]. Industrial Water Treatment, 2010, 30(1): 8-12.
王绍温, 陈胜, 孙德智. 物化法处理印染废水的研究进展 [J].工业水处理,2010, 30(1): 8-12.
[2]Fujishima A. Electrochemical photolysis of water at a semiconductor electrode[J]. Nature, 1972, 238: 37-38.
[3]Zhu Baiming, Jiang Yan, Peng Shaoqin, et al. Effect of ambient conductions on degradation of formaldehyde by F and N co-doped TiO2photocatalyst[J]. Nonferrous Metals, 2011, (4): 44-46.
朱百鸣, 江元, 彭绍琴, 等. 环境条件对氟、氮共掺杂TiO2光催化降解甲醛活性的影响[J]. 有色金属, 2011, (4): 44-46.
[4]Chen D, Jiang Z, Geng J, et al. Carbon and nitrogen co-doped TiO2with enhanced visible-light photocatalytic activity[J]. Industrial & Engineering Chemistry Research, 2007, 46(9): 2741-2746.
[5]Li Hui, Wang Jinshu, Li Hongyi, et al. Microstructure of nitrogen and sulfur co-doped mesoporous TiO2film and its photocatalytic activity[J]. Journal of inorganic materials, 2009, 24(5): 909-914.
李辉, 王金淑, 李洪义,等. 氮硫掺杂介孔TiO2薄膜结构及其光催化性能 [J].无机材料学报,2009, 24(5): 909-914.
[6]Dong F, Zhao W, Wu Z. Characterization and photocatalytic activities of C, N and S co-doped TiO2with 1D nanostructure prepared by the nano-confinement effect[J]. Nanotechnology, 2008, 19(36): 365607.
[7]Chen D, Ye J. SrSnO3nanostructures: synthesis, characterization, and photocatalytic properties[J]. Chemistry of Materials, 2007, 19(18): 4585-4591.
[8]Lin Y, Lin S, Luo M, et al. Enhanced visible light photocatalytic activity of Zn2SnO4via sulfur anion-doping[J]. Materials Letters,2009, 63(13-14): 1169-1171.
[9]Kim J Y, Kim C S, Chang H K, et al. Synthesis and characterization of N-doped TiO2/ZrO2visible light photocatalysts[J]. Advanced Powder Technology, 2011, 22(3): 443-448.
[10]Asahi R, Morikawa T, Ohwaki T, et al. Visible-light photocatalysis in nitrogen-doped titanium oxides[J]. Science, 2001, 5528(293): 269.
[11]Umebayashi T, Yamaki T, Itoh H, et al. Band gap narrowing of titanium dioxide by sulfur doping[J]. Applied Physics Letters, 2002, 81: 454.
[12]Ohno T, Tsubota T, Toyofuku M, et al. Photocatalytic activity of a TiO2photocatalyst doped with C4+and S4+ions having a rutile phase under visible light[J]. Catalysis Letters, 2004, 98(4): 255-258.
[13]Jiang L, Wang Q, Li C, et al. ZrW2O8photocatalyst and its visible-light sensitization via sulfur anion doping for water splitting[J]. International Journal of Hydrogen Energy, 2010, 35(13): 7043-7050.
[14]Irie H, Watanabe Y, Hashimoto K. Nitrogen-concentration dependence on photocatalytic activity of TiO2-xNxpowders[J]. The Journal of Physical Chemistry B, 2003, 107(23): 5483-5486.
[15]Lucky R A, Charpentier P A. N-doped ZrO2/TiO2bimetallic materials synthesized in supercritical CO2: Morphology and photocatalytic activity[J]. Applied Catalysis B: Environmental, 2010, 96(3-4): 516-523.
[16]Hu C, Yu JC, Hao Z, et al. Effects of acidity and inorganic ions on the photocatalytic degradation of different azo dyes[J]. Applied Catalysis B: Environmental, 2003, 46(1): 35-47.
Preparation and characterization of N/S-codoped SrSnO3for photocatalytic degradation of dyes under visible-light irradiation
HUANG Qiufeng, XIAO Hanbing, ZHANG Xiaofeng, LIN Shen
(College of Chemistry and Chemical Engineering, Fujian Normal University, Fuzhou 350007, China)
Abstract:N/S-codoped SrSnO3 composite compound was successfully prepared by hydrothermal method. The resulting product was characterized by XRD, XPS and DRS. It was found that N element replace O lattice sites and S element enter into the interstitial sites of SrSnO3 crystal, respectively. DRS observations showed that N/S-codoped SrSnO3 was sensitive to visible-light irradiation. The photocatalytic activity was tested with photodecomposition of rhodamine B, methylene blue and orange II. The results indicated that 100% of RhB was degraded after 6h, 96% of methylene blue was degraded after 3 h and 93% of orange Ⅱ was degraded after 3.5 h in the presence of N/S-codoped SrSnO3 composite materials under irradiation of visible light.
Key words:SrSnO3;co-doping; photocatalysis; degradation
DOI:10.3969/j.issn.1001-9731.2016.02.043
文献标识码:A
中图分类号:O614.4
作者简介:黄秋锋(1978-),男,福州人,副教授,博士,主要从事催化材料研究。
基金项目:国家自然科学基金资助项目(21003022);福建省科技厅(K类)资助项目(JK2014010)
文章编号:1001-9731(2016)02-02219-05
收到初稿日期:2015-04-20 收到修改稿日期:2015-07-31 通讯作者:黄秋锋,E-mail: qiufenghuang@fjnu.edu.cn;林深
