电位型痕量硫氢根模拟酶生物传感器研究
2016-04-12赵俊剑韩知璇杨秀惠韩晓微孙照琦朱永春
赵俊剑 韩知璇 杨秀惠 韩晓微 孙照琦 朱永春,2*
(1 沈阳师范大学 化学化工学院,沈阳 110034; 2 沈阳师范大学 化学化工学院 能源与环境催化研究所,沈阳 110034)
电位型痕量硫氢根模拟酶生物传感器研究
赵俊剑1韩知璇1杨秀惠1韩晓微1孙照琦1朱永春1,2*
(1 沈阳师范大学 化学化工学院,沈阳 110034; 2 沈阳师范大学 化学化工学院 能源与环境催化研究所,沈阳 110034)
以恒电位法在pH=9.0碱性水溶液中碳纤维簇电极上镀单层锌,在含有组氨酸和电解氧化锌镀层下原位合成了锌-组氨酸-羟基络合物修饰碳纤维电极,模拟了生物酶识别痕量的硫氢酸根离子,优化了电极制备的条件。建立了开路电位测定硫氢酸根离子的方法,在中性水溶液中,该电极以开路电位变化响应注入溶液中的硫离子浓度,并可用能斯特方程描述开路电位变化的规律。方法的最低检出限为1.0×10-15mol/L,检测范围为1.0×10-6~1.0×10-15mol/L,相对标准偏差为3.5%。对实际样品中硫氢酸根离子检测结果为1.12×10-13mol/L,加标回收率为109.2%。研制的电化学传感器具有响应快速,灵敏度高,检出限低,检测范围宽,仪器简单方便等特点。
硫氢酸根;电位法;电化学模拟酶生物传感器;电化学传感器
前言
硫化氢是一种无机化合物,化学式为H2S。正常情况下是一种无色、易燃的酸性气体,浓度较低时带恶臭,气味如臭蛋。硫化氢是一种急性剧毒气体,较高浓度的硫化氢可以麻痹嗅觉神经,导致浓度高时反而没有气味。吸入少量高浓度硫化氢可于短时间内致命。低浓度的硫化氢对眼、呼吸系统及中枢神经都有影响[1]。硫化氢气体在矿物、油田、水体临床、沼泽地开采等生产生活中都存在,并与氧气、二氧化碳、硫氧化物等气体共存。硫化氢也是生命过程的代谢产物之一[2-3],与很多疾病相关[4-6],因而是临床和环境微生物等领域重要的检测物之一。无机硫化物通常以H2S,HS-和S2-形式存在于不同的pH值水溶液中。在大多数的pH值下主要是HS-阴离子形式存在。H2S常用的分析方法有荧光光度法[7],检出限为0.80 ng/mL;分子吸收光谱法[8],检出限为0.010 μg/mL;化学发光法[9],检出限为0.32 ng/mL;色谱法[10],检出限1.9 ng/mL;极谱法[11],检出限为0.15 ng/mL。如何能够进一步提高灵敏度,降低检出限,以适应生物体系和临床医学中的检测需要,成为分析化学的重要任务。开路电位方法是一种电位测定型方法[12],常用于表征电极表面状况。目前,也开始成为一种电化学电位分析方法[13-14]而受到关注。
在生物体系中,结合和清除硫化物的酶是一种含锌的蛋白质[15],其中锌与周围的三个组氨酸形成配位化合物,留下一个位置键合水,羟基或硫化物。在中性pH值下主要是HS-阴离子存在,与络合锌离子键合的HS-阴离子被Zn2+/Zn氧化还原体系氧化成为SO32-及SO42-而脱离体系。本文根据生物体系HS-阴离子与酶活性中心结合的特点,将碳纤维簇电极[16-17]电沉积锌置于含有组氨酸溶液中进行电化学氧化,原位合成模拟酶的锌-组氨酸修饰电极,在此修饰电极与硫化物溶液接触时引起开路电位的变化为检测信号,分析原溶液中硫化物浓度,构成了灵敏度高、检出限低、检测范围宽的模拟酶生物传感器,并用于湖水中硫离子的检测,获得满意结果。
1 实验部分
1.1 实验仪器
CHI620B电化学分析仪(上海辰华仪器公司),铂丝电极为对电极(自制),修饰的碳纤维簇电极为工作电极(自制),甘汞电极为参比电极(上海雷磁仪器设备厂),超纯水机(德国milliQ公司)。
1.2 实验试剂
硫化钠(Na2S分析纯),L-组氨酸,氯化锌(ZnCl2分析纯),氢氧化钠、铁氰化钾、氯化氢均为分析纯。所有试液都由超纯水配制(MiliQ,18.2 MΩ·cm)。组氨酸(His, histidine)。
1.3 碳纤维簇电极制备
将适量的带状碳纤维涂好环氧树脂胶后,引入内径为6.0 mm的玻璃管中,一端连接导电金属丝作为引线。自然强化风干后,将另一端在不同粒度的砂纸上打磨成镜面,即成为基础的碳纤维簇盘电极。
2 结果与讨论
2.1 基础碳电极的循环伏安曲线
将自制的碳纤维(纤维直径约7.0 μm)簇电极(组成的簇电极内径约为6.0 mm)经13 μm砂纸打磨、硫酸纸抛光后用去离子水冲洗后,置于5.0 mL K3[Fe(CN)6]溶液(0.10 mol/L)+1.0 mL KCl溶液(0.20 mol/L)的铁氰化钾标准体系中(最终铁氰化钾浓度为0.083 mol/L,支持电解质KCl浓度为0.33 mol/L),混合均匀,在扫描速率为0.1 V/s时,采用循环伏安法检测其性能,获得的循环伏安曲线如图1。
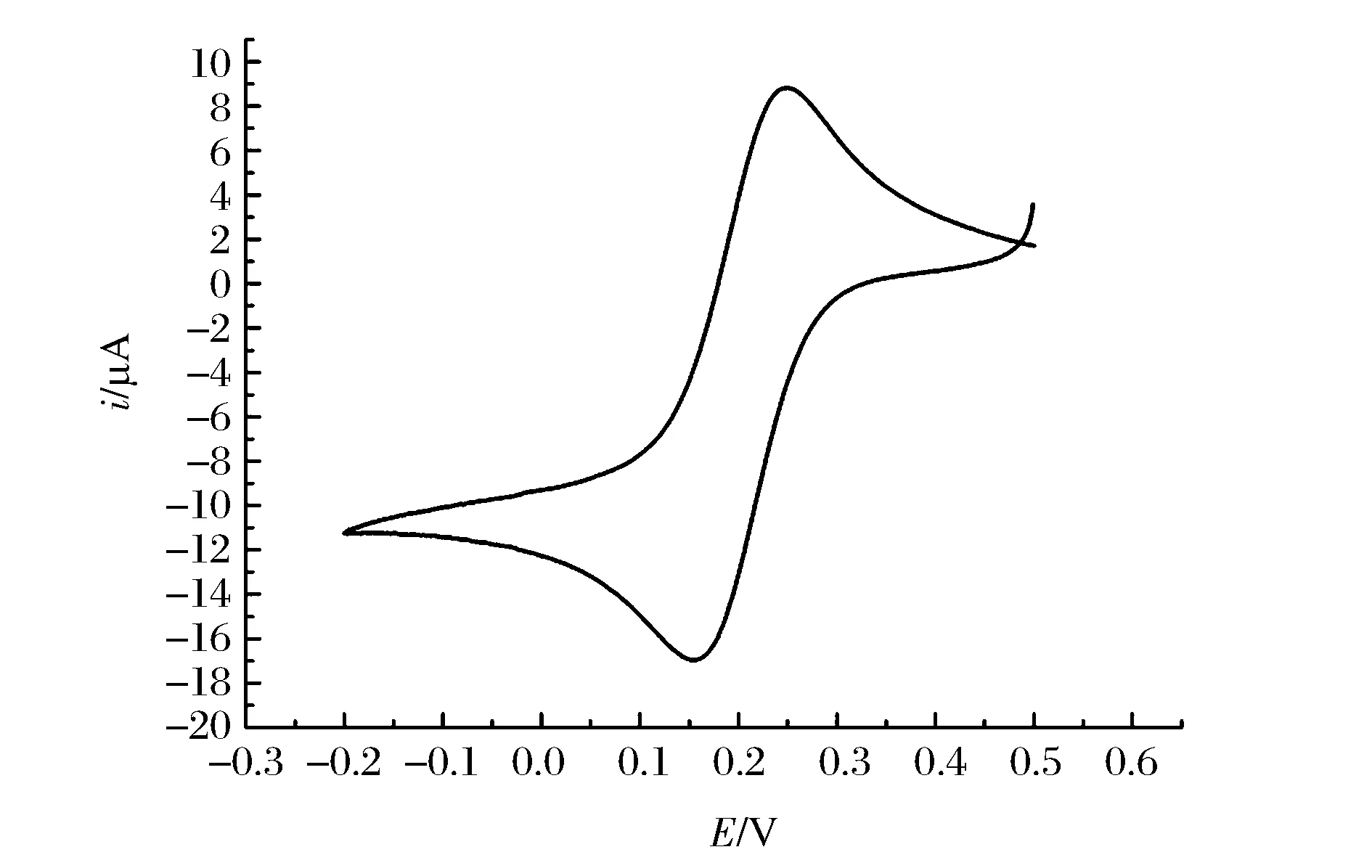
图1 铁氰化钾在碳纤维簇电极上的循环伏安图Figure 1 Cyclic voltammogram of potassium ferricyanate at carbon fiber cluster electrode.
由图1可知,电流-电位曲线具有典型的S型,表明该碳纤维簇电极具有微电极簇的性质。铁氰化钾的还原峰位于0.151 V处,峰电流为15.78 μA;氧化峰位于0.251 V处,峰电流为15.64 μA;峰-峰电位差为100 mV,峰-峰电流差为31.42 μA,属于铁氰化钾在碳纤维簇电极上的典型循环伏安曲线,表明该电极具有较好的电化学活性,可以作为基础电极进行化学修饰。
2.2 碳电极表面上的电沉积锌
为了获得锌的羟基化合物,并通过与组氨酸的络合形成带有羟基的组氨酸络合物[6],采用弱碱性条件沉积锌镀层[18]。将清洗好的碳电极置于ZnCl2(0.042 mol/L)和KCl(0.33 mol/L)的混合溶液中(pH=9.0),在电位为-1.2 V下进行恒电位电沉积500 s。为了检查镀锌的结果,在此溶液中,扫描速率为0.1 V/s,从-1.2 V到0.6 V电位范围内直接进行6圈循环伏安扫描,获得的循环伏安曲线如图2所示。
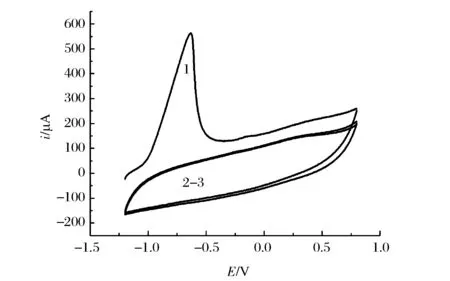
图2 镀锌电极在镀液中的循环伏安曲线Figure 2 Cyclic voltammetry of zinc deposited carbon fiber cluster electrode in deposition solution.
由图2可以看出,第一圈氧化峰位于-0.63 V,峰电流为570.2 μA,峰面积为1.003×10-3C;第二圈起,该氧化峰已经完全消失。第一圈氧化峰下的面积代表了在此过程中电沉积的总锌对应的电量,计算出大约有0.5 mmol的锌沉积在电极表面。如果采用恒电位氧化,氧化电位至少0.6 V,需要时间应该远大于15 s。
2.3 碳电极表面上的原位修饰
将镀锌的电极取出,去离子水淋洗表面后自然风干。将其置于5.0 mL KCl[1.0 mol/L,含有组氨酸(0.10 mol/L)]的溶液(pH=7.0)中,在0.8 V下恒电位氧化300 s,取出电极,去离子水淋洗表面后自然风干。此时的电极即为原位电化学氧化制备的锌-组氨酸-羟基络合物修饰的碳电极。
在此情况下,电极表面发生的反应为:
Zn2++4OH-→ [Zn2+(OH-)4]2-(在溶液中)
(1)
[Zn2+(OH-)4]2-+2e-→ [Zn0(OH-)4]4-
(恒电位电还原-锌电沉积)
(2)
[Zn0(OH-)4]4-+ 3His - 2e-→
[Zn2+(His)3(OH-)]++3OH-(恒电位电氧化-修饰)
(3)
2.4 修饰电极响应硫离子的开路电位曲线与条件优化
将制备的锌-组氨酸-羟基络合物修饰的碳电极置于5.0 mL KCl溶液(1.0 mol/L)中,设定时间为500 s,进行开路电位实验。在实验进行至300 s时,将5.0 mL Na2S溶液(1.00×10-6mol/L)沿电极注入电解池内,记录开路电位曲线如图3所示。
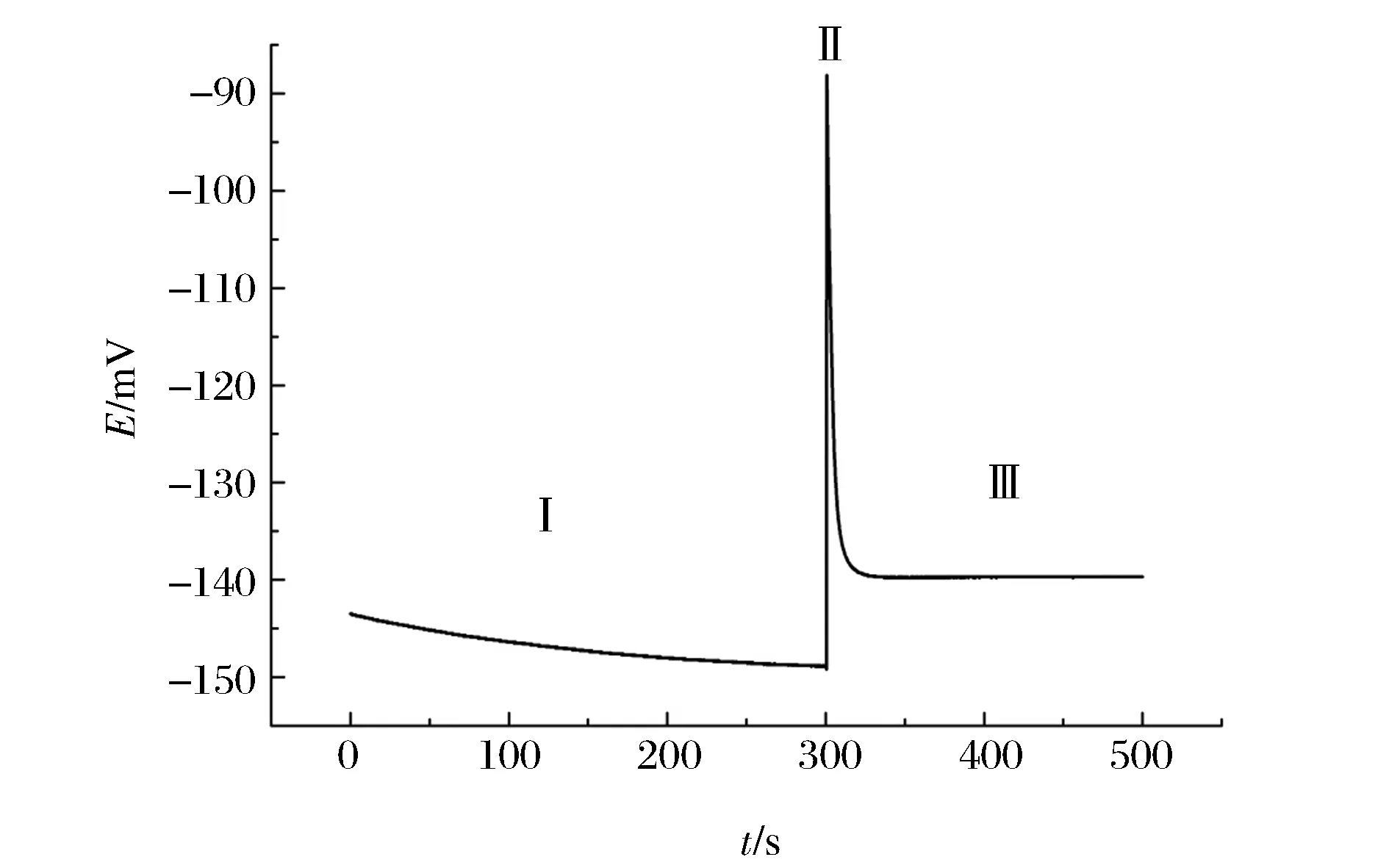
图3 修饰电极在支持电解质中的开路电位曲线Figure 3 An open circuit potential curve of the modified electrode in electrolyte solution.
曲线可以分成三个区域,在300 s之前I区内,修饰电极在KCl(0.10 mol/L)支持电解质溶液的平衡过程中,此时溶液中pH=7.0,羟基浓度远低于氯离子的浓度,尽管羟基络合物比氯离子络合物稳定,仍然可能发生氯离子取代羟基的反应,生成锌-组氨酸-氯离子络合物,此过程反应缓慢,开路电位值下降,持续到300 s左右,开路电位已经基本上不变化。其过程发生的反应式为:[Zn2+(His)3(OH-)]++ Cl-→ [Zn2+(His)3(Cl-)]++OH-
(4)
其能斯特方程为,
(5)
(6)
在300 s时注入硫化钠溶液后,开路电位相应曲线进入第II区。在pH=7.0下,硫化钠主要以硫氢酸根形式存在,电极表面上的锌-组氨酸-氯离子络合物已发生置换反应,生成锌-组氨酸-硫氢酸根-氯离子混合络合物,其反应式为:[Zn2+(His)3(Cl-)]++ HS-→[Zn2+(His)3(HS-)(Cl-)]
(7)
根据镀锌电极表面上锌电对的能斯特方程以及络合物形成常数
(8)
推导,此过程中伴随硫氢酸根离子浓度增加电位差是增大的,即
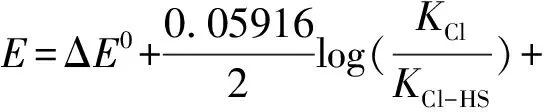
(9)
其中KCl大于KCl-His,硫氢酸根的浓度从没有增加到10-6mol/L,所以开路电位差是上升的。
在第Ⅲ区域内,锌-组氨酸-硫氢酸根-氯离子混合络合物不是稳定络合物,易于失去一个氯化氢分子生成稳定的锌-组氨酸-硫离子络合物,其反应式为: [Zn2+(His)3(HS-)(Cl-)] →[Zn2+(His)3(S2-)]+HCl
(10)
相应的能斯特方程为:
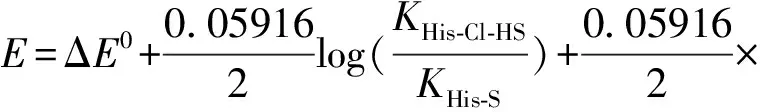
(11)
由于KHis-Cl-HS小KHis-S几个数量级,尽管[HS-]/[S2-]比值大于1,仍不能改变下降的总趋势,所以第Ⅲ区引起开路电位下降,反应达到平衡后获得稳定的开路电位值。
2.5 镀锌过程的条件优化
锌的电化学沉积是实现原位制备修饰电极的第一步,也是最为关键的一步,直接影响硫离子的测定结果。主要影响因素包括溶液pH值和溶液温度。通常的镀锌过程是在碱性条件下[18]进行的,特别是希望生成氧化锌纳米粒子,原位电化学氧化络合修饰过程中,碱性有利于络合物的形成,碱性太高可能降低锌离子的活度,为获得足够量的镀层,需要使用足够的锌离子浓度和长的电镀时间。为确定最佳反应条件,实验选择在pH值为8~10的弱碱性条件下镀锌。温度是电沉积的另一个重要影响因素,实验中,主要要求获得Zn(OH)2组分的沉积膜,根据文献[19]的锌电沉积膜组成的研究表明,最佳电沉积温度应该在25~30 ℃左右,从而获得Zn(OH)2组分,而不是脱水称为ZnO膜。
2.6 溶液pH值的优化
将自然干燥的修饰电极连同参考电极和对电极置于5.0 mL KCl溶液(0.10 mol/L)中,调节修饰溶液pH值,控制溶液温度为30 ℃,设置时间为500 s,进行开路电位实验,记录电位-时间曲线。在实验进行300 s时,注入5.0 mL准备好的温度为30 ℃的Na2S溶液,观察电位-时间曲线的变化,记录开始上升到峰值处的开路电位差。将开路电位差对溶液pH值作图,如图4所示。
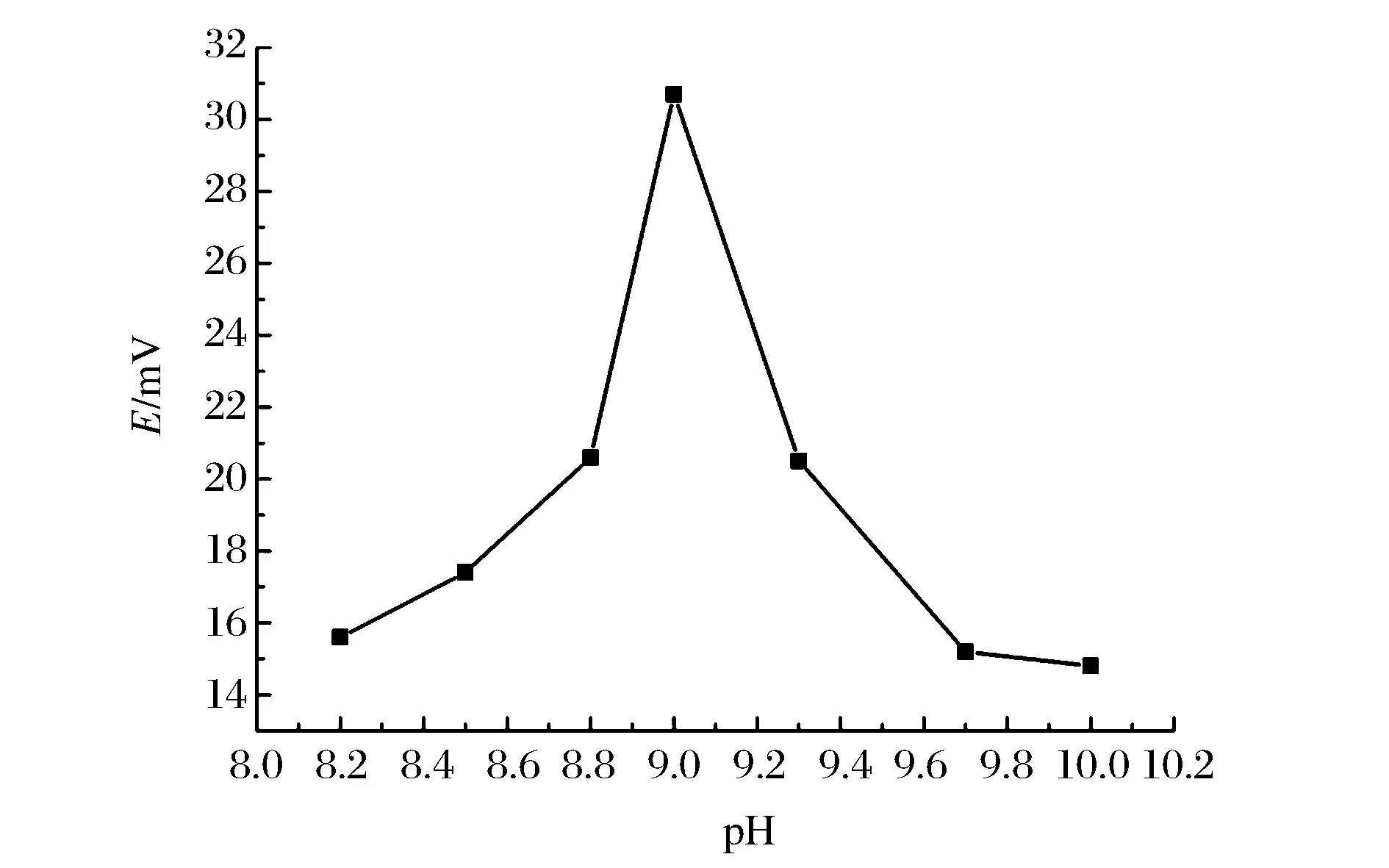
图4 开路电位差与pH值关系曲线 Figure 4 The dependence of open circuit potential difference on the pH of deposition solution.
图4可见,测定信号的确是溶液pH值的敏感函数,主要原因是因为所需要的物质为最好含有一个羟基的四元络合物,pH值控制了溶液中羟基浓度,羟基多了易于生成多羟基络合物,羟基少了易于生成没有羟基的组氨酸络合物,两者都不利于硫氢酸根的置换反应。在pH=9.0的条件下,开路电位差最大,在低于或高于pH=9.0的条件不适合测定。所以电沉积条件定为溶液pH=9.0,控制温度为30 ℃。
2.7 沉积时间的影响
在合适的电沉积条件下获得镀锌电极的另一个条件是沉积量,希望在电极表面的活性点上沉积单原子层的锌,从而在原位氧化和络合物形成过程中获得单分子层修饰,这对于置换反应有利。沉积量过多,氧化过程不完全,即使氧化完全,在络合物形成过程中可能形成多层分子修饰,造成修饰分子间相互作用而形成分子间交叉络合物,不利于置换反应。在给定电位下,沉积量与沉积时间相关,于是设计实验选择最佳沉积时间。
将清洗好的碳电极置于含有ZnCl2(0.042 mol/L)和KCl(0.33 mol/L)的混合溶液(pH=9.0)中,在电位为-1.2 V,不同沉积时间下,进行恒电位电沉积。将获得的修饰电极在优化条件下进行开路电位实验,将获得的开路电位差对沉积时间作图,如图5所示。
图5中可以看出,在-1.2 V沉积电位下,沉积时间从200~500 s之间,开路电位差线性增加;从500~1000 s范围内,开路电位差线性下降,其方程分别为式(12)、(13)。
ΔE200~500=6.26+0.081 4t;R2=0.992,SD=1.18
(12)
ΔE500~1 000=84.35-0.075 1t;R2=0.997,SD=1.56
(13)
因此,500 s是形成单原子层的最合适沉积时间。
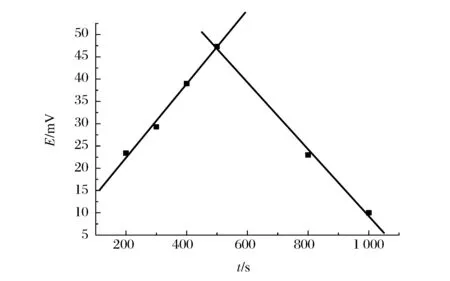
图5 开路电位差与电沉积时间的关系曲线 Figure 5 The dependence of open circuit potential difference on deposition time.
2.8 硫氢酸根浓度测定的标准曲线
将优化条件下获得的修饰电极置于5.0 mL KCl溶液(1.0 mol/L)中,设定时间为500 s,进行开路电位实验。在300 s下,注入5.0 mL不同浓度的硫化钠溶液。将获得的开路电位差对硫化钠溶液浓度的对数作图。实验发现,开路电位差在1.0×10-6~1.0×10-15mol/L浓度范围内,存在两条线性关系。
其中,在1.0×10-6~1.0×10-10mol/L范围内开路电位曲线及线性关系,如图6所示。
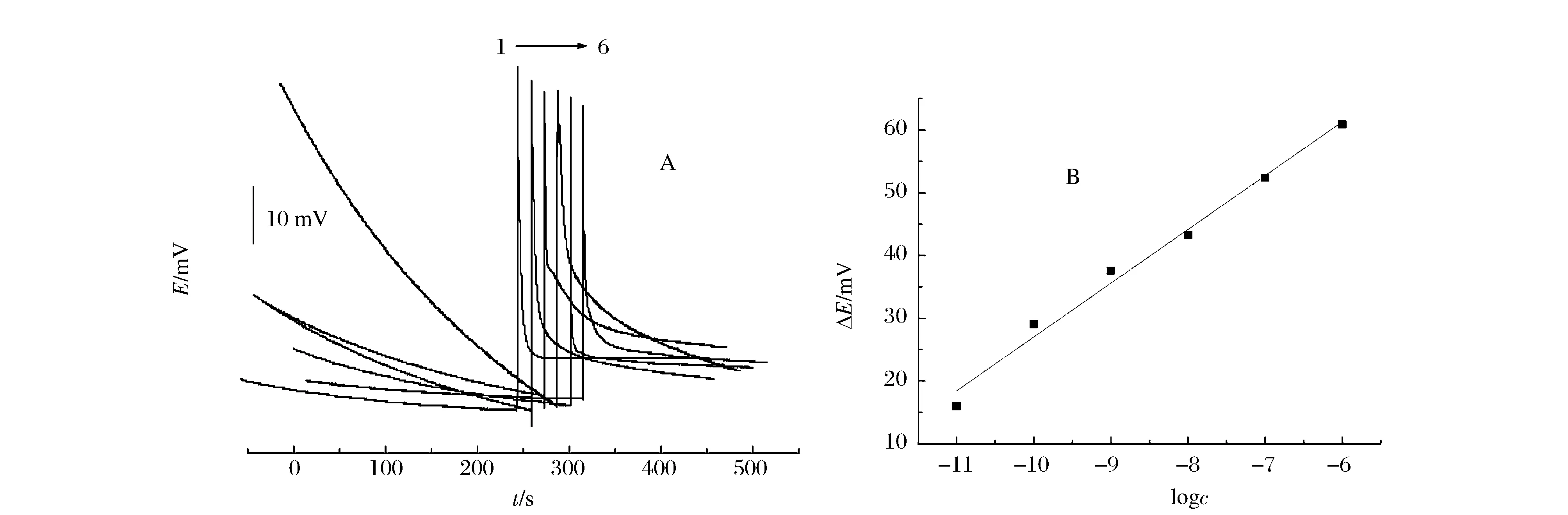
图6 开路电位-时间曲线(A)与开路电位差与浓度对数关系曲线(B)(1.0×10-6~1.0×10-10 mol/L)Figure 6 The dependence of open circuit potential on time(A) and a logarithmic relationship between open circuit potential difference and sodium sulfide concentration(B).
线性回归方程为:
ΔE1=112.76+8.74 logcNa2S;R2=0.988,SD=1.96
(14)
在1.0×10-12~1.0×10-15mol/L范围内开路电位曲线及线性关系如图7所示。
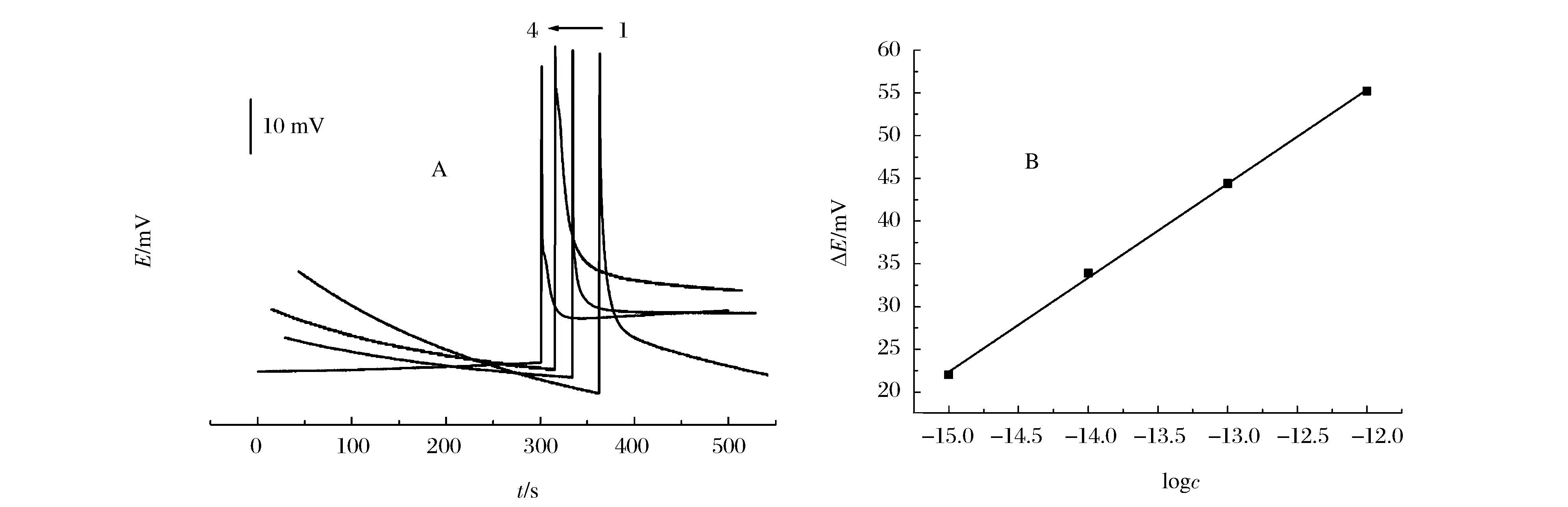
图7 开路电位-时间曲线(A)与开路电位差与浓度对数关系曲线(B)(1.0×10-12~1.0×10-15 mol/L)Figure 7 The dependence of open circuit potential on time (A) and a logarithmic relationship between open circuit potential difference and sodium sulfide concentration (B).
回归方程为:
ΔE2=187.5+11.01 logcNa2S;R2=0.9993,SD=0.47
(15)
从这些关系中可以看出,两条曲线都随着硫化钠离子浓度的增加,电位差增大,基本符合(11)式的能斯特方程,只是斜率小了些,可能是因为电极表面反应中,反应效率受到很多因素的影响,而没有真正达到反应平衡态所至。两条曲线都是线性增加直线,但是斜率不同,反映出对于不同的浓度,电极表面上的反应机理有所差异所至,根据这两个线性关系可以测定水溶液中的硫离子浓度。
2.9 精密度实验
在优化条件下,以Na2S(1.0×10-15mol/L)为注入溶液进行5次平行开路电位实验,获得的开路电位变化值分别为:21.0、22.0、21.6、22.4、23.0 mV,计算相对标准偏差(RSD)为3.5%。
2.10 河水中硫离子浓度测定
以沈阳师范大学校园湖为水样品,经煮沸20 min,杀死微生物和除去有机质溶解的CO2等可能的干扰物质,冷却至室温为注入样品溶液。将修饰好的电极置于5.0 mL KCl溶液(0.10 mol/L)中,设置时间为500 s,当反应进行到300 s时,注入5.0 mL水样,记录开路电位-时间曲线如图8(A)所示,计算出开路电位差四次结果取算术平均值为(44.9±2.4) mV。由于两条标准曲线有交叉,无法判别应该使用哪条标准曲线,将样品稀释10倍后继续做同样实验如图8(B)所示。三次结果的算术平均值为(33.1±2.8) mV,浓度稀释10倍,开路电位差减少了11.8 mV,与第二条曲线斜率一致。计算出湖水样品中含有硫离子为1.12×10-13mol/L。
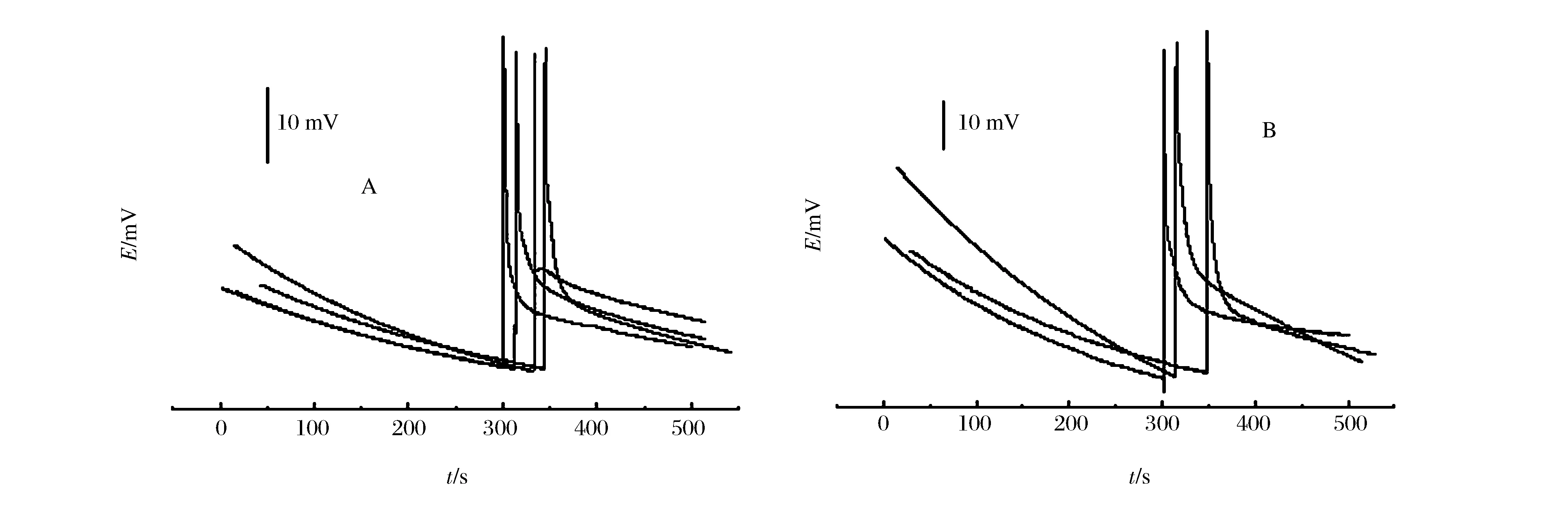
图8 稀释前(A)和稀释后(B)湖水样品的开路电位-时间曲线Figure 8 The dependence of open circuit potential on time for the samples before being diluted (A) and after being diluted (B).
2.11 加标回收实验
在相同的实验条件下,取校园湖水,过滤,煮沸后冷却,进行加标回收实验,平行测定4次,电位结果为46.1、47.3、49.7、51.4 mV,对应的样品浓度结果见表1,加标回收率平均值为109.2%,符合分析测定要求。

表1 样品测定结果
3 结语
通过将锌-组氨酸-羟基络合物电化学原位修饰在碳纤维簇电极上,构建成了电位型模拟酶电化学传感器,实现了对水中硫氢酸根的识别。建立了开路电位法检测水中硫氢酸根离子的方法。最低检出限为1.0×10-15mol/L,检测范围为1.0×10-6~1.0×10-15mol/L。对沈阳师范大学湖水中硫离子检测结果为1.12×10-13mol/L,加标回收率为109.2%。实验表明,该电化学传感器具有响应快速,灵敏度高,检出限低,检测范围宽,仪器简单方便等特点。
[1] 赵霞,田松柏,王志飞.石油及其产品中硫含量的测定方法[J].石油与天然气化工(Chemicalengineeringofoilandgas),2006,35(6):480-484.
[2] Tang K, Baskaran V, Nemati M. Bacteria of the sulphur cycle: an overview of microbiology, biokinetics and their role in petroleum and mining industries[J].Biochem.Engin.J.,2009,44(1):73-94.
[3] Wang M,Zhu J,Pan Y, et al.Hydrogen sulfide functions as a neuromodulator to regulate striatal neurotransmission in a mouse model of Parkinson's disease[J].J.Neurosc.Res., 2015,93(3):487-494.
[4] Li G, Xie Z, Chua J M W ,et al.Hydrogen sulfide protects testicular germ cells against heat-induced injury[J].NitricOxide,2015,46(1):165-171.
[5] Wallace J L,Wang R.Hydrogen sulfide-based therapeutics: exploiting a unique but ubiquitous gasotransmitter[J].NatureReviewsDrugDiscovery, 2015,14(5):329-345.
[6] Paul B D,Snyder S H.Modes of Physiologic H2S signaling in the brain and peripheral tissues[J].Antioxidants&RedoxSignaling,2015,22(5):411-423.
[7] 崔万苍,米俐.高灵敏度测定硫的荧光光度法研究及应用[J].分析化学(ChineseJournalofAnalyticalChemistry),1987,15(30):207,212-215.
[8] Jin Q H, Zhang H Q,Duan Y,et al. Trace determination of sulfide and sulphur dioxide by vapor molecular absorption spectrometry using magnesium and tellurium hollow cathode lamps[J].Talanta,1992,39(8):967-970.
[9] 吕九如,张新荣.利用Fe2+-鲁米诺-O2化学发光体系测定痕量S2-的研究[J].分析化学(ChinesejournalofAnalyticalChemistry),1989,17(6):542-544.
[10] Goodwin L R, Francom D, Urso A, et al. Determination of trace sulfide in turbid by gas dialysis/ion chromatography[J].Anal.Chem,1988,60(3):216-219.
[11] Milosavljevic E B, Solujic L, Hendrix J L, et al. Flow injection das diffusion method for preconcentration and determination of trace sulfide[J].Anal.Chem.,1988, 60(24):2791-2796.
[12] Keilin D, Mann T. Carbonic anhydrase.purification and nature of the enzyme[J].J.Nutr.Rev.,2009,43(5):150-152.
[13] 田红,王清林,陶思源,等. 光合细菌燃料电池的开路电位法研究[J].沈阳师范大学学报(JournalofShenyangNormalUniversity),2012,30(3):386-389.
[14] 梁镇海,张福元,孙彦平.镍电极开路电位测定微量硼氢根离子[J].分析化学(ChinesejournalofAnalyticalChemistry),2006,34(9):145-147.
[15] Wilburnl J P, Ciobanul M, Lowy D A. Characterization of acrylic hydrogels by open circuit potential monitoring[J].J.Appl.Electrochem., 2004,34(7):729-734.
[16] 周伟红,刘峻,丁建华,等.电化学预处理碳纤维电极用于毛细管电泳安培检测局部麻醉药[J].分析化学(ChinesejournalofAnalyticalChemistry),1995,23(8):880-884.
[17] 金根娣,杨阿喜.修饰碳纤维电极为工作电极-溶出伏安法测定银离子[J].理化检验:化学分册(PhysicalTestingandChemicalAnalysisPartB:ChemicalAnalysis),2008,44(12):1155-1158.
[18] Caillaud F, Smith A, Banward J F. Effect of pH of the solution on the deposition od zinc oxide films by spray pyrolysis[J].J.Am.Ceram.Soc.,1993,76(4):998-1002.
[19] 王艳坤,张建民,兰梦.温度对ZnO薄膜电沉积的影响[J].物理化学学报(ActaPhysico-ChimicaSinica),2009,25(10):1998-2004.
Study on Trace Hydrogen Sulfide Artificial Enzyme Potentiometric Biosensor
ZHAO Junjian1, HAN Zhixuan1,YANG Xiuhui1,HAN Xiaowei1, SUN Zhaoqi1, ZHU Yongchun1,2*
(1.CollegeofChemistryandChemicalEngineering,ShenyangNormalUniversity,Shenyang,Liaoning110034,China; 2.CollegeofChemistryandChemicalEngineering,InstituteofCatalysisforEnergyandEnvironment,ShenyangNormalUniversity,Shenyang,Liaoning110034,China)
In the present work, a single layer of zinc film was galvanized on the carbon fiber cluster electrode by potentiostatic method in alkaline aqueous solution with pH=9.0. In the presence of the coating layer of histidine and electrolytic zine oxide, a zinc-histine-hydroxyl complex modified electrode was in-situ prepared and used to mimic the process in which hydrogen sulfide ions are recognized by biological enzyme molecules. The experimental conditions of the modified electrode preparation method were optimized. An open circuit potential method for the determination of trace hydrogen sulfide was developed based on this modified electrode. In neutral aqueous solution, the open circuit potentials at the modified electrode had regular changes with the concentrations of the hydrogen sulfide ions which were injected into the solution. And the relationship between open circuit potentials and hydrogen sulfide ion concentration can be described by Nernst equation. The method was used to determine the concentration of sulfide in aqueous solution in the range of 1.0×10-6-1.0×10-15mol/L, with its lowest detection limit of 1.0×10-15mol/L. The relative standard deviation was 3.5% with the recovery of 109.2%. The advantages, including fast response speed, high sensitivity, low detect limits, wide detection range and easy operation, made the proposed method suitable for the determination of the concentration of hydrogen sulfide ions in river water.
hydrogen sulfide; open circuit potential; electrochemical biologic mimic enzyme biosensor; electrochemical sensor
10.3969/j.issn.2095-1035.2016.04.019
2016-03-28
2016-08-29
国家自然科学基金项目(20807563);沈阳师范大学大学生科研课题项目(201510166106)资助
赵俊剑,女,学生。
*通信作者:朱永春,男,教授,主要从事电化学分析和电化学研究。E-mail:yongchunzhu@126.com
O657.1;TH832
A
2095-1035(2016)04-0072-07
