阿尼西坦缓释片体内代谢产物的测定及药代动力学研究
2016-04-07李连坤张蕾王甜甜王雪张雯娜蔡广
李连坤 张蕾 王甜甜 王雪 张雯娜 蔡广知 贡济宇
[摘要] 目的 建立阿尼西坦缓释片体内代谢产物N-对甲氧基苯甲酰氨基丁酸(ABA)含量的测定方法。 方法 采用反相高效液相色谱法(HPLC法)测定ABA含量,Phenomenex ΜP-ODS C18色谱柱(250×4.6 mm,5 μm),流动相:乙腈∶0.1%醋酸=25∶75,检测波长:250 nm,柱温:35 ℃。 结果 以氯仿∶甲醇为2∶8,涡旋振荡30 s,离心10 min,于40℃下氮气吹干处理血样。在67.5~2150 μg/L范围内线性关系良好,回收率为86.67%~93.58%,均在85%以上,符合实验要求。主要药代动力学参数为:阿尼西坦缓释片的AΜC0-t为(342.13±110.23)μg/(min·ml),Cmax为(7.41±2.05)μg/ml,Tmax为(116.53±1.17)h;阿尼西坦普通片的AΜC0-t为(434.53±102.69)μg/(min·ml),Cmax为(7.46±1.87)μg/ml,Tmax为(28.29±1.11)h。 结论 本实验建立的HPLC法,可以准确测定阿尼西坦体内代谢产物ABA的含量,适用于阿尼西坦缓释片在家兔体内的药代动力学研究。
[关键词] 阿尼西坦;N-对甲氧基苯甲酰氨基丁酸;反相高效液相色谱法;血药浓度;药代动力学
[中图分类号] R284.2 [文献标识码] A [文章编号] 1674-4721(2016)02(c)-0008-04
[Abstract] Objective To establish the determination method of N-anisoyl-GABA (ABA) content of metabolites in vivo for aniracetam sustained release tablet. Methods The content of ABA was determined by reversed-phase high performance liquid chromatography (RP-HPLC method).Phenomenex ΜP-ODS C18 chromatographic column (250×4.6 mm,5 μm) was used and the mobile phase was set as acetonitrile∶0.1% acetic acid =25∶75,detection wavelength was set at 250 nm,and column temperature was 35℃. Results The blood sample were blow-dried by nitrogen at 40℃ (chloroform∶methyl alcohol=2∶8,vortex oscillation for 30 s and centrifugation for 10 min).The result showed favorable linear relation in range of 67.5~2150 μg/L.The recovery rate was 86.67%-93.58%,meeting the experiment requirements of above 85%.The main pharmacokinetic parameters was as follows:the aniracetam sustained release tablet,AΜC0-t=(342.13±110.23) μg/(min·ml),Cmax=(7.41±2.05) μg/ml,and Tmax=(116.53±1.17) h;the aniracetam conventional tablet,AΜC0-t=(434.53±102.69) μg/(min·ml),Cmax=(7.46±1.87) μg/ml,and Tmax=(28.29±1.11) h. Conclusion HPLC method established in this study can accurately determine the ABA content of metabolites in vivo for aniracetam,which is applicable to pharmacokinetic study of aniracetam sustained release tablet in rabbits in vivo.
[Key words] Aniracetam;N-anisoyl-GABA;Reversed-phase high performance liquid chromatography;Blood concentration;Pharmacokinetics
阿尼西坦是1-(4-甲氧基苯甲酰基)2-吡咯烷酮,可用于神经保护和增强记忆。有研究证明,阿尼西坦可改善中老年人记忆力,降低阿尔茨海默病的发病率,因此备受临床关注[1]。阿尼西坦口服吸收后,血中达峰时间为20~40 min,生物半衰期为22 min,4 h后血药浓度已很难测出,其代谢产物以N-对甲氧基苯甲酰氨基丁酸(ABA)为主(约占70%),故采用反相HPLC法[2],测定血液中ABA的浓度。本文旨在建立血浆中ABA血药浓度的反相HPLC法,并应用于家兔的阿尼西坦缓释片的药动学研究,为阿尼西坦缓释片的临床研究及开发提供依据。
1 仪器与试药
1.1 仪器
Agilent 1260高效液相色谱仪(自动进样器、柱温箱、DAD检测器,美国安捷伦公司);AB135-S型十万分之一电子天平(瑞士梅特勒一托利多公司); DCY-12S型氮吹仪(青岛海科仪器有限责任公司);XH-C涡旋振荡器(金坛市精达仪器制造有限公司);TGL-16B高速离心机(湖南星科科学仪器有限公司)。
1.2 试剂与试药
阿尼西坦缓释片、ABA对照品均为实验室自制[3]、阿尼西坦片(亚宝药业集团股份有限公司;批号:20130517;规格:100 mg/片);氢氯噻嗪对照品(中国药品生物制品检定所;批号:100309-201103;含量:99.4%);甲醇、乙腈、氯仿均为江苏汉邦公司色谱纯;水为自制超纯水;其他试剂均为分析纯[4]。
1.3 实验动物
健康家兔20只,雌雄兼用,体重为(2.0±0.2)kg,由辽宁省实验动物动物资源中心提供[5],许可证号:SCXK(辽)2014-0002。
2 结果
2.1 色谱条件
色谱柱:Phenomenex ΜP-ODSC18色谱柱(250×4.6 mm,5 μm);流动相:乙腈∶0.1%醋酸=25∶75(v/v);流速:1.0 ml/min;进样量:10 μl[6];柱温:35℃;检测波长250 nm。
2.2 溶液配制
2.2.1 ABA储备溶液的配制 精密称取ABA对照品10 mg,置于50 ml容量瓶中,用乙腈定容,得到浓度为200 μg/ml的ABA标准溶液,作为储备液[7]。
2.2.2 内标液的配制 精密称取氢氯噻嗪对照品约2 mg于10 ml容量瓶中,用乙腈溶解并定容,得到浓度为200 μg/ml的氢氯噻嗪储备液[8],用乙腈稀释,最后配得浓度为20 μg/ml的氢氯噻嗪溶液,作为内标液,置于4℃冰箱保存,备用。
2.2.3 空白血浆的制备 于家兔耳缘静脉采血1 ml,置于含0.1 ml肝素钠的离心管中,4000 r/min,离心10 min,将血浆取出,于-20℃冷冻层保存待测[9]。
2.3 血浆样品的处理方法
取200 μl的空白血浆于1.5 ml的EP管中,依次加入200 μl的氢氯噻嗪内标液(20 μg/ml)以及200 μl ABA标准溶液,涡旋30 s后,再依次加入 200 μl氯仿[10],800 μl甲醇后,涡旋振荡2 min,13 000 r/min,离心20 min,吸取1.0 ml的上清液于另一干净EP管中,40℃氮气仪下吹干,残渣用200 μl流动相溶解,精密进样10 μl后分析,记录色谱图。
2.4 方法学验证
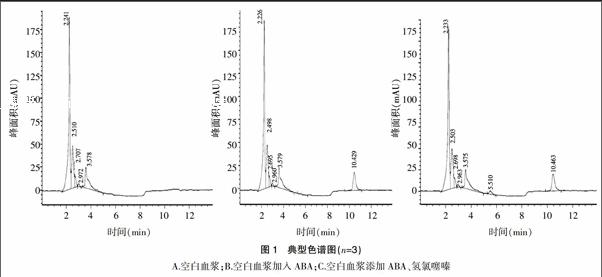
2.4.1 专属性考察 空白血浆,空白血浆添加ABA,空白血浆添加ABA、氢氯噻嗪,经处理后,进样分析;ABA、氢氯噻嗪的保留时间分别为10.463、5.510 min,内源性物质对ABA、氢氯噻嗪无干扰,结果见图1。
2.4.2 线性范围 用空白血浆稀释ABA储备液,得到67.5、134.5、269、537.5、1075、2150 μg/L ABA系列标准血浆样品。取各浓度标准血浆样品200 μl,按2.3项下进行操作[11],取10 μl进行反相HPLC分析,记录色谱图,ABA在67.5~2150 μg/L浓度范围内与峰面积呈良好线性关系。回归方程为Y=222.09X+85.664,r2=0.999。
2.4.3 回收率与精密度 配制低、中、高浓度分别为67.5、134.5、269、537.5、1075、2150 μg/L的ABA质控样品各5份,按照2.3项方法进行操作,得低、中、高浓度的日内RSD为3.01%~6.93%;日间RSD为3.27%~10.08%;相对回收率为86.67%~93.58%。
2.4.4 样品稳定性考察 取空白血浆,加入ABA对照品溶液,按2.3项下方法处理,将血样于4℃放置0、1、2、4、24 h,然后按反相HPLC条件测定,得到该浓度下ABA含量的RSD值为3.09%~10.75%。结果表明,兔子的血浆样品在24 h内基本稳定。
2.4.5 冻融稳定性考察 根据采集样品以及分析过程,同时考察低、中、高浓度(ABA血浆浓度分别为67.5、537.5、2150 μg/L的样品,各制备5份。按2.3项下方法处理后,反复冻融3次,然后按反相HPLC条件测定[12],得到该浓度下ABA含量的RSD值为3.14%~11.62%。结果表明在各种条件下样品稳定性良好。
2.5 药代动力学研究
2.5.1 实验动物 20只家兔(吉大实验动物中心),雌雄兼用,体重为(2.5±0.5)kg。将家兔置于清洁实验室中,给予标准饲料和饮用水,且控制室内温度为(22±1)℃,相对湿度为40%~50%。
2.5.2 给药方案与血样采集 将20只家兔分为两组,一组给予阿尼西坦普通片,一组给予阿尼西坦缓释片,禁食10 h后灌服2片阿尼西坦片[13](约相当于阿尼西坦主药200 mg),适量水冲服。4 h后统一进行喂食、饮水,此实验重复2个周期,每个周期中间间隔1周。普通片于及缓释片均于服药后10、20、30、40、120、160、240、360、540、720 min取血,每个时间点分别耳缘静脉取血1.5 ml,放于含0.1 ml肝素的离心管中,3000 r/min,离心10 min,将血浆取出放于-20℃冷冻层保存待测。
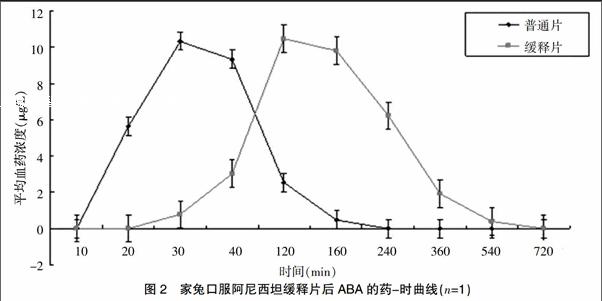
2.5.3 平均血药浓度-时间曲线 将冻存后的样品取出,按照2.3项下进行操作。分别测得普通片和缓释片的血药浓度,绘制两者的药-时曲线,结果见图2。
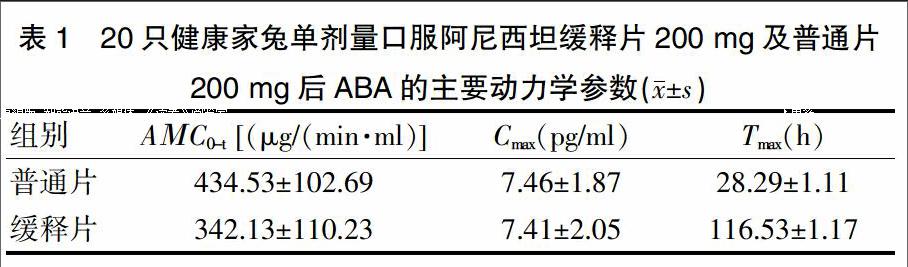
2.5.4 药代动力学参数 分别记录20只健康家兔单剂量口服阿尼西坦缓释片200 mg及普通片200 mg后ABA血药浓度值,采用3P97软件处理,其主要药代动力学参数见表1。
3 讨论
阿尼西坦口服进入人体后,很快代谢为主要代谢产物ABA,因此,阿尼西坦的血药浓度很低,难以准确测定[14],而ABA的血药浓度较高,稳定性好,便于测定。目前国外已有文献报道[15],采用反相HPLC法测定阿尼西坦及其代谢产物ABA含量,但样品预处理过程较复杂。本研究在此基础上,采用反相HPLC法对阿尼西坦缓释片活性代谢产物ABA的血药浓度进行测定,对实验条件及方法进行了改进和创新,直接采用甲醇∶氯仿(2∶8)两项配比的方法对血样进行一次性液液萃取,结果表明此种萃取方法的效果明显高于常规的单溶剂萃取法,大大提高了提取率,优化了提取方法。此外,本实验对不同内标物的选择进行了考察比对,结果发现以氢氯噻嗪作为内标,保留时间为5.510 min,与非那西丁、对羟甲基苯甲酸甲酯(JNB)等(保留时间均为9 min左右)比较,可有效缩短进样分析时间,利于大样本量待测物的分析,且可保证血中内源性杂质与ABA均可达到基线分离,互不影响[16]。
综上所述,本文建立的反相HPLC法操作简单,精密度高、重现性好,符合人体生物利用度实验要求,已成功应用于阿尼西坦的生物等效性研究,为进一步研究阿尼西坦在人体内的药代动学过程奠定了基础,具有可行性和可推广性。
[参考文献]
[1] 王红梅,曹玉瑗.阿尼西坦治疗老年脑器质性记忆障碍的临床观察[J].中国实用神经疾病杂志,2009,12(18):2-3.
[2] 吴松芝,伟忠民,刘茜,等.阿尼西坦胶囊人体药代动力学与生物等效性研究[J].南昌大学学报(医学版),2010, 50(2):365-369.
[3] 刘秀菊,张志清,杨秀岭,等.HPLC法测定大鼠血浆中奥拉西坦的浓度[J].中国药房,2012,21(5)403-404.
[4] 樊秦,许爱霞,陈宝英,等.阿尼西坦在老年痴呆患者体内的药动学[J].中国医院药学杂志,2001,25(5):400-402.
[5] 许晋星.HPLC法测定阿尼西坦分散片的有关物质[J].广东药学院学报,2009,12(4):512-514.
[6] 聂淑芳,刘辉,刘艳丽,等.几种亲水凝胶骨架材料相关性质的比较[J].药学学报,2011,46(3):96-101.
[7] 谢平,朱运贵,王峰,等.人血浆中阿尼西坦代谢物的HPLC-MS测定及药物动力学研究[J].中国医药工业杂志, 2011,9(6):481-486.
[8] 温慧娟,陈海增.新型缓释骨架片的研究进展[[J].黑龙江科技信息,2011,(29):17,109.
[9] 张志涛,赵怀清,李见春.茴拉西坦胶囊健康人体生物等效性与药代动力学研究[J].淮海医药,2007,25(1):1-4.
[10] 罗健,马虹英.高效液相色谱法测定人血浆中茴拉西坦活性代谢产物ABA及其在生物等效性研究中的应用[J].中南药学,2010,8(10),739-742.
[11] 刘海洲,刘爱云,高峰,等.渗透泵型控释片制备工艺研究进展[J].齐鲁药事,2008,27(8):486-487.
[12] 董晨东,刘建平,张文丽,等.阿替洛尔缓释微丸的制备及其大鼠体内药动学研究[J].药学与临床研究,2010, (3):231-232.
[13] 余超,邹梅娟,史一杰,等.酒石酸美托洛尔脉冲控释微丸的制备及Beagle犬体内药动学研究[J].中国药剂学杂志,2011,9(2):30-37.
[14] 杨晓的,陈儿同,周燕,等.微囊化技术在医学领域中的应用与进展[J].中国组织工程研究与临床康复,2010, 14(29):5848-5849.
[15] 陆彬.药物新剂型与新技术[M].2版.北京:人民卫生出版社,2005:436-445.
[16] 国家药典委员会.中国药典(一部)[M].北京:化学工业出版社,2010:附录ⅠD7.
(收稿日期:2015-09-07 本文编辑:许俊琴)
