10种含栀子中药制剂中栀子苷与西红花苷-Ⅰ的同时测定
2016-04-06张小琴汤晟凌吕伟旗温州医科大学附属第六医院丽水市人民医院药剂科浙江丽水323000
张小琴, 汤晟凌, 吕伟旗(温州医科大学附属第六医院,丽水市人民医院药剂科,浙江丽水323000)
10种含栀子中药制剂中栀子苷与西红花苷-Ⅰ的同时测定
张小琴, 汤晟凌*, 吕伟旗
(温州医科大学附属第六医院,丽水市人民医院药剂科,浙江丽水323000)
摘要:目的 采用HPLC法与一测多评法,同时测定10种含栀子中药制剂中栀子苷与西红花苷-Ⅰ的含有量。方法
制剂分析采用Ag1ient1200色谱柱;流动相为乙腈-0.1%磷酸水溶液,梯度洗脱;检测波长238 nm(0~20 min)、440 nm(20~30 min);柱温30℃。结果 HPLC图谱的峰形及分离度良好。以栀子苷为内标物,西红花苷-Ⅰ的相对校正因子为1.085(ISD=0.73%),其重现性不受色谱柱影响。结论 除清火栀麦片与小儿清热片外,其余8种含栀子中药制剂中栀子苷的含有量均符合药典标准。
关键词:中药制剂;栀子;栀子苷;西红花苷-Ⅰ;HPLC;一测多评
KEY W 0RDS:traditiona1Chinesemedicina1 preparations;Gardenia Jasminoides;geniposide;crocin-I;HPLC;quantitative ana1ysis ofmu1ti-components by sing1emarker(QAMS)
栀子是茜草科植物栀子Gardenia Jasminoides E1-1is的干燥成熟果实,性寒,味苦,归心、肺、三焦,具有泻火除烦、清热利湿、凉血解毒、消肿止痛等功效[1],是常用的大宗药材品种之一,临床用于热病心烦、黄疸尿赤、目赤肿痛、火毒疮疡等症。目前,市售含栀子中药制剂的种类繁多,其剂型包括散剂、片剂、丸剂、胶囊剂、注射水剂等,常见的有栀子金花丸、清火栀麦片、八正合剂、三子散、清开灵片等。
环烯醚萜苷及西红花苷是栀子的主要有效成分,其中栀子苷是环烯醚萜类的主要化合物。现代药理学研究表明,栀子苷具有保肝利胆、促进胰腺分泌、自由基损伤拮抗、保护神经细胞、抗菌消炎、降血糖与抗肿瘤等作用[2-5],而西红花苷具有降压、改善冠心病心绞痛导致血流变异常、抗血栓、保护血管内皮细胞、抗动脉粥样硬化、抗肿瘤、抗炎镇痛、清热利胆退黄与抗氧化等作用[6-10]。《中国药典》2010年版规定,含栀子中药制剂多以栀子苷含有量为栀子的质量标准,但对西红花苷暂无相关要求。由于西红花苷-Ⅰ是西红花苷类的主要化合物,而且活性显著[11-12],故本实验选取市售10种含栀子的中药制剂,建立同时测定其中栀子苷与西红花苷-Ⅰ的HPLC法与一测多评法,考察《中国药典》规定的栀子苷标准与西红花苷-Ⅰ含有量,为含其质量标准评价提供依据。
1 材料与方法
1.1 试验仪器与材料 Ag1ient1200高效液相色谱仪(美国Ag1ient公司);KQ5200DE数控超声清洗仪(昆山超声仪器有限公司);Mi11i-Q Academic超纯水仪(美国Mi11ipore公司);DGG-9070型电热恒温鼓风干燥箱(上海森信实验仪器有限公司);FA1004B电子天平(上海精密科学仪器有限公司)。
栀子苷对照品(四川省维克奇生物科技有限公司,批号116816);西红花苷-Ⅰ对照品(纯度>97%,成都曼斯特生物科技有限公司,批号MUST-12071108)。乙腈为色谱纯(美国Tedia公司);水为去离子水;其他试剂均为分析纯。市售含栀子中药制剂共10种,均为《中国药典》2010年版收录的成方制剂[1],具体信息见表1。
1.2 实验方法
1.2.1 色谱条件 Ag1igent ec1ipse XDB-C18、Thermo Syncronis C18、Syncronis C18色谱柱(4.6 mm× 250 mm,5 μm);流动相为乙腈(A)-0.1%磷酸水溶液(B),梯度洗脱(0 min,1∶9;15 min,2∶8;30 min,3∶7);体积流量1.0 mL/min;检测波长238 nm(0~20 min)、440 nm(20~30 min);柱温30℃;进样量50 μL。
1.2.2 溶液制备
1.2.2.1 对照品溶液制备 精密称取栀子苷与西红花苷-Ⅰ对照品适量,置于10 mL棕色量瓶中,甲醇溶解并定容至刻度,配制成含0.208 mg/mL栀子苷与0.032 mg/mL西红花苷-Ⅰ的混合标准品溶液,避光保存,备用。
1.2.2.2 供试品溶液制备 精密称取研磨至粉状的固体样品0.2 g(精密吸取液体样品0.2 mL),置于50 mL锥形瓶中,加入75%甲醇溶液25 mL,25℃下超声提取1 h,抽滤。吸取5 mL,75%甲醇定容至10 mL量瓶中,摇匀,0.45 μm微孔滤膜滤过,即得。
1.2.3 线性关系考察 精密吸取栀子苷标准品溶液0.25、0.5、1.0、2.0、4.0 mL,西红花苷-Ⅰ标准品溶液0.1、0.3、0.6、1.2、2.4 mL,用75%甲醇定容至10 mL量瓶中,在“1.2.1”项色谱条件下测定。以栀子苷与西红花苷-Ⅰ标准品溶液的质量浓度为纵坐标(Y),峰面积为横坐标(X)绘制标准曲线,计算出两者的线性范围分别为5.20~83.2 μg/mL和0.32~7.68 μg/mL,回归方程以及相关系数分别为Y=336.85X-290.77,R2=0.999 0;Y=149.76X-89.5,R2=0.999 2。1.2.4 稳定性试验 取同一清开灵片样品,按“1.2.2.2”项下方法制备供试品溶液,置于以下条件保存。(1)高温度试验:40℃,避光;(2)高湿度试验:室温,相对湿度(90±5)%,避光;(3)强光照射试验:室温,(5 000±500)Lux光照强度下照射。分别于0、1、2、4、6、8、12、24 h进样,在“1.2.1”项色谱条件下测定相应峰面积,计算出以上条件下栀子苷与西红花苷-Ⅰ峰面积的ISD值(n=8)分别为0.89%、1.83%;1.21%、2.08%;10.89%、15.08%。结果表明,供试品溶液在高湿度与40℃避光条件下24 h内稳定,而在强光照射条件下不稳定,故本实验样品均在室温24 h内避光条件下测定含有量。

表1 制剂基本信息Tab.1 Basic information of the preparations
1.2.5 精密度试验 取栀子苷标准品溶液,在“1.2.1”项色谱条件下连续进样6次,测得栀子苷峰面积ISD值为1.99%,西红花苷-Ⅰ峰面积ISD值为2.08%,表明仪器精密度良好。
1.2.6 重复性试验 取同一清开灵片样品6份,按“1.2.2.2”项下方法制备供试品溶液,在“1.2.1”项色谱条件下测定栀子苷与西红花苷-Ⅰ含有量,得前者平均含有量为0.368%,ISD值为2.35%,后者平均含有量为0.023 1%,ISD值为0.58%,表明该方法重复性良好。
1.2.7 加样回收率试验 精密称取含有量已知的三子散适量,精密加入栀子苷与西红花苷-Ⅰ对照品,配制成供试品溶液进行测定,计算公式为加样回收率=(H3-H1)/H2×100%(H1为样品中被测成分的含有量,H2为加入对照品的含有量,H3为实际测得含有量)。结果,栀子苷实际测得质量浓度在11.98~12.08 μg/mL之间,而西红花苷-Ⅰ在1.267~1.299 μg/mL之间,均在各自线性范围内。同时,前者平均回收率为99.41%,ISD值为0.86%(n=6),而后者平均回收率为100.01%,ISD值为0.76%(n=6),具体见表2。

表2 加样回收率试验结果(n=6)Tab.2 Results of recovery tests(n=6)
1.2.8 样品含有量测定 精密称取研磨至粉状的固体样品0.2 g(精密吸取液体样品0.2 mL),置于50 mL带塞锥形瓶中,按“1.2.2.2”项下方法制备供试品溶液,在“1.2.1”项色谱条件下,对10种中药制剂样品中栀子苷与西红花苷-Ⅰ的含有量进行测定,重复3次。
1.2.9 相对校正因子的测定 以栀子苷为内标物,测定西红花苷-Ⅰ的相对校正因子,计算公式为fks=(Wk×A's)/(Ws×A'k)[13-14](W为进样量,A'为峰面积,s为栀子苷,k为西红花苷-Ⅰ)。结果,西红花苷-Ⅰ的平均校正因子为1.085,ISD值为0.73%,详见表3。

表3 西红花苷-Ⅰ的相对校正因子Tab.3 Relative correction factors of crocin-I
2 结果与分析
2.1 中药制剂中栀子苷与西红苷-I含有量的HPLC法优化 在文献[12,15-16]的基础上,对这两种成分的提取方法进行优化,分别考察了50%、75%、85%甲醇,40、60、80 min提取时间,20、25、30、35℃提取温度下两者的提取效率。结果显示,市售中药制剂中栀子苷与西红花苷-Ⅰ在75%甲醇、25℃的条件下,超声提取1 h即可被完全提取,而且操作简便,杂质少。此外,还考察了乙腈-水、乙腈-0.2%磷酸水、乙腈-0.1%磷酸水流动相与梯度程序,发现两者在乙腈(A)-0.1%磷酸水(B)流动相下梯度洗脱(0 min,1∶9;15 min,2∶8;30 min,3∶7)时,出峰效果与分离度最好,具体见图1。
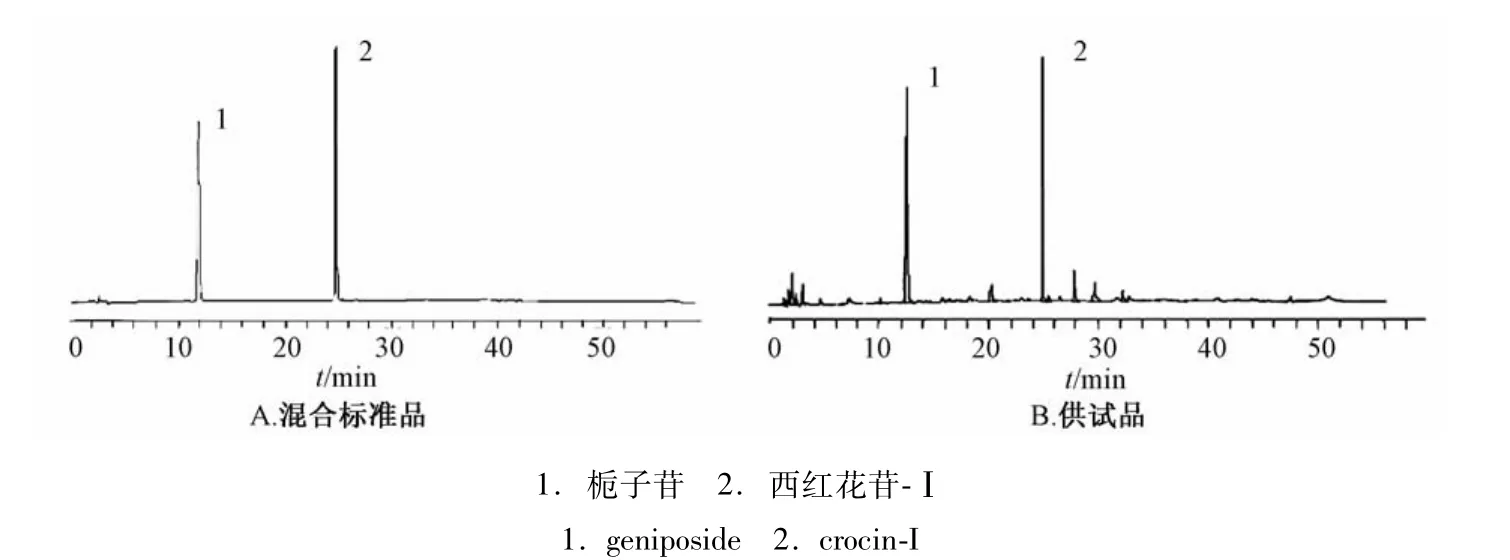
图1 高效液相色谱图Fig.1 HPLC chromatograms
2.2 制剂中栀子苷含有量比较 10种含栀子的中药制剂均为2010年版《中国药典》收录的成方制剂,其质量标准规定均包括栀子苷含有量。在本实验优化的HPLC方法下,10种中药制剂中栀子苷的含有量存在差异,见表4。其中,以三子散为最高,达0.781%,而清开灵注射液最低,仅0.058%,平均0.278%。另外,除清火栀麦片与小儿清热片药典无商品规格,故无法等量换算栀子苷标准外,其余8种制剂中栀子苷含有量均达到药典标准。

表4 制剂中栀子苷与西红花苷-Ⅰ的含有量Tab.4 Contents of geniposide and crocin-I in the preparations
2.3 制剂中西红花苷-Ⅰ含有量比较 10种中药制剂中西红花苷-Ⅰ的含有量存在差异,其中以三子散为最高,达0.063 8%,而清火栀麦片最低,仅0.004 2%,平均0.027 2%。为方便与本实验结果比较,根据《中国药典》2010年版规定的栀子苷标准,将其换算成百分含有量,换算公式为标准百分含有量=栀子苷限度值/单位规格质量× 100%,具体见表4。
2.4 一测多评法与HPLC法结果比较 根据西红花苷-Ⅰ的相对校对因子,用一测多评法测得供试样品中西红花苷-Ⅰ的含有量,见表4。由表可知,其平均含有量为0.026 8%,与HPLC法(0.027 2%)无显著性差异(P>0.05),表明一测多评法可用于中药制剂中的多指标成分的质量评价,具有较好的可信度。
3 结论与讨论
长期以来,中成药的质量大多以单一指标进行控制,难以真正体现中药的多效性和整体性。中药多靶点的作用特点要求对其进行多成分质量控制,因此相关模式应运而生,但商品化对照品的供不应求和多指标控制高昂的检测费用限制了其在实际生产、科研和监管领域的应用,而一测多评法为解决该矛盾提供了新思路,但是中药复方制剂的成分种类比单味中药饮片更多、更复杂,其应用难度更大[17-20]。因此,检测波长的确定、内参物的选择、色谱峰的定位、校正因子的重现性等因素都影响着该方法的可靠性。
栀子苷与西红花苷-Ⅰ是含栀子中药制剂中的主要化学成分,由于两者保留时间较近,故为本实验一测多评法的建立提供了良好的应用基础。在内标物的选择上,由于栀子苷含有量相对较高,分离度与稳定性较好,并且其标准品易得,价格低廉,而西红花苷对照品价格昂贵,故选择栀子苷为内标物。分别两者色谱峰进行全波长扫描,发现前者的最大吸收波长为238 nm,而后者为440 nm,故选择238 nm与440 nm为栀子苷与西红花苷-Ⅰ的检测波长。当仅使用栀子苷对照品时,鉴于西红花苷色谱峰与其色谱峰的保留时间较近,因此选用相对保留时间来定位目标色谱峰。分别用Agi1ent ec1ipse XDB-C18、Thermo Syncronis C18、Syncronis C183种色谱柱考察校正因子的重现性,发现不同色谱柱对其影响较小(ISD<3.0%),重复性较好,由于实验条件所限,故未对不同色谱仪考察校正因子重复性,将在后续工作中予以补充。
同时,本实验考察了甲醇浓度、提取时间、流动相等因素对含有量测定的影响。结果表明,栀子苷与西红花苷-Ⅰ在75%甲醇、25℃条件下超声提取1 h即可被完全提取,在乙腈(A)-0.1%磷酸水(B)流动相下梯度洗脱(0 min,1∶9;15 min,2∶8;30 min,3∶7)时,出峰效果与分离度最好。而且,一测多评法与HPLC法的分析结果无明显差异,均可用于同时测定这两种成分的含有量,此外在西红花苷标准品稀缺时,可优先选用一测多评法。
2010年版《中国药典》收录的成方制剂中,含栀子的中药制剂就有数十种之多,其中以栀子为主要成分,并规定栀子苷含有量标准的也有十余种,但均无西红花苷标准。本实验选取市售10种含栀子的中药制剂,建立一测多评法与HPLC法同时测得其中栀子苷与西红花苷-Ⅰ的含有量,可为含该制剂的质量评价提供参考依据。同时,比较了10种制剂中这两种成分的含有量,发现除清火栀麦片与小儿清热片在2010年版《中国药典》中无商品规格,无法等量换算栀子苷标准外,其余8种制剂栀子苷含有量均达到药典标准。因此,建议2015年版《中国药典》完善清火栀麦片与小儿清热片的“商品规格“一栏,同时在含有量测定指标中考虑增加西红花苷类成分。
参考文献:
[1] 国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010.
[2] 姚冬冬,舒 娈,杨 蕾,等.栀子及其活性成分栀子苷防治糖尿病作用机制研究进展[J].中国中药杂志,2014,39(8):1368-1373.
[3] 师永清,师永花.HPLC同时测定牛黄清胃丸中栀子苷和黄芩苷[J].中国实验方剂学杂志,2011,17(11):86-88.
[4] 王志超,杨小龙,张 珂,等.栀子苷药理作用的研究进展[J].河南科技大学学报:医学版,2012,30(2):159-160.
[5] 颜静恩,李晚忱,吕秋军,等.栀子苷的降糖作用和对PPAIγ受体的激活[J].四川农业大学学报,2007,25 (4):415-418.
[6] 朱 波,施林妹,徐象华,等.不同遮盖方式对番红花生长发育的影响[J].江苏农业科学,2013,41(8):232-233.
[7] 刘 瑛,古天明,周 红.西红花苷类成分药理作用研究概况[J].成都大学学报:自然科学版,2008,27(1):16-19.
[8] 绪广林,余书勤,龚祝南,等.西红花苷对大鼠实验性高脂血症的影响及其机制研究[J].中国中药杂志,2005,30(5):369-372.
[9] 侯金燕,罗 琳,窦志华,等.HPLC-DAD测定茵陈蒿汤中儿茶素、绿原酸、西红花苷I、西红花苷Ⅱ的含量[J].中国实验方剂学杂志,2015,21(6):48-51.
[10] 张晓岩,喻 静,张先钧,等.西红花苷-1对急性低氧条件下大鼠学习记忆及海马SIIT1表达的影响[J].中草药,2013,44(10):1314-1317.
[11] 施林妹,徐象华,朱 波,等.西红花主要活性成分含量变异规律[J].中国实验方剂学杂志,2014,20(13):113-116.
[12] 罗光明,陈 岩,李 霞,等.不同居群品系栀子中栀子苷和西红花苷-1含量的比较研究[J].中药材,2010,33 (9):1376-1378.
[13] 张 勇,张 玲,谢晓梅.一测多评法同时测定木瓜中2种常见三萜酸[J].中成药,2013,35(4):770-773.
[14] 刘 圆,魏惠珍,龚建平,等.一测多评法测定健脾丸中4种黄酮类成分[J].中成药,2015,37(5):995-999.
[15] 付建武,彭 红,周玉春,等.高效液相色谱波长转换法测定西红花苷-1和栀子苷的含量[J].时珍国医国药,2009,20(12):2939-2940.
[16] 石凤鸣,王文君,陈 雏,等.栀子指纹图谱及不同生长期西红花苷和栀子苷含量的研究[J].时珍国医国药,2011,22(8):1874-1876.
[17] 冯伟红,杨 菲,王智民,等.一测多评法与外标法测定双黄连制剂中黄酮类成分含量的比较分析[J].中国药学杂志,2012,47(20):1665-1669.
[18] 高慧敏,宋宗华,王智民,等.适合中药特点的质量评价模式—QAMS研究概述[J].中国中药杂志,2012,37 (4):405-416.
[19] 赵 倩,冯伟红,张启伟,等.“一测多评”法用于栀子金花丸多成分含量测定的可行性研究[J].中国中药杂志,2014,39(10):1826-1833.
[20] 刘志辉,顾 玮,常星洁,等.“一测多评”法测定麦贞花颗粒中不同类型成分的含有量[J].中成药,2012,34 (12):2342-2347.
Simultaneous determ ination of geniposide and crocin-I in ten traditional Chinese medicinal preparations containing Gardenia jasm inoides
ZHANG Xiao-qin, TANG Cheng-1ing*, LVWei-qi
(The Siχth Hospital Affiliated to Wenzhou Medical University;Department of Pharmacy,Lishui People’s Hospital,Lishui323OOO,China)
ABSTRACT:AIM To simu1taneous1y determine the contents of geniposide and crocin-I in ten traditiona1Chi-book=570,ebook=104nesemedicina1preparations containing Gardenia Jasminoides by HPLC and quantitative ana1ysis ofmu1ti-components by sing1emarker(QAMS).METH0DS The ana1yses of preparations were conducted on Ag1ient 1200 co1umn,mobi1e phase was acetonitri1e-0.1% phosphorus acid in a gradient e1ution manner,detection wave1engths were set at238 nm(0 -20 min)and 440 nm(20 -30 min),and co1umn temperature wasmaintained at 30℃.RESULTS Manifesting good peaks and reso1utions of HPLC chromatograms,crocin-Idisp1ayed its re1ative correction factor of1.085(ISD=0.73%)with geniposide as the interna1standard,whose reproducibi1itywas independentof co1umns.C0NCLUSI0N Except for Qinghuo Zhimai Tab1ets and Xiao’er Qingre Tab1ets,another eight traditiona1Chinesemedicina1preparations containing Gardenia Jasminoides accord with Chinese Pharmacopoeia criteria.
*通信作者:汤晟凌(1977—),女,副主任药师,从事中药新药开发与临床药学研究。E-mai1:aurora0119@163.com
作者简介:张小琴,女,主管药师,从事医院制剂与中成药活性成分研究。E-mai1:1stracy1027@163.com
收稿日期:2015-09-08
doi:10.3969/j.issn.1001-1528.2016.03.019
中图分类号:I 927.2
文献标志码:A
文章编号:1001-1528(2016)03-0569-06
