离子电流对心脏组织中螺旋波的影响
2016-01-25陈绍英袁国勇
陈绍英 袁国勇
(1.呼伦贝尔学院学报编辑部 内蒙古 海拉尔区 021008;2.河北师范大学物理科学与信息工程学院 河北 石家庄 050016)
引言
心脏对人体来说是极其重要的器官,很长的一段时间内,西方国家尤其在美国患心脏病的人数不断增加,因心脏病发作而死亡的人数比同时期患其他疾病死亡的人数多很多。但由于伦理道德的限制和人体心脏组织三维结构的复杂性,对心脏结构、功能的实验研究和临床研究十分困难,通常人们只能借助心电图、导管介入技术、心脏彩超等仪器来进行,给研究工作带来极大的不便。因此,人们基于心脏构造的基本性质和工作特点,提出了不同种类的心脏动力学模型,在用这些模型的模拟研究中人们发现了很多心脏组织的新现象。如可激发心肌组织螺旋波的产生,螺旋波破碎导致心颤现象,动作电位时程(action potential duration,简称 APD)恢复曲线理论[1]等,从而能够方便地模拟研究心脏中出现的多种现象。心脏的正常节律来源于窦房结附近节律性最高并能自动激发的 P细胞,其控制心脏的正常节律。心脏的心肌、蒲氏纤维等也可能产生节律,这种异位节律跟细胞膜内外的动作电位有关,对心脏的正常节律要产生一定的影响。另外,心脏内部还存在多种随机因素亦会影响心脏的正常节律,通常这些异位起搏点的节律会被窦房结的节律所湮灭。相反,一般某些心脏疾病的产生,往往是异位起搏点产生的节律控制了心脏正常的节律。迄今为止人们认识到,当心脏电信号中出现螺旋波时,心脏将出现心室心动过速(室速)[2],当螺旋波破碎而形成时空混沌时,将出现心室纤维性颤动(室颤)[3]。室颤是一种极其严重的心律失常。发生室颤时,心脏的电活动完全失去同步性而趋于紊乱,导致心脏不能泵血、脉搏和心音消失、心脏正常供血功能丧失,具有突发性和抢救难度大的特点,室颤在极短的时间内可能夺去人的生命。至今,人们对心脏中螺旋波产生、破碎机理还不十分清楚,临床上使用电除颤和药物消除方法还存在一定的副作用。因此,人们希望通过对螺旋波动力学研究找到更好的去除螺旋波方法。这样,对螺旋波和时空混沌控制方法研究成为当今数学、物理学、医学工作者研究的热点。那么要想降低心脏病的病发率,首先应该在离子通道的水平上了解心律失常和室颤发生的基本机制以及单个心肌细胞的动作电位(action potential, AP)的变化性质。
1.描述心肌组织的离子模型
长此以来,人们对心脏功能的研究从未停止过。但在实验上研究心脏的成本极高,这就迫切需要建立心脏的动力学模型以降低研究成本,提高研究效率。由于计算机仿真技术的快速发展,模拟心肌组织的电生理活动的想法得以逐步实现。目前用于研究心肌组织模型主要有两类:一类是离子通道模型,另一类是FHN模型。离子模型中由于参量较多,计算比较复杂,所以在研究心脏组织问题时人们多用简易的FHN模型。FHN模型,是R.Fitz Hugh和J.S.Nagumo二人在20世纪五六十年代分别提出的[4,5],它是用唯象的方法描述跨细胞膜的离子电流的总和。这类模型通过简单的实验数据拟合就可模拟可激发性、APD恢复曲线,复极期等心肌组织的基本性质。该类模型的特点是理论分析简单,模型维数低,便于大规模数值计算。但存在不能分析离子电流变化对动作电位的影响、离子通道药物对某种离子电流的作用等缺点。因此,对于心脏中更复杂的现象研究,还是用离子模型。上世纪80年代以来,随着单通道记录技术和单细胞的发展,细胞内外的环境得到控制,而且从单通道记录的数据奠定了膜离子电流和定量描述动力学的基础。哺乳动物的心脏是一个很复杂的系统,心脏细胞内有细胞液和各种离子,随着心肌细胞的活动以及新陈代谢的进行,由于三磷酸腺苷(ATP)和离子通道的作用,这些离子可以发生转移而产电流,这样在心肌细胞的生命活动中就有了膜内外电位的变化,我们将其称之为生物电(bioelectricity),由于心肌细胞的这种电现象主要发生在细胞膜的内外两侧,我们又把这种电位称之为跨膜电位(trans membrane potential)。当心肌细胞在没受到外界刺激的时候,细胞处于静息状态,这时候细胞膜两侧的电位差处于稳定值,我们称之为静息电位(resting potential)也可以称为跨膜静息电位。这种电位的值在一般情况是内负外正。人和哺乳类动物心室肌细胞的静息电位约为-90mV,在实验或者临床上,我们可根据动作电位的出现与否和引起兴奋的强度來判断兴奋性的有无和大小,动作电位是引起肌肉收缩、神经递质释放等生理过程的先导。心肌细胞属于可激发细胞,当可激发细胞受到外部电刺激时,就会使细胞去极化,膜电位由负值变正或者是接近与零。去极化是一个很快的过程,紧随其后的是较慢的复极化过程,这个过程是将膜电位恢复到它静息态的值,一完整的去极化和复极化的循环叫做一个动作电位。与骨骼肌和神经细胞的动作电位相比心室肌细胞的动作电位与其有明显的不同。例如,骨骼肌细胞动作电位的时程很短,仅能持续几个毫秒,它的复极化和去极化速度相近,动作电位曲线表现为上升支和下降支基本对称的尖锋状。心室肌细胞的动作电位复极化过程比较复杂是其主要特征,持续时间也很长,并且动作电位的上升支和下降支呈现不对称。一般将心室肌细胞动作电位分为五个分期,即0期,1期,2期,3期,4期。其中0期是去极过程,其余是复极化过程。图 1为心脏模型中一个去极和复极过程中的动作电位[6]。动作电位是实现神经传导和肌肉收缩的生理甚础,也是可兴奋细胞产生、传导的客观标志。动作电位的形成和细胞膜上离子通道幵关紧密相关。对于初始刺激,如果达到了阈值,就能够引起一系列离子通道的或幵启或关闭,不同离子电流在膜内外交换,从而形成离子电流的流动,改变了细胞的跨膜电位,同时又引起临近位置上细胞膜电位改变,把兴奋沿着一定的路径传导下去。图 2是单个离子通道的通道电流[7],由图可见离子通道的开放与关闭迅速且随机。但不同通道都有其特有的平均开放时间,并且在其平均开放时间上下波动。

图1 一个动作电位曲线(引自[6])
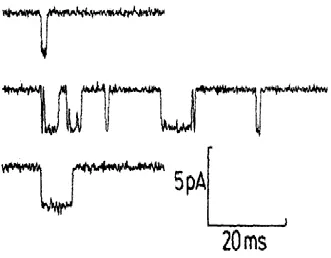
图2 膜片钳技术记录的单个离子通道电流的三条轨迹分别对应的膜电压(引自[7])
心肌细胞的电学行为是由通过离子通道的电流决定的,因为在细胞尺度上看,带电离子只能通过离子通道进出细胞。这样人们把离子通道看成一个有一定电阻的电流通道,因此把细胞膜等效成一个带电阻的“电容器”。这个“电容器”和可变电阻、电池并联在一起正好能够体现出不同的离子电流和泵的作用[6,8,9],如图3所示。L-R 相I心脏模型是1991 年Luo和Rudy提出的刻画心室细胞膜间电压变化规律的模型[10]。由于该模型较好的反映心肌细胞的动力学行为,被广泛应用于数值模拟研究中。模型示意图如图 4所示,它含有6个膜电流,7个门变量,单个心室肌细胞动作电位模型可以用如下方程表示:
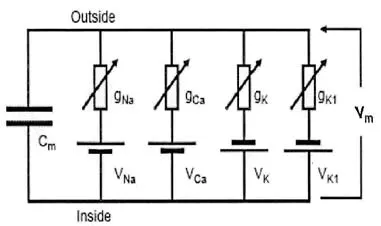
图3 心脏细胞膜的简单等效电路(引自文献[8])

图4 L-R 相I模模型示意图(引自[10])
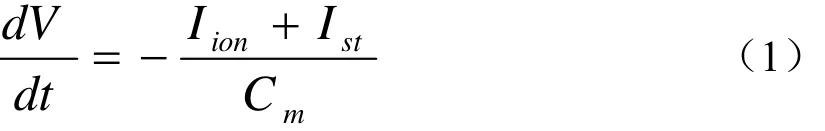
对方程(1)求解就可以得到单个心肌细胞的去极、复极的动力学演化过程。由于该模型能较好地反映心肌细胞的动力学行为,因此在心脏动力学的研究中被经常使用。式中,V表示心肌细胞膜间电压,单位:mV;mC是理想化的膜间电容,单位:;t表示时间,单位:ms;是所有跨膜离子电流的总和,单位:;Ist是外部驱动电流,如无外部驱动电流,这一项为零。细胞动作电位要受离子电流的影响,它是生物电信号传输的一个关键因素。在心肌细胞的现象研究中,通常将细胞的离子流分为内向离子电流和外离子电流两种。在LuoRudy91模型中,Iion由六种离子电流组成:
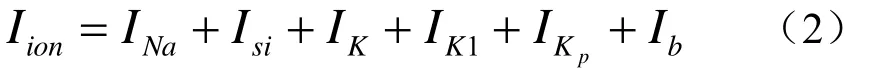
在这些电流表达式中和E分别代表相应离子电流的最大电导率和能斯特平衡电位,m,h,j,d,f,X,X1,Kp,K1∞都是无量纲的门变量,描述相应的离子通道打开和关闭。门变量满足下列类型的微分方程:

其中y是门变量,αy,βy是跟电压有关的函数。
这六种离子电流的主要作用是:在细胞的去极化过程中,INa,IK1,起主要作用;在细胞处于激发态上的不应期时Isi,IK起主要作用,起辅助作用;在细胞恢复到静息态过程中IK1起主要作用,Isi,IK起辅助作用;Ib在细胞的整个生理过程中只是随着模电压的变化而变化;只在细胞去极化的一段很小的时间内出现很大的电流,其它时间都为零。
心脏的组织模型可以认为是由大量细胞通过缝隙连接而成,外界刺激产生的兴奋性能够在心肌细胞之间传播,形成激发波。动作电位在匀质组织中的传导一般用反应扩散方程形式描述,即在细胞动作电位方程中根据组织的维数不同加入相应的空间扩散项[11]:

其中,D是与细胞间缝隙连接有关的扩散系数,
2.心肌细胞的几种主要离子电流对心脏中螺旋波和时空混沌的影响
以Luo Rudy91 模型为基础,人们对离子电流对心肌组织的影响进行了较深入的探讨,得到一些有益的结论。许多研究结果表明,心律失常本质是细胞膜中离子通道的特性发生了变化,因此对心肌细胞膜离子通道特性变化的研究可进一步加深人们对室颤等心律失常机理的认识。
2.1 钙离子电流对心脏螺旋波和时空混沌的影响
很多重要的生理过程的都是由作为细胞信使之一的钙离子来控制的,例如神经传导、细胞收缩、基因表达、荷尔蒙分泌及细胞的生长、凋亡等[12,13]。哺乳动物从精子与卵子的结合触发生命信息开始,到细胞的死亡,钙离子几乎参与控制生命体中的一切活动,为心脏的正常跳动提供基本生理上的保障。钙离子从心肌细胞的肌质网释放到细胞基质中的过程受钙致钙释放机理调控,此过程通过心肌细胞的肌质网上的钙通道—兰尼定受体完成。心肌细胞中的钙释放具有在时空上具有不连续性,钙释放以钙火花的形式呈现,并且在细胞质低钙浓度下,其在时空上是独立随机分布的。由于钙致钙释放机理的作用,当细胞质局域浓度变高时,几个近邻的钙火花在相近的时间出现时,释放的钙离子可能扩散到下一个释放位点并引起此位点的释放,当这一过程连续发生时就形成由钙火花组成的具有跳跃式波前的钙波。因此,钙火花和钙波是心肌细胞中钙离子表现出的两种基本形式。单个钙通道分子的生理学研究自1993年发现钙火花现象以来,已取得了很多的成果[14,15],与此对照研究进展有些相对滞后的是心肌细胞中钙波的动力学行为的研究,特别是由钙火花如何形成钙波,以及钙波在钙火花干扰作用下如何演变过程的研究,这个过程同时也是生理系统中微观机理到宏观机理的转变过程,它对深刻理解从微观的生理现象到宏观的生理过程是十分有益的。
研究表明,心脏中的可激发波的稳定性与心脏心肌细胞的APD恢复曲线的斜率有关[16]。心脏组织中的钙离子电流的大小直接影响着螺旋波的稳定性。通过有效减少钙离子电流的大小,可以有效缩短心肌细胞的动作电位持续时间,形成较整齐的APD序列,并能明显地降低APD恢复曲线的斜率,从而有效地增加了心脏组织螺旋波的稳定性。减弱钙离子电流的幅度不同,则APD恢复曲线的斜率减小的幅度也不同,进而造成心脏组织中的螺旋波稳定性的不同。文献[17]也指出,如果在取钠离子电导为恒量,钙离子电导为变量,可得到随着钙离子电导增加,螺旋波波头轨迹所占面积逐渐增大,图形也更趋于不规则化。从环长(CL )Poincare散点图来看,随着钙离子电导的增加,散点图所占面积逐渐变大,CL值主要集中部位的值也更大。证明了钙离子电导的增加,增加了组织的动态不稳定程度,螺旋波状态也更不稳定。但如钙离子电导确定情形下,钠离子电导增加,可增强螺旋波的稳定性,因此,可认为组织兴奋程度提高,能提高心脏系统的稳定性。当然,对如何控制或消除心脏中螺旋波和时空混沌,还没有一个统一的控制方法,人们通过不同角度做了多方面探索和尝试。例如有的采取在钙离子通道上应用激动剂提高钙离子内流,有的采用钙离子通道阻滞剂方式等来抑制心脏组织中螺旋波和时空混沌。
在医学临床上一般把黄连素(Berberline,简称BR)等作为钙离子通道激动剂来提高钙离子内流,一般只要黄连素浓度达到 1 0-5mol /L就能使钙离子流增大近一倍,这充分表明钙离子通道对黄连素是比较敏感的。如果在此之后加入异博定,BR使钙离子通道开放的作用会立即消失[18]。因此,人们提出通过提高慢速内行钙离子通道最大电导率,来控制心肌组织的室和室颤。在文献[19]中研究表明,虽然当钙离子电流最大电导率时,系统螺旋波的破碎进入混沌状态,但当把钙离子通道最大电导率提高到足够大时,即使介质中存在外行钾离子电流的最大电导率不均匀情况,该方法也能有效抑制螺旋波和时空混沌。需要注意的是根据人体的实际,增大是有一个限度的。因为钙离子电导率过大会产生钙离子流严重超载会导致其他严重的病变发生。因此,控制中使用选择的最大钙离子电导率的上限需要通过实验来选定。最好的钙离子通道激动剂应是短效而且敏感:既可快速提高钙离子流,又能药效持续时间短暂,使细胞能很快回到正常态,进而避免钙离子流严重超载带来的不利影响。其控制的基本机理是增大电导率系统出现早期后除极化现象,对系统动作电位时程产生影响。这种控制方式控制时间很短,在临床上抢救病人和心脏复苏有重要实际意义。
对钙离子通道人们也采用通道阻滞剂来控制螺旋波和时空混沌,但只能稳定螺旋波,不能消除螺旋波和时空混沌,效果不是很好,而且长期使用还会破坏心肌组织离子平衡,给病人治疗带来副作用,甚至产生室颤[20,21]。对于使用钙离子通道阻滞剂单纯降低钙离子流的最大电导率不能达到控制目的,肖向华等提出了用钙离子阻滞剂按行波方式调节钙电导率的方法来消除心脏中的螺旋波和时空混沌[22]。在恰当选择控制参数下,通过数值模拟发现,螺旋波和时空混沌都能有效被抑制。但这种控制实现的前提是能够在实际中找到一种起效快但又短效的钙离子阻滞剂。这样的药物如果存在,可借助临床上心导管技术加以实现。这种抑制室颤方法比较安全,因为用钠离子和钾离子通道阻滞剂抑制室颤如处理不当,将会影响心脏的起搏。在控制过程中观察到时空混沌转变成螺旋波的现象,说明控制螺旋波和控制时空混沌的机制相同。上述控制方法能够实现基于以下两方面:(1)减小钙电导率有效提高了介质的可激发性,使得螺旋波更稳定,状态之间可以转换;(2)对钙电导率实施行波调制,相当于给螺旋波波头施加运动的力,该力大小与介质分布的不均匀性和波峰曲率有关。
2.2 钾离子电流对心脏螺旋波和时空混沌的影响
1977 年,通过刺激提高兔子的心房搏动频率实验,Kunze 发现了心肌细胞外钾离子浓度延迟恢复现象 (迟滞现象)。心脏中发生的很多现象在一定条件下都能产生依赖频率的迟滞现象,弄懂这些迟滞现象对心脏螺旋波有何影响十分必要。数值模拟实验表明细胞外钾离子浓度延迟恢复对螺旋波有一定的影响[23]。在螺旋波态下,细胞外钾离子浓度延迟恢复会导致细胞外钾离子浓度出现周期振荡,其振荡周期和振幅随延迟恢复时间的增加而增加,进而导致出现呼吸螺旋波、多螺旋波共存、螺旋波做 Lévy[24]飞行式漫游、螺旋波通过不同方式消失等现象,这些模拟结果与实验中得到结果一致。在细胞外钾离子浓度周期振荡下,螺旋波或做均匀、或做非均匀的无规则的漫游。当控制参数选取合适时,如果细胞外钾离子浓度能升到某一转变值时,螺旋波和时空混沌都会消失。螺旋波消失的主要原因是螺旋波漫游或漂移出系统形成,时空混沌消失是因为时空混沌转变成螺旋波态,然后漂移出系统或者是直接消失。在心肌缺血、缺氧时,细胞外钾离子浓度可以在短时间内从较低值上升到导致螺旋波或时空混沌消失的值。因此,细胞外钾离子浓度延迟恢复现象可以帮助我们理解心脏中常见的交替现象和螺旋波的自动消失现象,并利用螺旋波消失机理治疗心脏病。
钾离子通道还对心肌细胞的复极化过程有着重要的影响,从而影响心肌细胞的功能[25]。研究发现,当心肌细胞的复极化过程被干扰,有可能导致心律失常的出现。以LR91模型为基础人们提出了通过限制钾离子电流最大值来控制螺旋波和时空混沌的思想。结果表明:当设定恰当目标电流和限制幅度后,限制钾离子总电流能有效抑制螺旋波和时空混沌。在此控制过程中,含时和不含时外行钾离子电流非常重要,两者之一如不被抑制将会增大抑制螺旋波和时空混沌难度,甚至控制失败。这种控制的机理是显著地延长了心肌细胞的有效不应期,导致螺旋波和时空混沌不能维持而湮灭。
3.联合通道控制方法来抑制心脏组织中的螺旋波和时空混沌
心肌细胞的钙通道和钾通道的性质对心律失常有重要影响,因此,人们对用钙通道和钾通道控制系统的螺旋波和时空混沌分别进行了探讨。文献[26]研究得到:将钙通道阻滞剂注入心肌组织中,结果表明单独抑制钙通道并不能从根本上消除螺旋波和有效除颤。文献[27]中也指出,阻滞钾通道将延长二维异质性组织的易损窗,使系统不稳定性增加,增加了时空混沌的控制难度。已有的研究知道单独使用钙通道激动剂抑制螺旋波和时空混沌,需要用高浓度钙通道激动剂提高钙离子最大电导率到很高值,且容易产生较大的副作用。而且独立使用钙通道激动剂或钾通道阻滞剂在介质存无扩散功能缺陷时不能有效抑制螺旋波和时空混沌。由此,联合使用钙通道激动剂和钾通道阻滞剂的方法来抑制心脏组织中的螺旋波和时空混沌的思想被提出来[28]。这种控制的对策是只需要低浓度的钙通道激动剂将钙离子最大电导率提高一点,同时用低浓度的钾通道阻滞剂将钾离子最大电导率减少一点,就能达到控制效果。这在临床应用上很有意义,相当于减少了用药量,又达到降低了副作用的目的,而且这种控制方法即使介质中存在无扩散功能的缺陷也同样有效。
4.改变扩散系数控制心脏组织的螺旋波和时空混沌
研究中也发现通过提高心肌细胞的扩散系数,可以控制心脏中的螺旋波和时空混沌。如钙离子最大电导取值在一定范围内,系统可产生螺旋波和时空混沌现象。根据心脏病人临床上抢救的实际方法,引导人们可以考虑通过改变扩散系数来加以控制。在适当选择提高扩散系数和把握时机的条件下,可以有效抑制螺旋波;而对系统产生的时空混沌,必须采用交替改变扩散系数的方式才能有效抑制[29]。这种控制方式的机理可理解为提高扩散系数,使波在均匀介质传播时出现传导障碍,从而导致波不能维持而消失。这种控制思想是有其实际意义的。临床上,多次手按压胸和电击除颤抢救心脏病人都和交替改变扩散系数相当。电击除颤会导致扩散系数的变化,由此研究也可以进一步理解电除颤的复杂机制,为开辟新的除颤方法提理论供参考。
5.结语
通过对心脏离子电流和动力学模型的研究,了解心脏的各种动力学行为是很有意义的工作,对于临床上治疗心律失常等疾病具有指导意义。LRd 系列模型中最早的Luo Rudy91模型较好地反映了心脏的动力学性质,在研究中经常采用。但该模型没有对细胞的渗透电流进行描述,对细胞的复极化过程的描述也不够充分,因此,此后人们又相继提出LRd94、LRd95、LRd99等一系列新模型,这些模型对心肌细胞的描述更加详细。2011年Thomas O’Hara 和Yoram Rudy又提出研究人心肌细胞的更精确模型—ORd离子模型。他们重新测量了100位健康人提供的心脏在稳定状态下的速率依赖性、心室动作电位恢复的数据,以及心肌细胞的ICaL、IK、INaCa,并将这些新数据和以前发表过的实验结果结合起来建立了这个模型。和Tusscher-Panfilov(TP)[30]模型、Grandi-Bers(GB)[31]模型相比,ORd 模型能够详细、精准地模拟健康人心肌细胞电生理现象和钙离子循环、验证生理频率的全部范围以及描述人心肌细胞电生理机制的细节特性。同时,一般的研究工作都是在二维的系统中进行的,而实际的心脏系统是三维的,因此,今后的工作向三维的系统推广才能更好的贴近实际系统。
