液相色谱-串联质谱法检测牛奶中的四环素类药物
2015-12-24文∕贾涛
文∕贾 涛
(北京市饲料监察所)
四环素类药物(tetracyclines,TCs)为一类具有共同多环并四苯羧基酰胺母核的衍生物,对革兰氏阳性菌、阴性菌、螺旋体、霉形体、立克次氏体、衣原体、原虫等均可产生抑制作用,故又称为广谱抗生素。但该类药物的不合理使用及滥用会诱导动物体内耐药菌株的产生并可导致牛奶中该类药物的残留问题,对人类健康造成影响,如四环素类药物易与骨骼中的钙结合,抑制骨骼和牙齿的生长;治疗剂量的四环素还具有致癌作用等。本文以液相色谱-串联质谱法检测牛奶中的四环素类药物残留,结果表明,该方法具有较好的灵敏度、准确度和精密度。
1 方法
试料中残留的四环素、土霉素、金霉素和多西环素经Mcllvaine-Na2EDTA缓冲液提取,HLB柱净化。用液相色谱-串联质谱法测定,外标法定量。
2 试剂和仪器设备
2.1 试剂
以下所用的试剂,除特别注明外均为分析纯试剂;水为符合GB/T 6682规定的一级水。
标准品:盐酸四环素(纯度≥97%),盐酸土霉素(纯度≥96%),盐酸金霉素(纯度≥93%),多西环素(纯度≥93%);甲醇:色谱纯;乙腈:色谱纯;甲酸;氢氧化钠;柠檬酸(C6H8O7•H2O);磷酸氢二钠(Na2HPO4•12H2O);乙二胺四乙酸二钠(C10H14N2Na2O8•2H2O);氢氧化钠溶液(1 mol/L):称取氢氧化钠4 g,加水溶解并稀释至100 mL,即得;柠檬酸溶液(0.1 mol/L):称取21.01 g柠檬酸,用水溶解并定容至1 000 mL,即得;磷酸氢二钠溶液(0.2 mol/L):称取28.41 g磷酸氢二钠,用水溶解并定容至1 000 mL,即得;Mcllvaine缓冲液:将0.1 mol/L柠檬酸溶液1 000 mL与0.2 mol/L磷酸氢二钠溶液625 mL混合,用1 mol/L氢氧化钠溶液调pH值至4.0±0.5;Mcllvaine-Na2EDTA缓冲液(0.1mol/L):称取60.5 g乙二胺四乙酸二钠放入 1 625 mL Mcllvaine缓冲液中,使其溶解,摇匀即得;1 mg/mL标准储备液:准确称取适量的盐酸四环素、盐酸土霉素和盐酸金霉素对照品适量,用甲醇溶解并稀释成浓度均为1 mg/mL的溶液,作为标准储备液,置-20 ℃冰箱中保存,有效期为1 个月;标准工作液:准确量取标准储备液适量,用甲醇-水(3∶7,V/V)溶液稀释成适宜浓度的四环素、土霉素、金霉素和多西环素标准工作液,临用前配制。
2.2 仪器和设备
液相色谱-串联质谱仪(配电喷雾离子源);分析天平:感量0.00001 g;天平:感量0.01 g;涡旋混合器;水平振荡器;组织匀浆机;离心机;酸度计;离心管:50 mL;固相萃取柱:HLB小柱(60 mg/3 cc);氮吹仪;微孔滤膜:0.22 µm。
3 测定步骤
3.1 试料的制备
取混匀后的供试样品,作为供试试料;取混匀后的空白样品,作为空白试料;取混匀后的空白样品,添加适宜浓度的标准工作液,作为空白添加试料。
3.2 提取
称取(2±0.05)g混合均匀的牛奶样品,置50 mL离心管中,加Mcllvaine-Na2EDTA缓冲液18 mL,涡旋混匀,8 000 r/min离心10 min(温度低于15 ℃),取上清液于另一离心管内备用。
3.3 净化
HLB小柱依次用甲醇、水各5 mL预洗。取备用液10 mL过柱,依次用水、5%甲醇水溶液各5 mL淋洗,减压抽干。用甲醇-乙酸乙酯溶液(1∶9,V/V)3 mL洗脱,洗脱液用氮气吹干(温度低于40 ℃)。用甲醇-水(3∶7,V/V)0.5 mL溶解残余物,过滤膜后供液相色谱-串联质谱仪测定。
3.4 标准曲线的制备
精密量取标准储备液适量,用甲醇-水(3∶7,V/V)溶液稀释成含四环素、土霉素、金霉素和多西环素分别为10、20、50、100、200、500 ng/mL的系列工作液,供液相色谱-串联质谱仪测定。
3.5 测定
3.5.1 液相色谱条件
色谱柱:BEH C18(5 mm0×2.1 mm,1.7 µm),或相当者;流动相A:0.3%的甲酸乙腈溶液;流动相B:0.3%的甲酸水溶液;梯度洗脱:0~5 min,15%A线性变化至35%A,5~6 min,35%A线性变化至15%A。流速:0.3 mL/min;柱温:20 ℃;进样量:10 µL。
3.5.2 质谱条件
离子源:电喷雾离子源;扫描方式:正离子扫描;检测方式:多反应监测;电离电压:2.5 kV;源温:100 ℃;雾化温度:300 ℃。锥孔气流速:50 L/h;雾化气流速:500 L/h;定性、定量离子对及锥孔电压、碰撞能量见表1。
3.5.3 测定方法
取试样溶液和相应的标准溶液,作单点或多点校准,按外标法以峰面积计算。对照溶液及试样溶液中四环素、土霉素、金霉素和多西环素的响应值均应在仪器检测的线性范围之内。空白实验:除不加试料外,采用完全相同的测定步骤进行平行操作。
3.5.4 结果计算和表述
按下式计算试料中四环素、土霉素、金霉素和多西环素的残留量:
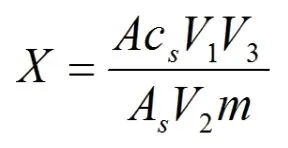
式中:
X——试料中四环素、土霉素、金霉素和多西环素的残留量(ng/g);
A——试样溶液中相应药物的峰面积;
AS——标准溶液中相应药物的峰面积;
cs——标准溶液中相应药物的浓度(ng/mL);
V1——提取试料后缓冲液的总体积(mL);
V2——过固相萃取柱所用备用液体积(mL);
V3——溶解残余物的体积(mL);
m——供试试料的质量(g)。
注:计算结果需扣除空白值,测定结果用平行测定的算术平均值表示,保留3 位有效数字。
3.6 检测方法灵敏度、准确度、精密度
3.6.1 灵敏度
四环素、土霉素、金霉素和多西环素在牛奶中的检测限为5 ng/g,定量限为10 ng/g。
3.6.2 准确度
本方法在10~200 ng/g添加浓度的回收率为70%~120%。
3.6.3 精密度
本方法的批内变异系数≤20%,批间变异系数≤20%。
4 结果讨论
4.1 研究用液质联用法检测牛奶中四环素类药物的意义
欧盟和我国政府都规定了牛奶中四环素类药物的最高残留限量,即四环素、土霉素和金霉素的单个或混合物含量不得超过100 μg/kg。目前,TCs类药物残留检测方法主要有:微生物法、酶联免疫法(ELISA法)和液相色谱法(HPLC法),但这些方法存在特异性差等缺点。液相色谱-串联质谱法(LC-MS/MS法)由于具有特异性强和灵敏度高的特点,常用于兽药残留的结构确证分析。目前,国外已有不少用LC-MS/MS法测定动物性食品中TCs类药物残留的报道,国内相对来说起步较晚,报道也不多。本文以牛奶为试材,建立了LC-MS/MS法检测TCs类药物残留的方法,可为牛奶样品中TCs类药物的残留监控和监督检验等提供技术支持。
4.2 方法的编写过程
在本方法研制过程中,通过查阅有关文献,全面掌握了四环素类药物的化学结构、理化性质、药理毒理作用等,尤其是该类药物的不稳定性:TCs类药物为金黄色或黄色晶粉,无臭,味苦,遇光色渐变暗,需密封、避光、干燥处保存;易溶于水,但水溶液稳定性差,一般均需新鲜配制,可置于低温下保存;较强酸性环境(pH值<2.0)中可降解生成脱水四环素,弱酸性环境(pH值2.0~6.0)中可发生差向异构化,形成差向四环素,碱性环境(pH值>7.0)下降解生成内酯结构的异四环素。在对该类药物材料全面掌握的基础上,参照美国农业部食品安全与监督署(FSIS)颁布的己有的检测方法中前处理方法,针对牛奶的检测方法进行多次实验,发现结果能很好满足欧盟、美国和我国在制定兽药残留检测方法方面的要求,并通过具体实验数据的实验,最终确定了该方法的可行性。
4.3 提取条件的确定
由于甲醇、乙腈等有机溶剂提取的样品峰形和灵敏度较差,水溶液的稳定性较差,因此在提取时用Mcllvaine-Na2EDTA缓冲液(pH值=4.0±0.5),这样既可以利用EDTA络合剂与系统内的金属离子进行结合,同时该pH值也能保证该类药物的稳定性,另外在离心过程中温度控制在15 ℃以内,也能防止该类药物的改变分解。
4.4 净化条件的确定
本方法使用Oasis HLB固相萃取小柱,使得方法的回收率以及重复性稳定可靠。过柱后洗脱液用氮气吹干时温度控制在40 ℃以内,残余物用30%的甲醇水溶液溶解,也能确保其稳定性和灵敏度。
4.5 离子对的确定
TCs类药物属于欧盟指令96/23/EC附录ⅠB组所列物质,根据欧盟2002/657/EC要求,要确证该类物质,至少需要3 个识别点(IP),因此,实验中选择了母离

表2 牛奶中四环素类药物的添加回收率结果
子以及对应产生的2 个响应较强的子离子作为定性定量的依据,可以达到4 个IP点的要求,这样完全按照违禁药物对IP点的要求进行方法定性分析,可以获得要求更严格的结果。
4.6 线性范围
分别取四环素、土霉素、金霉素和多西环素标准储备液适量,用甲醇稀释定容成100 μg/mL,再用30%甲醇水溶液稀释成1 μg/mL的混合标液,依次取0.1、0.2、0.5、1.0、2.0、5.0 mL于10 mL容量瓶内,用30%甲醇稀释定容至刻度,制得10、20、50、100、200、500 ng/mL的系列标液,按低浓度到高浓度的顺序依次进样,结果以系列标液浓度为横坐标,对应峰面积为纵坐标进行线性回归,得出的回归方程及R2值表明:四环素、土霉素、金霉素和多西环素在10~500 ng/mL范围内呈现良好的线性关系,R2均大于0.990(图1)。
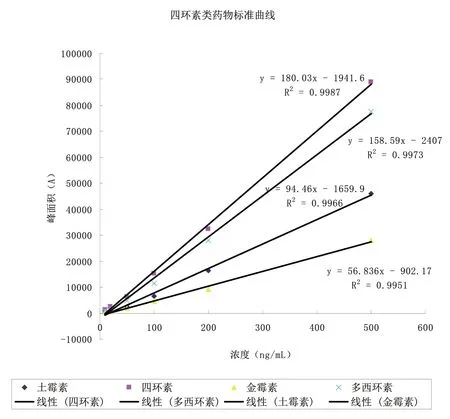
图1 四环素类药物标准曲线
4.7 方法的灵敏度
空白试料按相同的步骤处理后,测定结果表明:在相应的保留时间,空白试料对所测分析物无干扰。定量限(LOQ):进行添加浓度为10 ng/g的标准添加时,经提取后测定,发现信噪比S/N>10(按PtP算),表明方法的定量限为10 ng/g。检测限(LOD):进行添加浓度为5 ng/g的标准添加时,经提取后测定,发现信噪比S/N>3(按PtP算),表明方法的检测限为5 ng/g。
4.8 检测方法的精密度实验
采用标准添加法,在空白牛奶中添加4 个不同浓度(定量限,低、中、高浓度)的四环素类药物进行回收率实验,各浓度进行5 个样品平行实验,重复3次,求出批内、批间相对标准偏差(表2)。
4.9 McIlvaine-Na2EDTA 缓冲液的配制
对于Mcllvaine-Na2EDTA缓冲液的配制可以采用本方法中的配制方法配制,且每种化合物都使用其带结晶水的化合物来称量配制,使用时要选好带有多少个结晶水,如果和标准中的结晶水的数量不一致时可以进行适当折算,然后再配制。
4.10 固相萃取柱的选择
对于实验中使用的萃取柱理论上市场上出售的C18柱和HLB柱都能满足前处理的要求,但在使用C18柱时一定要注意不能在预洗活化以及上样过程中出现柱床干涸现象,否则对四环素类药物的回收率影响很大,为避免此现象的发生,最好使用亲水亲脂的HLB柱子,该柱子柱床是否干涸对回收率基本没有影响。另外,在使用时考虑到是否容易过柱,可以使用60 mg/3 cc较大规格的柱子。根据实际实验,在处理牛奶样品时使用60 mg/3 cc的HLB柱子含给前处理过程带来很大便利。
5 结论
采用液相色谱-串联质谱技术、外标法定量测定了牛奶中四环素类药物,明确规定了方法的适用范围,确定了取样量、提取净化方法和液相色谱-串联质谱条件等。结果表明,该方法具有较好的灵敏度、准确度和精密度。
