红花中羟基红花黄色素A的提取动力学研究
2015-12-14史亚军
王 卉,史亚军,邓 辉,宋 蕊,王 媚
(陕西中医药大学药学院,陕西咸阳 712046)
红花,又称刺红花或草红花,药用红花为菊科植物红花(Carthamus tinctorius L.)的干燥花,味辛性温,归心、肝经,是临床常用的活血化瘀药物[1-6],常用于痛经闭经、跌打损伤、血脉闭塞及心脑血管疾病的治疗[7-12]。红花最早记载于汉代张仲景的《金匮要略》中,在我国大部分地区均有分布和栽培,主要分布于四川、河南、浙江、新疆等地。大量的研究得出,红花中含有黄酮类物质、酚酸、色素、挥发油等多种活性成分,其中羟基红花黄色素A,是其发挥药理作用的物质基础[13-17]。羟基红花黄色素A等有效成分热稳定性较差[18],遇热易分解,不易长时间浸提,提取温度及提取时间对提取率都具有一定的影响,实际研究和生产中多采用水为溶剂进行提取[2],考虑到有效成分的热敏性,本研究以羟基红花黄色素A的含量为指标[19],通过温浸的提取方法,考察不同温度条件下有效成分的动态提取率,优选较佳的提取工艺,并通过数学手段,运用EXAL拟合曲线的方式,得到羟基红花黄色素A在浸提过程中的数学模型,为红花的提取工艺提供可靠的参考依据。
1 试验材料
1.1 药材、试剂 红花(西安盛兴饮片有限公司提供,批号:140301)由陕西中医学院胡本祥教授的鉴定为菊科植物红花的干燥花,羟基红花黄色素A(批号:11637-201308)由中国食品药品检定研究院提供,甲醇、乙腈均为色谱纯,其余试剂均为分析纯,水为高纯水。
1.2 仪器 电热恒温水浴锅(上海科恒实业发展有限公司),KDM型调温电热套(上海树立仪器仪表有限公司),U-3000高效液相色谱仪(德国戴安公司)。
2 方法与结果
2.1 提取方法 取红花药材10 g共6份,精密称定,置于圆底烧瓶中并加设冷凝装置,加14倍量水,置于水浴锅或电热套中,分别于50、60、70、80、90℃以及微沸的条件下回流提取,各样品分别于提取 5、10、15、20、30、45、60、90 min 时取样1 mL,同时补充1 mL溶剂。
2.2 含量测定
2.2.1 色谱条件[20]以十八烷基硅烷键合硅胶为填充剂;以甲醇—乙腈—0.7%磷酸溶液(26∶2∶72)为流动相;检测波长为403 nm,理论塔板数按羟基红花黄色素A峰计算应不低于3 000。
2.2.2 对照品溶液的制备 精密称取羟基红花黄色素A对照品适量,加25%甲醇制成每1 mL含对照品0.128 mg的溶液,即得。
2.2.3 供试品溶液的制备 于不同时间段(5、10、15、20、30、45、60、90 min)精密量取不同温度(50、60、70、80、90℃及微沸)浸提液 1 mL,置于 5 mL 量瓶中,用25%的甲醇稀释至刻度,摇匀,用微孔滤膜滤过,取续滤液,即得。
2.2.4 标准曲线的绘制 取对照品溶液1、2、4、8,10、12、14μL分别进样,测定峰面积,以峰面积Y对进样量X进行线性回归,见图1,得回归方程Y=24.378X -1.101 7,相关系数为0.999 7,结果表明,羟基红花黄色素 A 在0.128~1.792 mg·L-1范围内线性关系良好。
2.2.5 样品测定 精密吸取各供试品溶液5μL,注入HPLC仪,测定。色谱图见图2,3。
2.2.6 含量测定结果 按照上述色谱条件,分别测定不同温度下不同时间提取液中羟基红花黄色素A含量,结果见表1。
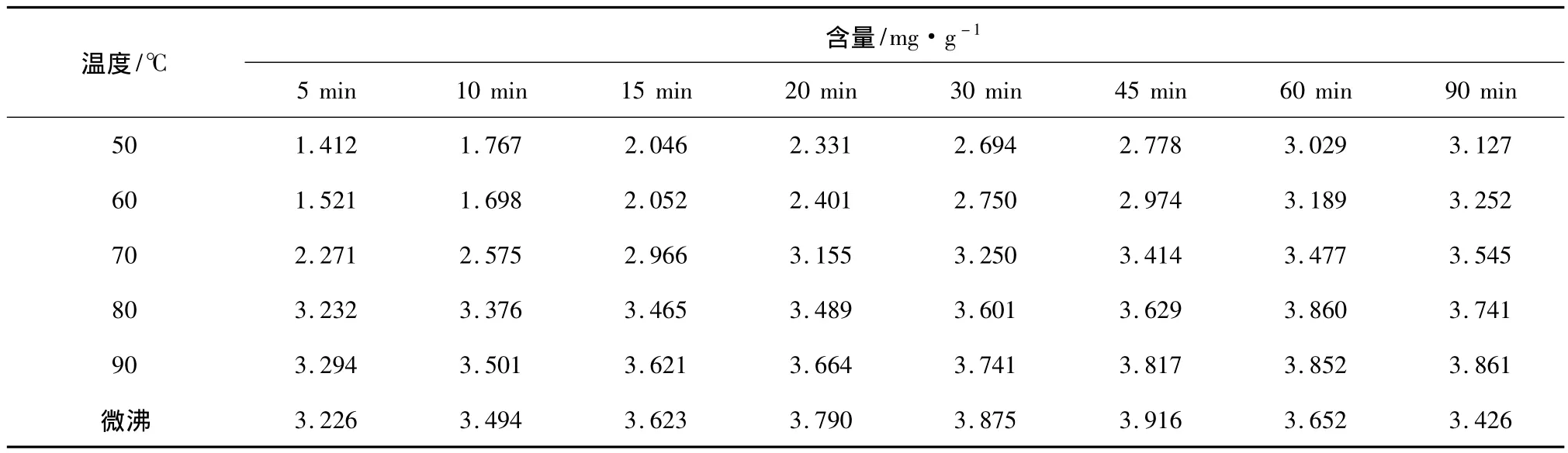
表1 不同温度不同时间浸提液中提取物的含量
由图4可知,随着提取时间的延长,浸提液中羟基红花黄色素A的含量逐渐升高,60 min时曲线趋于平衡。相同提取时间,温度越高,提取率越高,提取温度对羟基红花黄色素A含量有较大影响。由于羟基红花黄色素A存在热不稳定性,长时间高温环境会引起浸提液中羟基红花黄色素A的水解。温度较高条件下,60 min达到平衡后,提取含量会有不同程度下降。根据含量测定结果,最终选择提取条件为在90℃条件下温浸提取60 min。
2.3 动力学研究
2.3.1 速率常数k的求解 以时间t为横坐标,以ln[Ceq/(Ceq - C)]为纵坐标,对 50、60、70、80、90℃条件下的数据进行拟合,得图5,拟合方程见表2。不同温度下的羟基红花黄色素A浓度与提取时间均具有较好的线性关系(R2>0.96),符合一级动力学模型(Ceq为提取平衡时固相外溶质质量浓度,C为该时刻固相外溶质质量浓度)。本实验选取50、60、70、80、90℃为反应温度,故在 50 ~90℃范围内,温度固定的条件下,羟基红花黄色素A的提取速率为速率常数 k。经拟合所得 50、60、70、80、90 ℃时的 k 值分别为 0.028 9、0.035 2、0.052 2、0.023 4、0.035 2 s-1。于微沸状态进行提取,由于温度过高,羟基红花黄色素A发生水解,ln[Ceq/(Ceq-C)]与t不存在线性关系,不符合一级动力学方程。

表2 不同温度的拟合方程
2.3.2 提取活化能(Ea)的求解 提取活化能(Ea)是指在中药的提取过程中,提取物从药材中扩散到溶剂中所需的最小能量。一般情况下,速率常数k与温度的关系服从Arrhe-nius公式,即ln k与1/T呈线性关系,方程为k=Ae-(Ea/RT),公式两边取自然对数,整理可得 ln k—1/T的直线方程:lnk=(-Ea/R)(1/T)+lnA。式中,k为提取速率常数(min-1);A为指前因子;R为气体常数;T为提取温度(K);Ea为提取活化能(kJ·mol-1)。根据所得数据对lnk—1/T做拟合曲线,得到线性方程为lnk= -3 263.3(1/T)+6.524 4,R2=0.957 7。经计算,羟基红花黄色素A提取过程中的活化能为27.13 kJ·mol-1,证实为内扩散控制动力学模型,温度变化对提取速率常数的影响可以由提取活化能来反映。
3 讨论
红花中的羟基红花黄色素A为水溶性成分,相关文献中考察了以水、乙醇、正丁醇、正己烷、乙酸乙酯等溶剂为提取溶媒的提取率情况,考虑到经济问题及毒性问题,本文采用水作为提取溶媒,进行提取工艺的考察。水溶性成分的传统提取方法有回流提取、渗漉提取、浸渍提取和煎煮提取等[21-23],羟基红花黄色素A具有热不稳定性,温度过高会发生热降解,保存率也随着下降,不宜在高温下长时间提取;渗漉法耗时较长,且使用溶剂的量过大;室温浸渍则提取较慢,耗时过长;实验室和大生产中通常采用温浸的方法提取。本实验通过在不同温度条件下采用温浸法进行红花的提取工艺研究,考察温度对提取效果的影响,确定提取条件,为工业化大生产提供可靠依据。
在提取时,回流装置上加装有冷凝装置,可以防止在温浸过程中溶剂的损失,减小了系统误差。在分时间段取样过程中,及时补充溶剂损失,以保证每次取样量所占总提取液的比例不变。在计算不同时间的浸提液浓度时应将前次所取样品中成分的含量计算在内,以确保提取药物量为总提取量。
在传统中药制剂大生产中,提取工艺都是以经验为主,往往存在提取效率底下的问题,需要一定的理论指导。近年来,数学模型被应用到中药学的研究中[24-28],通过对数学公式的推导拟合,建立数学模型与提取过程之间的关系,为提取工艺提供可靠的参考依据。
本实验以Fick第一定律为基础,通过对所得数据进行拟合,得到红花中羟基红花黄色素A提取过程中的动力学方程:ln k=-3 263.3(1/T)+6.524 4,并得到其相关数学参数。在实验所选温度范围内,有 Ea=27.13 kJ·mol-1,温度越高,k 越大,反应速率越快。由于羟基红花黄色素A具有热不稳定性,80、90℃条件下发生水解,拟合所得的k有所下降,不能完全的代入方程,但实际提取率升高,符合Fick第一定律定律。
本实验通过对羟基红花黄色素A的提取工艺研究,确定了最佳提取工艺为适量水,在90℃条件下温浸提取60 min。并通过数学手段,得出相关的提取动力学模型,为今后的工业化大生产提供了科学的方法及参考依据。
[1]贾佼佼,苗明三.红花的现代药理与新用[J].中医学报,2013,28(11):1682-1685.
[2]袁淑娟,张志伟,高天红,等.红花注射液抗血栓作用机制研究[J].中国中药杂志,2011,36(11):1528 -1529.
[3]汪宏雷.红花的药理作用[J].中医药临床杂志,2014,26(5):519.
[4]杨丹丹,张家鑫,吴小鹏,等.西红花药理作用的研究进展[J].中国民族民间医药杂志,2011,20(13):45-46.
[5]万先惠,秦亚利,颜 涛.红花注射液药理作用研究进展[J].中医药学报,2011,39(6):109 -110.
[6]易善勇,官丽莉,杨 晶,等.红花药理作用及其开发与应用研究进展[J].北方园艺,2015(5):191-195.
[7]杨晓君,穆合塔尔,包晓玮,等.红花黄色素与双亚酸的抗血栓作用[J].食品科学,2013,34(3):264 -266.
[8]郭晓金.红花黄色素治疗下肢深静脉血栓形成的疗效观察[J].中医中药,2013,11(2):281 -282.
[9]杨晓媛,任玉芳.红花黄色素药理作用研究进展[J].热带医学杂志,2015,15(3):421 -424.
[10]曲伟良.红花的药理作用分析[J].黑龙江科技信息,2013(11):144.
[11]袁 靖,陈卫东.红花黄色素在心脑血管系统疾病治疗中的应用进展[J].医学研究生学报,2015,28(5):557 -560.
[12]李宝军,刘志强.红花药理分析及临床应用研究[J].亚太传统医药,2014,10(15):44 -45.
[13]张宏宇,陈 沫,熊文激.红花黄色素抗血栓和降血脂作用的实验研究[J].中国实验诊断学,2010,14(7):1028 -1031.
[14]陈 梦,赵丕文,孙艳玲,等.红花及其主要成分的药理作用研究进展[J].环球中医药,2012,5(7):556 -560.
[15]张 欢,张立伟.红花黄色素抗氧化活性研究[J].化学研究与应用,2012,24(5):715 -721.
[16]姜 华.羟基红花黄色素A对大鼠脑缺血-再灌注损伤的保护作用及机制[J].中药材,2013 36(3):462-464.
[17]杨小虎,王丹丹,朱 彦.羟基红花黄色素A的现代研究新进展[J].湖南中医药大学学报,2013,33(3):102 -106.
[18]王 慧,张立伟,晋民杰,等.羟基红花黄色素A稳定性研究[J].太原科技大学学报,2010,31(1):81 -84.
[19]梁 颖,裴 瑾,万德光.红花黄色素中主要成分的含量测定[J].中国现代应用药学,2011,28(13):1349 -1351.
[20]国家药典委员会.中国药典(一部)[S].北京:中国医药科技出版社,2010:141-142.
[21]宗晓菲,时东方,张慧荣,等.不同溶剂和提取方法对红花提取物抗氧化活性的影响[J].贵州农业科学,2012,40(10):44-46.
[22]吴继东,刘晓燕,刘桂萍.不同方法水提取红花中红花黄色素的研究[J].牡丹江医学院学报,2011,32(3):34 -35.
[23]玛依努尔·叶尔肯别克,周 凡,马 芹.正交实验优选新疆红花总黄酮提取工艺[J].中国中医药科技,2014,21(2):167-169.
[24]张 晋,陈 杨,曹飒丽,等.水煎煮法提取葛根总黄酮的动力学模型适用性研究[J].中国中药杂志,2013,38(17):2788-2792.
[25]虞 立,何 昱,金伟锋,等.数学模型在中药研究方面的应用进展[J].中草药,2014,45(14):2106 -2110.
[26]苏 辉,王伯初,刘玮琦,等.天然药物提取过程的动力学数学模型[J].中草药,2011,42(2):384 -391.
[27]王伯初,苏 辉,杨 宪,等.天然药物提取过程的传质动力学模型[J].中成药,2012,43(12):2309 -2312.
[28]边名鸿,左 勇,宗绪岩,等.黄连提取动力学模型 研究[J].四川理工学院学报,2012,25(4):26 -29.
