H PLC同时测定干蟾皮中华蟾酥毒基和酯蟾毒配基成分的含量
2015-11-11汪元符
汪元符
(南昌市食品药品检验所,江西南昌330038)
H PLC同时测定干蟾皮中华蟾酥毒基和酯蟾毒配基成分的含量
汪元符
(南昌市食品药品检验所,江西南昌330038)
目的:建立干蟾皮中华蟾酥毒基和酯蟾毒配基2种化学成分含量测定的高效液相色谱法。方法:采用DIKMA C18色谱柱(250 mm×4.5 mm,5 μm),流动相为磷酸盐缓冲液(30 mmol/L磷酸二氢钾以磷酸调节pH值为3.0)及乙腈,梯度洗脱,柱温为35℃,流速为0.8 mL/min,进样量为10 μL,检测波长为296 nm。结果:2种化学成分检出限浓度均为1.0 μg/mL,定量限浓度均为2.5 μg/mL,线性范围为2.5~100.0 μg/mL,在线性范围内相关系数均在0.99以上,平均加样回收率为98.8%~99.9%。结论:本方法简便、准确、快速、重复性好、专属性高,可用于干蟾皮中华蟾酥毒基和酯蟾毒配基2种化学成分的含量测定。
高效液相色谱;干蟾皮;中华蟾酥毒基;酯蟾毒配基
干蟾皮至今未收载于历版《中国药典》,而见于《江苏省中药材标准(1989)》、《河南省中药材标准(1993)》、《江西省中药材标准(1996)》。干蟾皮为蟾蜍除去内脏的干燥全体。功能与主治:清热解毒,利水消肿;用于小儿疳积,咽喉肿痛,肿瘤;外治痈肿疔疮。以干蟾皮为原料药的中药单味制剂包括:华蟾素口服液、华蟾素注射液、华蟾素片、华蟾素胶囊等,用于恶性肿瘤晚期、乙型肝炎。以干蟾皮入药的中药成方制剂包括:大败毒胶囊(清热败毒,消肿止痛,用于梅毒及扁平疣)、鹤蟾片(解毒除痰,凉血祛瘀,消痰散结,用于原发性支气管肺癌,肺部转移癌)、季德胜蛇药片(清热解毒,消肿止痛,用于毒蛇、毒虫咬伤)等。可见干蟾皮是一味比较常用的、重要的动物类中药材。在现有的干蟾皮药品标准中,只收载了性状、水分(检查项),过于简单。本法建立干蟾皮中华蟾酥毒基和酯蟾毒配基2种化学成分含量测定的高效液相色谱法(HPLC),为干蟾皮的质量控制提供了参考。
1 仪器、试剂与材料
Waters e2695高效液相色谱仪,METTLER TOLEDOME204E电子分析天平,METTLERTOLEDO XS105电子分析天平,昆山KQ-300DB型数控超声波清洗器,Sartorius PB-10 pH计,TG16-WS台式高速离心机(湘仪离心机),Millipore超纯水系统。
甲醇(色谱纯,Merck),乙腈(色谱纯,Merck),磷酸(分析纯,Macklin),磷酸二氢钾(分析纯,Macklin)。
对照品:华蟾酥毒基对照品(110803-200605),酯蟾毒配基(110718-201108),均由中国食品药品检定研究院提供。
样品:干蟾皮10批次(批号:120406、120410、120412、120418、120610、120612、120614、121015、121016、121018),购自市场或流通企业,产地分别为江西、湖北、安徽、辽宁、山东、贵州、黑龙江、吉林。
2 方法与结果
2.1高效液相色谱分析条件
分析柱:DIKMA C18(250 mm×4.5 mm,5 μm)。柱温:35℃。流速:0.8 mL/min。进样量:10 μL。检测波长:296 nm。流动相:A为30 mmol/L磷酸二氢钾(以磷酸调节pH值为3.0),B为乙腈。按表1进行梯度洗脱。
2.2对照品溶液的配制
取华蟾酥毒基对照品、酯蟾毒配基对照品各约10 mg,精密称定,以甲醇制成每1 mL中各含1 mg的溶液作为对照品储备液。取对照品储备溶液以甲醇等比稀释,可得到各含2.5,5.0,10.0,20.0,30.0,40.0,50.0,60.0,70.0,80.0,90.0,100.0 μg/mL的标准系列溶液。

表1 梯度洗脱
2.3供试品溶液的配制
将10批样品分别研细,各取约2.0 g,精密称定,置具塞锥形瓶中,精密加入甲醇50 mL,密塞,称定质量,超声30 min,放冷,再称定质量,用甲醇补足减失的质量,摇匀,以10 000 r/min离心10 min后,取上清液,用0.2 μm的滤头滤过,取续滤液测定。
2.4检测波长的确定及专属性试验
按“2.2”的方法配制对照品溶液,取各含50.0 μg/mL的混合对照品溶液试验。按“2.3”的方法制备供试品溶液、供试品加标溶液。分别取混合对照品溶液、试剂空白溶液、供试品溶液、供试品加标溶液,按“2.1”项下的条件检测。结果见图1~6。其中华蟾酥毒基对照峰保留时间为22.644 min,酯蟾毒配基对照峰保留时间为23.726 min。
由各成分的紫外吸收光谱图可知,华蟾酥毒基的最大吸收波长为294.0 nm,酯蟾毒配基的最大吸收波长为298.7 nm,选择检测波长为296 nm时,华蟾酥毒基、酯蟾毒配基都能得到较好的检测灵敏度。
由混合对照品溶液、试剂空白溶液、供试品溶液、供试品加标溶液所采集的色谱图比较可知,试剂空白及供试品对各成分的检测无干扰,各成分峰均能基线分离,分离度(R)均在2.0以上,实测理论塔板数均在4 000以上。

图1 试剂空白296 nm波长采集色谱图

图2 混合对照296 nm波长采集色谱图

图3 在22.644 min及23.726 min提取的华蟾酥毒基、酯蟾毒配基对照紫外吸收光谱图
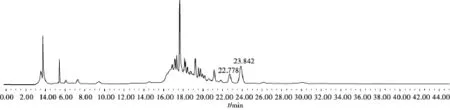
图4 供试品296 nm波长采集色谱图
2.5线性关系及检出限、定量限考察
采用“2.1”项下的色谱条件,以“2.2”项下的标准系列溶液进样检测。以检测所得峰面积为纵坐标,以标准系列溶液浓度(μg/mL)为横坐标,进行线性拟合。以采集的色谱图中检出峰的信噪比大于3时的浓度(μg/mL)为检出限,信噪比大于10时的浓度(μg/mL)为定量限。以在一定浓度范围内,相关系数大于0.99,为线性范围。结果如表2。

图5 在22.778 min及23.842 min提取的华蟾酥毒基、酯蟾毒配基紫外吸收光谱图

图6 供试品加标296 nm波长采集色谱图

表2 2种成分标准曲线测定、检出限和定量限检测
2种成分在各自的线性范围内具有良好的线性关系,检出限均为1.0 μg/mL,定量限均为2.5 μg/mL,灵敏度较高。
2.6精密度试验
选用标准系列溶液中各成分浓度为50 μg/mL的标准溶液,连续进样6针,计算各成分峰面积的相对偏差。结果如表3,各成分RSD值在0.04%~0.05%之间,精密度良好。
2.7稳定性试验
选用标准系列溶液中各成分浓度为50 μg/mL的标准溶液,在0,2,4,8,12,24 h分别进样,以各成分峰面积计算。结果如表4,各成分RSD值在0.46%~1.06%之间,表明24 h内能稳定检测。

表3 2种成分精密度检测结果

表4 2种成分稳定性检测结果
2.8重复性试验
选用批号为120406的干蟾皮,按“2.3”项下的方法制备6份平行样品,按本法检测其中华蟾酥毒基、酯蟾毒配基的含量。结果如表5,各成分RSD值在0.15%~0.34%之间,表明重复性良好。

表5 2种成分重复性检测结果
2.9回收率试验
取批号为120406的干蟾皮(华蟾酥毒基0.134 7 mg/g,酯蟾毒配基0.087 4 mg/g)试验。准确称取1.00 g样品,按“2.3”项的方法制备供试液,2种成分理论浓度为:华蟾酥毒基2.69 μg/mL,酯蟾毒配基1.75 μg/mL。分别准确加入0.125,2.500,4.500 mL各含1 mg/mL的对照品储备液,再按“2.3”项的方法制备成供试液,2种成分理论加入浓度各为:2.5,50.0,90.0 μg/mL;加入后的理论加标浓度应为:华蟾酥毒基5.19,52.69,92.69 μg/mL,酯蟾毒配基4.25,51.75,91.75 μg/mL。以5次平行测定结果的均值与加标浓度相比较,回收率如表6所示,2种成分高、中、低3个浓度的回收率均在99.3%~99.7%之间。

表6 干蟾皮中加样回收试验
2.10样品测定结果
检测了10批干蟾皮,结果如表7所示。
3 讨论
3.1液相色谱条件的选择
参照《中国药典》2010年版一部“蟾酥”含量测定项下的色谱谱条件:以乙腈-0.5%磷酸二氢钾溶液(50∶50)(用磷酸调节pH值为3.2)为流动相,检测波长296 nm,柱温40℃。采集的混合对照品色谱图如图7所示。结果2种成分对照品峰不能分离,需要对液相色谱条件进行优化。

表7 干蟾皮中2种成分测定(mg/g)
试采用梯度洗脱的方式,结果2种成分对照品峰能够完全分离,而且能大大提高柱效(n>4 500)。因此采用了本法梯度洗脱的方式。

图7 混合对照296 nm波长采集色谱图
流动相试用了磷酸盐缓冲液-乙腈、磷酸盐缓冲液-甲醇系统,结果以磷酸盐缓冲液-乙腈系统分离效率高,峰型好,柱效高。但高于50 mmol/L磷酸盐缓冲液浓度与乙腈混合,很有可能产生盐析,危害色谱系统,所以采用本法的30 mmol/L,以保护色谱系统。
流动相pH值的选择:所测的2种成分化合物在酸性条件下分离较好,试用了pH值为3.0,4.0,5.0等不同pH值的磷酸盐缓冲液,结果表明在pH值为3.0时,分离最好,柱效最高。
柱温的选择:在其他条件不变的前提下,试用不同的柱温:25,35,40℃。结果显示,柱温40℃时柱效反而不如柱温25℃。但柱温35℃与柱温25℃柱效相当。因此选用本法的条件,柱温35℃。
流动相流速的选择:考察了0.8 mL/min和1.0 mL/min两个流速下的色谱图。结果显示在0.8 mL/min流速下的柱效及分离优于1.0 mL/min的流速。因此选用本法的条件,流速0.8 mL/min。
3.2供试品提取方法选择
曾试用不同提取溶剂:甲醇、50%甲醇、乙腈、50%乙腈、乙醇、50%乙醇。结合不同提取方式:超声、索氏回流。结果表明,甲醇提取效率最高,且超声与索氏回流无明显差异,可以选用甲醇超声提取的方式。
考察了不同的超声时间:15,20,30,45 min。结果表明15 min提取不够完全,20,30,45 min提取时间的提取结果没有明显差异。因此,本法选用了30 min的提取时间。
以取样量2.0 g,考察了不同提取溶剂体积:10,25,50 mL对提取结果的影响。结果表明10 mL甲醇提取不够完全,25,50 mL甲醇提取结果没有明显差异。因此,本法选用了50 mL甲醇的提取体积。
[1]国家药典委员会.中华人民共和国药典(一部)[S].北京:中国医药科技出版社,2010:360.
[2]陈伟.干蟾皮药材中华蟾酥毒基的含量测定[J].中国医药导报,2013,10(17):122-124.
[3]徐洪锋.干蟾皮药材中华蟾酥毒基的测定[J].海峡药学,2013,25(2):52-53.
[4]曲婷.蟾蜍类药材中吲哚生物碱和蟾毒配基类成分的含量[J].中国中药杂志,2012,37(20):92-97.
[5]曹蔚.蟾皮药材质量标准研究[J].陕西中医,2010,33(11):101-103.
[6]黄玉叶.蟾皮的提取和含量测定及临床应用研究进展[J].中华中医药学刊,2011,29(7):190-192.
[7]缪珠雷.蟾皮和蟾蜕脂蟾毒配基含量测定与比较[J].时珍国医国药,2010,21(4):113-114.
[8]艾颖娟.HPLC法测定蟾皮中蟾毒配基类成分的含量[J].沈阳药科大学学报,2009,26(4):45-47,70.
[9]张振海.不同品种及产地蟾皮中抗肿瘤活性成分含量比较[J].中华中医药杂志,2011,26(11):228-231.
[10]王宏洁.HPLC测定不同种蟾皮药材中不同部位蟾蜍噻咛的含量[J].中国实验方剂学杂志,2012,18(11):76-78.
[11]吴毅.HPLC法同时检查华蟾素片中蟾毒灵、华蟾酥毒基及酯蟾毒配基限量和测定蟾蜍噻咛的含量[J].中国药事,2012,26(1):55-58.
[12]王宏洁.高效液相色谱法测定不同种蟾皮中蟾蜍噻咛的含量[J].中国中医药信息杂志,2012,19(11):49-50.
[13]王捧英.HPLC同时测定人参强心滴丸中华蟾酥毒基和脂蟾毒配基的含量[J].药物分析杂志,2012,32(5):76-79.
Simultaneous Determination of Cinobufagin and Resibufogenin in Dried Toad Skin by HPLC
Wang Yuanfu
(Nanchang Institute for Food and Drug Control,Jiangxi Nanchang 330038,China)
ABSTRACRObjective:To develop a HPLC method for determination of two components,cinobufagin and resibufogenin,in dried toad skin.Methods:DIKMA C18column(250 mm×4.5 mm,5 μm)was used,with phosphate buffer solution(30 mmol/L potassium dihydrogen,of which the pH value was adjusted to 3.0 with phosphoric acid)-acetonitrile as a mobile phase for gradient elution at a column temperature of 35℃and a flow rate of 0.8 mL/min.The sample loading was 10 μL,and the detection wavelength was 296 nm.Results:Both the detection limits of the two components were 1.0 μg/mL,while the quantitative detection limits were 2.5 μg/mL,the linear ranges were 2.5~100 μg/mL(r>0.99),and the recovery rates were 98.8%~99.9%.Conclusion:The HPLC method is simple,accurate,rapid,and of a good reproducibility and a high specificity,which may be used for simultaneous determination of cinobufagin and resibufogenin in toad skin.
High Performance Liquid Chromatography(HPLC);Dried Toad Skin;Cinobufagin;Resibufogenin
10.3969/j.issn.1672-5433.2015.12.005
2015-08-09)
汪元符,男,主管药师。研究方向:中药理论、药物检测及食品安全。E-mail:wanngel@126.com
