PAC投加对絮体破碎后再絮凝特性和颗粒去除的影响
2015-09-21赫俊国何开帆董志虎袁一星
赫俊国,刘 剑,何开帆,于 淼,董志虎,袁一星,2,张 杰,2
(1.哈尔滨工业大学市政环境工程学院,150090哈尔滨;2.城市水资源与水环境国家重点实验室(哈尔滨工业大学),150090哈尔滨)
给水处理过程中,混凝是去除水中胶体或悬浮颗粒最常用的方法,也是关键的工艺步骤之一[1].混凝过程一般分为凝聚和絮凝两部分,凝聚包括金属离子水解、粒子迁移及颗粒脱稳等一系列过程,而絮凝是脱稳后的胶体或微小悬浮物逐渐成长为较大絮凝体的过程[2-3].混凝的目的是使胶体脱稳和脱稳后的胶体-絮体达到一定的尺寸和强度,从而提高胶体及悬浮颗粒的去除效果.合理地进行絮凝工艺设计,必须保证各构筑物单元内絮体破碎率最小化.在实际生产过程中,具有较大剪切强度的区域普遍存在于给水处理厂各构筑物单元[4].当絮体暴露在较高强度的剪切力条件下时会被打碎[5],打碎后形成的小颗粒在沉淀池去除率降低,从而影响后续工艺的处理效能[6-7].
破碎可以分为表面破损和大尺度破碎两种模式[8].前者是指微小的颗粒从絮体表面掉落,致使微小絮体的数量增加;后者是指大絮体分裂为具有相似大小的絮体,微小絮体的数量并没有明显增多.目前,针对絮体破碎再絮凝的研究主要集中于不同混凝剂种类形成的絮体,在不同破碎强度下破碎后能否恢复到原有水平.Wang等[9-10]对氯化铝(AlCl3)和聚合氯化铝(PAC)形成的絮体破碎再絮凝过程进行了研究,认为破碎后的絮体发生再絮凝时,絮体大小很难恢复到破碎前的水平.Xu 等[11]对 Al13、PAC 与腐殖酸形成的絮体的研究结果表明,两种药剂形成的絮体破碎再絮凝过程均不可逆,Al13絮体强度小于PAC絮体,但Al13絮体的恢复能力强于PAC絮体.Jarvis等[12-13]认为Fe-高岭土絮体及Fe-天然有机物(NOM)絮体破碎后的再絮凝能力较差,絮体大小不能恢复到未破碎前的水平.然而,部分研究表明,絮体破碎-再絮凝过程完全可逆.Lin等[14]认为高岭土与阳离子淀粉形成的絮体的破碎再絮凝过程完全可逆,同时,中性或碱性条件下形成的絮体的抗剪切能力强于酸性条件下形成的絮体.Yukselen等[15-16]对正电荷聚合电解质进行了研究,认为其在长时间搅拌条件下形成的絮体破碎后基本能恢复到未破碎前的大小.Yu等[17-18]对不同混凝机理条件下絮体破碎与再絮凝进行了研究,认为电中和条件下形成的絮体的破碎再絮凝过程可逆,而网捕卷扫条件下形成的絮体破碎再絮凝过程不可逆.目前,对不同混凝剂形成的絮体的破碎再絮凝过程研究较多,而关于如何提高破碎再絮凝过程不可逆絮体再絮凝能力的研究较少,且对再絮凝阶段絮体的生长速率变化也未进行系统研究.同时,如何改善低温低浊水条件下形成的絮体破碎后的沉降性能鲜有报道.本文以低温低浊水为处理对象,以PAC为混凝剂,分别考察了再絮凝阶段补投PAC对絮体粒径、生长速率、粒径分布变化,浊度及颗粒数去除效果的影响,以期改善絮体破碎后的再絮凝能力,提高颗粒的去除效率,从而为低温低浊水的混凝处理提供技术支持.
1 实验
1.1 实验原水及材料
实验原水来自青海省西宁市第七水厂,该水厂原水为雪山融化水,水质具有较好的稳定性.实验在2012年11月~2013年3月进行,实验期间原水水质:水温为1.4~4.3℃,浊度为 1.89~1.96 NTU,pH 为 8.01~8.07,颗粒数为 367~389个·mL-1,颗粒粒径为 1.12~1.78 μm.
PAC(化学纯)为实验所在水厂使用的混凝剂,盐基度为40%~90%,铝质量分数(以氧化铝计)≥30%.每次实验前2 h,将PAC溶于蒸馏水,配成质量分数为5%的使用溶液.
1.2 实验方法
絮凝-破碎-再絮凝实验用六联搅拌器(MY3000-6M,中国武汉梅宇仪器设备有限公司)完成.将1 L的实验原水置于1 L的圆形烧杯中,并按以下条件进行絮凝实验:依据水厂现状及前期药剂优选实验,首先将15 mg/L的PAC使用溶液投加到烧杯中,以300 r/min的转速快速搅拌0.5 min,然后以120 r/min的转速搅拌1.5 min,最后以70 r/min的转速慢搅6 min.絮凝结束后,立即进行破碎实验,破碎条件为:转速500 r/min,时间1 min.当破碎实验结束后,向烧杯中再次投加不同量的PAC使用溶液,并立即进行再絮凝实验,再絮凝搅拌强度为70 r/min,搅拌时间为1~6 min,并沉淀20 min.分别利用浊度仪(2100P,美国哈希公司)和在线颗粒计数仪(2200PCX,美国哈希公司)测定不同再絮凝时间沉后水上清液中的剩余浊度和剩余颗粒数.
利用激光粒度仪(Mastersizer2000,英国马尔文仪器公司)对絮凝、破碎、再絮凝过程的粒径变化进行在线监测[19],实验中粒径均为絮体的平均粒径[20].实验过程中,在蠕动泵的作用下,圆形烧杯中的原水以2.0 L/h的速度缓慢地进入粒度仪,仪器中的光检测单元可以测定絮体的粒径,经过检测后的水样回流至烧杯[7].再絮凝过程中絮体粒径分布同样采用激光粒度仪进行监测[21].
2 结果与分析
2.1 絮体粒径的变化
絮凝过程中,絮体粒径可以间接反映絮体的沉降性能,一般大絮体沉降性好,小絮体沉降性差;同时,絮凝、破碎及再絮凝过程粒径的变化可以直观地表征絮体形态的变化.不同PAC补投量时絮凝、破碎及再絮凝过程絮体粒径变化如图1所示.

图1 不同PAC补投量时絮体粒径的变化
由图1可以看出,絮凝过程可以分为3个阶段:停滞期、快速增长期和稳定期.停滞期,混凝剂与原水进行充分混合,其水解产物与原始颗粒发生反应,在此阶段,絮体大小变化甚微.快速增长期,随着反应时间的延长,絮体粒径迅速增大,当絮凝时间从1 min延长至6 min时,絮体粒径由17 μm增大到370 μm.在此阶段,原始颗粒表面所带的负电荷被PAC所带的大量正电荷强烈中和,粒子之间相互碰撞形成较大的絮体;同时,由于PAC混凝剂的网捕架桥作用,可以将较小的颗粒吸附在大颗粒上,从而使絮体尺寸不断增大.絮凝时间超过6 min后,继续延长絮凝时间,絮体大小几乎不发生变化,此时絮体生长已处于稳定期,在该阶段,絮凝过程为絮体生长和破碎的动态平衡过程.
破碎开始后,絮体粒径急剧减小.破碎0.5 min时,絮体粒径由 370 μm 下降到 176 μm.继续延长破碎时间,絮体粒径继续减小,破碎完成时的絮体粒径为109 μm.由于絮体极易破碎,当作用于絮体表面的剪切力大于絮体的内部结合力时,絮体将发生破碎,粒径下降.破碎后的絮体粒径小、沉降性能差,在沉淀过程难以去除,从而影响后续工艺的处理效能.
再絮凝阶段,在混凝剂补投与不补投的条件下,絮体粒径均随着搅拌时间的增加逐渐增大,说明PAC絮体破碎后具有一定的再絮凝能力.再絮凝阶段并没有出现停滞期,这可能与破碎后絮体的表面活性有关.絮凝阶段,当向水中投加混凝剂后,微小絮体在电中和、网捕卷扫作用下快速凝聚,当絮体发生破碎后,絮体内部的结合键断裂并暴露在外,絮体活性并没有消失.当再次投加PAC后,破碎后的絮体能够很快地发生碰撞,絮体粒径迅速增大.不补投混凝剂时,絮体粒径变化非常缓慢,再絮凝结束时,絮体粒径为225 μm,仅为破碎前的59.5%,说明PAC絮体破碎后不能完全恢复.随着混凝剂补投量的增大,絮体的再絮凝能力呈现先升高后下降的趋势,再絮凝末期絮体粒径也先增大后减小.PAC补投量较低时(1 mg/L),絮体粒径不能完全恢复到破碎前的水平;补投量增大到2 mg/L时,絮体粒径由118 μm增大到400 μm,明显大于未破碎前的 370 μm,絮体粒径增长率为8.11%;补投量为4 mg/L时,絮体粒径达到最大,为408 μm,但相较于2 mg/L时的增加幅度并不明显.当絮体破碎后,絮体表面的电荷发生变化,且分布更加均匀[10].随着投药量的升高,PAC表面所带的大量电荷会与裸露在外的负电荷发生中和反应;由于PAC的网捕卷扫作用,破碎后的小絮体迅速碰撞并形成大絮体.同时,随着投药量的升高,体系中发生电中和作用和网捕卷扫作用的载体不断升高,更多的微小絮凝体逐渐形成较大的絮体,故絮体粒径逐渐增大.当投药量为4 mg/L时,体系中的原有电荷基本被中和,故投药量的增加对絮体粒径增长影响不大.继续增加投药量,絮体的粒径反而减小.补投量为8 mg/L时,絮体粒径减小到345 μm,小于破碎前的粒径.这是因为在初始絮凝过程中,已经投加了大量的PAC,絮体表面的电荷已被中和,虽然破碎后絮体表面的电荷进行了重新分布,但当PAC的投加量过大时,小絮体发生再稳,阻碍了微小絮体的相互碰撞,致使絮体粒径变小.
2.2 再絮凝过程絮体生长速率的变化
随着PAC补投量的升高,再絮凝阶段絮体粒径达到平衡粒径所需的时间不断缩短(图1).不补投PAC时,絮体再絮凝的整个过程均在生长;投加量为1,2 mg/L时,粒径达到平衡所需时间分别为4.5,3.5 min;较大补投量(4~8 mg/L)时,絮体粒径达到稳定所需时间基本维持在2.5 min.由图1还可以看出,再絮凝阶段絮体生长过程中,粒径与絮凝时间基本呈线性关系.因此,对絮体生长曲线进行线性拟合,拟合直线的斜率即为再絮凝过程絮体的生长速率,结果如表1所示.
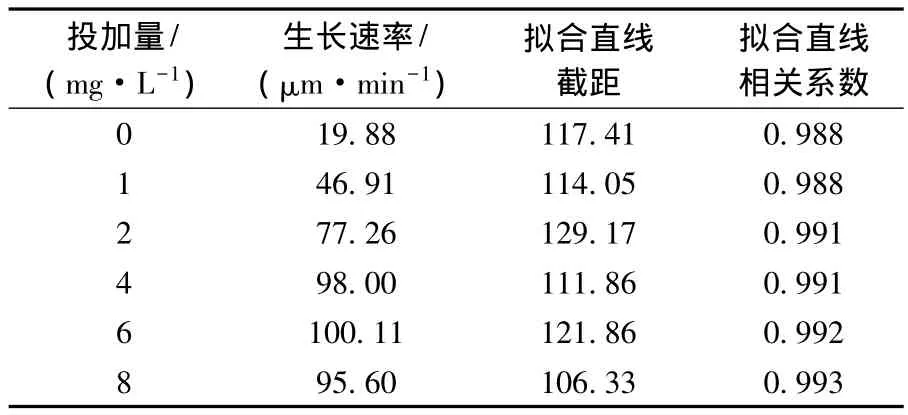
表1 PAC再次投加量对絮体生长速率的影响
不同补投量时,絮体粒径与絮凝时间之间存在良好的线性关系,相关系数均达0.98.代表破碎后絮体尺寸的拟合直线截距基本相同,维持在106~129,说明实验的重复性较好,这与絮凝-破碎条件一致有关.随着PAC补投量的升高,再絮凝速率呈现先增加后降低的趋势.不补投PAC时,絮体破碎后的再絮凝速率为19.88 μm/min,补投少量(1 mg/L)的 PAC时,再絮凝速率为46.91 μm/min,增加了 2.4倍,说明补投少量的PAC即可加快絮体破碎后的再絮凝速率.当PAC补投量为2 mg/L时,再絮凝速率提高到77.26 μm/min.PAC补投量为6 mg/L时,速率达到最大,为 100.11 μm/min,继续提高补投量,再絮凝速率缓慢下降.随着补投量的升高,与颗粒发生反应的电荷数量不断增多,且参与网捕卷扫作用的官能团数量不断提高,从而提高了絮体的生长速率[22].当补投量过大时(8 mg/L),絮体的再稳使得再絮凝速率下降.对比图1、表1及图3可得,PAC为6 mg/L时,絮体破碎后的再絮凝速率达到最大,但再絮凝结束后的絮体粒径并非最大,且此时的剩余浊度较高,说明生长速率的快慢只是反映絮凝好坏的一个因素,不能单纯以再絮凝速率来比较絮体破碎后的再絮凝能力,应综合考虑絮体的粒径及对颗粒的去除能力.
2.3 絮体粒径分布的变化
为分析絮体生长过程中不同粒径颗粒的迁移变化规律,分别考察了PAC补投量为0及2 mg/L时,再絮凝阶段絮体粒径分布的变化,结果如图2所示.
不补投混凝剂时,随着絮凝时间的延长,絮体粒径分布曲线逐渐向大粒径的方向移动,但移动速度较慢(图2(a)).当絮体发生破碎后,絮体粒径分布曲线呈现双峰,说明絮体破碎后微小絮体的数量急剧增多.絮体粒径分布曲线双峰对应的粒径大小分别为22和115 μm,所占体积分数分别为2.98%和7.63%.由图2(a)可得,粒径在22 μm附近的微小絮体的粒径分布范围较宽,而粒径在115 μm附近絮体的粒径分布范围较窄,说明絮体破碎后,系统中以微小粒径的絮体为主.当絮凝时间为2 min时,粒径分布曲线仍有双峰,但微小絮体的数量明显减少,较大的絮体在不断形成.双峰所对应的絮体粒径分布为31和178 μm,且粒径为31 μm的絮体所占的体积分数为1.91%,明显小于0 min时小粒径峰值所占的体积分数.当再絮凝时间大于4 min时,粒径分布曲线上的双峰消失,峰值所对应的粒径逐渐增大.再絮凝结束时,粒径分布范围由破碎时的1.12~447 μm变为再絮凝后的1.78~1 588 μm.由图2(a)还可以看出,随着絮凝时间的增加,粒径分布峰值对应的絮体所占的体积分数逐渐减少,絮凝时间由2 min增加到6 min时,峰值所占百分比由7.35%降低到6.57%,说明当无混凝剂补投时,絮体粒径范围随着絮凝时间的增加而变宽,絮体的粒径分布更加分散.
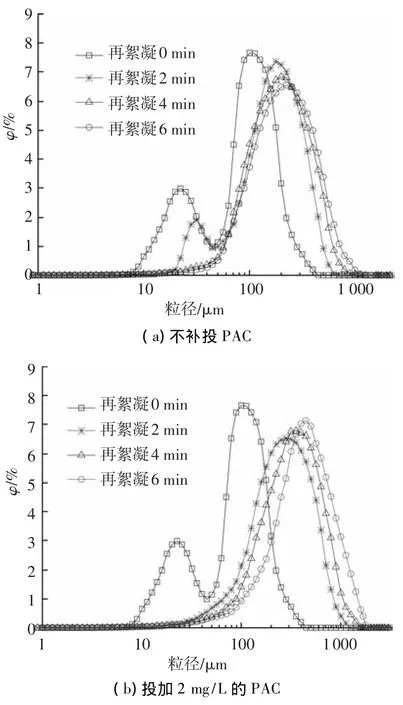
图2 补投PAC对再絮凝过程粒径分布的影响
补投2 mg/L PAC时,随着絮凝时间的增加,絮体粒径分布同样向大粒径的方向移动,但移动速度明显加快(图2(b)).再絮凝2 min时,絮体粒径分布曲线上的双峰已经消失,峰值对应的絮体粒径增大到282 μm,明显大于无投药时的178 μm.随着絮凝时间的继续增加,粒径分布曲线峰值对应的絮体粒径也不断增大,再絮凝结束时,峰值对应的粒径为400 μm,且絮体粒径分布范围为4~1 782 μm,说明大粒径絮体的数量明显增多.图2(b)表明,随着絮凝时间的增加,粒径分布曲线逐渐变窄,说明絮体的粒径分布更加紧密、均匀.同时,粒径分布曲线峰值对应的絮体所占的体积分数逐渐升高,由2 min时的6.55%升高到6 min时的7.13%,进一步说明大絮体的数量不断增加.导致上述现象的原因可能是,当再次投加PAC后,破碎后形成的小絮体相互碰撞,逐渐形成较大粒径的絮体,同时由于PAC的吸附架桥及网捕卷扫作用,大部分微小絮体被吸附进入大絮体的孔隙中,从而使系统中小颗粒数量变少,絮体的粒径分布更加狭窄、均匀[23].
比较图2(a)、(b)可得,当补投2 mg/L PAC后,粒径范围为280~630 μm的大絮体所占体积分数由22.85%升高到46.36%,而粒径范围为4~35 μm的小絮体所占体积分数由1.21%降低到0.19%,说明投加PAC能明显减少小絮体的体积分数,增加大絮体的数量,从而提高絮体的再絮凝能力.
2.4 剩余浊度的变化
浊度是考察给水处理工艺运行好坏最直接的指标.图3为不同PAC补投量条件下,沉后水剩余浊度随再絮凝时间的变化.
不同PAC补投量条件下,沉后水上清液剩余浊度均随再絮凝时间的增加而不断降低.补投量为0时,剩余浊度随时间的变化非常缓慢.絮凝6 min后,剩余浊度由再絮凝前的2.74 NTU降到再絮凝后的2.32 NTU,浊度去除率仅为15.33%.这是因为在絮体破碎过程中,絮体表面活性降低,影响了絮体的再絮凝能力,系统中微小颗粒不能被沉淀去除,从而导致浊度较高[24].补投PAC后,剩余浊度明显降低,随着再絮凝时间的增加,剩余浊度快速下降.当投药量为2 mg/L时,沉后水剩余浊度为0.79 NTU,完全能够满足生活饮用水水质标准对浊度的要求;当絮凝时间为5 min时,剩余浊度小于1 NTU,说明再次投加PAC可以明显提高系统对浊度的去除能力.上述现象的产生可能与破碎后絮凝体的表面特性有关,由于PAC中含有部分与再絮凝能力有关的单体铝(Ala),当絮凝体发生破碎后,体系中的Ala分布在絮凝体的表面,从而提高了絮体的再絮凝能力[25].当 PAC 补投量为 4 mg/L,沉后水剩余浊度变化并不明显.当PAC补投量大于等于6 mg/L时,沉后水剩余浊度反而比低投药量时高,这一结果与图1中粒径的变化趋势一致.
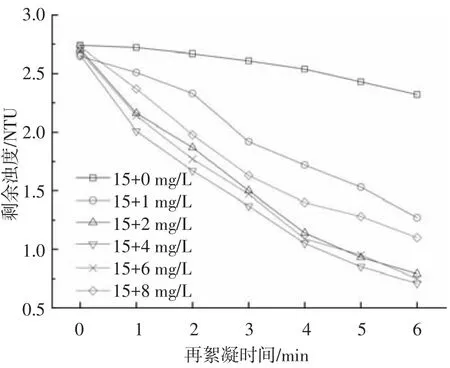
图3 再次投加PAC对浊度去除效能的影响
2.5 剩余颗粒数的变化
剩余颗粒数可以直观反映水中杂质颗粒的含量.不同PAC补投量条件下,再絮凝不同时间后的沉后水剩余颗粒数的变化如图4所示.可以看出,随着再絮凝时间的增加,沉后水剩余颗粒数不断降低,但颗粒数降低的速率与投药量有关.不补投PAC时,剩余颗粒数的变化非常缓慢,再絮凝结束时,沉后水剩余颗粒数为275个·mL-1,去除率仅为19.35%.该现象说明PAC絮体发生破碎后,产生了大量的微小絮体颗粒,该部分颗粒在再絮凝过程中不能有效地凝结为大絮体,沉降性能降低.再次投加PAC后,随着投药量的升高,沉后水剩余颗粒数呈现先降低后升高的趋势.补投量较低时(1 mg/L),颗粒数有较高的去除效率,再絮凝结束后,沉后水剩余颗粒数为145个·mL-1,去除率为56.06%.再次投加PAC后,由于其较强的电中和能力及网捕卷扫能力,可以很好地将微小絮体颗粒凝结成较大的絮体,从而降低了系统中颗粒的数量.提高PAC的补投量,剩余颗粒数进一步降低,当补投量为2 mg/L时,剩余颗粒数降低到90个·mL-1,去除率为73.45%,继续增加混凝剂的补投量,剩余颗粒数降低并不明显.当PAC补投量较高时(>6 mg/L),剩余颗粒数随投药量的升高也不断提高,这可能是过量的PAC使得絮体表面的电荷发生转换,增大了颗粒间的排斥力,阻碍了颗粒间的有效碰撞,进而导致剩余颗粒数增多.
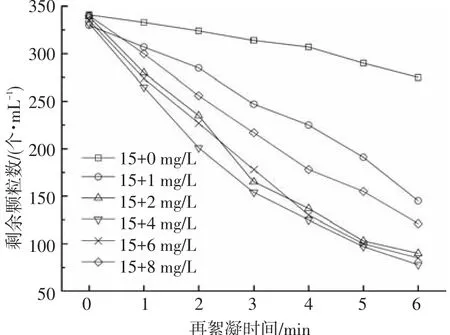
图4 再次投加PAC对出水剩余颗粒的影响
比较图3、4可知,沉后水剩余浊度与剩余颗粒数的变化规律基本相似,说明水中浊度与颗粒数具有一定的相关性.由此可得,浊度和颗粒数均可用于表征原水中胶体及杂质颗粒的含量.
3 结论
1)再次投加PAC可以明显改善絮体破碎后的再絮凝能力,增大絮体粒径及生长速率,提高浊度及颗粒数的去除效果,降低沉后水浊度及颗粒数.
2)随PAC补投量的升高,絮体的粒径先增大后减小,投药量为4 mg/L时,粒径达到最大为408 μm;絮体生长速率先升高后降低,生长速率达到最大值100.11 μm/min所需投药量为6 mg/L.
3)当PAC补投量从0升高到2 mg/L时,大絮体明显增多,小絮体显著降低,280~630 μm絮体颗粒由22.85%增大到46.36%,4~35 μm絮体颗粒由1.21%减小至0.19%.
[1]SUN J,QIN L,LI G S,et al.Effect of hydraulic conditions on flocculation performances and floc characteristics in Chinese herbal extracts by chitosan and chitosan hydrochloride[J].Chemical Engineering Journal,2011,225:641-649.
[2]TAMBON, WATANABEY.Physicalaspect of flocculation — I:fundamental treatise[J].Water Research,1979,13:429-439.
[3]XIAO F,HUANG J C H,ZHANG B J,et al.Effects of low temperature on coagulation kinetics and floc surface morphology using alum[J].Desalination,2009,237:201-213.
[4]JARVIS P,JEFFERSON B,GREGORY J,et al.A review of floc strength and breakage [J].Water Research,2005,39:3121-3137.
[5]LI T,ZHU Z,WANG D S,et al.The strength and fractal dimension characteristics of alum-kaolin flocs[J].International Journal of Mineral Processing,2007,82:23-29.
[6]YU W Z,GREGORY J,CAMPOS L.The effect of additional coagulant on the re-growth of alum-kaolin flocs [J].Separation and Purification Technology,2010,74(3):305-309.
[7]WEI J C,GAO B Y,YUE Q Y,et al.Strength and regrowth properties of polyferric-polymer dual-coagulant flocs in surface watertreatment[J].Journalof Hazardous Materials,2010,175:949-954.
[8]MIKKELSEN L H,KEIDING K.The shear sensitivity of activated sludge:an evaluation of the possibility for a standardised floc strength test[J].Water Research,2002,36:2931-2940.
[9]WANG Y,GAO B Y,XU X M,et al.Characterization of floc size,strength and structure in various aluminum coagulants treatment[J].Journal of Colloid and Interface Science,2009,332:354-359.
[10]MCCURDY K,CARLSON K,GREGORY D.Floc morphology and cyclic shearing recovery:comparison of alum and polyaluminium chloride coagulants [J].Water Research,2004,38:486-494.
[11]XU W Y,GAO B Y,YUE Q Y,et al.Effect of shear force and solution pH on flocs breakage and re-growth formed by nano-Al13polymer[J].Water Research,2010,44:1893-1899.
[12]JARVIS P,JEFFERSON B,PARSONS S.Breakage,regrowth,and fractal nature of natural organic matter flocs[J].Environmental Science and Technology,2005,39:2307-2314.
[13]JARVIS P,JEFFERSON B,PARSONS S.The duplicity of floc strength [J].Water Science and Technology,2004,50(12):63-70.
[14]LIN Q T,PENG H L,LIN Q L,et al.Formation,breakage and re-formation of flocs formed by cationic starch [J].Water Science and Technology,2013,68(6):1352-1358.
[15]YUKSELEN M A,GREGORY J.The effect of rapid mixing on the break-up and re-formation of flocs[J].Journal of Chemical Technology and Biotechnology,2004,79:782-788.
[16]YUKSELEN M A,GREGORY J.Breakage and reformation of alum flocs[J].Environmental Engineering Science,2002,19(4):229-236.
[17]YU W Z,LI G B,XU Y P,et al.Breakage and regrowth of flocs formed by alum and PACl[J].Powder Technology,2009,189:439-443.
[18]YU W Z,GREGORY J,CAMPOS L C.Breakage and re-growth of flocs formed by charge neutralization using alum and polyDADMAC [J].Water Research,2010,44:3959-3965.
[19]WANG D S,WU R B,JIANG Y Z,et al.Characterization of floc structure and strength:role of changing shear rates under various coagulation mechanisms[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects,2011,379:35-42.
[20]RONGH Y, GAOBY, DONGM, etal.Characterization of size,strength and structure of aluminum-polymer dual-coagulant flocs under different pH and hydraulic conditions[J].Journal of Hazardous Materials,2013,252/253:330-337.
[21]VAHEDIA,GORCZYCA B.Application offractal dimensions to study the structure of flocs formed in lime softening process[J].Water Research,2011,45:545-556.
[22]YU W Z,GREGORY J,CAMPOS L.Breakage and regrowth of Al-Humic flocs-effect of additional coagulant dosage [J].Environmental Science and Technology,2010,44:6371-6376.
[23]ZHAO Y X,GAO B Y,SHON H K,et al.The effect of second coagulant dose on the regrowth of flocs formed by charge neutralization and sweep coagulation using titanium tetrachloride (TiCl4) [J].Journalof Hazardous Materials,2011,198:70-77.
[24]XOAO F,ZHANG X R,LEE C.Is electrophoretic mobility determination meaningful for aluminum(III)coagulation of kaolinite suspension[J].Journal of Colloid and Interface Science,2008,327:348-353.
[25]YU W Z,GREGORY J,CAMPOS L.Breakage and regrowth of flocs:effect of additional doses of coagulant species[J].Water Research,2011,45:6718-6724.
