富锂正极材料0.5Li2MnO3·0.5LiNi1/3Co1/3Mn1/3O2的微波合成及电化学性能研究
2015-08-22解亚峰江学范
解亚峰,章 涵,徐 越,钱 斌,江学范,杨 刚
(1.常熟理工学院 化学与材料工程学院,江苏 常熟 215500;2.中国矿业大学 化工学院,江苏 徐州 221116)
富锂正极材料0.5Li2MnO3·0.5LiNi1/3Co1/3Mn1/3O2的微波合成及电化学性能研究
解亚峰1,2,章涵2,徐越2,钱斌1,江学范1,杨刚1
(1.常熟理工学院 化学与材料工程学院,江苏 常熟 215500;2.中国矿业大学 化工学院,江苏 徐州 221116)
采用共沉淀制备前驱体,微波高温固相烧结制备富锂正极材料0.5Li2MnO3·0.5 LiNi1/3Co1/3Mn1/3O2.通过X射线衍射(XRD)、电镜扫描SEM、循环伏安(CV)、充放电性能等材料结构的表征和电化学性能测试,研究了不同烧结时间(微波3 min、5 min、7 min、15 min)对材料结构电化学性能的影响.发现较佳的合成条件所合成的富锂正极材料0.5Li2MnO3·0.5 LiNi1/3Co1/3Mn1/3O2结构是α-NaFeO2型,为二维层状结构.在2.0~4.8 V的截止电压范围、17 mAh·g-1的电流密度,首次放电容量为284.6 mAh·g-1,20个循环容量的保有率为75.6%.通过微波高温烧结合成正极材料,研究了制备工艺对材料结构和电化学性能的影响,并探讨了该体系的应用前景.
锂离子电池;富锂正极材料;共沉淀;微波高温固相合成
1 引言
在21世纪,能源是各国关注的重点.面对日益枯竭的石油资源,寻找过渡能源或者新能源成为共识[1].在我国,汽车排放污染已成为城市大气污染的重要因素.因此,发展零排放的电动汽车可以大大减少有害气体排放.可充电锂离子电池因其具有高电压、比能量大、循环寿命长、安全性能好、自放电小、可快速充放电、工作温度范围高等优异性能而成为电动交通工具的储电单元[2-3].
电极材料是锂电池的核心,是决定电池基本特性的重要组成部分.锂离子电池性能的提高在很大程度上取决于正极材料的发展,因此锂离子电池正极材料的研究比较活跃.目前商业化的锂离子电池均采用LiCoO2作为正极材料,但钴为战略资源,储量有限且有毒,虽然理论容量为274 mAh·g-1,但实际可逆容量只有140 mAh·g-1,在较高温度下LiCoO2热稳定性和安全性能差[4].LiNiO2实际容量可达190~210 mAh·g-1,但制备条件苛刻,材料的热稳定性差,可逆容量下降较快,容易产生安全问题,因此较难得到工业应用[5].层状的LiMnO2在循环过程中会发生晶型的转变[6];而尖晶石LiMn2O4成本虽低,但比容量和循环性能差[7].综合考虑LiCoO2良好的循环性能,LiNiO2高比容量和LiMn2O4高安全性和低成本等特点,可组成含有镍、钴、锰三元素协同的新型过渡金属嵌锂氧化物复合材料.在该复合材料中,Co能使锂离子脱嵌更容易,能提高材料的导电性和改善其充放电循环性能[8].但随Co的比例增加,材料的可逆嵌锂容量下降[9].Ni的存在有利于提高材料的可逆嵌锂容量,但过多Ni的存在会使材料的循环性能恶化.Mn的含量太高容易出现尖晶石相而破坏材料的层状结构[10].一般认为电极材料应具有单相、高纯、均一的颗粒和窄的尺寸分布以及大的比表面积[11].目前,具有Ni-Co-Mn三元素协同效应的功能材料备受国内外关注,已经成为新材料研究的热点.
锂电池正极材料的制备方法很多,有溶剂热法合成、高温反应法、传统共沉淀法、溶胶-凝胶法、低温固相反应法、电化学合成法.最常用的方法是固相反应法,热能通过对流、传导、辐射等方式传递到被加热物体上,被加热体由表及里传热使物体达到某一温度.而微波加热是介质材料自身损耗电磁场能量而发热,属整体加热方式,电磁场直接作用于介质分子转换成热,且透射性能使介质内外同时受热,不需要热传导,并具有加热速度快、均匀加热、节能高效等优点.
尽管已有溶剂热法合成、高温反应法、传统共沉淀法、溶胶-凝胶法、低温固相反应法等制备富锂型锂电池正极材料的报道,不过微波高温固相合成该类材料尚未见报道.本文采用共沉淀方法制备前躯体,在不同微波合成条件下制备一系列0.5Li2MnO3·0.5 LiNi1/3Co1/3Mn1/3O2材料,系统研究了所得材料的晶体结构、形貌及其电化学性能,探讨了微波水热合成条件对材料结构和性能影响的关键因素.
2 实验部分
按化学计量称量定量的分析纯CoAc2·4H2O、NiAc2·4H2O、MnAc2·2H2O、LiOH·H2O、柠檬酸,其中LiOH· H2O过量10%.将三种醋酸盐用去离子水搅拌溶解并混合,制成溶液A.以柠檬酸作为螯合剂,将其与氢氧化锂一起用去离子水溶解,制成溶液B.将A液滴入B液中,控制每秒钟1滴,使OH-1能完全和金属离子形成沉淀.滴定完成后,将所得溶液静置2~3 h,再离心多次洗涤,洗去其中的Li+离子,放入120℃的烘箱中干燥12 h.称取适量共沉淀前躯体,按照化学计量比加入LiOH·H2O研磨,在空气中450℃下预烧3 h,随后在氧气氛下900℃分别用微波烧结3 min、5 min、7 min、15 min,所制的正极材料分别命名为co-3 min,co-5 min,co-7 min,co-15 min.
对以上所得的样品进行XRD和SEM表征测试:采用日本理学D-MAX 2200PC型X射线粉末衍射仪对所得样品的晶体结构进行分析,使用Cu-Ka辐射源,波长为1.546 Å,采用Ni滤波片,管流为20 mA,管压为40 kV,扫描速率为4°/min,扫描范围10°~80°,步长为0.02°.通过Rietveld分析,使用常规结构分析系统(GSAS)来测定上述合成的晶胞参数[2-3],形貌通过电子扫描电镜(SEM,Hitachi-X650 microscope,20 kV)测量获得.
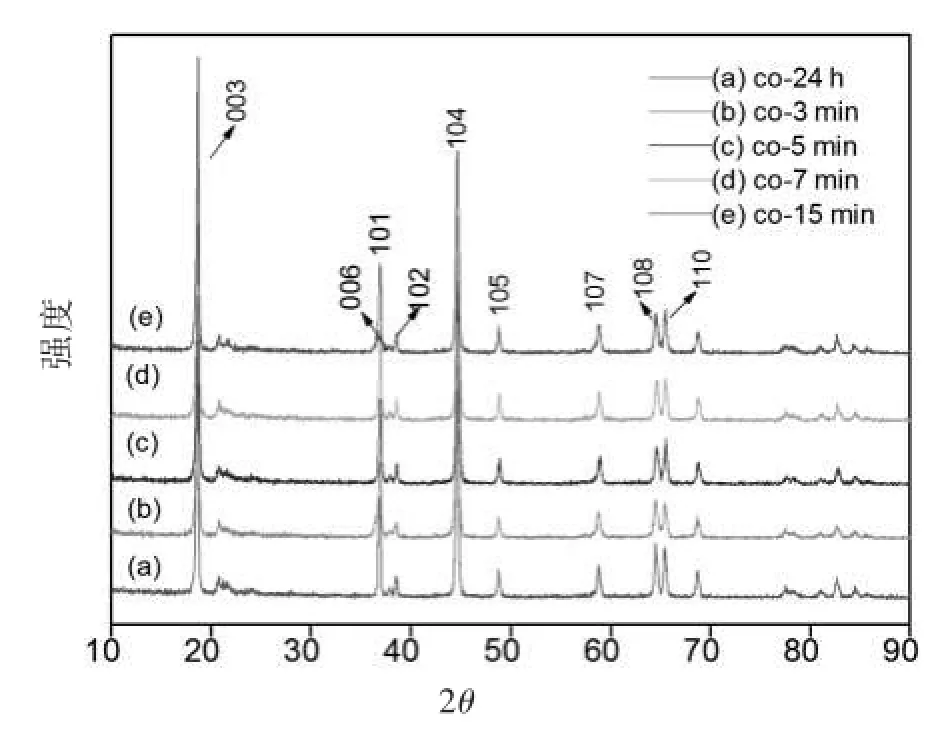
图1 不同微波烧结时间所得样品的XRD图谱
为了对合成的正极材料的电性能进行综合评估,将合成的正极材料装配成CR2016锂离子钮扣式电池.样品0.5Li2MnO3·0.5 LiNi1/3Co1/3Mn1/3O2、乙炔黑和PTFE按照质量比70:20:10称量,先将样品和乙炔黑研磨约0.5 h成细腻的黑色物质,在加入粘合剂PTFE黏结成片状,然后用擀膜机将混合物擀成光亮厚度均匀的膜,120℃真空干燥,切成片状,称量质量,最后在手套箱中组装电池.本实验使用2016纽扣电池壳,负极材料用锂片,隔膜为celgardC480,313电解液(溶解有六氟磷酸锂的碳酸酯类溶剂的有机电解液),使用泡沫镍为电池填充物.充放电性能在Land CT2001A上测试,截止电压为2.0~4.8 V,17 mAh·g-1的充放电电流密度.采用恒流-恒压(CC-CV),恒流放电(CC).活性物质按正极材料质量的百分比计算.电化学阻抗测试条件为:频率在10 mHz~100 KHz,交流电压幅值为5 V.循环伏安测试前将组装好的电池静置6 h,在2.0~4.8 V之间,以17 mAh·g-1电流密度进行循环性能测试,考察材料的循环性能.
3 结果与讨论
图1为不同微波合成时间制备的样品XRD谱图.从图中可以看出,与标准图谱一致,在20°~25°之间有Li2MnO3的特征峰,可按层状α-NaFeO2结构指标化,即Li+占据3a位置,M(Ni2+、Co3+、Mn4+)离子均匀占据3b位置,O2-占据6c位置,说明制备的材料中无杂质相,为很好的二维层状结构的化合物. (108)峰和(110)峰分裂明显,说明富锂材料层状结构良好,结构为α-NaFeO2型.通常XRD图谱中(003)与(104)衍射峰的强度之比I(003)/I(004)应高于1.2,意味着层状结构存在极少的离子混杂现象(即少量锂离子占据过渡金属离子位,而相同数量的过渡金属离子占据了锂位),如果出现离子混杂程度提高则比值将下降,我们制得的正极材料I(003)/I(004)的比值均超过1.2,表明微波快速合成的材料具有较理想的层状结构.

图2 微波合成样品(a)co-3 min,(b)co-5 min,(c)co-7 min,(d)co-15 min的SEM图谱
微波合成样品的扫描电镜图示于图2.四个样品形貌均为固体颗粒状,粒径大约在0.5~3 μm之间.随着微波合成时间的延长,颗粒尺寸逐渐增大.不过5 min样品具有较为严重的颗粒团聚现象,对其电化学性能影响将比较大.电极材料的形态和粒径对锂离子电池的性能有着重要的影响.球形电极材料具有较高的堆积密度,有利于提高活性物的装填量,从而提高电池的体积比容量.7 min样品具有较小粒径和较为均匀的颗粒度分布.球形电极材料颗粒拥有较小的比表面积,可减少与电解液的接触面积,抑制电解液分解对电池性能产生的恶性作用,可改善电池的循环特性.
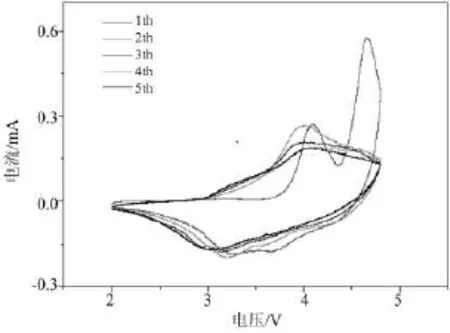
图3 co-7 min样品的循环伏安曲线(扫描速率0.1 mV s-1)
图3为co-7 min样品的循环伏安测试.在2.0~4.8 V范围内,不同循环次数显示出谱峰的变化曲线.在首次充电过程中,出现了两个氧化峰,分别为过渡金属离子Co3+的氧化和“Li2O”的脱出,其电位分别为4.0 V和4.5 V[12];首次放电过程在3.7 V的还原峰表示Co4+的还原,而后续循环中也出现了3.5 V以下的还原峰,该还原峰表示Mn4+还原成Mn3+的过程.后续循环充电过程的4.5 V峰没有再次出现,说明“Li2O”的脱嵌是不可逆的.
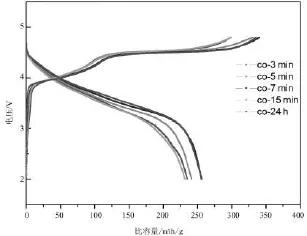
图4 微波合成样品的首次充放电曲线
充放电容量是衡量电池材料的一个重要指标,图4为不同微波烧结条件合成样品的首次充放电曲线.从上图可以看出,在首次充放电过程中,所有样品均出现了富锂材料的特征曲线.即充电过程中4.1 V和4.5 V有两个平台,位于4.1 V左右的充电平台是由于在充电过程中锂离子脱出的同时Co3+被氧化;位于4.5 V的平台是基于Li2MnO3的富锂材料电化学活化过程,此平台的出现是富锂材料比容量较大的原因之一.表1列出各个样品前两圈放电比容量和放电效率.可以看出随着微波反应时间的增加,容量呈先递增再递减的趋势,其中首圈容量最高的是co-7 min正极材料,其比容量为256.1 mAh·g-1,其次co-5 min的正极材料,其比容量为241 mAh·g-1,co-15 min的正极材料最差为216 mAh·g-1,和最高的相差40 mAh·g-1,这表明反应时间对材料的电化学性能有较大影响.反应时间适当延长可使一些中间产物通过进一步反应,最终获得结晶度较高的正极材料,但是过长或过短虽能得到所需结构,但是容量都会有所衰减.这可能是反应时间过长导致结晶时间的增加,会在原有的颗粒基础上继续结晶造成颗粒过大,粒径也变大,影响了电化学性能.而反应时间过短会造成晶粒生长不完全,不能达到理想的结构形态,导致容量不高.
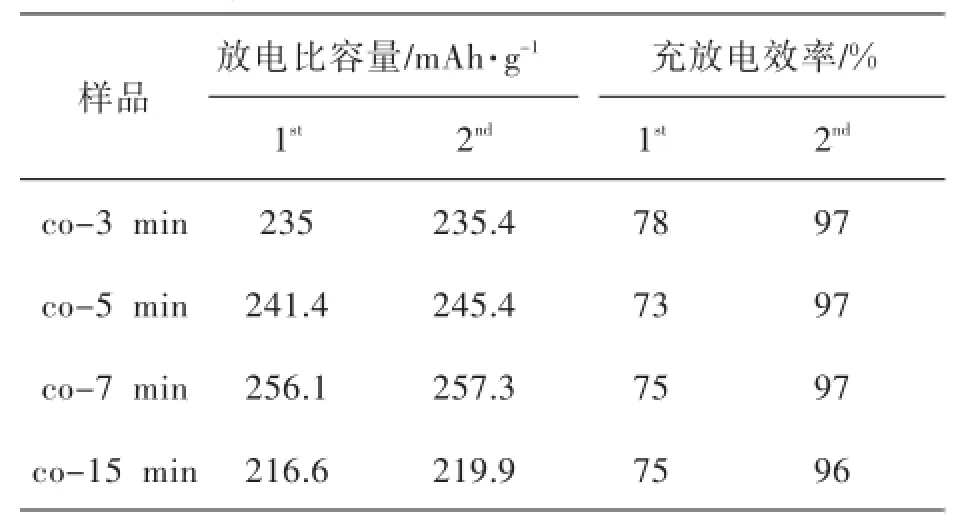
表1 微波合成样品的前两圈放电比容量和放电效率
由表1可看出,不同条件下共沉淀样品都有一个共性,首次充放电的效率比较低,表现出较大的不可逆容量.这是因为Li2MnO3类富锂材料存在首次电化学活化过程,同时由于Ni2+的半径和Li+的半径比较接近,存在少量Ni2+占据Li+晶格点的趋势,发生阳离子混排[13].阳离子混排会破坏电极材料的性能,降低电极的可逆容量,增加电极的极化.由于发生了一定程度的阳离子混排,在放电结束时,发现Ni2+/Ni4+间的不充分还原,这可能是首次充放电过程中容量损失的原因之一.但在随后的充放电过程中,所有样品的放电效率就明显提高,容量损失不大.如表1,co-3 min、co-5 min、co-7 min、co-15 min的第二次循环的充放电效率分别为97%、97%、97%和96%.
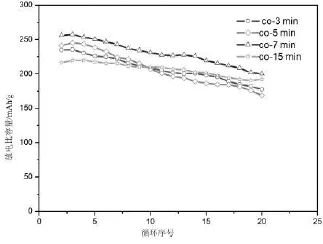
图5 微波合成样品的前20圈充放电循环曲线
循环性能也是衡量正极材料电化学性能的一个重要指标.图5是微波高温合成样品的充放电循环性能,容量都有一定幅度的衰减.其中,样品co-7 min显示出较好的充放电循环性能,在20个循环的时候co-7 min样品的容量仍有225 mAh·g-1,而co-3 min、co-5 min、co-15 min样品的放电容量分别为190、202和188 mAh·g-1.
当电流通过电极时,在电极上发生四个基本的电极过程:溶液中离子的电迁移过程;反应物和产物的扩散过程;电极界面双电层的充放电过程;电化学反应过程.这些过程都会对电流产生一定的阻抗,可以通过电化学阻抗谱来测定.通过电化学交流阻抗研究,可以获得富锂材料在充放电过程中的电化学行为.图6为微波合成样品的交流阻抗谱,Nyquist谱图主要包括三个部分:一是高频区的第一个半圆弧,反映的是锂离子通过表面膜层的迁移电阻和表面膜层的电容;二是位于中频区的第二个半圆弧,反映的是传荷电阻和电极与电解液之间界面电容;三是位于低频区的一条斜率为45°的直线,反映的是锂离子在固体电极材料中的扩散能力,即Warburg阻抗.在不同充放电循环后,样品的高频弧变化都较小,这说明SEI膜一经形成,相对比较稳定,不随循环圈数的增加而有很大变化.但同时也可以看出随着圈数的增加,其高频弧的直径再增大,说明其界面阻抗在增大,降低了Li+的导电率,不利于锂离子过程的快速迁移.此外,随着循环圈数的增加,中频区域得到一个发展不完全的半圆弧,且其直径随循环圈数的增加在不断的增大,以至于和低频区的Warburg阻抗混合在一起无法识别,这表明电荷转移引起的阻抗随循环圈数的增加逐步增大,由于大量的锂离子在电压平台区间迁移,且首次充电过程中会有“Li2O”的脱出,这是导致电荷转移阻抗增加的主要原因,另外,电解液与富锂材料0.5Li2MnO3·0.5 LiNi1/3Co1/3Mn1/3O2的副反应的发生,导致Li+脱嵌阻力增大也是其原因之一.
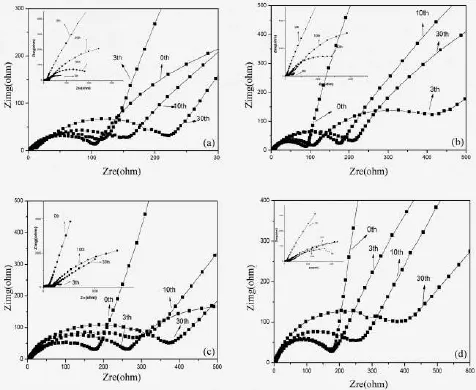
图6 微波高温合成样品(a)co-3 min(b)co-5 min(c)co-7 min(d)co-15 min交流阻抗谱图
4 结论
本文采用共沉淀制备前驱体,采用微波高温固相烧结制备了富锂正极材料0.5Li2MnO3·0.5 LiNi1/3Co1/3Mn1/3O2.微波快速合成的材料具有较理想的层状结构和较高的结晶度.微波合成样品形貌均为固体颗粒状,粒径大约在0.5~3 μm之间,其中7 min样品具有较小粒径和较为均匀的颗粒度分布.微波反应时间对所得材料的电化学性能有较大影响.在较长的微波反应时间,中间产物能够进一步反应生成结晶度较高的材料.但是反应时间过长,导致材料颗粒度偏大,锂离子和电子的扩散与传输难度增加,进而材料的电化学性能有所降低.反应时间过短,虽然产物颗粒度较小,但是会造成晶粒生长不完全,不能达到理想的结构形态,导致材料的电化学容量不高.通过优化微波合成条件,其中co-7 min正极材料具有较佳的晶体结构和形貌及较好的电化学性能,其比容量为256 mAh·g-1,在20个循环后仍有225 mAh·g-1.
[1]Tarascon J M,Armand M.Issues and challenges facing rechargeable lithium batteries[J].Nature,2001,414:359-367.
[2]Song H K,Lee K T,Kim M G,et al.Recent Progress in Nanostructured Cathode Materials for Lithium Secondary Batteries[J].Adv Funct Mater,2010,20:3818-3834.
[3]Zhang X,Yu C,Huang X,et al.Novel composites Li[LixNi0.34 xMn0.47Co0.19]O2(0.18≤x≤0.21):Synthesis and application as high-voltage cathode with improved electrochemical performance for lithium ion batteries[J].Electrochim Acta,2012,81:233-238.
[4]Madhavi S,subbaRao G V,Chowdari B V R,et al.Effect of Cr dopant on the cathodic behavior of LiCoO2[J].Electrochimica Acta, 2002,48:219-226.
[5]Zou M J,Yoshio M,GoPukumar S.Synthesis of High-Voltage(4.5 V)Cycling Doped LiCoO2for Use in Lithium Rechargeable Cells [J].Chem Mater,2003,15:4699-4702.
[6]Li X,Wei Y J,Ehrenberg H.Characterizations on the structural and electrochemical properties of LiNi1/3Mn1/3Co1/3O2prepared by a wet-chemical process[J].Solid State Ionics,2008,178%1969-1974.
[7]Yabuuchi N,Ohzuku T.Electrochemical behaviors of LiCo1/3Ni1/3Mn1/3O2in lithium batteries at elevated temperatures[J].J PowerSources,2005,146:636-639.
[8]Sébastien P,Marca MD.Direct synthesis of LiNi1/3Co1/3Mn1/3O2from nitrate precursors[J].Electrochemistry Communications,2004, 6:767-772.
[9]Belharouak I,Sun Y K,Liu L.Li(Ni1/3Co1/3Mn1/3)O2as a suitable cathode for high power applications[J].J Power Sources,2003,123: 247-252.
[10]Itagaki M,Kobari N,Yotsuda S.In situ electrochemical impedance spectroscopy to investigate negative electrode of lithium-ion re⁃chargeable batteries[J].J Power Sources,2004,135:255-261.
[11]Itagaki M,Kobari N,Yotsuda S.LiCoO2electrode/electrolyte interface of Li-ion rechargeable batteries investigated by in situ elec⁃trochemical impedance spectroscopy[J].J Power Sources,2005,148:78-84.
[12]Johnson C S,Li N,Lefief C,et al.Synthesis,Characterization and Electrochemistry of Lithium Battery Electrodes:xLi2MnO3·(1-x)LiMn0.333Ni0.333Co0.333O2(0≤x≤0.7)[J].Chem Mater,2008,20:6095-6106.
[13]Shi S J,Tu J P,Tang Y Y,et al.Combustion synthesis and electrochemical performance of Li[Li0.2Mn0.54Ni0.13Co0.13]O2with improved rate capability[J].J Power Sources,2013,228:14-23.
Microwave-assisted Preparation of 0.5Li2MnO3·0.5 LiNi1/3Co1/3Mn1/3O2and the Enhanced Electrochemical Performances
XIE Ya-feng1,2,ZHANG Han2,XU Yue2,QIAN Bin1,JIANG Xue-fan1,YANG Gang1
(1.School of Chemistry and Material Engineering,Changshu Institute of Technology,Changshu 215500,China;
2.College of Chemical Engineering,China University of Mining and Technology,Xuzhou 221116,China)
With the increasing global demand for energy,one of the specific requirements is positive electrode material with high capacity,low cost and environmental.Recently,Li-rich cathodes written as Li1+x[M]1-xO2(M: Mn,Ni,and Co;x>0)have caught great attention for the novel electrode materials of lithium ion batteries. 0.5Li2MnO3·0.5 LiNi1/3Co1/3Mn1/3O2has been synthesized by co-precipitation and microwave sintering(MW).MW time is systematically optimized.The crystal structure and morphology are characterized by XRD,SEM,etc. XRD patterns are refined by two sets of diffraction data(R-3m and C2/m)and indicate that the as-synthesized material is pure and has good crystallinity.0.5Li2MnO3·0.5 LiNi1/3Co1/3Mn1/3O2synthesized at 900°C for 7 min has the best discharge capacity and cyclic performance.Within the cut-off voltage between 2.5 and 4.8 V,the initial discharge capacity is 325 mAh·g-1 at 0.1 C rate;and after 50 cycles the discharge capacity remains 284.6 mAh·g-1,with good reversibility(75.6%).Through the studies of this paper,the authors have a further understanding of the preparation,structure,morphology and electrochemical performance of Li-rich cathode ma⁃terial,which helps to provide a basic research and practical application for Li-rich cathode material in the fu⁃ture.
lithium-ion battery;cathode materials;co-precipitation;microwave-assisted solid-state synthesis
TM242
A
1008-2794(2015)02-0037-06
2015-01-08
国家自然科学基金项目“石墨烯/LiMPO4(M=Mn,Fe)原位复合结构的制备及其锂离子电池领域的应用”(51172032);江苏省自然科学基金项目“高性能锂电池正极材料镍锰酸锂的合成及其电化学性能”(BK20141229)
通讯联系人:杨刚,教授,博士,研究方向:储电功能材料,E-mail:gyang@cslg.cn.
