三种性状赭石不同煎出液中铅溶出度对比研究
2015-05-04康莲薇熊南燕许忠新
康莲薇, 熊南燕, 许忠新
(1. 河北工程大学 理学院, 河北 邯郸 056001; 2. 河北工程大学 医学院, 河北 邯郸 056001)
三种性状赭石不同煎出液中铅溶出度对比研究
康莲薇1, 熊南燕2, 许忠新2
(1. 河北工程大学 理学院, 河北 邯郸 056001; 2. 河北工程大学 医学院, 河北 邯郸 056001)
目的:观察肾状、鲕状、豆状3种性状赭石生品及其制品中铅元素在醋煎液、水煎液2种不同溶剂中的溶出度差异;方法:采用紫外分光光度法,在一定波长下测定样本在不同煎出液中铅含量;结果:3种性状赭石在醋煎液和水煎液中铅的溶出度有较大差异(P<0.01);结论:3种性状赭石同等入药不妥。
赭石; 醋煎液; 水煎液; 铅元素溶出度
矿物药赭石(Haematitum)为常用中药,为氧化物类矿物刚玉族赤铁矿,主含三氧化二铁(Fe2O3)。赭石存在有3种性状,鲕状、豆状、肾状, 2010年版中国药典赭石项下,将3种性状的赭石均作为赭石入药[1]。课题组在前期对3种性状赭石成分、药理等方面的研究结果显示,3种性状赭石无论从所含成分上,还是药理作用上均存在有较大差异,同为赭石入药似有不妥[2-3]。本研究采用紫外分光光度法进一步对3种性状赭石及其制品进行了水煎液、醋煎液中铅溶出度的对比研究。结果显示,不同煎出液中各样本间铅溶出度亦存在较大差异,将3种不同性状赭石同为赭石入药可能会因为铅的溶出度不同而使疗效有所差异。还由于矿物质中铅含量的高低会影响到用药者的安全,所以,建议药典委员会应在新版药典中有铁含量的质量标准前提下同时建立赭石生品及制品含铅量的限量标准。
1 仪器与材料
仪器:紫外分光光度计(Lambda 35,美国)。
材料:无铅水、硝酸、氨水、柠檬酸铵、盐酸羟胺和硝酸铅(分析纯),氯仿、双硫腙、酚红。豆状、肾状、鲕状赭石采自张家口市庞家堡铁矿,经邯郸市药品检验所鉴定;豆状、肾状、鲕状赭石醋制品由邯郸市滏华中药颗粒饮片有限公司制备,邯郸市药品检验所鉴定。
2 方法与结果
2.1 溶液的配制
0.5%双硫腙氯仿储备液[4]:溶解0.05 g双硫腙于50 mL氯仿中(如有不溶物质须过滤);将溶液移入250 mL的分液漏斗中,用100 mL稀氨水溶液分4次提取,此时双硫腙进入氨水溶液中,弃去氯仿层;将氨提取液经脱脂棉过滤,于分液漏斗中,用稀盐酸酸化至有双硫腙沉淀析出;用氯仿萃取2~3次,每次约20 mL,此时双硫腙进入氯仿层;用水洗氯仿萃取液2次,弃去洗液,加氯仿至100 mL,使成为约0.05%双硫腙氯仿溶液,放入棕色瓶中,保存在冰箱中备用[4]。
双硫腙氯仿应用液[5]:取双硫腙氯仿储备液1 mL,加入氯仿至10 mL,用0.5 cm比色杯,以氯仿为参比液调零,于波长510 nm处用分光光度计测吸光度A,用下式计算配制100 mL双硫腙氯仿应用液(透光度85%)所需双硫腙氯仿储备液的体积V:V=10×(2-lg85)/A=2.22/A,计算得到V为0.15 mL。取0.15 mL氯仿储备液于100 mL的容量瓶中,加氯仿至刻度,制得双硫腙氯仿应用液[5]。
0.04%酚红溶液的配制[6]:称取0.1 g酚红放入小研钵中,加无铅水研磨溶解后,倒入250 mL容量瓶中,加水至刻度[6]。
50%柠檬酸铵溶液[7]:称取25 g柠檬酸铵,加适量水溶解后,加入酚红指示剂数滴,用氨水调节溶液为红色,加水稀释至50 mL;将其转移至250 mL分液漏斗中,每次用0.01%双硫腙氯仿溶液5 mL萃取铅,直至新加入的双硫腙氯仿溶液振摇2 min后,保持绿色不变为止。残留的双硫腙用氯仿反复洗涤至氯仿无色为止,弃去氯仿层[7]。
铅标准溶液配制(1.0 g/L)[8]:精密称取硝酸铅0.159 8 g(105 ℃烘干2 h),加入10 mL浓硝酸(优级纯)及少量无铅水溶解,倒入100 mL容量瓶中,加无铅水至刻度,混匀,储存备用[8]。
2.2 波长的选择
用铅的标准储备液配制式0.3 mg/L、0.35 mg/L浓度的铅标准溶液,以紫外分光光度计进行波长扫描,测得铅的最大吸收波长为520 nm。测定结果见表1,表中A1、A2分别为0.3 mg/L和0.35 mg/L标准储备液的吸光度。
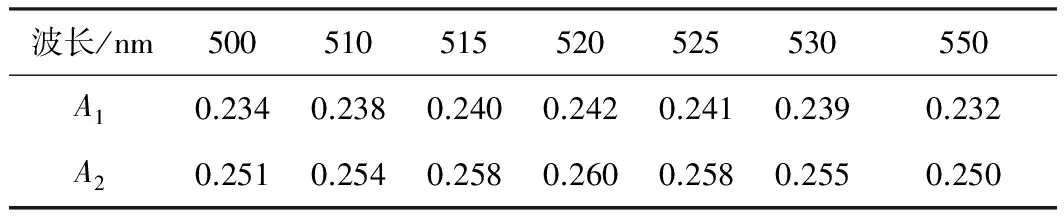
表1 铅标准溶液的吸收波长与吸光度
2.3 标准曲线制备
准确量取1.0 g/L硝酸铅的标准溶液0.2、0.3、0.4、0.5、0.6 mL分置于50 mL的容量瓶中,各加入50%柠檬酸铵0.5 mL、20%的盐酸羟胺溶液2滴及酚红指示剂2滴,摇匀;用1∶1氨水调至溶液呈红色,摇匀;加入双硫腙氯仿溶液5 mL,充分振摇;静置10 min,弃去水层,氯仿定容。在520 nm波长下以空白溶液为参比,测定各样品吸光度[9],结果见表2。
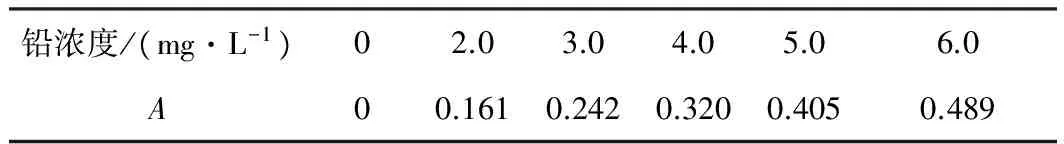
表2 铅系列标准溶液的浓度与吸光度
以铅浓度为横坐标,吸光度为纵坐标,绘制工作曲线。计算得到回归方程:y=0.8150x+0.01100,相关系数r=0.9801。
2.4 样品的制备
2.4.1 醋煎液样本的制备
豆状、肾状、鲕状赭石生品、制品各8批,研细过200目筛备用;精密称取各样本0.5 g分置于100 mL三角瓶中,分别加入pH为3.6的醋酸-醋酸钠缓冲溶液50 mL,加热,保持微沸30 min,冷却,过滤;滤液移入50 mL容量瓶以醋酸-醋酸钠缓冲溶液定容,制得生品24个、制品24个样本。
2.4.2 水煎液样本的制备
豆状、肾状、鲕状赭石生品、制品各8批,研细过200目筛备用;精密称取各样本0.5 g分置于100 mL的三角瓶中,加入50 mL纯化水,加热,保持微沸30 min,冷却,过滤;滤液移入50 mL容量瓶中,加纯化水定容,制得生品24个、制品24个样本。
2.5 测定方法的回收率实验
以一份肾状赭石生品样本为例操作如下。
2.5.1 醋煎液回收率实验
取50 mL容量瓶2只并标注为A和B。精密量取已制得的肾状赭石生品中任意一个醋煎液样本10 mL置于A瓶中,加入50%柠檬酸铵0.5 mL,20%的盐酸羟胺溶液2滴,酚红指示剂2滴,摇匀;用1∶1氨水(pH值为9~10)调至溶液呈红色,摇匀,加入2 mL、10%的氰化钾溶液,加入双硫腙氯仿应用液5 mL,用氯仿定容,充分振摇,静置10 min,弃去水层。精密量取同一样本10 mL置于B瓶中,加入2.1中铅标准溶液,其余与A处理相同。A样做本底,B样做加标样本,在520 nm波长下,以空白溶液作为参比,测定该样本的吸光度[10]。以第2.3节中的标准曲线计算铅的含量。结果见表3。
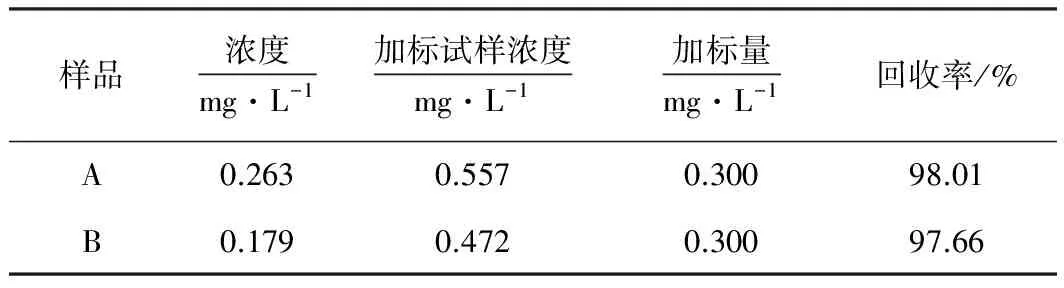
表3 赭石醋煎液回收率测定
2.5.2 水煎液回收率实验
取50 mL容量瓶2只并标注为A′和B′。精密量取已制得的肾状赭石生品中任意一个水煎液样本10 mL置于A′瓶中,加入50%柠檬酸铵0.5 mL,20%的盐酸羟胺溶液2滴,酚红指示剂2滴,摇匀;用1∶1氨水(pH值为9~10)调至溶液呈红色,摇匀;加入2 mL、10%的氰化钾溶液,加入双硫腙氯仿应用液5 mL,以氯仿定容充分振摇,静置10 min,弃去水层。精密量取同一样本10 mL置于B′瓶中,加入2.1中铅标准溶液,其余与A′法处理相同。A′样做本底,B′样做加标样本,在520 nm波长下,以空白溶液作为参比,测定该样本的吸光度[11]。以第2.3节中的标准曲线计算铅的含量。结果见表4。
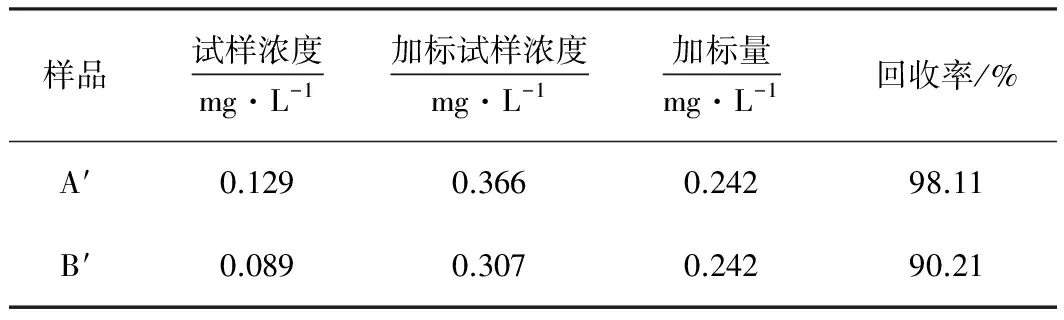
表4 赭石水煎液回收率测定
从回收率可看出,该方法可用于测定不同性状赭石样品中的铅含量。
2.6 实验测定
2.6.1 醋煎样品的测定
用第2.5.1节中的方法测定48个样本的醋煎液,各经5次重复实验,测得各样本中铅含量(数据略),对生品及制品测定结果分别经统计学处理,数据见表5。
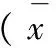
表5 各样本赭石醋煎液中铅含量比较±s,n=8)
注:组间两两比较,经q检验:均P<0.01。
2.6.2 水煎样品的测定
用第2.5.2节中的方法测定48个样本的水煎液,各经5次重复实验,测得各样本中铅含量(数据略),对生品及制品测定结果分别经统计学处理,数据见表6。
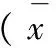
表6 各样本赭石水煎液中铅含量比较±s,n=8)
注:组间两两比较,经q检验:均P<0.01。
3 讨论
3.1 对结果的讨论
由表5可见,3种赭石生品在醋煎液中铅的溶出度有较大差异(P<0.01),制品在醋煎液中铅的溶出度也有较大差异(P<0.01)。由表6可见,3种赭石生品在水煎液中铅的溶出度有较大差异(P<0.01),制品在水煎液中铅的溶出度也有较大差异(P<0.01)。以上结果表明,3种赭石从铅在不同煎液中的溶出度差异较大,如果处方仅为赭石而没有写出给付的品种,则疗效会打折扣,3种性状赭石同等入药不妥。
实验结果表明:赭石醋煎液中铅的含量比水煎液中的铅含量高;赭石制品的水煎液和醋煎液中的铅含量低于赭石生品的水煎液和醋煎液的铅含量。赭石制品的水煎液铅含量很低。铅作为一种重金属元素,摄入过量会引起铅中毒,危害人体健康。临床上对赭石的生品、制品的水煎液和醋煎液应区别应用,且病终即止,不可久服。
3.2 对测定中影响因素的讨论
(1) pH值的影响。用双硫腙法测定铅的含量,溶液的pH值影响很大,无论单色法或混色法,pH值都应予以控制,最适宜pH值范围为8.5~11,仅铋、二价锡、铊等有干扰。在pH值为2~3时用双硫腙氯仿溶液进行萃取,则可除掉铋、二价锡的干扰。用碱性溶液对双硫腙氯仿进行反萃取,可使铅进入水层而与铊分离[12]。
(2) 溶剂的影响。氯仿作为溶剂,控制pH值在10左右,是提取铅的适宜条件。因该溶剂对双硫腙溶解度小,过量的双硫腙大部分留在水相中,仅双硫腙铅的螯合物及少量游离双硫腙进入有机相,因而形成的测定液几乎为单色[13]。
(3) 干扰的消除。盐酸羟胺作为还原剂,可保护双硫腙不被高价金属、过氧化物、卤族元素等氧化。柠檬酸铵在广泛的pH 范围内具有较强的络合能力,它的主要作用是络合钙、镁、铝、铁等阳离子,防止在碱性溶液中形成这些金属的氢氧化物沉淀。氰化钾络合剂的加入,可使许多金属离子形成稳定的络合物而被掩蔽[14]。
用配制好的试剂空白溶液作为参比溶液。由于反射以及溶剂、试剂等对光的吸收会造成透射光强度的减弱,为了使光强度的减弱仅与溶液中待测物质的浓度有关,必须对反射、溶剂、试剂的影响进行矫正。为此采用光学性质相同、厚度相同的比色皿贮参比溶液,调节仪器使透过参比皿的吸光度为零,然后让光束通过样品池,测得试液显色液的吸光度。通过参比皿的光强度作为样品池的入射光强度,这样测得的吸光度比较真实地反映了待测物质对光的吸收,也就能比较真实地反映待测物质的浓度[15]。
References)
[1] 国家药典委员会.《中华人民共和国药典》2005年版一部[M].北京:化学工业出版社,2005:257.
[2] 熊南燕,姜燕,王永艳,等.三种性状矿物药赭石指纹图谱研究[J].中药材,2008(1):36-38.
[3] 熊南燕,王永艳,姜燕.3种性状赭石的药理作用研究[J].时珍国医国药,2010(5):1133-1134.
[4] 胡亮,陈加希,王鲁民,等.双硫腙水相光度法快速测定水中微量铅[J].昆明理工大学学报:理工版,2007,32(6):81-83.
[5] 鲁长豪.食品理化检验学[M].北京:人民卫生出版社,1993:121-124.
[6] 陈正才,牟志浩,何忠绪.饮用水中铅测定方法的改进[J].中国卫生检验杂志,2008,18(12):2818,2842.
[7] 宋永华.改良双硫腙分光光度法测定水中铅的评价[J].四川省卫生管理干部学院学报,2007,26(4):266-267.
[8] 纪双利,杨丽,崔清华.双硫腙比色法测定空气中铅的质量控制[J].职业与健康,2008,24(19):2028-2029.
[9] 郭文录,丁卫国.双硫腙萃取分光光度法测定色漆涂料中的铅[J].电镀与精饰,2006,28(5):50-52.
[10] 王莹,辛士刚.化妆品中铅含量的测定[J].沈阳师范学院学报:自然科学版,2002,20(4):292-294.
[11] 郑典元,王春景,周雯,等.人工养殖海产品鲜样中铅的荧光分光光度测定法[J].环境与健康杂志,2008,25(5):433-435.
[12] 张毅忠,蒋玲,冯辉.在课堂教学中对食品样品中微量铅的研究与测定[J].中国科教创新导刊,2010(10):39-40.
[13] 汤明河.双波长分光光度法测定人发中痕量铅[J].温州大学学报,2001,14(3):88-90.
[14] 马淞江, 李方文, MA Song-jiang,等.用分光光度法测定电镀废水中的微量铅(Ⅱ) [J].材料保护,2007,40(2):75-76.
[15] 武汉大学.分析化学[M].5版.北京:高等教育出版社,2006:313-315.
Comparative study of dissolved lead from kidney-shaped ocher,oolitic ocher and lenticular ocher in different decoctions
Kang Lianwei1, Xiong Nanyan2, Xu Zhongxin2
(1. College of Science,Hebei University of Engineering,Handan 056001,China;2. School of Medicine,Hebei University of Engineering,Handan 056001,China)
Aim To investigate the dissolution discrepancy of lead element from the raw products and their products of kidney-shaped ocher,oolitic ocher and lenticular ocher in vinegar decoction and water decoction. Method Using the ultraviolet spectrophotometer under certain wavelength. Results The dissolution of lead from the three kinds of ochers in vinegar decoction and water decoction has a significant difference(P<0.01). Conclusion The three different kinds of ochers can’t be used as the same one in medicine.
ocher; vinegar decoction; water decoction; dissolution of lead element
2014- 09- 30
康莲薇(1965—),女,河北邯郸,硕士,研究方向为化学教学与研究.
R282.76;R282.5
B
1002-4956(2015)5- 0055- 04
