模拟训练(一)
2015-04-28王程杰
王程杰
1. 某些用途的钢材在出厂之前常经过发蓝处理,使其表面生成一层四氧化三铁,其主要目的是( )。
A. 增加钢材的硬度
B. 增强钢材的抗腐蚀能力
C. 使钢材美观
D. 增加钢材的韧性
2. 用自来水养观赏鱼时,通常先将自来水经日晒几天后,再注入鱼缸,其最主要目的是( )。
A. 利用紫外线杀死水中的细菌
B. 提高水温,有利于观赏鱼生长
C. 增加水中氧气的含量
D. 促使水中的次氯酸等余氯分解
3. 用人工方法在舞台上制造云雾缭绕的幻境的方法是( )。
A. 燃烧白磷
B. 燃烧镁粉
C. 施放干冰
D. 浓盐酸与浓氨水同时喷洒
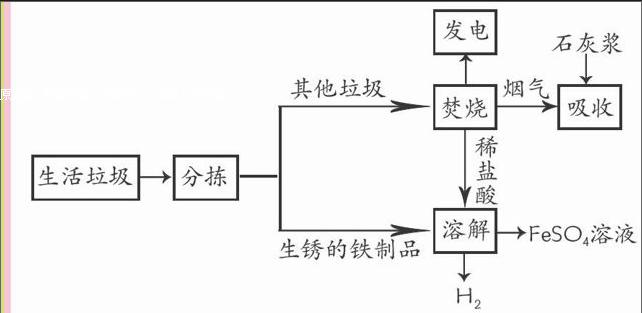
4. 城市生活垃圾的处理是世界性难题,某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程如下。
资料1:垃圾焚烧产生的烟气中含有SO2、HCl等有害气体。
资料2:+2价的铁元素容易被空气中的氧气氧化。
试回答下列问题:
(1)发电厂是利用垃圾焚烧产生的____转变为电能。
(2)吸收步骤中,石灰浆的作用是______________。
(3)溶解步骤中,产生H2的化学方程式为_____________。除此反应外,溶解步骤还能发生以下两个反应:
① Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
② Fe + Fe2(SO4)3 → 3FeSO4
其中属于化合反应的是___(填序号),反应前后铁元素的化合价不变的是___(填序号)。
(4)将所得硫酸亚铁溶液在氮气环境中加热蒸发浓缩、冷却结晶、_____(填操作名称),得到硫酸亚铁晶体,其中氮气的作用是_________。
(5)请你就城市生活垃圾处理提一条合理化建议:___________。
(适合初中学生)
5. 硫酸亚铁盐(FeSO4·7H2O)是一种重要的食品和饲料添加剂。实验室通过下列实验由废铁屑制备FeSO4·7H2O晶体:
①将5% Na2CO3溶液加入到盛有一定量废铁屑的烧杯中洗涤铁屑,并加热数分钟,用倾析法除去Na2CO3溶液,然后再将废铁屑用蒸馏水洗涤2~3次;
②向洗涤过的废铁屑加入过量的稀硫酸,温度控制在50~80℃,至铁屑耗尽;
③趁热过滤,将滤液转入到密闭容器中,静置、冷却结晶;
④待结晶完毕后,滤出晶体,用少量冰水洗涤晶体2~3次,再用无水乙醇洗涤;
⑤将制得的FeSO4·7H2O晶体放在一个小广口瓶中,密闭保存。
(1)加入5% Na2CO3溶液洗涤的目的是________,将废铁屑用蒸馏水洗涤2~3次的目的是____________。
(2)待结晶完毕后,滤出晶体,用少量冰水洗涤晶体2~3次的目的是________;选择用冰水来洗涤的原因是__________。
(3)最后还用无水乙醇洗涤晶体的目的是______________。
6. 在标准状况下,用一定量的水吸收氨气后,制得了浓度为12mol/L、密度为0.915g/cm3的氨水。试计算:
(1)在标准状况下,1L该氨水中含氨的质量多少?
(2)1体积水吸收多少体积的氨气可制得标准状况下上述浓度的氨水(氨的式量以17计,水的密度以1g/cm3计)?
7.(1)邻苯二甲酸氢钾(相对分子质量为204.2)可以用来标定NaOH溶液的浓度,反应如下:KHC8H4O4 + NaOH = KNaC8H4O4 + H2O。准确称取KHC8H4O4晶体0.5105g,溶于水后加入酚酞指示剂,用某待测的NaOH溶液滴定至该溶液呈淡红色,消耗NaOH 20mL。计算该NaOH溶液的物质的量浓度(结果保留4位有效数字)。
提示:由质量、摩尔质量以及体积、浓度分别求出酸和碱的物质的量,再根据中和反应中酸碱物质的量关系列式求得碱的浓度。
(2)食醋中除了醋酸外,还含有其他有机酸,食醋的总酸度以每1000mL食醋中含醋酸(其他酸也折算作醋酸)的质量(g)表示,通常写作CH3COOH%。用移液管移取市售食醋50mL,置于250mL容量瓶中,用水稀释至刻度。再从容量瓶中移取25mL,用上小题中已知浓度的NaOH溶液滴定 ,消耗碱液体积为V(mL),试写出该食醋中CH3COOH%的计算式。
提示:在上题求得CNaOH的基础上,同样利用酸碱中和反应,求得食醋稀释液中CH3COOH的物质的量,经换算后得出CH3COOH%的表示式。
(适合高中学生)
