HPLC法同时测定三黄滴丸中5种蒽醌类成分的含量
2015-03-09魏艳婷张静宜张华潭李春花河北医科大学研究生学院石家庄050017河北中医学院药学院石家庄050091
魏艳婷,张静宜,张华潭,李春花(1.河北医科大学研究生学院,石家庄 050017;2.河北中医学院药学院,石家庄 050091)
三黄滴丸由大黄、黄芩浸膏、盐酸小檗碱组成,是按照临床常用的非处方药三黄片组方比例进行投料,运用固体分散技术制成的中药复方制剂,具有清热解毒、泻火通便的功效。三黄滴丸较传统片剂具有溶散速度快、药物颗粒小、生物利用度高等优点。对于这一新型制剂,目前生产工艺、含量测定等的研究均较少,质量标准暂不统一。因此,本研究采用高效液相色谱(HPLC)法,同时测定了该复方制剂中5 种蒽醌类成分的含量,操作简便,结果准确,在2010 年版《中国药典》(一部)三黄片[1]的基础上提高了质量标准,现报道如下。
1 材料
LC-15C 型HPLC 仪,包括SPD-15C 紫外检测器、LCsolution色谱工作站(日本岛津公司);1810-BC型石英自动双重高纯水蒸馏器(江苏金坛市白塔石英玻璃仪器厂);TG328B型分析天平(上海精科分析仪器厂);KQ-100E型超声波清洗器(昆山市超声仪器有限公司);有机微孔滤膜(0.22 μm)。
三黄滴丸(河北中医学院药学院自制,批号:20130315-01、20130315-02、20130315-03)。芦荟大黄素对照品(批号:20120412,纯度≥98%)、大黄酸对照品(批号:MUST-11032801,纯度≥98%)、大黄素对照品(批号:MUST-12022715,纯度≥98%)、大黄酚对照品(批号:20120320,纯度≥98%)、大黄素甲醚对照品(批号:PF0223 SA13,纯度≥98%)均由上海源叶生物科技有限公司提供;甲醇为色谱纯,磷酸为分析纯,水为超纯水(河北中医学院药学院自制)。
2 方法与结果[2-6]
2.1 色谱条件
色谱柱:Diamonsil C18(250 mm×4.6 mm,5 μm);流动相:甲醇-0.23%磷酸溶液(85∶15,V/V);流速:1.0 ml/min;检测波长:440 nm;柱温:室温;进样量:10 μl。
2.2 溶液的制备
2.2.1 混合对照品溶液 取芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚对照品各适量,精密称定,分别置于10 ml量瓶中,加适量甲醇,超声(功率:250 W,频率:33 kHz)处理20 min,使溶解,加甲醇定容,即得对照品贮备液。取对照品贮备液各5 ml,置于同一25 ml量瓶中,制成质量浓度分别为0.035、0.323、0.065、0.075、0.037 mg/ml的混合对照品溶液。
2.2.2 供试品溶液 取三黄滴丸1.0 g,精密称定,置于25 ml量瓶中,加甲醇适量,超声(功率:250 W,频率:33 kHz)处理20 min,加甲醇定容,即得供试品溶液。
2.2.3 阴性对照溶液 按处方比例和三黄滴丸的制备工艺制备缺大黄药材的阴性样品,按“2.2.2”项下方法制备阴性对照溶液,即得。
2.3 系统适用性试验
精密吸取“2.2”项下混合对照品溶液、供试品溶液和阴性对照溶液各10 μl,按“2.1”项下色谱条件进样测定,记录色谱,详见图1。由图1可知,供试品溶液与混合对照品溶液均在相同保留时间处出现芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚吸收峰,阴性对照溶液在该处无吸收。芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚峰与其他组分峰达到基线分离,分离度均大于1.5,阴性对照溶液在该处无吸收峰。理论板数以相应色谱峰计均不低于10 000。

图1 高效液相色谱图A.供试品;B.混合对照品;C.阴性对照;1.芦荟大黄素;2.大黄酸;3.大黄素;4.大黄酚;5.大黄素甲醚Fig 1 HPLC chromatogramsA.test samples;B.mixed reference;C.negative control;1.aloeemodin;2.rhein;3.emodin;4.chrysophanol;5.physcion
2.4 线性关系考察
精密量取“2.2.1”项下混合对照品溶液2、5、8、10、15、18、20 μl,按“2.1”项下色谱条件进样测定,记录峰面积。以进样量(x,μg)为横坐标、峰面积(y)为纵坐标进行线性回归,回归方程与线性范围见表1。
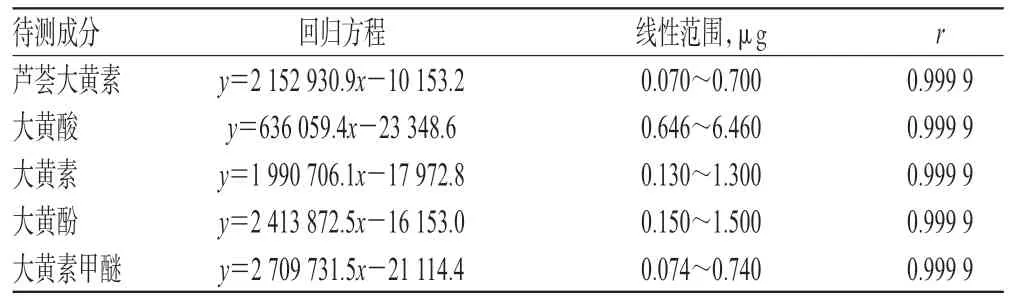
表1 回归方程与线性范围Tab 1 Regression equation and linear ranges
2.5 精密度试验
精密量取“2.2.1”项下混合对照品溶液适量,按“2.1”项下色谱条件重复进样6次,记录峰面积。结果,芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚峰面积的RSD分别为0.31%、0.25%、0.27%、0.27%、0.23%(n=6),表明仪器精密度良好。
2.6 稳定性试验
精密量取同一供试品(批号:20130315-01)溶液适量,分别于放置0、6、12、18、24、36 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果,芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚峰面积的RSD分别为0.91%、1.86%、1.96%、1.31%、1.17%(n=6),表明供试品溶液在36 h内稳定性良好。
2.7 重复性试验
取样品(批号:20130315-01)6 份,精密称定,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积。结果,芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚的平均含量分别为0.70、4.69、1.24、2.03、0.75 mg/g,RSD分别为1.56%、1.53%、1.65%、1.80%,1.51%(n=6),表明该方法重复性良好。
2.8 加样回收率试验
精密称取已知含量的样品(批号:20130315-01)9份,每份0.1 g,分别精密加入一定量的芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚对照品溶液,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积,并计算加样回收率,结果见表2。
2.9 样品含量测定
精密称定3批样品各适量,每批2份,每份1.0 g,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,并计算样品含量,结果见表3。
3 讨论
3.1 测定波长的选择
将配制的芦荟大黄素、大黄酸、大黄素、大黄酚及大黄素甲醚对照品溶液,采用紫外-可见分光光度计进行扫描,结果发现5 种蒽醌类成分在440 nm 波长左右均有较强吸收。因此,选择440 nm为本研究的检测波长。
3.2 流动相的选择
经查阅文献[7-8],笔者曾试用甲醇-0.1%磷酸溶液(90∶10,V/V)为流动相,但芦荟大黄素与大黄酸并未得到较好分离,拖尾现象严重,考虑到加入适当磷酸可以改善色谱峰的拖尾现象,又尝试以甲醇-0.23%磷酸溶液(85∶15,V/V)为流动相,结果发现5 种蒽醌类成分均可较好的分离,且峰形较好;芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚与相邻峰分离度分别为1.568、2.890、4.723、6.106、9.995,理论板数分别在70 000、16 000、10 000、20 000、40 000以上。
3.3 含量限度的确定
测定100 粒滴丸,平均质量为50 mg/丸。本试验选取了3批滴丸进行5 种蒽醌类成分的含量测定,结果芦荟大黄素、大黄酸、大黄素、大黄酚及大黄素甲醚平均含量分别为0.703 72、4.693 09、1.241 60、2.033 54、0.749 34 mg/g,考虑到药材来源、制备过程中的损耗、储存中损失等诸多因素的影响,按平均值的80%计算[9],暂定三黄滴丸中芦荟大黄素、大黄酸、大黄素、大黄酚及大黄素甲醚的含量分别不得小于0.028 15、0.187 72、0.049 66、0.081 34、0.029 98 mg/丸。

表2 加样回收率试验结果(n=9)Tab 2 Results of recovery test(n=9)
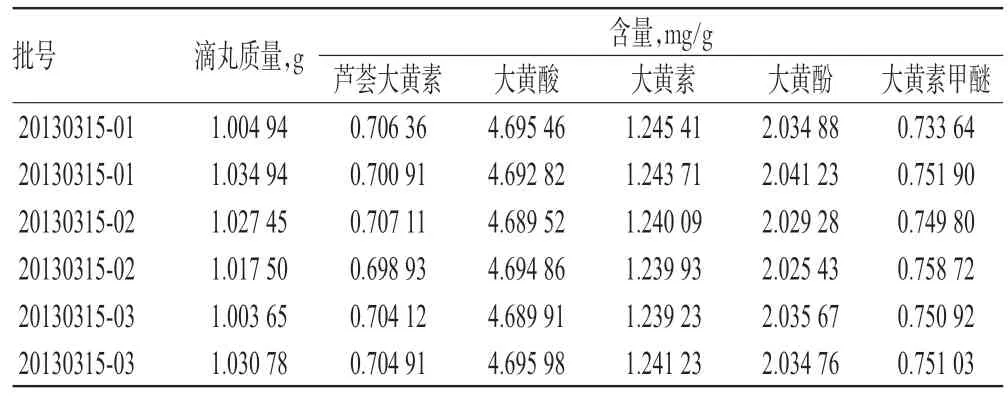
表3 样品含量测定结果(n=2)Tab 3 Results of samples content determination(n=2)
3.4 质量标准的提高
2010年版《中国药典》(一部)对三黄片的质量标准进行了规定,对大黄中的大黄素和大黄酚进行了含量测定,大黄中其余成分并未规定。本研究采用HPLC法,同时测定了大黄中5种蒽醌类成分,全面反映了成品质量,提高了质量标准。该方法简便、准确、专属性强,可作为三黄滴丸中5种有效成分的含量控制方法。
[1]国家药典委员会.中华人民共和国药典:一部[S].2010年版.北京:中国医药科技出版社,2010:457-458.
[2]王捧英,陈琳,侯芳洁,等.HPLC同时测定人参强心滴丸中华蟾酥毒基和脂蟾毒配基的含量[J].药物分析杂志,2012,32(5):802.
[3]夏从龙,周浓,种佳.HPLC 测定不同厂家牛黄消炎片中5 种蒽醌类衍生物的含量[J].中国实验方剂学杂志,2011,17(2):83.
[4]阚红玉,宋殿荣,王跃飞,等.HPLC 法同时测定黄芩中5种黄酮类成分的含量[J].中国药房,2010,21(11):1 016.
[5]祝忠民,卢晓荣.HPLC法同时测定三黄片中4 种成分的含量[J].西北药学杂志,2008,23(5):300.
[6]毛泉明,张钰泉,叶福媛,等.用RP-HPLC 法测定三黄片中四种组分的含量[J].药学服务与研究,2009,9(4):292.
[7]柳仁民,丁瑞芳.高效液相色谱法测定三黄片中蒽醌类衍生物的含量[J].中国现代应用药学,2005,22(5):411.
[8]王钰莹,冯伟红,杨菲,等.“一测多评”法测定三黄片中的大黄蒽醌类成分[J].中国中药杂志,2012,37(2):212.
[9]李文霞,宋平顺.HPLC法同时测定三黄片中黄芩苷和盐酸小檗碱的含量[J].药学进展,2011,35(4):178.
