HPLC 指纹图谱结合共有模式识别评价重庆市售青蒿饮片质量的一致性Δ
2015-03-09贾成友赵凤平杨荣平王云红成都中医药大学药学院成都637重庆市中药研究院重庆400065
贾成友,赵凤平,李 微,陈 娇,杨荣平,#,王云红(.成都中医药大学药学院,成都 637;.重庆市中药研究院,重庆 400065)
青蒿(Artemisia apiacea)系菊科植物黄花蒿(Artemisia annuaL.)的干燥地上部分,具有清热、解暑、除蒸、截疟的功效,主治暑热、暑湿、湿温、阴虚发热、疟疾、黄疸等证[1]。现代药理研究表明,青蒿在抗疟、抗肿瘤、抗菌杀虫、抑制免疫功能亢进、抗心律失常、抗孕、抗单纯疱疹病毒等方面作用明显,同时可用于红斑狼疮的治疗及降低机体本身对类风湿性关节炎的过度免疫[2-3]。从青蒿中提取分离出的青蒿素,具有抗疟、抗菌、抗肿瘤、解热、增强免疫等药理活性,尤其适宜于恶性疟疾、脑型疟疾的治疗,是世界卫生组织推荐的治疗疟疾的首选药物[4-5]。目前,国内有关青蒿质量评价的研究多以青蒿素、青蒿酸等指标性成分为主。本研究采用高效液相色谱(HPLC)指纹图谱对不同批次的青蒿的相似度进行评价,并采用主成分分析、聚类分析相结合的方法对指纹图谱进行共有模式识别,探讨饮片质量的差异性,以为客观评价青蒿饮片质量提供参考。
1 材料
20A系列HPLC仪,配有二元泵、在线脱气、二极管阵列检测器、自动进样器、柱温箱(日本岛津公司);AUW-220 型万分之一电子天平(日本岛津公司);CPA225D 型十万分之一电子天平[赛多利斯科学仪器(北京)有限公司];SY2000 型旋转蒸发仪(上海亚荣生化仪器厂);SB-5200DT超声波清洗机(宁波新芝生物科技股份有限公司,功率:300 W,频率:50 kHz)。
东莨菪内酯、青蒿素对照品(中国食品药品检定研究院,批号:110768-200504、100202-201004);青蒿酸对照品(四川生物试剂有限公司,批号:120628);甲醇(安徽时联特种溶剂股份有限公司,色谱纯),磷酸(重庆申渝化学试剂厂,分析纯),95%乙醇[重庆川东化工(集团)有限公司,分析纯],水为自制超纯水。
青蒿饮片(批次:S1~S12)购自重庆市各大药店,经重庆市中药研究院李隆云研究员鉴定为菊科植物黄花蒿A.annuaL.的干燥地上部分。
2 方法与结果
2.1 色谱条件
色谱柱:Waters XTerra C18(250 mm×4.6 mm,5 μm);流动相A 为甲醇,流动相B 为0.1%磷酸水溶液,梯度洗脱(洗脱程序见表1);流速:1.0 ml/min;检测波长:220 nm;柱温:30 ℃;进样量:10 μl。

表1 梯度洗脱程序Tab 1 Gradient elution procedure
2.2 溶液的制备
2.2.1 对照品溶液 取青蒿素、青蒿酸、东莨菪内酯对照品各适量,精密称定,分别加入甲醇制成每1 ml含青蒿素、青蒿酸、东莨菪内酯0.300、0.096、0.030 mg的单一对照品溶液,经微孔滤膜(0.22 μm)滤过,即得。
2.2.2 供试品溶液 取青蒿药材粉末(过40 目筛)2.5 g,精密称定,置于250 ml 圆底烧瓶中,加入95%乙醇150 ml,加热回流2 h,冷却,分取乙醇液,续滤液经旋转蒸发仪回收溶剂,残渣加甲醇溶解并移至50 ml 量瓶中,定容,摇匀,经微孔滤膜(0.22 μm)滤过,即得。
2.3 方法学考察
2.3.1 精密度试验 精密吸取“2.2.1”项下对照品溶液10 μl,按“2.1”项下色谱条件连续进样6 次。结果,青蒿素、青蒿酸、东莨菪内酯峰面积的RSD分别为0.81%、0.73%、0.69%,表明仪器精密度良好。
2.3.2 稳定性试验 精密称取药材粉末(S3)约2.5 g,按“2.2.2”项下方法制备供试品溶液,分别于放置0、2、4、8、12、24 h时按“2.1”项下色谱条件进样测定,以东莨菪内酯为内参峰。结果,各主要共有峰相对保留时间的RSD 为0.11%~2.04%,相对峰面积的RSD 为0.15%~2.47%,相似度>0.99,表明供试品溶液在24 h内较稳定。
2.3.3 重复性试验 精密称取药材粉末(S3)约2.5 g,按“2.2.2”项下方法平行制备6 份供试品溶液,按“2.1”项下色谱条件进样测定,以东莨菪内酯为内参峰。结果,各主要共有峰相对保留时间的RSD 为0.09%~2.28%,相对峰面积的RSD为0.11%~2.53%,相似度>0.99,表明本方法重复性良好。
2.4 数据分析方法[6-7]
利用国家药典委员会《中药色谱指纹图谱相似度评价系统》(2004 A 版)进行HPLC 指纹图谱相似度分析;采用SPSS 17.0软件进行主成分分析和聚类分析。
2.5 样品测定
分别取青蒿饮片粉末(S1~S12,过40 目筛)适量,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录色谱,详见图1、图2。利用《中药色谱指纹图谱相似度评价系统》(2004 A版)软件,以S1为参照图谱,经多点校正,中位数法生成青蒿对照指纹图谱[8],从中筛选出16个主要特征指纹峰,并对5、14、16 号色谱峰进行指认,分别为东莨菪内酯、青蒿素、青蒿酸。
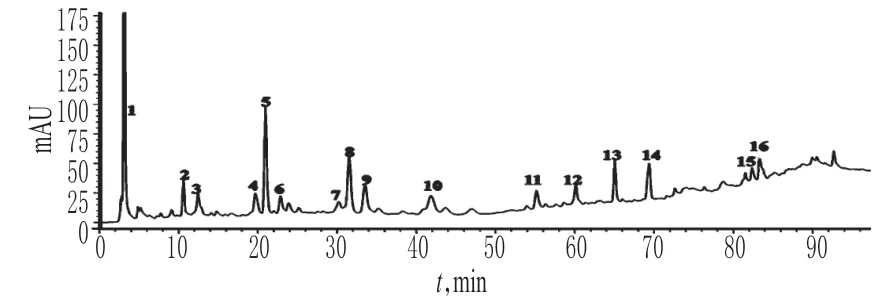
图1 青蒿样品高效液相色谱图Fig 1 HPLC chromatograms of A.apiacea samples

图2 对照品重叠空白甲醇色谱图a.青蒿素;b.青蒿酸;c.空白溶液;d.东莨菪内酯Fig 2 Overlapping chromatograms of referencesa.artemisinin;b.artemisinic acid;c.blank solution;d.scopoletin
2.6 相似度计算
根据生成的对照指纹图谱,计算各批样品的相似度。结果,除S11与对照图谱相似度为0.460外,其余各批样品相似度均在0.962~0.998之间,其中S1、S6、S7、S8、S10、S12与对照图谱相似度达到0.996以上。可见,不同批次样品之间存在一定差异。
2.7 主成分分析和聚类分析
2.7.1 主成分分析 将12 批青蒿饮片色谱数据,以各样品总峰个数、共有峰占总峰面积比值、与对照图谱相似度及各样品3 个主要特征峰(1.东莨菪内酯;2.青蒿素;3.青蒿酸)与S1中各特征峰峰面积比值为数据源,形成6个样本数据矩阵[6],详见表2。运用SPSS 17.0 软件对数据矩阵进行KMO 检验和Bartlett球形检验。结果,KMO统计量(0.689)>0.5,Bartlett球形检验P<0.05,表明各指标间相互独立,适用于主成分分析。取特征值较大的两个主成分(方差贡献率为91.37%),以各样品的得分建立坐标系,详见图3。由图3 可知,S6、S7、S8,S5、S10、S9分散相对集中,说明S6、S7、S8之间,S5、S10、S9之间成分种类和含量相接近,而S11 与其他样品距离相对较远,因此S11 可排除建立共有模式所需样品之外。

表2 数据矩阵表Tab 2 Data matrix table
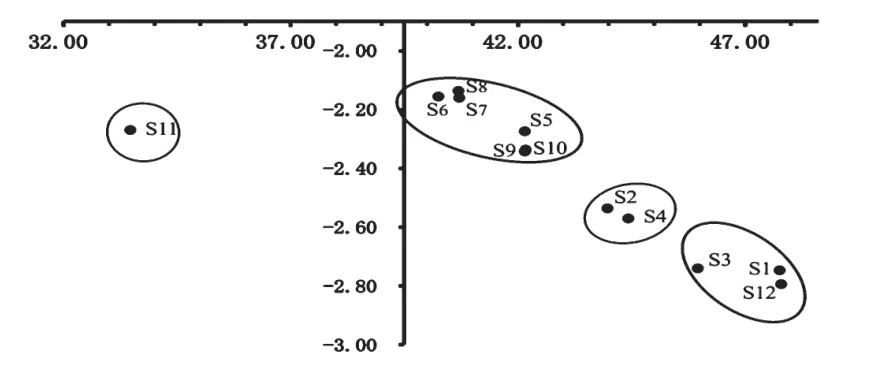
图3 青蒿样品主成分分析图Fig 3 Principal component analysis of A.apiacea samples
2.7.2 聚类分析 将不同批次青蒿样品HPLC图谱中的16个共有峰的峰面积值标准化,组成12×16 阶数据矩阵[9],运用SPSS 17.0软件以组间联接聚类法、欧氏平方距离法[6]作为测量的距离变量,并对其进行聚类分析,详见图4。

图4 青蒿样品聚类分析图Fig 4 Cluster analysis of A.apiacea samples
聚类结果表明,以虚线α为界,可以将12 批样品聚类为两大类:S11单独聚为一类,其余11批样品聚为另一类;以虚线β为界,可以将其聚为三大类:S11聚为一类,S1、S12、S3、S2、S4聚为一类,其余为一类;以虚线γ为界,可以将其聚为四大类:Ⅰ(S6、S7、S8、S5、S10、S9),Ⅱ(S2、S4),Ⅲ(S1、S12、S3),Ⅳ(S11)。根据以上聚类结果,样品S6、S7、S8、S5、S10、S9 聚为一类,说明它们之间具有一定的统一性。其中,Ⅰ类中S7、S8、S6聚为一类,S9、S10、S5聚为一类,表明同一类别中饮片又存在一定的差异性。同样,S12、S1聚为一类后又与S3聚为一类形成Ⅲ,说明它们之间既存在一定的统一性又存在一定的差异性;S11 单独聚为一类,说明S11 与其他批次样品之间差别显著,分析原因可能与青蒿药材的栽培、饮片加工和存放等多种因素有关,或企业自身饮片生产过程不规范,存在掺假掺杂等问题。可见,不同市售饮片之间存在一定差异,聚类分析对青蒿进行化学模式识别具有一定的科学道理,与主成分分析结果相吻合。
2.8 青蒿标准HPLC指纹图谱的建立
根据相似度计算结果,参考主成分分析和聚类分析结果,将S11以外的其余11批青蒿样品AIA格式数据文件再次导入《中药色谱指纹图谱相似度评价系统》(2004A 版)软件,以S1为参照图谱,经多点校正,中位数法生成青蒿HPLC 指纹图谱和对照指纹图谱[8],详见图5、图6。
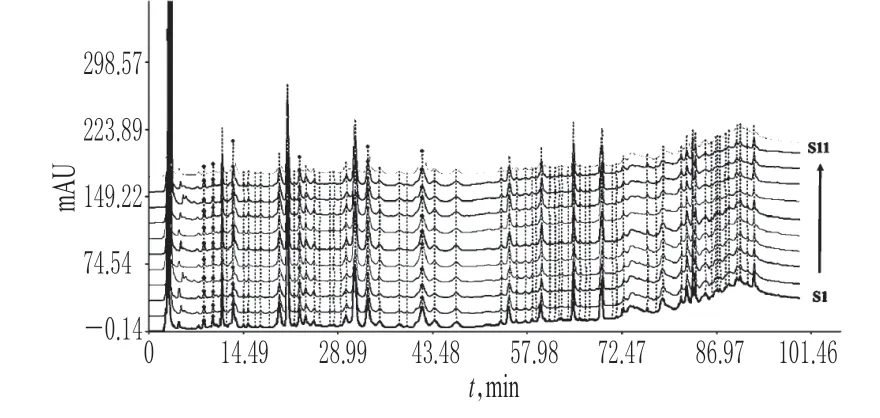
图5 11批样品的高效液相色谱指纹图谱Fig 5 HPLC fingerprint of 11 batches of samples
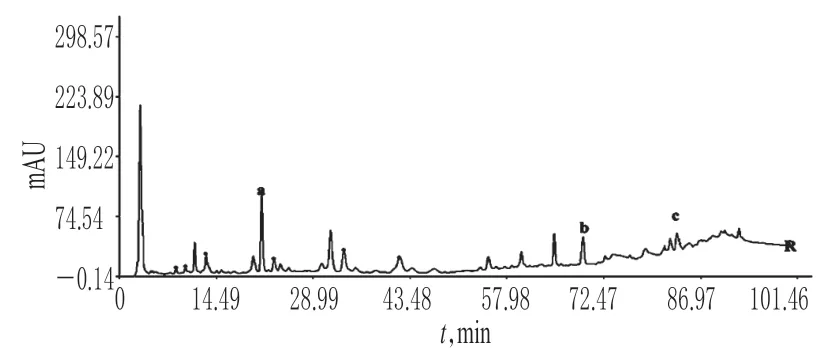
图6 对照指纹图谱a.东莨菪内酯;b.青蒿素;c.青蒿酸Fig 6 Reference fingerprinta.scopoletin;b.artemisinin;c.artemisinic acid
经计算,11 批样品的相似度分别为0.998、0.996、0.996、0.990、0.992、0.997、0.998、0.995、0.994、0.997、0.998,均在0.990以上,表明各批饮片之间相似性高,差异性小,间接说明重庆市售青蒿饮片质量虽然存在一定差异性,但总体质量较好。
3 讨论
3.1 提取条件的考察
本试验考察了不同提取溶剂(水、甲醇、50%乙醇和95%乙醇),比较了超声提取、加热回流、冷浸等不同提取方法,结果表明,以95%乙醇回流提取法2 h提取率较高。
3.2 色谱条件的优化
笔者尝试了分别以甲醇-水、甲醇-0.1%磷酸水溶液、乙腈-水等为流动相的分离效果,结果以甲醇-0.1%磷酸水溶液为流动相进行全波长扫描,在220 nm波长处色谱峰数目较多,经梯度洗脱程序洗脱后,峰形、出峰时间和分离效果相对较好。
3.3 12批饮片的质量评价
根据相似度计算结果,12 批青蒿饮片中有1 批相似度过低,该分析结果与主成分分析和聚类分析结果相同,其余11批饮片之间相似性较高、差异性较小,化学成分种类和含量接近,间接说明重庆市售青蒿饮片质量总体较好。个别样品存在质量问题,这可能与青蒿药材的栽培、饮片加工和存放等多种因素有关,也不排除不法商贩以假充真,以次充好的可能性,具体原因有待深入研究。为解决此问题,相关部门仍应着重加大对青蒿药材种植,饮片加工、贮存方式的监督管理,以保证良好的药材、饮片供应。
(致谢:重庆市中药研究院中药种植研究所李隆云研究员对青蒿饮片进行了鉴别)
[1]国家中医药管理局《中华本草》编委会.中华本草[M].上海:上海科学技术出版社,1999:658-661.
[2]金美花.青蒿的药理作用与临床新用[J].现代医药卫生,2009,25(15):2 352.
[3]丁小芬,胡红.青蒿治疗类风湿性关节炎的免疫药理作用[J].中国中医基础医学杂志,2006,12(1):75.
[4]呼文亮,姚丽,谢红,等.青蒿素抗肿瘤作用机制研究[J].中国药房,2008,19(36):2 804.
[5]杨忠顺,李英.与青蒿素相关的1,2,4-三烷及臭氧化物的研究进展[J].药学学报,2005,40(12):1 057.
[6]尹海波,王吉华,涂秀文,等.老鹳草的HPLC指纹图谱及模式识别研究[J].中国药房,2014,25(27):2 538.
[7]刘永锁,孟庆华,蒋淑敏,等.相似系统理论用于中药色谱指纹图谱的相似度评价[J].色谱,2005,23(2):158.
[8]白根本,王敏,彭玉帅,等.市售青蒿饮片的质量一致性的高效液相色谱指纹图谱法分析[J].时珍国医国药,2013,24(9):2 283.
[9]雷欣潮,杨焕琪,赖茂祥,等.广西不同产区两面针HPLC指纹图谱研究[J].中草药,2012,43(5):1 003.
