EC-T剂量密度与常规剂量在淋巴结阳性乳腺癌患者辅助化疗中的比较研究
2015-03-07江联萍吴海霞成少华
江联萍,张 宁,吴海霞,成少华,左 丽,李 纲
(复旦大学附属肿瘤医院闵行分院化疗科,上海 200240)
EC-T剂量密度与常规剂量在淋巴结阳性乳腺癌患者辅助化疗中的比较研究
江联萍,张宁,吴海霞,成少华,左丽※,李纲
(复旦大学附属肿瘤医院闵行分院化疗科,上海 200240)
摘要:目的观察环磷酰胺联合表阿霉素序贯紫杉醇剂量密度化疗在淋巴结阳性乳腺癌辅助化疗中的安全性和耐受性,探讨密度方案化疗的临床效果及对乳腺癌患者预后的影响。方法选择2005年9月至2007年4月复旦大学附属肿瘤医院闵行分院收治的60例采用EC序贯T方案进行辅助化疗的女性淋巴结阳性乳腺癌术后患者为研究对象,按照随机数字表法分为剂量密度组(29例)和常规剂量组(31例),计划每例患者接受EC×4序贯T×4的化疗。剂量密度组每2周重复,常规剂量组每3周重复。观察两组患者的临床特点,Ⅲ~Ⅳ级毒性反应(包括粒细胞减少、恶心、呕吐和脱发),复发及生存情况。结果两组患者均按计划完成化疗。剂量密集组Ⅲ~Ⅳ级粒细胞减少发生率为20.7%(6/29),显著低于常规剂量组的58.1%(18/31),差异有统计学意义(P=0.034);两组均无血小板降低、贫血、心脏毒性、神经毒性发生。两组5年无病生存率和生存率比较差异无统计学意义(P>0.05)。结论EC序贯T剂量密度方案用于淋巴结转移乳腺癌患者的辅助化疗,不良反应可以耐受,是一个安全、有潜力的方案。剂量密度方案辅助化疗与常规方案辅助化疗有相似的临床效果,均能改善乳腺癌患者预后。
关键词:乳腺癌;辅助化疗;剂量密度
剂量强度这一名词在肿瘤治疗领域中已出现近20年[1],在临床实际应用中选择化疗药物的剂量对于恶性肿瘤疾病,尤其是对化疗药物敏感的肿瘤治疗效果具有很大影响。Hudis[2]首次提出剂量密集这一概念,即剂量密集是指标准的化疗药物剂量和缩短的化疗给药间歇。随着乳腺癌抗肿瘤药物的发展,仍然有部分患者不能从传统化疗中获益,单纯提高药物剂量,甚至采用超高剂量化疗不能进一步提高化疗疗效[3]。本研究旨在比较淋巴结阳性的乳腺癌患者术后给予EC-T的剂量密集辅助化疗与常规剂量辅助化疗的疗效、安全性、耐受性。
1资料与方法
1.1一般资料选择2005年9月至2007年4月复旦大学附属肿瘤医院闵行分院收治的女性乳腺癌术后淋巴结阳性患者60例,年龄28~75岁,平均(50±11)岁,均经病理证实,切缘无肿瘤浸润,无远处转移。卡氏评分(Karnofsky scores,KPS)≥80分,无严重心脏疾患,治疗前血常规、肝、肾功能正常,心电图大致正常。上述患者按照随机数字表法分为剂量密度组(29例)和常规剂量组(31例)。
1.2治疗方法剂量密度组:表阿霉素(辉瑞公司生产,批号:20000496)90 mg/m2第1日,环磷酰胺(德国 ASTA Medica AG生产,批号:20010114)600 mg/m2第1日,第3~10日应用粒细胞集落刺激因子(granulocyte colony-stimulating factor,G-CSF)(麒麟中国制药有限公司生产,批号:S20010062)5 μg/kg,每2周1次,共4个周期;序贯紫杉醇(百时美施贵宝公司生产,批号:20130359)175 mg/m2,3 h,第1日,第3~10日应用G-CSF 5 μg/kg,每2周1次,共4个周期。常规剂量组:表阿霉素90 mg/m2第1日,环磷酰胺600 mg/m2第1日,每3周1次,共4个周期;序贯紫杉醇175 mg/m2,3 h,第1日,每3周1次,共4个周期。出现Ⅱ度及Ⅱ度以上粒细胞降低时可给予G-CSF。每个周期化疗前查血常规、肝肾功能、心电图,必要时检查左心室射血分数。化疗过程中,每周至少进行2次血常规检查,同时在每个化疗周期后必须对化疗产生的毒性反应进行评价。在整个化疗完成后,根据患者身体状况和腋窝淋巴结转移情况继续进行治疗。
1.3毒性反应评估根据世界卫生组织抗癌药物常见不良反应分级标准评定。患者化疗后不良反应由正常向危重分为0~Ⅳ度,其中Ⅲ~Ⅳ级应视为严重反应[4]。生存指标包括总生存(overall survival,OS)和无病生存期(disease-free survival,DFS),OS是指手术日至死亡或末次随诊时间,DFS是指手术日至肿瘤转移或疾病首次复发的时间。
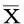
2结果
2.1 两组患者的临床特征和肿瘤特征比较两组患者在年龄、临床分期、浸润性导管癌、区域淋巴结分期、激素受体阳性、人类表皮生长因子受体2阳性、三阴性、绝经前、放疗、脉管阳性患者比例等比较差异无统计学意义(P>0.05),见表1。
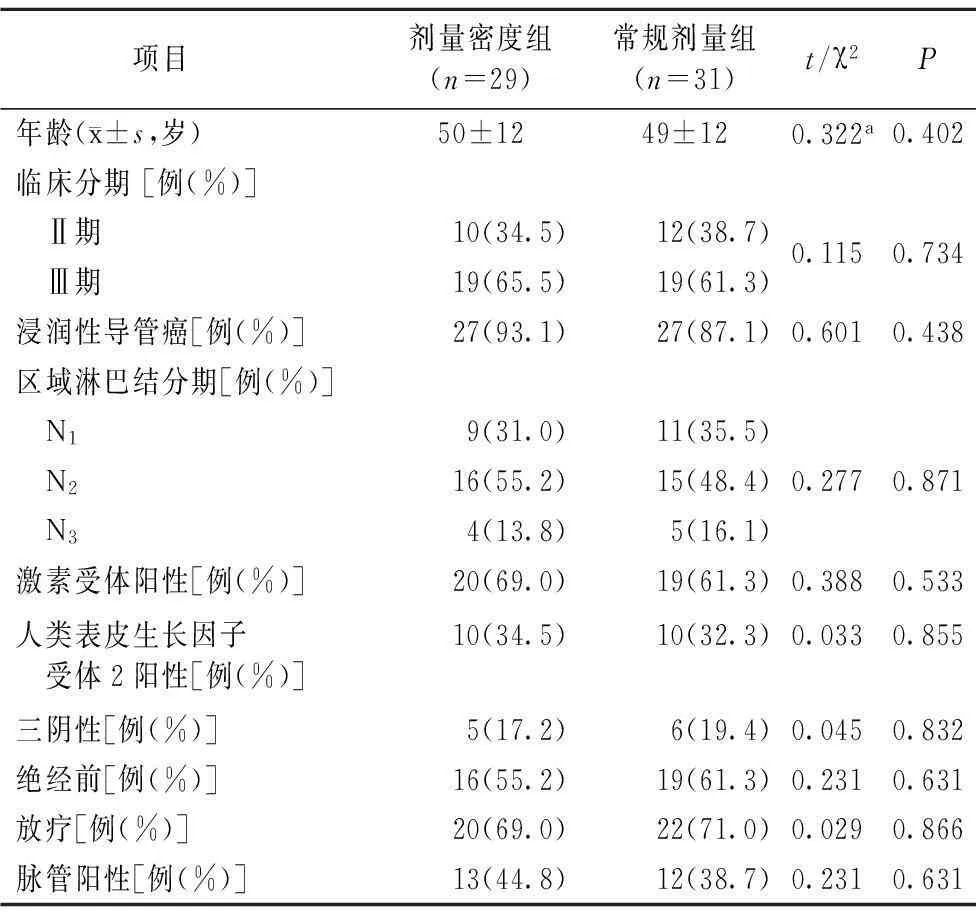
表1 两组女性乳腺癌术后淋巴结阳性患者的临床特征和肿瘤特征比较
a为t值,余为χ2值
2.2两组Ⅲ~Ⅳ级毒性反应比较两组患者均无治疗相关性死亡。剂量密集组恶心呕吐发生率为13.8%(4/29),常规剂量组为16.1%(5/31),两组比较差异无统计学意义(χ2=1.350,P=0.210);剂量密集组Ⅲ~Ⅳ级粒细胞减少发生率为20.7%(6/29),显著低于常规剂量组的58.1%(18/31),差异有统计学意义(χ2=5.640,P=0.034);两组均无血小板降低、贫血、心脏毒性、神经毒性发生。
2.3两组患者复发及生存情况随访5年,剂量密度组和常规剂量组分别有6例和8例复发,4例和7例死亡。DFS分别为65.5%(19/29)、51.6%(16/31),OS分别为86.2%、77.4%,两组比较差异均无统计学意义(χ2=0.219,P=0.640;χ2=0.773,P=0.379)。
3讨论
20 世纪70 年代开始出现乳腺癌术后辅助化疗的临床研究报道。为提高疗效,新的药物不断被引入化疗方案。早期乳腺癌临床试验联合研究组通过对全球28 000例参与辅助化疗临床试验的患者随访资料分析得出联合辅助化疗可以延长乳腺癌患者术后的DFS、OS并显著降低复发率[5]。但是乳腺癌术后辅助化疗的方案并无统一规范,临床上的药物选择、给药顺序、药物使用剂量和化疗周期及化疗间隔时间均存在很大差异。早期乳腺癌研究者合作组织研究显示,早期乳腺癌术后采用环磷酰胺+氨甲蝶呤+氟尿嘧啶方案辅助化疗可以使复发风险降低24%,死亡风险降低13%[6]。随着蒽环类、紫杉类药物在乳腺癌辅助化疗中的不断使用,乳腺癌的术后复发风险持续下降。对已知药物的治疗方案进行给药方式的改进,也是提高辅助化疗疗效的方法之一。近年来,大量临床试验结果证实,单纯提高药物剂量不能进一步提高疗效,只会增加不良反应。化疗药物的给药时机对于成功治疗至关重要。基于Norton-Simon理论[7]和肿瘤生长的动力学的模型(Gompertzian模型)可知,肿瘤及肿瘤细胞实际上的生长增殖并不是匀速生长过程,而是按照非指数动力学模型进行的,肿瘤的体积越小生长速度就会越快。然而化疗虽使肿瘤体积暂时变小,但残留瘤体内耐药的肿瘤细胞会于化疗间歇期再次进入细胞周期而迅速生长。若此时应用化疗药物可强力抑制或杀灭肿瘤细胞,在此理论基础上有研究表明每2周或间隔更短的时间给予化疗药物可以最大程度地抑制肿瘤增殖和生长,显著阻断耐药的肿瘤细胞再一次进入新的细胞周期。
临床上常通过提高化疗药物剂量强度的应用来达到加强疗效的目的。但化疗药物临床应用剂量具有阈值效应,即当单次剂量达到特定的化疗药物阈值后,额外再增加药物剂量并不会对疗效产生显著促进效果,反而会增加化疗药物的不良反应。近年来乳腺癌的辅助化疗似乎到了一个平台期。临床治疗通过提高药物剂量,甚至高剂量联合骨髓或干细胞移植均未能进一步提高疗效,直至2003年JCO发表了CALGB9741 临床试验的结果[8],才改变了辅助化疗疗效停滞不前的局面。该试验依据Norton-Simon理论[7],即肿瘤生长动力学的数学模型显示每2周给药较常规3周给药对肿瘤细胞的杀伤作用最大,且肿瘤细胞不易恢复正常生长。剂量密集方案可以明显地改善乳腺癌患者的生存,含紫杉和蒽环的剂量密集方案现已被美国国家癌症综合网推荐使用,被用于对高危乳腺癌患者治疗的辅助化疗。肿瘤科临床医师及学者们将剂量密集化疗方案应用于淋巴瘤、卵巢癌、小细胞肺癌、乳腺癌等肿瘤性疾病已经取得了显著的临床疗效。Hudis[2]首次于1996年证实将剂量密集化疗方案应用于乳腺癌临床的辅助治疗具有很好的DFS,但还是不可避免地存在较大毒性。自剂量密集的方法应用于临床以来,已有众多的乳腺癌医师将其应用于乳腺癌的治疗和研究。CALGB9741试验结果显示,密集化疗方法能显著降低复发风险、死亡风险、患者对侧乳腺癌的发病率及中性粒细胞减少的发生率,并显著提高4年DFS,说明剂量密集化疗方法可以使患者取得良好预后,更新了传统辅助化疗方案中每3周重复一次的治疗观点[9]。2008 年发表于新英格兰医学杂志ECOG1199 研究比较多柔比星+环磷酰胺序贯两个给药间歇时间(每周或每3周)的紫杉醇或多西紫杉醇方案。该研究共纳入4950例腋窝淋巴结阳性或高危的淋巴结阴性早期乳腺癌患者,中位随访时间为63.8个月。综合考虑疗效和安全性数据,该研究提示多柔比星+环磷酰胺序贯紫杉醇方案可能是一个较优秀的辅助化疗方案[10]。McArthur和Hudis[6]的研究证实,含蒽环类药物的密集化疗方案可以显著降低人类表皮生长因子受体2高表达所造成的乳腺癌患者DFS和OS率降低的不良影响。本研究结果显示,剂量密集组和常规剂量组的5年DFS分别为65.5%和51.6%,5年OS分别为86.2%和77.4%,差异无统计学意义。由此可以看出,密集化疗与常规治疗对患者预后影响差异无统计学意义,且密集化疗产生的不良反应与常规治疗组比较,除Ⅲ~Ⅳ级粒细胞发生率外其他不良反应发生率差异均无统计学意义。若能有效控制密集化疗引起的不良反应,剂量密集化疗可缩短患者治疗时间,为患者节约治疗费用,从卫生经济学角度来说更有利于减轻患者的经济负担和国家公共医疗资源负荷。而近年来随着粒细胞集落刺激因子的广泛应用,由于粒细胞缺失引起的化疗实施瓶颈已不再困扰化疗疗程的完成,在粒细胞集落刺激因子支持下的密集化疗是安全、有效的治疗方式。
总之,术后剂量密集辅助化疗可能给早期乳腺癌患者带来益处。对于年轻、激素受体阴性、人类表皮生长因子受体2基因扩增,多个淋巴结转移的高危患者,剂量密集化疗方案可能更有益。
参考文献
[1]Ziegler J,Citron M.Dose-dense adjuvant chemotherapy for breast cancer [J].Cancer Nurs,2006,29(4):266-272.
[2]Hudis C.New approaches to adjuvant chemotherapy for breast cancer[J].Pharmaco Therapy,1996,16(3 Pt 2):88-93S.
[3]胡夕春,杨新苗,高惠冰,等.剂量-密集辅助化疗在淋巴结阳性乳腺癌中应用的疗效和安全性分析[J].循证医学,2009,9(2):88-90.
[4]周际昌.实用肿瘤内科学[M].2版.北京:人民卫生出版社,1999:29.
[5]吴芳,胡春宏,蒋少艾,等.赫赛汀联合辅助化疗对人类表皮生长因子受体2阳性早期乳腺癌患者预后影响的Meta分析[J].中南大学学报:医学版,2007,32(4):684-689.
[6]McArthur HL,Hudis CA.Dose-dense therapy in the treatment of early-stage breast cancer:an overview of the data[J].Clin Breast Cancer,2007,8 Suppl 1:S6-10.
[7]Bear HD.Neoadjuvant chemotherapy for operable breast cancer:individualizing locoregional and systemic therapy[J].Surg Oncol Clin N Am,2010,19(3):607-626.
[8]Loibl S,von Minckwitz G,Raab G,etal.Surgical procedures after neoadjuvant chemotherapy in operable breast cancer:results of the GEPARDUO trial[J].Ann Surg Oncol,2006,13(11):1434-1442.
[9]Lalisang RI,Erdkamp FL,Rodenburg CJ,etal.Epirubicin and paclitaxel with G-CSF support in first line metastatic breast cancer:a randomized phase Ⅱ study of dose-dense and dose-escalated chemotherapy[J].Breast Cancer Res Treat, 2011,128(2):437-445.
[10]Sparano JA,Wang M,Martino S,etal.Weekly Paclitaxel inthe adjuvant treatment of breast cancer[J].N Engl J Med,2008,358(16):1663-1671.
The Effects of Dose-dense EC-T Chemotherapy for the Prognosis of Breast Cancer with Lymph-node MetastasisJIANGLian-ping,ZHANGNing,WUHai-xia,CHENShao-hua,ZUOLi,LIGang.(DepartmentofChemotherapy,FudanUniversityCancerCenterMinxingBranch,Shanghai200240,China)
Abstract:ObjectiveTo evaluate the effect of dose-dense adjuvant chemotherapy epirubicin/cyclophosphamide followed by docetaxel(EC-T) on the clinical efficacy and prognosis of breast cancer patients with lymph-node metastasis.MethodsA total of 60 patients of breast cancer treated with epirubicin/cyclophosphamide followed by docetaxel(EC-T) admitted to the Fudan University Cancer Center Minxing Branch during Sep.2005 and Apr.2007 were divided into dose-dense group(29 cases) and conventional dose group(31 cases) according to random number table method.It was planned to give every patient EC×4 sequential T×4 chemotherapy, repeated every two weeks in the dose-dense group and every three weeks in the conventional dose group.The clinical characteristics,the grade Ⅲ-Ⅳ toxicity(including the reduction of the granulocyte,nausea,vomiting and alopecia),and the recurrence and survival of the two groups were observed.ResultsBoth groups finished the chemotherapy as planned.The gradeⅢ-Ⅳ granular cells reduction incidence of dose-dense group was 20.7%(6/29),which was significantly lower than that of the conventional dose group′s 58.1%(18/31),the difference was statistically significant(P=0.034);there were no thrombocytopenia,anemia,cardiac toxicity,neurotoxicity in both groups.The 5-year disease free survival and survival rate of the two groups had no statistically significant difference(P>0.05).ConclusionDose-dense adjuvant chemotherapy using epirubicin/cyclophosphamide followed by docetaxel can achieve similar clinical results as conventional adjuvant chemotherapy in breast cancer patients with lymph-node metastasis,with tolerable adverse effects,and can improve the prognosis as well as the conventional therapy.
Key words:Breast neoplasm; Adjuvant chemotherapy; Dose-dense
收稿日期:2014-07-08修回日期:2015-06-19编辑:伊姗
doi:10.3969/j.issn.1006-2084.2015.22.042
中图分类号:R737
文献标识码:A
文章编号:1006-2084(2015)22-4144-03
