脂肪酶催化Michael加成反应合成苄丙酮香豆素抗凝血剂及其衍生物
2014-11-27彭瑞光樊大业谢帮华
彭瑞光,杨 禹,樊大业,谢帮华*
(1.阆中市人民医院,四川 阆中 637450;2.泸州市环境监测中心站,四川 泸州 646000)
随着绿色化学的兴起和发展以及人们的环境保护意识的加强,酶作为生物催化剂,因其具有高效性、专一性、反应条件温和、后处理简单和对环境友好等优点而备受化学家和生物学家的关注.传统理论认为,生物酶只在水溶液中才发挥催化作用,在有机溶剂中酶蛋白因变性而失活.而大多数有机物因不溶于水而极大的限制了酶催化反应在有机合成中的应用与发展.直到80年代中期,KLIBANOV[1]和ZAKS等[2]发现酶在接近无水的有机溶剂中不但能保持良好的催化活性,而且对其催化天然底物以外的其他化学反应也具有良好的催化活性和立体选择性[3],这一特性被称为酶催化的多功能性[4],并激起了一股研究酶催化反应的热潮.苄丙酮香豆素作为最有效的抗凝血剂,被广泛应用于医学及临床上.目前合成苄丙酮香豆素及其衍生物的方法主要有四种.DEMIR等[5]用LDA和路易斯酸为催化剂,利用外消旋体的4-羟基香豆素和苄叉丙酮的Michael加成反应得到了中等收率的苄丙酮香豆素及其衍生物;LI等[6]采用外消旋体的苄丙酮香豆素通过氧化和不对称氢化反应合成手性苄丙酮香豆素;CRAVOTTO等[7]利用串联Knoevenagel反应和hetero-Diels-Alder反应的方法合成外消旋体的苄丙酮香豆素及其衍生物;XIE等采用脯氨酸及其衍生物类催化剂手性合成苄丙酮香豆素及其衍生物[8-9].而生物酶催化合成苄丙酮香豆素及其衍生物的方法还少见报道,本文作者采用天野脂肪酶M作为生物催化剂,利用4-羟基香豆素和α,β-不饱和酮的Michael加成反应一步合成了抗凝血剂苄丙酮香豆素及其衍生物.
1 实验部分
1.1 仪器和试剂
爪哇毛霉的天野脂肪酶M(MJL),黑曲霉的天野脂肪酶A,雪白根酶脂肪酶,皱褶假丝酵母脂肪酶,来自荧光假单胞菌的天野脂肪酶和卡门柏干酪青霉脂肪酶均购自Sigma-Aldrich上海贸易有限公司.α,β-不饱和酮按照文献方法[8]制备.其他试剂全部来自商业渠道且未经进一步的纯化.薄层色谱检测(TLC)和柱层析都是使用青岛海洋化工生产的GF254型硅胶,柱层析硅胶为100~200目.1H NMR、13C NMR谱用Brucker AV-300型超导核磁共振波谱仪测定.
1.2 实验方法
在25mL的圆底烧瓶中加入4-羟基香豆素1(0.5mmol),α,β-不饱和酮2(0.75mmol),DMSO(0.90 mL),去离子水(0.10mL),天野脂肪酶M(50mg),在45℃条件下搅拌反应.TLC监测反应,待反应完成后用乙酸乙酯稀释反应液使酶析出,过滤去掉酶,用乙酸乙酯少量多次的洗涤滤纸,使产品全部溶解在洗涤液中.向洗涤液中加入大约20mL的水,用乙酸乙酯少量多次萃取之后,多余溶剂经减压旋转蒸发除去,粗产品经柱层析纯化后得产品3.
2 结果与讨论
2.1 催化剂的选择
首先,我们以4-羟基香豆素1和苄叉丙酮2a的Michael加成反应生成苄丙酮香豆素3a作为模型反应,以水为溶剂,对一系列脂肪酶催化活性进行了筛选(图1,表1).从表1可以看出,当反应在无酶催化条件下进行时只得到了痕量产物;而天野脂肪酶M表现出较好的催化活性,获得了25%的产率;黑曲霉的天野脂肪酶A,雪白根酶脂肪酶有一定的催化活性,分别获得了10%和8%的收率;皱褶假丝酵母脂肪酶,荧光假单胞菌的天野脂肪酶和卡门柏干酪青霉脂肪酶几乎不催化此反应,只得到了痕量的产物.通过以上综合分析,我们选择天野脂肪酶M作为反应体系的催化剂.

图1 脂肪酶催化4-羟基香豆素和苄叉丙酮的Michael加成合成苄丙酮香豆素Fig.1 The Michael addition of 4-hydroxycoumarin 1 to benzylideneacetone 2afor the formation of warfarin

表1 不同脂肪酶催化Michael加成的反应活性Table 1 The catalytic activities of different lipases in Michael addition
2.2 溶剂的选择
反应溶剂体系对底物溶解性和酶的催化活性有重要影响[10-11],因此我们研究了不同有机溶剂-水体系对酶的催化活性的影响(表2).当溶剂为DMSO时,酶的催化活性最高,获得了48%的收率(表2序号1);当溶剂为Cyclohexane、EtOH、1,4-dioxane和H2O时,有一定的催化活性,获得了9%~25%的收率(表2序号2-6);当溶剂为CH2Cl2、Anisole、MeCN时,酶几乎没有催化活性,只有痕量的产物生成(表2序号7-8).因此,我们选择DMSO作为反应的最佳溶剂.
2.3 温度和投料比对天野脂肪酶M催化Michael加成反应的影响
温度是影响酶的催化活性的重要因素之一,因此我们研究了不同温度对天野脂肪酶M催化4-羟基香豆素和苄叉丙酮的Michael加成反应的影响(表3).从表3可以看出,随着温度的升高,酶的催化活性显著提高,当反应温度为45℃时酶的活性最好,获得了84%的收率(表3序号4);继续提高温度到50℃时,对酶的催化活性无显著提高(表3序号7);当反应体系的温度为100℃时,酶因高温变性而失去催化活性(表3序号8).确定反应体系的最佳温度45℃后,我们进一步研究了4-羟基香豆素和苄叉丙酮的投料比(物质的量之比)对反应收率的影响.当苄叉丙酮与4-羟基香豆素的投料比为1.5∶1时(表3序号5),反应的收率达到了90%,继续增大投料比,产率无显著增加.因此我们最后选择苄叉丙酮与4-羟基香豆素的投料比为1.5∶1.

表2 溶剂对猪胰脂肪酶催化Michael加成反应的影响Table 2 Influence of solvents on the MJL-catalyzed Michael reaction
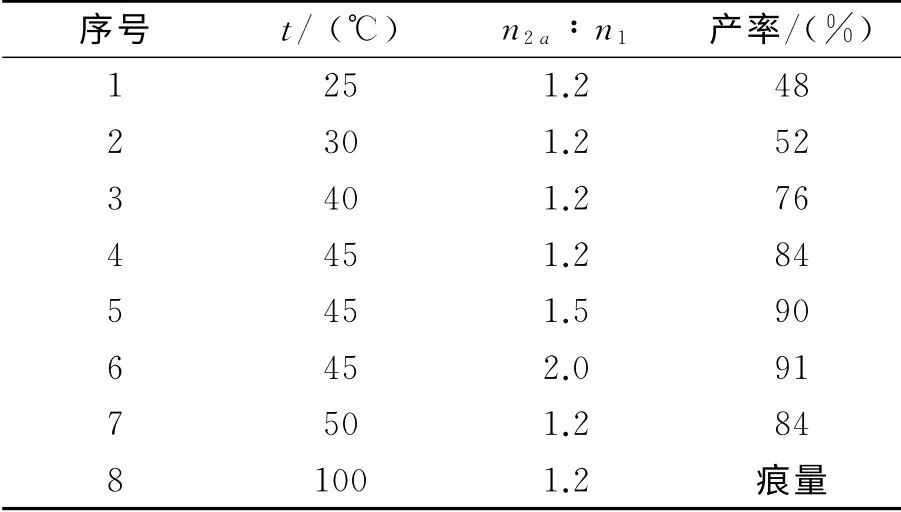
表3 温度和投料比对天野脂肪酶M催化Michael加成反应的影响Table 3 Influence of temperature and molar equivalents of benzylideneacetone(2a)on the MJL-catalyzed Michael reaction
2.4 天野脂肪酶M催化Michael加成反应底物扩展
通过对反应体系条件进行优化后,我们研究了天野脂肪酶M对4-羟基香豆素与其他α,β-不饱和酮的Michael加成反应的催化活性(表4).从表4可以看出,天野脂肪酶M对4-羟基香豆素与一系列的α,β-不饱和芳香酮,杂环α,β-不饱和芳香酮,环己烯酮的Michael加成反应都具有良好的催化活性,获得了75%~98%的收率.对于α,β-不饱和芳香酮来说,取代基的性质和位置对反应的收率有一定的影响,这可能是由于酶自身的催化结构决定的.比如对于4-羟基香豆素与邻甲氧基取代的α,β-不饱和酮Michael加成反应收率高于对甲氧基取代(表4序号2-3),邻氯取代的α,β-不饱和酮高于间氯和对氟取代的α,β-不饱和酮(表4序号4-6).同时,天野脂肪酶M对4-羟基香豆素与杂环的α,β-不饱和芳香酮的Michael加成反应也具有较好的催化活性,获得了80%和75%的收率(表4序号7-8).天野脂肪酶M对4-羟基香豆素与环状的环己烯酮的Michael加成反应也具有很好的催化活性,获得了94%的收率(表4序号9).
3 结论
报道了天野脂肪酶M作为生物催化剂催化4-羟基香豆素与α,β-不饱和酮的Michael加成反应一步合成具有生物活性的抗凝血剂及其衍生物的方法,反应条件温和,收率高,有一定的实际应用意义.

表4 天野脂肪酶M催化4-羟基香豆素与α,β-不饱和酮的Michael加成反应底物范围Table 4 Scope of the MJL-catalyzed Michael addition of 4-hydroxycoumarin toα,β-unsaturated ketones
[1]ZAKS A,KLIBANOV A M.Enzyme-catalyzed processes in organic solvents[J].Proc Natl Acad Sci,1985,82(10):3192-3196.
[2]KLIBANOV A M.Enzymes that work in organic solvents[J].Chemtech,1986,16(6):354-359.
[3]KLIBANOV A M.Enzymatic catalysis in anhydrous solvents[J].Trends Biochem Sci,1989,14(4):141-144.
[4]O′BRIEN P J,HERSCHLAG D.Catalytic promiscuity and the evolution of new enzymatic activities[J].Chem Biol,1999,6(4):91-105.
[5]ROBINSON A,LI H Y,FEASTER J.The first practical asymmetric synthesis of Rand S-warfarin[J].Tetrahedron Lett,1996,37(46):8321-8324.
[6]DEMIR A S,TANYELI C,GKLBEYAZ V,et al.Enantioselective synthesis of 4-hydroxy-3-(3-oxo-1-phenylbutyl)-2H-1-benzopyran-2-one(warfarin)[J].Turk J Chem,1996,20(2):139-145.
[7]CRAVOTTO G,NANO G M,PALMISANO G,et al.An asymmetric approach to coumarin anticoagulants via hetero-Diels-Alder cycloaddition[J].Tetrahedron:Asymmetry,2001,12(5):707-709.
[8]HALLAND N,HANSEN T,JORGENSEN K A.Organocatalytic asymmetric michael reaction of cyclic 1,3-dicarbonyl compounds andα,β-unsaturated ketones—A highly atom-economic catalytic one-step formation of optically active warfarin anticoagulant[J].Angew Chem Int Ed,2003,42(40):4955-4957.
[9]XIE J W,YUE L,CHEN W,et al.Highly enantioselective Michael addition of cyclic 1,3-dicarbonyl compounds toα,βunsaturated ketones[J].Org Lett,2007,9(3):413-415.
[10]CHENG Y C,TSAI S W.Effects of water activity and alcohol concentration on the kinetic resolution of lipase-catalyzed acyl transfer in organic solvents[J].Enzyme Microb Technol,2003,32(3/4):362-368.
[11]HUDSON E P,EPPLER R K,BEAUDOIN J M,et al.Active-site motions and polarity enhance catalytic turnover of hydrated subtilisin dissolved in organic solvents[J].J Am Chem Soc,2009,131(12):4294-4300.
