大豆乳清蛋白提取工艺的研究
2014-07-27
(河南城建学院生命科学与工程学院,河南平顶山 467036)
蛋白质是人们日常生活中必需的重要营养物质,而大豆是目前蛋白含量最为丰富的一种(蛋白质含量在40%以上)植物,大豆蛋白中含有人体必需的8种氨基酸,特别是大豆中赖氨酸、亮氨酸、苏氨酸含量较高,对人体有很高的利用价值。大豆蛋白制品包括大豆蛋白粉、浓缩大豆蛋白、大豆分离蛋白等,大豆分离蛋白含量在90%以上,被广泛用来加工豆制产品[1]。目前以提取大豆分离蛋白为目的的大豆深加工企业每天都要排放大量的乳清废水。在典型的碱溶酸沉工艺中,每生产1 t大豆分离蛋白会排放30 m2~50 m2的乳清废水[2],其中大部分直接排入了自然水体,造成了严重的资源浪费和环境污染[3-5]。由于乳清蛋白具有很好的酸溶解性和优越的乳化性和起泡性,长期食用还具有抗肿瘤效果及增强免疫作用,因此在食品加工中有广泛的应用前景[6-7]。为了更好地开发和回收利用大豆乳清废水中的乳清蛋白,本文以生产大豆分离蛋白产生的大豆乳清废水为原料,对大豆乳清蛋白的提取工艺进行了详细的描述。采用壳聚糖作为絮凝剂将大豆乳清蛋白沉降,得到的大豆乳清蛋白-壳聚糖复合物用水溶解离心后可除去壳聚糖,得到可溶性大豆乳清蛋白。回收大豆废水中的乳清蛋白不仅节约资源,生产附加值产品,而且有效的控制了污染,对延长大豆产业链、推动大豆产业发展、有效控制污染具有重要的意义[8]。
1 材料与方法
1.1 材料与仪器
1.1.1 材料与试剂
大豆乳清废水:平顶山市天晶植物蛋白有限公司;牛血清蛋白,考马斯亮蓝:北京索莱宝科技有限公司;溴酚蓝:北京中生瑞泰科技有限公司;无水氯化钙:分析纯,潍坊祥坤化工有限公司;壳聚糖:上海鹤善实业有限责任公司。
1.1.2 主要仪器设备
循环水式多用真空泵(SHB-III):郑州长城科工贸有限公司;低速离心机(KDC-1044):科大创新股份有限公司中佳分公司;pH计(pHSJ-3SJ):上海精密科学仪器有限公司;电热恒温水浴锅(HWS28):上海一恒科学仪器有限公司;紫外可见分光光度计(T6):北京普希通用通用仪器有限责任公司;冷冻干燥机(AIpHAl-2LD):德国 Christ。
1.2 方法
1.2.1 实验流程
大豆废液→离心→真空抽滤泵抽滤→CaCl2预处理→离心→壳聚糖处理→离心→除盐→冷冻干燥→大豆乳清蛋白粉
1.2.3 蛋白质含量检测
根据文献[9] ,操作步骤如下。
1)蛋白质标准曲线测定:分别取 0、0.01、0.02、0.04、0.06、0.08、0.10 mL 的 1 mg/mL 牛血清蛋白标准溶液于试管中,再加蒸馏水至0.10 mL,然后取5 mL考马斯亮蓝试剂于试管中,摇匀,并在2 min~5 min内,测其595 nm下的光吸收值,以标准牛血清蛋白的浓度为横坐标,以对应的595 nm下的光吸收值为纵坐标,绘制标准曲线。
2)取0.10 mL乳清废液于试管中,然后取5 mL考马斯亮蓝试剂于试管中摇匀,在2 min~5 min内,测其595 nm下的光吸收值,同时做2个平行组。空白对照用蒸馏水代替废液。最后将测得的光吸收值代入标准曲线,换算出蛋白含量。
1.2.4 大豆乳清废液的预处理
1)离心。由于大豆废液中含有比较明显的固体杂质,不利于抽滤的顺利进行,所以首先在4 000 r/min的条件下对废液进行离心处理,时间15 min。
2)抽滤。用循环水式多用真空泵对离心后得到的上清液进行抽滤,以除去大豆废液中残余的蛋白质和其它杂质,取其滤液。
3)CaCl2处理。根据前人多次对絮凝效果的实验研究[10],本课题选择氯化钙作为絮凝剂,预处理大豆废液。实验选取1 mol/L CaCl2对抽滤过的废水进行处理,除去废水中未完全沉降的大豆分离蛋白。首先对其加入量进行研究,选取 15、16、17、18、19 mL/L 5 个水平,将抽滤后的废液分装5瓶(每瓶各40 mL),在如下条件下进行处理:pH8、温度50℃、缓慢搅拌时间15 min对大豆废液进行预处理,选取最佳条件。
1.2.5 壳聚糖沉淀大豆乳清蛋白
本实验以壳聚糖为絮凝剂将大豆乳清蛋白沉淀下来,将壳聚糖溶液以一定的用量加到经氯化钙预处理的大豆废液中,在一定的温度下絮凝一定时间。以得率为指标,考察处理温度(15、20、25、30、35、40 ℃)、废液 pH(5.0、5.5、6.0、6.5、7.0、7.5)、壳聚糖加入量(0.05、0.1、0.2、0.3、0.4、0.5 g/L) 和处理时间(20、25、30、35、40、45 min)这4个因素对葡萄糖异构效果的影响。首先进行单因素实验,在此基础上,通过四因素三水平的正交实验确定最佳工艺条件。实验中每次废液处理量为40 mL,每组实验平行3次。
在本实验中,壳聚糖使用前用3%醋酸进行溶解。然后絮凝预处理之后的大豆废液,得到大豆乳清蛋白-壳聚糖复合物之后,烘干称重。大豆乳清蛋白-壳聚糖复合物加蒸馏水搅拌,由于大豆乳清蛋白可溶于水,而壳聚糖不溶于水,沉淀下来,再经过离心,实现絮凝剂的去除。
1.2.6 离心
用正交试验得出的壳聚糖最佳沉淀效果对大豆废液进行处理,在4 000 r/min条件下离心20 min,留沉淀弃上清。
1.2.7 除盐
将离心得到的沉淀用水溶解(溶于水部分是可溶性乳清蛋白),4 000 r/min条件下离心20 min(除去不溶性的杂质和壳聚糖),弃沉淀,上清液在4℃条件下透析24 h。
1.2.8 冷冻干燥
采用真空冷冻干燥法得到可溶性大豆乳清蛋白粉。
1.2.9 得率计算
大豆乳清蛋白得率/%=(大豆乳清蛋白-壳聚糖复合物质量)/氯化钙絮凝后废水蛋白含量×壳聚糖絮凝所用废液体积×100%
2 结果与讨论
2.1 蛋白质标准曲线
采用考马斯亮蓝G-250法测废水中蛋白质含量,得到的蛋白质标准曲线如图1所示。

图1 蛋白质标准曲线Fig.1 The standard curve of protein
通过做标准曲线,得到直线方程y=0.641 4x-0.005 1,相关系数R2=0.999 6。根据此标准曲线测得大豆废液中含蛋白质1.62 mg/mL,用CaCl2预处理除去大豆分离蛋白及部分杂质后上清液蛋白质含量为1.49 mg/mL。
2.2 不同CaCl2用量对大豆分离蛋白除去效果
大豆废水经不同用量氯化钙处理,除去大豆分离蛋白得到的结果如图2所示。

图2 氯化钙用量对除大豆分离蛋白效果的影响Fig.2 The effect of calcium chloride content on the removal of soy protein isolated
图2中横坐标为每升大豆乳清废水所需1 mol/L CaCl2的量,纵坐标为得到的大豆分离蛋白的质量(大豆分离蛋白-CaCl2复合物干重减去加入氯化钙质量)。由图2可知,CaCl2用量不同时,除去大豆分离蛋白的效果有显著差异,且去除效果随CaCl2用量的增加呈现先升高后降低的趋势,在1 mol/L CaCl2用量为18 mL/L时,除去大豆分离蛋白效果最好。另外由图2可知,几乎每个点的纵坐标值都超过了废液中蛋白质的含量,这是因为加入氯化钙与溶液中的离子生成沉淀,与大豆分离蛋白同时沉淀下来,这同时减少了溶液中的杂质离子含量。因此,在处理大豆乳清废液时可以采用每升加入1 mol/L CaCl218 mL为最终用量,与吴海波等的研究结果一致[11],即每升废液中添加无水CaCl2(Mr=110.99 g/mol)的质量约为 2 g。
2.3 不同的处理温度对大豆乳清蛋白得率的影响
在pH6.5,壳聚糖用量为0.3 g/L,加热时间35 min条件下,选取实验温度为 15、20、25、30、35、40 ℃处理废液,离心得到沉淀,计算大豆乳清蛋白得率,结果如图3所示。

图3 处理温度对大豆乳清蛋白沉淀效果的影响Fig.3 The effect of tempreture on the removal of soy whey protein
由图3可知,随着处理温度的升高,40 mL经氯化钙预处理的乳清废液中用壳聚糖沉淀出的大豆乳清蛋白的得率呈现降低趋势[12],温度越低,越有利于大豆乳清蛋白的沉降,在处理温度为15℃时,所沉淀出的大豆乳清蛋白的质量最多,即得率最高。
2.4 不同pH对大豆乳清蛋白得率的影响
在温度为30℃,壳聚糖用量为0.3 g/L,加热时间35 min 条件下,选取 pH 为 5.0、5.5、6.0、6.5、7.0、7.5 处理废液,离心得到沉淀,计算大豆乳清蛋白得率,结果如图4所示。
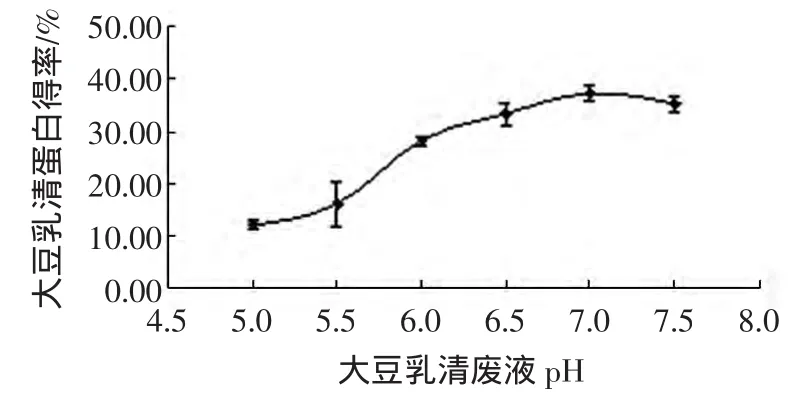
图4 废液pH对大豆乳清蛋白沉淀效果的影响Fig.4 The effect of wastewater pH on the removal of soy whey protein
由图4可知,随着废液pH的升高,40 mL经氯化钙预处理的乳清废液中用壳聚糖沉淀出的大豆乳清蛋白的得率呈现上升的趋势,在pH为7时达到最大值,pH继续增大时,大豆乳清蛋白的得率反而略有降低。比较各pH条件下所得到的大豆乳清蛋白的得率可知,pH为6.5~7.5之间时,废液絮凝蛋白效果最好。
2.5 不同的壳聚糖用量对大豆乳清蛋白得率的影响
在温度为30℃,pH6.5,加热时间35 min条件下,选取壳聚糖用量为 0.05、0.1、0.2、0.3、0.4、0.5 g/L 处理废液,离心得到沉淀,计算大豆乳清蛋白得率,结果如图5所示。

图5 壳聚糖用量对大豆乳清蛋白沉淀效果的影响Fig.5 The effect of the amount of chitosan on the removal of soy whey protein
由图5可知,随着壳聚糖用量的增多,40 mL经氯化钙预处理的乳清废液中所沉淀出的大豆乳清蛋白的得率呈现先升高后降低的趋势。在壳聚糖用量为0.3 g/L时,所沉淀出的大豆乳清蛋白的得率最高。
2.6 不同的处理时间对大豆乳清蛋白得率的影响
在温度为30℃,pH6.5,壳聚糖用量为0.3 g/L条件下,选取处理时间为 20、25、30、35、40、45 min 处理废液,离心得到沉淀,计算大豆乳清蛋白得率,结果如图6所示。
由图6可知,随着絮凝时间的增加,40 mL经氯化钙预处理的乳清废液中所沉淀得出大豆乳清蛋白的得率先升高后降低,在处理时间为40 min时得率达到最高。

图6 处理时间对大豆乳清蛋白沉淀效果的影响Fig.6 The effect of the time on the removal of soy whey protein
2.7 正交试验结果
根据上述四个单因素实验结果,分析各个因素对沉淀效果的影响程度,确定正交实验各个因素水平,设计正交实验,以每瓶40 mL废液进行实验,各试验均平行三组,根据正交实验结果,对数据进行正交分析,确定各因素对沉淀效果的影响程度的大小,从而得到最佳沉淀条件。

表1 L9(34)正交试验因素水平表Table 1L9(34)factors and levels of orthogonal test
根据表1进行四因素三水平正交试验,结果如表2。
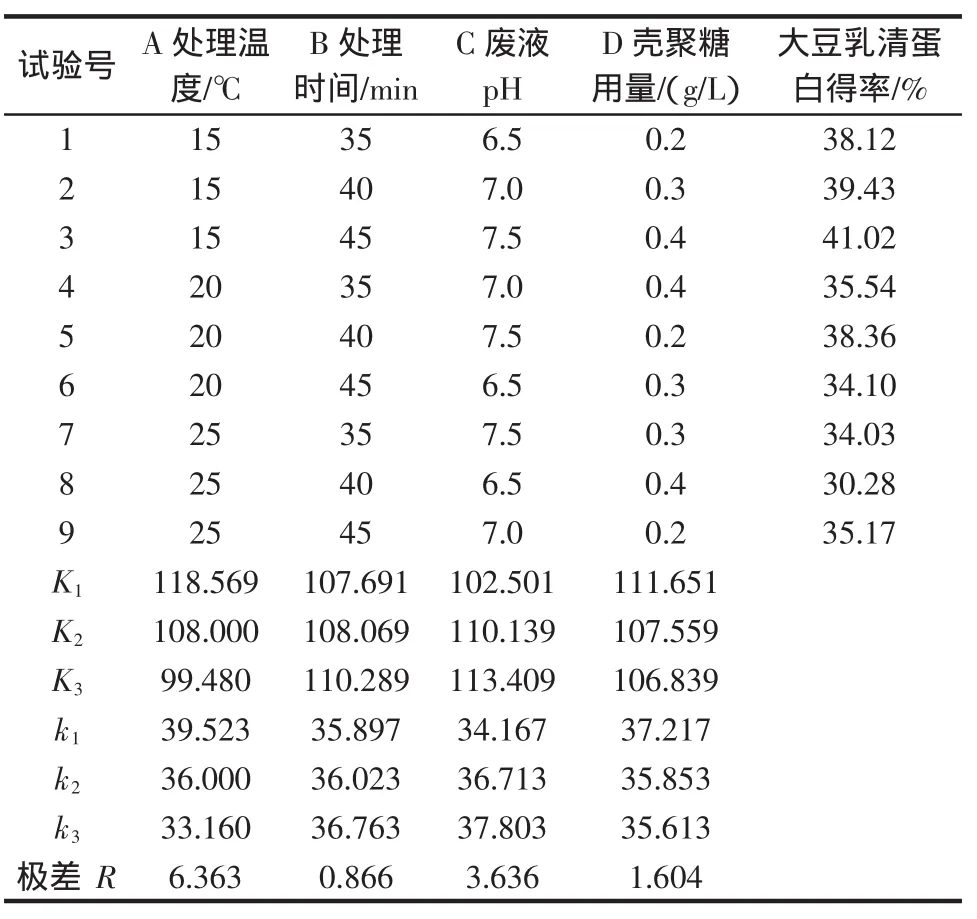
表2 四因素三水平正交试验结果Table 2 The results of four factors three levels orthogonal
由表2可知,大豆乳清废水中蛋白质的最优絮凝工艺条件为A1B3C3D3,即絮凝温度为15℃,絮凝处理时间为45 min,废液pH为7.5,絮凝剂壳聚糖用量为0.4 g/L。由极差分析可知,因素主次关系为A>C>D>B,即处理温度为主要因素,其次为废液的pH、絮凝剂壳聚糖用量和处理时间。在最佳工艺条件下,实验室处理1 L废水可得到大豆乳清蛋白-壳聚糖复合物干重1.018 g。将复合物用蒸馏水溶解,离心除去壳聚糖沉淀,测得上清液蛋白含量为0.618 mg/mL,计算得大豆乳清蛋白得率为41.48%。
3 结论
本研究采用二步絮凝法从大豆乳清废水中提取可溶性大豆乳清蛋白,确定了最佳提取工艺条件。一步絮凝采用CaCl2作为预处理剂,在其用量为18 mL/L时,效果最好,可除去大部分大豆分离蛋白;二步絮凝采用壳聚糖作为絮凝剂,在处理温度15℃,处理时间45 min,废液pH7.5,壳聚糖用量为0.4 g/L时,大豆乳清蛋白-壳聚糖复合物最高得率可达68.3%,此复合物加入蒸馏水后,不溶性的壳聚糖可以采用离心方法去除,得到可溶性大豆乳清蛋白,然后对可溶性大豆乳清蛋白透析脱盐真空冷冻干燥,最终蛋白得率为41.48%,即每升大豆乳清废液可以得到0.618 g可溶性大豆乳清蛋白。此技术工艺简单易行,条件温和,可用于工业生产,但是对所得到的大豆乳清蛋白的功能性研究还要进一步探讨,以期为大豆乳清蛋白的工业化生产提供基础参考。
[1] 赵冬梅.豆制品生产中高浓度废水的检测与分析[J] .食品与发酵工业,2006,3(1):68-71
[2] 刘国庆,朱翠萍.大孔树脂对大豆乳清废水中异黄酮的吸附特性研究[J] .离子交换与吸附,2003,19(3):229-234
[3] Pouliot Y,Wijers M C,Gauthier S E,et al.Fraetionation of whey protein hydrolysates using charged UF/NF membranes[J] .Journal of Membrance Science,1999,158(1/2):105-11
[4] Zydney A L.Protein separations using membrane filtration:new opportunities for whey fractionation[J] .Int Dairy Journal,1998,8(3):243-250
[5] Alkhatim H S,Alcaina M,Sofiano E,et al.Treatment of whey effluent from dairy industries by nanofihration membranes[J] .Desalination,1998,119(1/3):177-184
[6] 陈爱梅,江连舟,欧阳占亮.大豆乳清蛋白功能特性的研究[J] .中国油脂,2006,31(2):28-30
[7] Mugio BN,Vebersax M A.Characterization and bioconversion of great northern bean blanch effluent[J] .J Food Sci,1985,50(4):918-921
[8] V Lagranye.乳清蛋白及其新组分的性质、功能和新用途[J] .中国乳品工业,1999,27(2):24-27
[9] 许家喜.蛋白质的检测方法与乳制品中蛋白质含量测定[J] .大学化学,2008,24(1):66-69
[10] 刘国庆,罗敏,龙国萍,等.大豆乳清的预处理[J] .膜科学与技术,2003,23(5):42-46
[11] 吴海波,江连洲,陈爱梅.超滤法回收大豆乳清蛋白前预处理的研究[J] .食品与发酵工业,2006,36(14):104-110
[12] 赵丽颖,符群.膜分离技术在大豆乳清废水回收中应用[J] .粮食与油脂,2002(9):48-49
