逆流等温尿素合成的热力学分析(续二)
2014-06-26
(中国化工学会化肥专业委员会,上海 200062)
5.4 盘管外尿素合成液的热力学分析
前已述,在理想状态下,十字盘管出口处,L1物系已是不含气体NH3和CO2的熔融液,为全液相状态的NH4COONH2―NH3―H2O物系,仅含少量惰性气体。当其输出并与底部进入的30%液氨混合后,成为L2物系,亦为全液相物系,见图8(a)中F1点。由此可见,经过上述顶部进料逆流换热法处理,克服了传统底部进料方式在尿塔底部不可避免地会产生气液两相流的弊端,从而使液相物料在尿塔中停留时间增加,也保障了所有甲铵均享有相同且足够长的停留时间,促使尿素转化率提高。
下面讨论盘管外尿素合成液的热力学过程。
塔底溶液L2密度大,约为1 100 kg/m3。其在塔内缓慢向上移动过程中,随着时间的推移,液相中的甲铵会发生尿素合成第二反应,即甲铵脱水转化为尿素的反应:

此反应是一个速度较慢的弱吸热反应,热量由盘管内热物料中甲铵生成放出的热量提供。
反应生成物尿素和水都是高沸点物质,它们在溶液中浓度的提高,犹如在溶剂中加入了盐类物质,一方面使得物系平衡压下降;另一方面又促使尿素合成液的沸点升高。盘管内高温物料的热量除了作为甲铵脱水热之外,还使管外溶液温度升高至沸点。随着尿素合成转化率的增加,上行溶液中尿素和水浓度逐渐升高,物系平衡压逐渐下降,温度逐渐升高,此过程一直持续到塔顶。在反应时间保证的情况下,到达塔顶的尿素合成液可近乎达到化学平衡状态。
上述上行之尿素合成液的热力学过程可用图8(a)来描述。相图中的F1对应于L2物料点,随着反应的进行,上行物系之相图,由原先介稳态相图B1Z1C1(p22 MPa)逐渐向稳态相图过渡,直到F3,处于稳态相图(p17 MPa)B2Z2C2的液相区,近沸点状态。F3对应物料点为L3。
可见物系平衡压由22 MPa降到17 MPa,温度由180 ℃升高到192 ℃。
从温度变化图(图9)可见,塔底温差最大(Δt=14 ℃),塔顶温差最小(Δt=4 ℃)。这样呈梯形的温差配置也是符合尿素合成反应动力学需要的。
6 UTI等温尿素合成塔的动力学分析
NH3和CO2生成尿素的合成反应由两个串连的化学反应组合而成,先是NH3和CO2生成中间产物氨基甲酸铵(简称甲铵),然后液态甲铵脱水生成尿素。
(1)甲铵生成反应的动力学模型[5]
反应式:

尿素合成条件下,NH3与CO2呈超临界态,以F表示,是似气态的相态。
NH3与CO2生成甲铵的反应历程,可进一步分解为:
超临界态的NH3与CO2必须先溶解在液相中(第①步),然后才能进行第②步。换言之,甲铵生成反应也由两步组成,并且只有第②步是化学反应,没有物理溶解成为液态NH3与CO2的第①步,是不可能进行甲铵生成反应的。
甲铵生成反应速度常数k与绝对温度T之间的关系可用Arrhenius方程表示,即:
式中,A0为频率因子;Ec为化学反应活化能;Rg为气体常数。
甲铵生成反应的活化能Ec=2 420 cal/mol(1 cal=4.18 J,下同)。
经验告诉我们,阿氏活化能Ec小于10 000 cal/mol,反应速度不能由实验测出。一般化学反应之Ec为15 000~60 000 cal/mol,如后述的甲铵脱水转化为尿素的反应及大多数有机合成反应活化能均在此范围。
我们从动力学参数、活化能数据说明了甲铵生成反应是一个飞速反应,几乎在瞬间达到化学平衡。在尿素合成条件下,当NH3过量时,溶解态的CO2极快地几乎全部转化(化学平衡显示,有97%~98%的CO2转化)为液态甲铵。
(2)甲铵脱水生成尿素的动力学模型[5]
反应式:

此反应是一个在液相中进行的可逆化学反应,反应速度比较慢,需要一定时间,才能趋于化学平衡。因而本反应是尿素合成的控制步骤。
对于有水循环的动力学方程式,可用下式表示:
r=k1·cAM-k2·cU·cH2O
若将上式以CO2转化率(x)表示,则为:

积分表达式为:
可见,工业生产上连续反应器的尿素转化率x是一个隐函数:x=f(p,L,w,t,τ)
反应速度常数k1随温度变化规律亦可用Arrhenius方程式表示。
式中,A0=8.8×1013h-1
Ec=27 852 cal/mol
符号说明
F——超临界态;
l——液态或NH3/CO2(摩尔比);
w——H2O/CO2(摩尔比);
k——反应速度常数,h-1;
k1——正反应速度常数,h-1;
k2——逆反应速度常数,h-1;
A0——频率因子,h-1;
Ec——化学反应活化能,cal/mol;
Rg——气体常数,1.987 cal/(mol·K);
r——反应速度,kmol/(m3·h);
c——液相浓度,kmol/m3;
τ——反应时间,h;
t,T——摄氏温度,绝对温度;
x——实际CO2转化率;
p——物系压力。
下角标:
AM——甲铵;
H2O——水;
U——尿素;
平——平衡态。
应用上述动力学模型,可考察UTI尿塔稳态流动过程中,各反应区域,不同截面各参数(t,p,浓度)的变化情况。从而进一步认识UTI等温合成反应的技术真谛。
以UTI尿素合成塔的稳态物流图[图10(a)]为基础,反应可分为三个区域:混合区(LEn―Lin―L0);盘管区(L0―L1);尿素生成区(L2―L3―Lout)。
下面分别讨论各区的合成反应过程。
6.1 混合区反应过程
(1)化学反应 以尿素合成的第(1)反应为主,第(2)反应可以忽略。因为物料在本区内停留时间极短。
(2)传热状态 绝热,与外界无热交换。
(3)反应过程说明 NH3、CO2、甲铵液三股物料一起由物料总管从顶部进入,由于管径甚小,混合以高速方式进行。湍流促进了三股物料之间的混合,入料总管即为混合器。在混合物料氨过量的条件下,CO2瞬间全部生成甲铵,并溶入甲铵液,成为NH3―AM―H2O熔融液。无气态物(注:暂不考虑惰气影响)。
稳态流动状态下,a―a截面即属于上述情况[图10(a)]。

图10 UTI逆流等温尿塔动力学分析图
另一方面,因为第(1)反应是放热反应,因而伴随着甲铵的生成,还会同时瞬间放出大量反应热,从而使上述物系发生过热现象。过程如下。
在绝热和一定外压下(p外=21.38 MPa),上述氨―甲铵混合溶液成为受热介质(放出的热量首先被它吸收),并且,瞬间放出的强热必然导致受热介质迅速转变为过热态。由于该混合溶液的升温速度小于放热速度,因而,从时空概念来考察,即随着时间的流逝(或推移),过热溶液迅速以升高温度来处理热量。另一方面,在流动过程中,各截面上物料温度不断快速升高。
稳态流动状态下,到达b―b截面时(图10),即混合器入口,温度187 ℃。由相图可知,此时物系尚处于液相区,未到达沸点。从热平衡可知,物系仍为过热态。由以上分析可知,UTI所谓的混合器实际上主要作为液体物料分配器,将仍为过热态的液体物料均匀分配到各支盘管内。
随着时间的推移和空间的延长,在一定外压下均布于各支盘管内的过热物系将经历到达沸点,溶液中一部分甲铵及过剩氨分解、逸出为气体CO2和NH3的过程,物系由过热态转变为气液共存平衡的混合物。
由以上分析可知,顶部加料的另一重要作用在于,尽量缩短“时间”和“空间”,以使物系处于单一的液相状态。这样的处理保障物料均匀分布于各支盘管;反之,若延长“时间”和“空间”,物系可能成为气液混合物,则难以保障均匀分配至各支盘管。
稳态流动状态下,到达c―c截面时(图10)支盘管内温度196 ℃。
本区动态参数见表4。
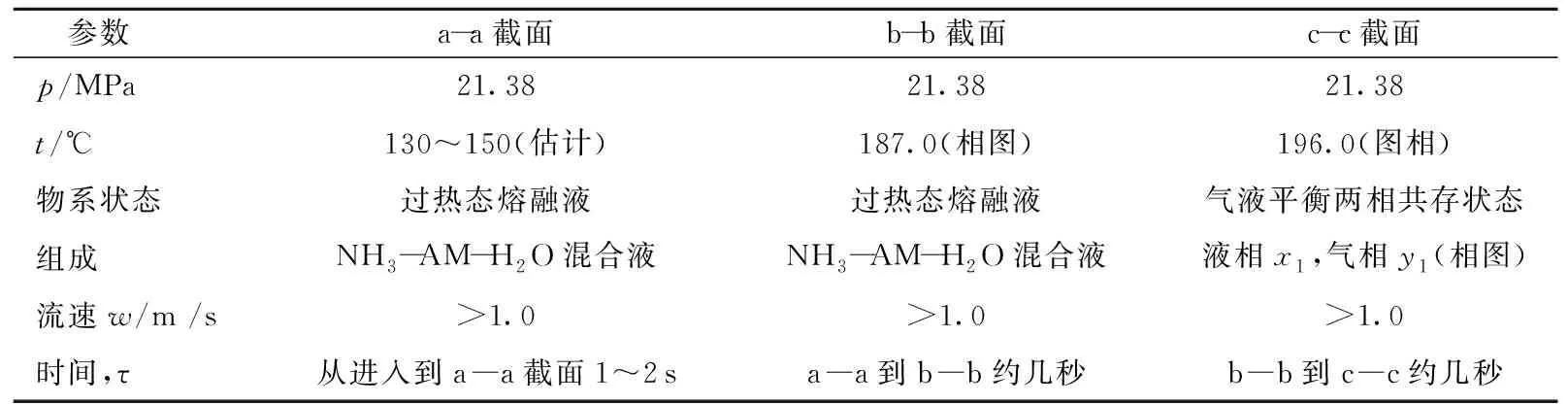
表4 混合区动态参数
6.2 盘管区的反应过程
(1)化学反应 仍以合成第(1)反应为主,因为在盘管内物料停留时间很短,可忽略合成第(2)反应。
(2)传热状态 输出热量。
(3)反应过程说明 c―c截面,支盘管顶端的物料均为呈平衡状态的气液两相之物流。随着盘管内气液混合物的下移,进行着甲铵生成反应与热量、质量传递相互交联在一起的动态反应。反应推动力来自于管壁内外的热量传递。说明于下。
由于盘管内物流(t196 ℃)与管外溶液(t192 ℃)存在温差,管内温度高,管外温度低,按热力学第二定律,管内热量向管外传递,从而推动盘管内动态反应的反复进行。
反应微元表达如下。
① 传热过程 盘管内物料向管外输出热量,管内物料温度降低。
② 相平衡 盘管内物料不再处于气液平衡状态,其平衡压逐渐降低,从而促使气相中NH3与CO2冷凝至液相。
③ 合成第(1)反应 上述的冷凝过程,推动着甲铵生成反应的进行:

④ 焓平衡 放出的热量QAM输出至盘管外,作为甲铵脱水热。
稳态流动状态下,随着时间的推移,动态反应的进行,物料下移,气相中NH3与CO2不断冷凝,盘管内气液混合物中液相量增加,气相量减少,物系温度亦逐渐下降。到达d-d截面[图10(a)]时,温度降为195 ℃[图10(b)]。
若设计合理,操作优化,当物料到达e-e截面时,盘管内所有的有效气体(即NH3与CO2)能全部冷凝溶入液相,成为全液态的混合物,NH3-AM-H2O。其甲铵生成热全部输出至盘管外的尿素合成溶液,作为甲铵脱水热。物系最终到达泡点,温度为194 ℃。
盘管区动态参数见表5。

表5 盘管区动态参数
6.3 尿塔区合成溶液反应过程
(1)化学反应 以合成第(2)反应为主。尿塔庞大的体积使液态物料有足够的停留时间来保证甲铵脱水转化为尿素。
(2)传热状态 溶液呈吸热状态。
(3)反应过程说明 流出盘管的液态物流与底部进入的30%液NH3混合后成为本区反应物流,为NH3-AM-H2O混合液,180 ℃。
合成溶液中甲铵脱水转化为尿素的条件有二。其一,为反应时间。因为合成第(2)反应是速度较慢的化学反应,需要足够的反应时间(在180~190 ℃,需30~40 min)才能达近于化学平衡。其二,热量供应。因为合成第(2)反应是弱吸热反应,需要不断提供热量才能使合成反应在一定温度下进行。同时,因为反应生成物(尿素和水)是高沸点物质,这些物质在溶液中的浓度提高,导致溶液沸点上升。由此,同样需要输入热量,保证反应速度。
稳态流动状态下,本区动态反应过程的优劣取决于两个因素:液态甲铵的停留时间;流动过程中热量的供给。
① 全液相溶液的制得 UTI尿塔在塔底得到NH3-AM-H2O液态混合物,为甲铵脱水反应时间提供了充分保证。
② 热量 反应所需热量从布置于溶液流经的高温盘管取得。
初始截面J-J 合成物料,xCO2约为0,t180 ℃;对应盘管t194 ℃。
顶部截面K-K 合成物料xCO2近于化学平衡,t192 ℃;对应盘管t196 ℃。
尿塔区动态参数见表6。

表6 尿塔溶液动态参数
7 UTI尿素转化率分析
UTI设置逆流盘管换热,最终目标是克服传统尿塔的弊病,提高尿素合成转化率。
通过热力学和动力学综合分析,可以看出逆流进料换热方式将盘管打造成一个恒温发热部件,热源温度为196~194 ℃,如同静态高压釜的电热丝,用来加热吸热端物料,尿素合成液。
如果设计合理,盘管底部输出的应为纯液态氨-甲铵-水熔融物,如同静态高压釜的配料。
通过这样的处理,UTI逆流换热法便克服了传统合成塔底部进料带来的问题与缺陷。
第一,由于底部生成的物料全部为液相,不含气态CO2和NH3,故而密度高。相比之下,传统法气液混合物的密度低,因而UTI物料在塔内停留时间长,液相甲铵脱水反应时间随之增加,有利于尿素转化率的提高。
第二,所有甲铵已在塔底全部生成,而传统法则由于过热现象,在塔底仅有85%的甲铵生成,因而UTI的所有甲铵均享有全程脱水转化为尿素的反应时间。而传统法上中部“晚生成之甲铵”则由于停留时间大大低于底部甲铵而导致脱水反应时间严重不足。
由此,可以分析UTI的尿素实际转化率将趋近于平衡转化率;而传统法的实际转化率,则出现瓶颈现象。
下面试计算UTI合成的实际转化率。
(1)计算基础 以我国中型尿塔为计算基础。
设备参数 塔有效体积VR40 m3,塔径D1.4 m,塔高 26.4 m。
工艺条件p22 MPa,NH3/CO24.2,H2O/CO20.85,t192 ℃。
生产强度I=10 t/(d·m3)
(2)实际尿塔示意图(图11)
尿塔内设置混合器及盘管,占有一定体积,还设置有多层挡板及涡流板,以增强液流湍动,强化混合和提高传热效率。液流以活塞流从塔底缓慢上移,直到塔顶排出塔外。
(3)体积计算
混合器及盘管占塔总体积的15%~17%
惰气体积约3%
液相体积约80%(忽略挡板涡流板体积)
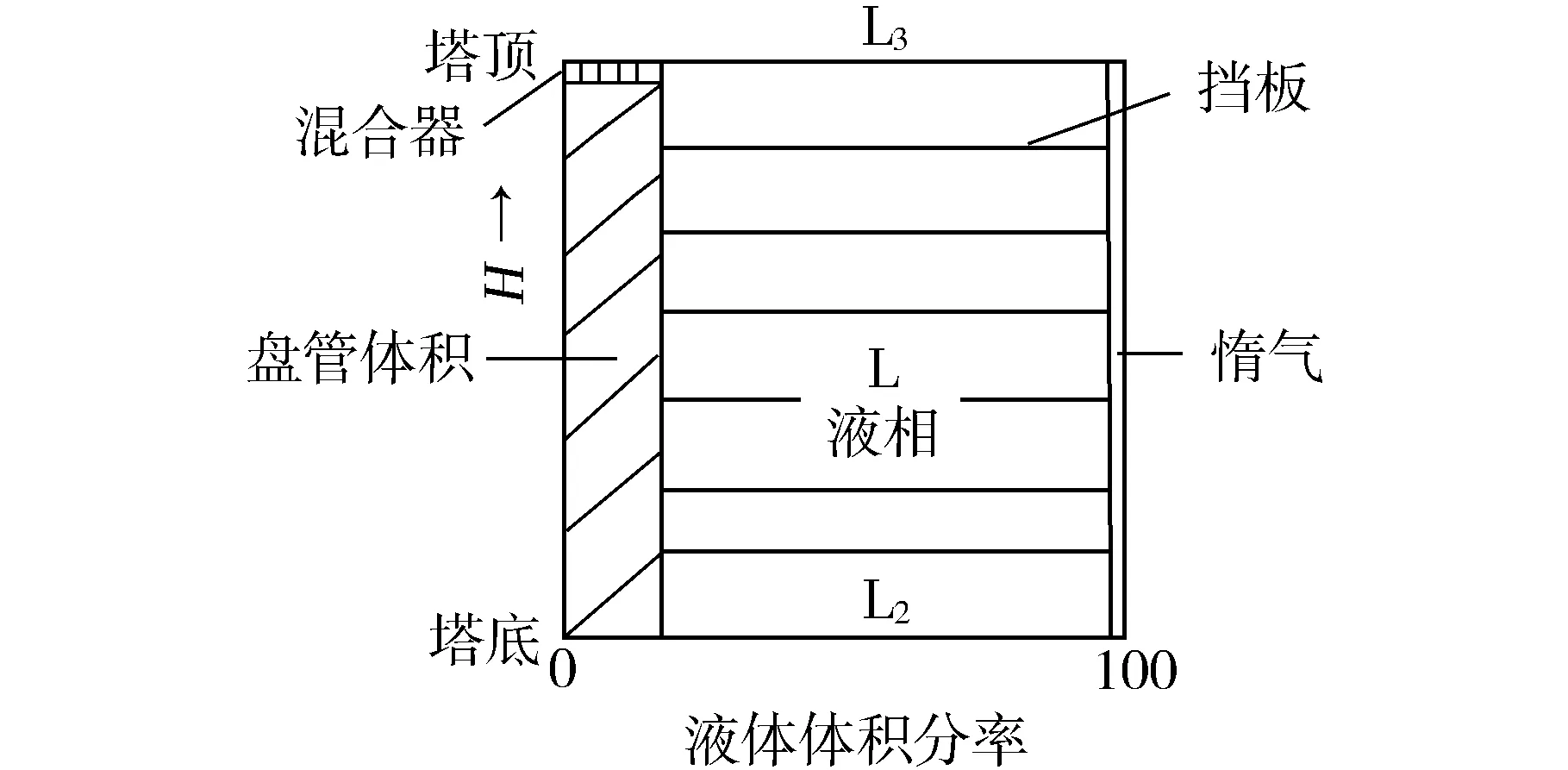
图11 UTI塔高-液相体积关系图
(4)溶液密度计算
塔底液相物料密度ρ底1 100 kg/m3。溶液从底部缓慢上移。甲铵脱水生成尿素和水,密度略有降低。当到达塔顶时物料趋于达化学平衡,ρ顶1 050 kg/m3。
(5)停留时间计算
VR——液相体积,m3;
ρav——平均密度,t/m3;
wt——质量流率,t/h。
经计算,VR=40×0.8=32 m3
ρav=(1 100+1 050)/2=1 075 kg/m3
=1.075 t/m3
wt=16.7×3.0=50.1 t/h
τ=32×1.075/50.1=0.69 h=41 min
(6)尿素实际转化率x实
由文献[4]可知,在160~190 ℃,液态甲铵在尿塔内停留20~30 min便能达化学平衡。
用动力学模型计算[5],当停留时间为40 min时,x实与x平基本上一致。

表7 逆流等温尿素合成工业数据
表7列出了UTI逆流换热等温尿塔工业装置实际转化率数据。可见实际合成转化率都高于平衡转化率,令人惊奇!本文暂且不去讨论x实大于x平的理论问题。工业装置需要的是x实越
高越好。因为x实越高,能耗越低。
参考文献:
[1]沈华民.工业装置尿素合成动态模型及其应用[J].氮肥与甲醇,2007,2(3):50~54;2007,2(4):54~58;2007,2(5):67~77;2007,2(6):45~51;2008,3(1):50~63;2008,3(2):50~54;2008,3(3):55~60;2008,3(4):62~68;2008,3(5):43~50;2008,3(6):37~47;2009,4(1):28~35;2009,4(3):54~63;2009,4(4):54~62.
[2]沈华民.工业尿素合成理论[J].化肥工业,2009,36(5):9~19;2009,36(6):17~26;2010,37(1):7~16;2010,37(2):11~17.
[3]沈华民.创新是尿素技术进步的灵魂[J].化工设计通讯,2012,38(2):1~12;2012,38(3):10~16.
[4]大连工学院无机化工专业译.日产1620公吨二氧化碳汽提法尿素操作手册[M].1975.
[5]沈华民.动力学模型[J].氮肥与甲醇,2008,3(2):50~54;中氮肥,2008,(6):10~13.
[6]Mavrovic.I.UTI尿素技术的开发[J].大氮肥,1989,(1):64.
