三水碳酸镁粒度分布影响因素的研究
2014-05-08沙作良LouhiKultanenMarjatta
韩 冰 ,沙作良 ,Louhi-Kultanen Marjatta
(1. 天津市海洋资源与化学重点实验室,天津科技大学海洋科学与工程学院,天津 300457,中国;2. 拉彭兰塔理工大学化学工艺学院,拉彭兰塔 53851,芬兰)
碳酸镁是一种非常复杂的化合物,是白色无气味的粉末状物质,依据其制备过程中MgCO3、Mg(OH)2和 H2O组成的不同量的比例和不同的形成条件可以形成不同的晶形和复盐,如无水菱镁矿(MgCO3)、三水碳镁石(MgCO3·3H2O)、五水碳镁石(MgCO3·5H2O)、纤菱镁矿(Mg5(CO3)4(OH)2·3H2O)和水菱镁矿(Mg5(CO3)4(OH)2·4H2O)等.由于这些化合物有着特殊的性质,因此可以应用到不同的工业领域,如药物、化妆品、橡胶、涂料和作为其他含镁化学材料的前体等[1–3].其中三水碳镁石和水菱镁矿有着独特的物理化学性质,它们的分解是吸热反应,分解出的二氧化碳和水都是无毒无害的,因此,在一定程度上这两种镁化合物可以用作阻燃物[4].
文献中报道了很多通过液液反应合成碳酸镁的过程.例如,用 MgCl2溶液与(NH4)2CO3或 Na2CO3溶液反应[5–7],或是通过 MgSO4·7H2O 溶液与 Na2CO3溶液反应[8]制备三水碳酸镁.如今,全球变暖已经变得越来越严重,所以二氧化碳的吸收是一个研究的热点,二氧化碳可以为碳酸镁的制备提供碳源.一些文献[9–11]已经报道了用二氧化碳作为反应物合成碳酸镁的沉淀结晶过程.Botha等[12]研究了通过鼓吹二氧化碳气体到氢氧化镁悬浊液中来析出碳酸镁化合物的过程,探讨了悬浊液的温度、盐酸的加入量、干燥温度和干燥时间等因素对沉淀过程的影响. Mitsuhashi等[13]介绍了改变氢氧化钠的加入量对氢氧化镁和二氧化碳反应生成碳酸镁结晶过程的影响,发现针状颗粒分布是由氢氧化钠的浓度决定的.结晶温度、反应物浓度、pH等因素会形成不同形态和大小的碳酸镁晶体.这些学者只考虑了在不同实验条件下会产生何种产品,然而,如何控制最终产品的粒度分布以及何种因素是影响产品的主要因素还没有阐述透彻.
本文以氢氧化镁和二氧化碳为反应物,研究不同因素对碳酸镁水合物的半间歇反应结晶过程的影响,找到在结晶过程中控制粒度分布的基本方法.
1 实 验
1.1 实验方法
实验用氢氧化镁(分析纯)和二氧化碳(纯度≥99.7%)作为初始反应物,用去离子水来配制氢氧化镁悬浮液.
实验装置如图1所示.
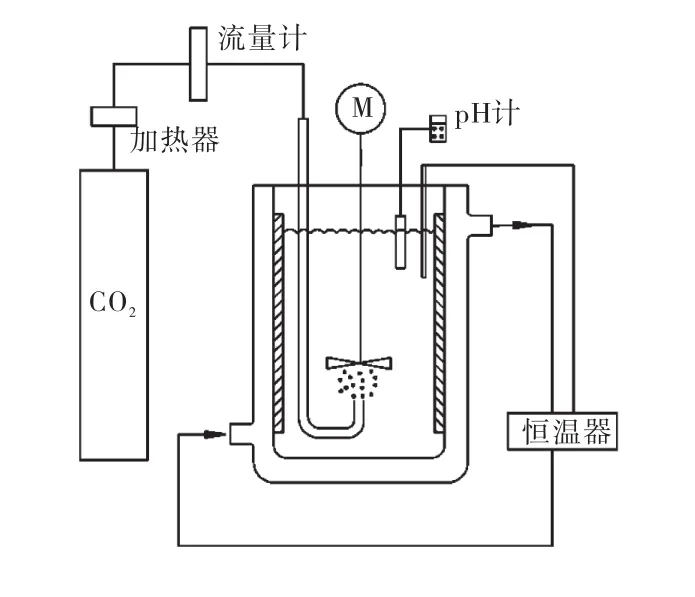
图1 实验装置示意图Fig.1 Schema of experimental set-up
间歇操作中,在一个带有夹套的玻璃结晶器中放入一定量的氢氧化镁和3,L去离子水,通过搅拌使其混合均匀.为了能够使悬浮液较好地悬浮和防止漩涡的产生,将 4个挡板均匀地放置在结晶器的内壁上.氢氧化镁悬浮液的温度采用连接于恒温器的外置探针监测.当悬浮液温度到达预期温度时,通过多孔气体分布器从结晶器的底部通入二氧化碳.在结晶过程中,pH计用于监测反应体系 pH的变化,当pH达到稳定时停止通入二氧化碳气体.反应结束时取出固液样立即进行过滤分离,将固相样在室温自然条件下晾干.这主要是因为在温度高的情况下晶体的组成和形态在干燥过程中可能会发生改变[12].
1.2 晶体分析
采用 Beckman Coulter LS13320 型激光粒度分析仪分析固相样的颗粒粒度分布.通过 X射线粉末衍射仪来鉴定产品的组成和水合物的形态.
2 结果与讨论
2.1 温度对产品粒度分布的影响
在二氧化碳通气流量为 9,L/min、搅拌速度为310,r/min、气体分布器孔径为60,µm和初始固体含量为 3.8%的情况下,选用了 25、40、62,℃ 3个温度进行半间歇反应结晶的研究,温度对最终产品粒度分布的影响如图2所示.
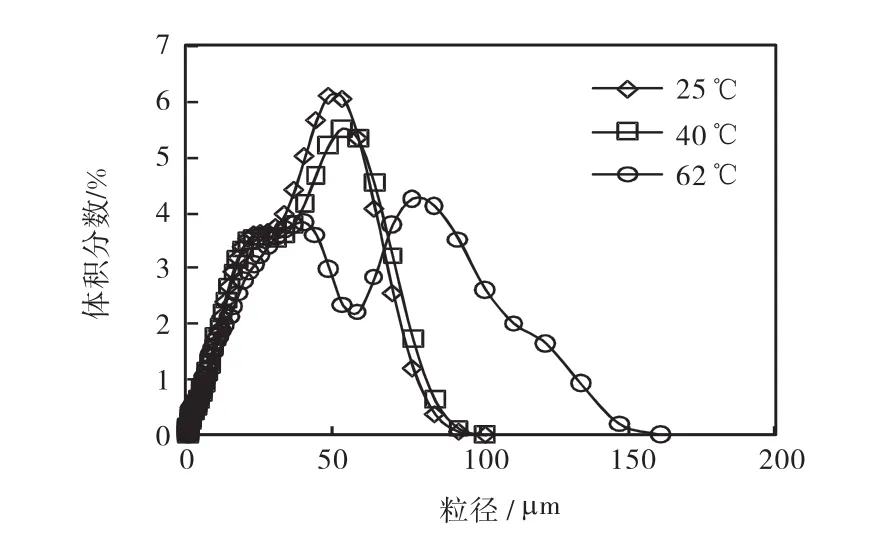
图2 温度对产品粒度分布的影响Fig.2 Effect of temperature on crystal size distribution of the final product
从图2可以看出:产品粒度随着温度的升高而逐渐增大,这与Wang等[5]得到的结果一致.从25,℃到40,℃,产品的粒度略有增大.在 62,℃时,粒度分布呈现了双峰形态,经 XRD鉴定,产品组成并没有发生改变,仍然是三水碳酸镁.由于温度的升高有利于气液两相的传质,增大了 CO2的溶解速率.当温度在25~40,℃时,CO2溶解速率的增加对于晶体生长有促进作用,因而造成晶体粒度有所增大.当 CO2溶解速率达到一定程度,在短时间内形成大量的碳酸镁,其主要是以成核的形式形成晶体,因而导致了晶核团聚现象.因此,62,℃时产品会出现双峰.另一方面,在温度较高时,溶液的黏度相对较低,溶液的表面张力较小,也是促进初级成核的另一因素.通过 pH监测结果可以得知反应温度越高,pH下降的速度越快,从而证实了 CO2的溶解速率随温度升高而加快的假设.
2.2 气体分布器孔径对产品粒度分布的影响
在 25,℃、固体含量 3.8%、二氧化碳通气流量9,L/min、搅拌速度 310,r/min的实验条件下,选择了40,µm与60,µm两个不同孔径大小的气体分布器,得到的最终产品粒度分布特征如图3所示.
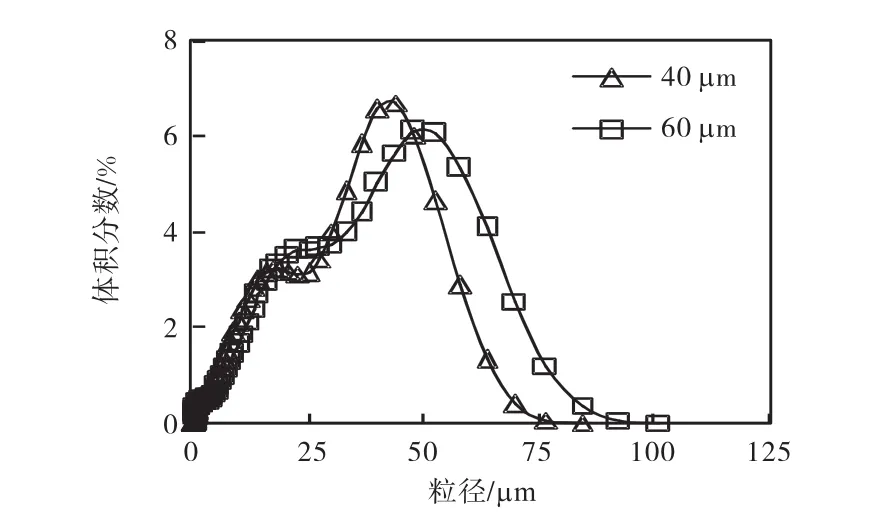
图3 气体分布器孔径对产品粒度分布的影响Fig.3 Effect of pore size of sparger on the particle size distribution of the final product
由图 3可以看出:随着气体分布器孔径的变大,产品的粒度增大.其原因是气体分布器孔径越小,气体在悬浮液中分散程度越好,气泡越小,从而增加了气液两相的接触面积,提高了两相间的传质速率,且增加了CO2的溶解速率.气体更易溶于液相中,液相中碳酸根的浓度越高,过饱和度越大,成核过程就越占优势,所以导致产品的粒度变小.从产品的粒度来看,过程主要还是成核,生长起的作用不太显著.
2.3 氢氧化镁悬浮液的初始固体含量对产品粒度分布的影响
Park等[14]发现氢氧化钙的初始固体含量能够影响结晶析出的碳酸钙的晶体粒度分布.因此,在本文研究的体系中,认为氢氧化镁的初始固体含量也有可能对碳酸镁的产品粒度产生影响.
在恒温 25,℃、搅拌速度 310,r/min、通气流量9,L/min、气体分布器孔径为40,µm的实验条件下,设置了 3个不同的氢氧化镁初始固体含量,分别为3.8%、2.9%、2.0%,研究它们各自的半间歇反应结晶过程,3个过程体系的 pH变化趋势如图 4所示.由图 4可知:随着氢氧化镁悬浮液初始固体含量的降低,体系的 pH降低速度加快.然而,在氢氧化镁悬浮液的初始固体含量为 2.0%时,反应结束时并没有晶体析出.这种情况有可能是二氧化碳把氢氧化镁都转化成了碳酸氢镁溶液,如文献[13]中采用二氧化碳和氢氧化镁制备碳酸氢镁溶液,然后再通过滴加氢氧化钠来控制三水碳酸镁的晶形.这很可能是二氧化碳的通气流量太大,导致 pH降低得太快而不能形成碳酸镁所造成的.为了证实我们的猜测,准备了相同固体含量(2.0%)的氢氧化镁悬浮液,其他条件均相同的情况下,以比较低的通气流量(1,L/min)进行测试,反应最后有极少量的晶体析出.由此可见,pH在整个结晶过程中起着非常重要的作用.
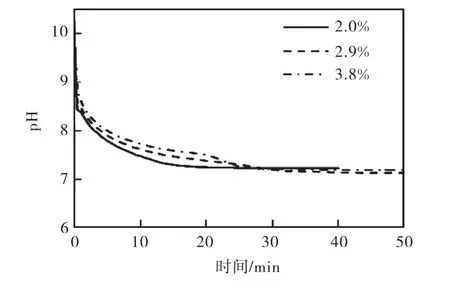
图4 氢氧化镁初始固体含量对体系pH的影响Fig.4 Effect of the initial slurry concentration of magnesium hydroxide on pH
在氢氧化镁初始固体含量为2.9%和3.8%的情况下与二氧化碳反应所得到的产品粒度分布结果如图5所示.
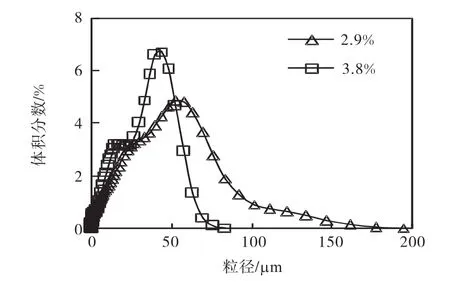
图5 氢氧化镁初始固体含量对产品粒度分布的影响Fig.5 Effect of initial slurry concentration of magnesium hydroxide on the particle size distribution of the product
从图 5可以看出:相比于初始固体含量为 2.9%的氢氧化镁悬浮液,固体含量为3.8%的悬浮液得到的碳酸镁晶体颗粒小.在反应开始阶段,不同固含量的悬浮液中镁离子的浓度是一样的,随着二氧化碳的通入,体系的pH降低,促进了氢氧化镁的溶解速率.在较高的氢氧化镁悬浮密度的情况下,具有较多的氢氧化镁颗粒,固液之间的界面面积相对较高,从而具有较高的溶解速率,提高了碳酸镁的过饱和度,加快了碳酸镁的成核速率,因此产品的颗粒粒度变小.
2.4 氢氧化镁晶体粒度对产品粒度分布的影响
为了研究氢氧化镁的晶体粒度对产品粒度分布是否存在影响,在结晶实验开始前,首先手工研磨氢氧化镁原料形成细小颗粒,采用激光粒度分析仪测量的晶体粒度分布如图6所示.由图6可知:研磨前氢氧化镁原料的中值粒径为 6.6,µm,研磨后的中值粒径为 2.9,µm.
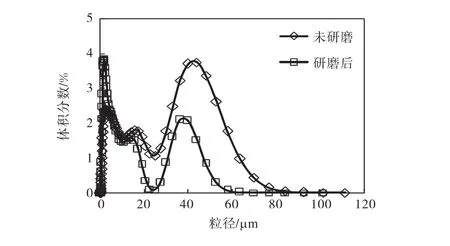
图6 研磨前和研磨后氢氧化镁晶体的粒度分布Fig.6 Crystal size distribution of raw and milled magnesium hydroxide
在恒温 25,℃、搅拌速度 310,r/min、初始氢氧化镁悬浮液固体含量 3.8%、气体分布器孔径为 40,µm时,采用5,L/min和9,L/min的通气流量,研究氢氧化镁初始晶体粒度对产品粒度分布的影响.在二氧化碳通气流量为 5,L/min时,使用不同粒度的氢氧化镁作为反应物,pH随时间的变化完全一样,而且结晶析出的碳酸镁产品的粒度分布也几乎完全相同.但是,在二氧化碳通气流量为 9,L/min情况下,氢氧化镁初始粒度的减小,促使体系 pH降低的速度加快,形成了较大颗粒的碳酸镁晶体,其产品粒度分布如图7所示.
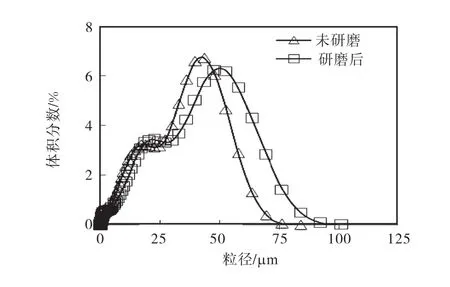
图7 二氧化碳气流量为 9,L/min时氢氧化镁初始粒度对最终产品粒度分布的影响Fig.7 Effect of the initial particle size of magnesium hydroxide on the particle size distribution of the final product at a flow rate of 9,L/min
粒度的减小,增大了溶解表面,提高了溶解速率,但是结晶过程主要还是由二氧化碳的溶解速率控制.当二氧化碳通气流量低的情况下,对于产品的粒度并没有很大影响,而高速率的气流量通入的时候,使得气液传质加快,相对提高了溶液的过饱和度,增加了生长速率,使得晶体变大.
2.5 结晶产物的鉴定
通过 XRD对所有产品进行鉴定,反应结晶所得到的最终产品均为三水碳酸镁,即三水碳镁石,与参考数据库中的 JCPDS 20-0669卡片匹配.该结果与文献[15]中报道的在室温条件下通常形成三水碳镁石的结果一致.但邵平平等[16]发现当温度高于323,K时三水碳酸镁会变为碱式碳酸镁.这与本文在 62,℃条件下仍然得到三水碳酸镁并不一致,不同温度下结晶产品的XRD谱图如图8所示.这可能是由于反应的体系,或者是液液反应和气液反应的机制不同所造成的.文献[17]中采用分子动态模拟方法说明:尽管镁离子比钙离子仅仅略小(因此有着较高的电荷密度),但是在镁离子周围的水分子寿命却约为数百皮秒,而像钙、钾、钠等离子周围水分子的寿命只有几皮秒.所以镁离子的亲水性极强,这对于在反溶剂过程中镁离子形成无水碳酸盐造成了很大的限制,所以一般条件下镁离子都会形成镁的水合物.
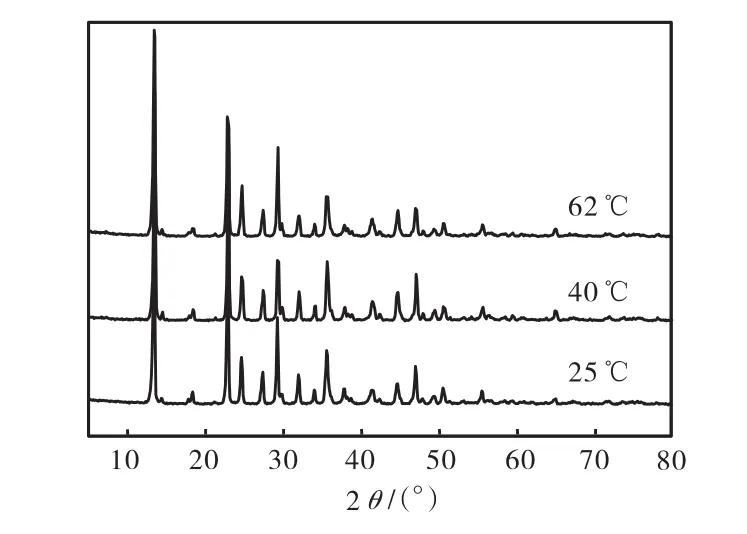
图8 不同温度下产品的XRD图Fig.8 XRD patterns of the products at different temperatures
3 结 语
在常温常压条件下,通过适当地调整操作参数,三水碳酸镁可以通过氢氧化镁悬浮液和二氧化碳的反应结晶得到,且三水碳酸镁一般在 pH 7~7.6形成.温度的升高和气体分布器孔径的增大,都会使最终三水碳酸镁产品的粒度增大.然而,氢氧化镁悬浮液初始固体含量的增大会形成较小的三水碳酸镁颗粒.研究结果还表明氢氧化镁粒度的大小对最终产品的粒度分布在二氧化碳通气流量低的情况下并没有影响,而在通气流量高的情况下产生了显著的影响.本文所研究的内容能够提供在气液固复杂的反应结晶过程中如何控制产品粒度分布的基本方法,这将对于结晶过程中最优操作条件的选取和过程的优化设计起到至关重要的作用.
[1] Birchal V S S,Rocha S D F,Ciminelli V S T. The effect of magnesite calcination conditions on magnesia hydration[J]. Minerals Engineering,2000,13(14/15):1629–1633.
[2] Freitag F,Kleinebudde P. How do roll compaction/dry granulation affect the tableting behaviour of inorganic materials? Comparison of four magnesium carbonates[J]. European Journal of Pharmaceutical Sciences,2003,19(4):281–289.
[3] Rittidech A,Portia L,Bongkarn T. The relationship between microstructure and mechanical properties of Al2O3–MgO ceramics[J]. Materials Science and Engineering:A,2006,438/439/440:395–398.
[4] Hollingbery L A,Hull T R. The thermal decomposition of huntite and hydromagnesite:A review[J]. Thermochimica Acta,2010,509(1/2):1–11.
[5] Wang Y,Li Z B,Demopoulos G P. Controlled precipitation of nesquehonite(MgCO3·3H2O)by the reaction of MgCl2with(NH4)2CO3[J]. Journal of Crystal Growth,2008,310(6):1220–1227.
[6] Cheng W T,Li Z B. Precipitation of nesquehonite from homogeneous supersaturated solutions[J]. Crystal Research and Technology,2009,44(9):937–947.
[7] 程文婷,李志宝,柯家骏. MgCO3·3H2O 晶体生长及晶形的影响因素[J]. 中国有色金属学报,2008,18(s1):230–235.
[8] Ohkubo T,Suzuki S,Mitsuhashi K,et al. Preparation of petaloid microspheres of basic magnesium carbonate[J].Langmuir,2007,23(11):5872–5874.
[9] Hänchen M,Prigiobbe V,Baciocchi R,et al. Precipitation in the Mg-carbonate system:Effects of temperature and CO2pressure[J]. Chemical Engineering Science,2008,63(4):1012–1028.
[10] Ferrini V,Vito C D,Mignardi S. Synthesis of nesquehonite by reaction of gaseous CO2with Mg chloride solution:Its potential role in the sequestration of carbon dioxide[J]. Journal of Hazardous Materials,2009,168(2/3):832–837.
[11] Teir S,Eloneva S,Fogelholm C J,et al. Fixation of carbon dioxide by producing hydromagnesite from serpentinite[J]. Applied Energy,2009,86(2):214–218.
[12] Botha A,Strydom C A. Preparation of a magnesium hydroxy carbonate from magnesium hydroxide[J]. Hydrometallurgy,2001,62(3):175–183.
[13] Mitsuhashi K,Tagami N,Tanabe K,et al. Synthesis of microtubes with a surface of “house of cards” structure via needlelike particles and control of their pore size[J].Langmuir,2005,21(8):3659–3663.
[14] Park S Y,Choi W S. Effects of operating factors on the particle size distribution and particle shape of synthesized precipitated CaCO3:Effect of reaction temperature,blowing rate of CO2gas and initial slurry concentration of Ca(OH)2on reaction completion time[J]. Advanced Powder Technology,2004,15(1):1–12.
[15] Langmuir D. Stability of carbonates in the system MgOCO2-H2O[J]. The Journal of Geology,1965,73(5):730–754.
[16] 邵平平,李志宝,密建国. 碳酸镁水合物在 283~363,K范围内的晶体组成及晶型[J]. 过程工程学报,2009,9(3):520–525.
[17] Jiao D,King C,Grossfield A,et al. Simulation of Ca2+and Mg2+solvation using polarizable atomic multipole potential[J]. The Journal of Physical Chemistry B,2006,110(37):18553–18559.
