电解液中氯化钾杂质对石墨电极性能的影响
2014-04-23彭琴,张志业,李宣丽等
电解液是电池的重要组成部分之一,对电池性能有着重要的影响[1]。而锂离子电池电解液中不可避免地含有少量杂质,如水、氟化氢、醇和其它金属杂质离子。杂质的含量对锂离子电池性能会产生重要影响[2-3]。电解液中水会引起LiPF6的分解形成LiF,氟化氢也会对六氟磷酸锂的水解起催化作用,同时电解液中的氟化氢会与电极表面上的SEI膜反应生成LiF。LiF导锂能力差,导致SEI膜性能变差,从而影响电池电性能[4]。U.Heider[5]等研究了向LiPF6电解液中掺杂一定含量的水后,HF含量呈现增长的趋势。郭亚菊[6]等也报道过在LiPF6电解液中,1个LiPF6分子能与2个H2O分子发生反应。庄全超[7]等研究了电解液甲醇杂质含量对石墨电极性能的影响,研究发现甲醇含量超过0.5%时,在首次充放电过程中,其会在2.0 V左右(vs.Li)分解,形成甲氧基锂沉积在石墨负极表面,影响电池的性能。
目前,其它杂质对锂离子电池电性能影响的报道较少,本实验室通过液相法制备六氟磷酸锂[8],产品中可能会残留微量的氯化钾。由此本文研究了氯化钾(KCl)对锂离子电池性能的影响。所用锂离子电池电解液为l mol/L LiPF6/(EC+DMC+EMC)(体积比1∶1∶1)。通过恒电流充放电测试、循环伏安测试研究KCl对天然石墨循环性能的影响,同时采用SEM、傅里叶红外分析研究了KCl对SEI膜的影响。
1 实验
1.1 仪器与试剂
真空手套箱(型号为5623103);新威电池测试系统(CT-3008W-5V5mA-S4); 电 化 学 分 析 仪 (LK9805);JSM-T500F型扫描电子显微镜;傅里叶变换红外光谱仪(Nicolet6700)。
基准电解液为1moL/L LiPF6/(EC+DMC+EMC)(体积比1∶1∶1)(电池级),氯化钾(分析纯),天然石墨(BTR-168)。
1.2 电池制备
石墨电极制备方法:将石墨、乙炔黑和聚偏氟乙烯(PVDF)按照85∶5∶10的质量比混合,添加一定量的N-甲基吡咯烷酮(NMP)调整浆料的粘度,置于球磨机中球磨,使浆料混合均匀,然后均匀的涂覆在铜箔上,在120℃下真空干燥12 h以上。冷却至室温后取出,用冲片机冲成直径为14mm的圆形电极片。
电池的组装在充满氩气的手套箱 (H2O<0.1×10-6,O2<10×10-6)中进行,使用CR2032型扣式电池壳,金属锂片为负极,锂片直径为15.6mm,Celgard 2400膜为隔膜。组装天然石墨/Li扣式半电池。
1.3 电池测试
扣式半电池组装好后,静置10 h在新威电池测试系统上进行恒电流充放电测试。充放电完成后用LK9805电化学分析仪对电池进行循环伏安(CV)扫描。工作电极为石墨负极,参比电极为金属锂片,扫描速度为0.1mV/s,电位为2~0.005 V。
经过CV测试后的电池在手套箱内拆开,石墨极片用碳酸二甲酯(DMC)清洗,除去表面的不溶物,在手套箱内自然干燥后,进行极片表面SEI膜形貌观察及成分分析。
2 结果与讨论
2.1 电池的循环性能
图1为室温下天然石墨/Li半电池以0.1 C循环5次,0.5C循环40次的充放电容量循环曲线。从图可知,KCl添加比例低于0.06%(质量分数)时对电池的放电比容量和循环性能影响不明显,添加0.06%KCl的电池与未添加KCl的电池放电比容量相当,一直保持在350mAh/g左右,且循环性能基本一致,较稳定。而添加0.1%、0.2%KCl的电池不仅放电比容量小于未添加KCl的电池放电比容量,而且循环性能不稳定。说明当KCl质量分数小于0.06%时,基本不影响石墨电极的充放电循环性,但大于0.1%时,则会影响电池的放电比容量和循环性能。

图1 室温下以0.5 C倍率充放电的天然石墨/Li电池的循环性能曲线
2.2 首次充放电性能
图2为石墨/Li半电池的首次充放电曲线。从图中可以看出,不同电解液首次充电比容量基本一致。而首次放电比容量有差别,添加0.06%KCl的电池与未添加KCl的电池首次放电比容量相当,在391mAh/g左右。而添加0.1%、0.2%KCl的电池首次放电比容量小于未添加KCl的电池,其中0.1%的首次放电比容量为364 mAh/g,0.2%的首次放电比容量为372 mAh/g。综上所述,KCl含量大于等于0.1%时,会降低天然石墨/Li半电池的首次放电比容量。
2.3 CV结果

图2 天然石墨/Li半电池的首次充放电曲线
图3为天然石墨电极在不同电解液中的首次循环伏安曲线。结果表明,天然石墨电极在所有电解液中的首次负向扫描过程中均出现两个还原电流峰,电极电位在0 V附近是锂离子的嵌入石墨层的还原峰[9],0.14 V左右的还原峰对应着EC还原分解形成烷基碳酸锂的过程[10],这一还原峰与SEI膜的成膜过程相关。添加0.06%KCl的氧化峰与未添加的曲线大致相同,氧化峰高而尖锐,对应锂的脱出过程,说明锂离子较完全脱出,这与充放电容量结果相符。而添加0.1%,0.2%KCl的氧化峰明显不尖锐,0.2%KCl还出现两个氧化峰,这一峰形变化也与KCl杂质含量有密切关系。说明添加KCl后没改变膜的成分,但添加质量分数大于0.1%KCl杂质时会影响锂离子在石墨电极的脱嵌,从而影响电池的电性能。

图3 天然石墨电极在不同电解液中的首次循环伏安图
2.4 天然石墨电极表面SEM表征
图4为天然石墨极片CV测试5次后的SEM图,结果表明,添加0.06%KCl的电解液与未添加KCl的电解液形成的SEI膜形貌相似,形成的SEI膜均匀疏松,有利于锂离子的迁移,而含0.1%,0.2%KCl的负极极片形成的SEI膜致密,影响锂离子的迁移,从而降低了电池的放电比容量和循环性能。

图4 天然石墨电极表面SEM图
2.5 天然石墨电极上SEI膜的结构与成份
图5为天然石墨电极在不同电解液中电化学循环后的FTIR图谱,结果表明,各极片在3 418 cm-1处的吸收峰可能是样片转移的过程中遇水吸潮导致出现O-H的伸缩振动峰。石墨电极在未添加KCl电解液中循环后的FTIR特征峰,在1 400 cm-1处出现的吸收峰为LiCO3的特征吸收峰[11]。在1 640、1 082、841 cm-1处出现吸收峰,为 EC的还原产物ROCO2Li的特征吸收峰[12-13]。添加0.06%、0.1%、0.2%KCl后分别在 1 502、1 400、1 503 cm-1处出现 LiCO3的特征吸收峰[11-14]。分别在 1 435和 1 088、1 039和 837、1 088 cm-1处出现ROCO2Li的特征吸收峰[12-13,15]。说明石墨电极表面在添加KCl前后的电解液中形成的SEI膜的主要化学组成基本相同,添加KCl后没有改变SEI膜的主要化学组成,只是各物质出现特征峰的位置有所变化。
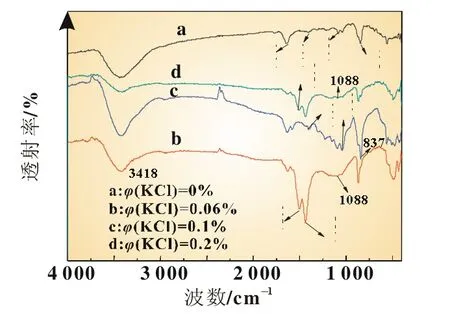
图5 天然石墨在不同电解液中电化学循环后的FTIR图谱
3 结论
通过充放电测试、CV研究了在l mol/L LiPF6/(EC+DMC+EMC)电解液中,不同氯化钾杂质含量对天然石墨电极性能的影响。研究结果表明,KCl对石墨电极性能的影响与电解液中KCl的含量有关,当KCl杂质质量分数小于0.06%时,基本不影响石墨电极的充放电循环可逆性,但大于0.1%时会降低石墨电极的循环性能和首次放电比容量。CV研究说明添加质量分数大于0.1%KCl杂质时会影响锂离子在石墨电极的脱嵌。由SEM、FTIR分析知,添加大于0.1%KCl时石墨电极表面SEI膜的主要化学组成没有改变,但使得SEI膜过于致密,影响了电化学循环过程中的嵌脱锂性能。结果显示,当KCl质量分数小于0.06%时,基本不影响电池电性能,该结论对液相法制备六氟磷酸锂工艺有一定的指导意义。
[1]郭炳焜,徐徽,王先友,等.锂离子电池[M].长沙:中南大学出版社,2002:202.
[2]郑洪河.锂离子电池电解质[M].北京:化学工业出版社,2006:43-44.
[3]郑洪河,姬建刚,张虎成,等.电解液中痕量HF对LiMn2O4电化学性能的影响[J].电源技术,2004,28(4):210-212.
[4]庄全超,武山,刘文元.锂离子电池电解液杂质的影响及去除技术[J].电池工业,2006,11(1):48-52.
[5]HEIDERU,OESTEN R,JUNGNITZM.Challenge inmanufacturing electrolyte solutions for lithium and lithium ion batteries quality control and m inim izing contam ination level[J].Journal of Power Sources,1999,81-82:119-122.
[6]郭亚菊,杨立,王保.LiPF6电解液对水的稳定性研究[J].电源技术,2007,31(2):136-139.
[7]庄全超,陈作锋,董全峰,等.锂离子电池电解液中甲醇杂质对石墨电极性能影响机制的电化学阻抗谱研究[J].高等学校化学学报,2005,26(11):2073-2076.
[8]王辛龙,李宣丽,张志业,等.一种六氟磷酸锂的制备:中国,102-659090A[P].2012-09-12.
[9]郑洪河,王显军,李苞,等.钾盐添加剂改善天然石墨负极的嵌脱锂性质[J].无机材料学报,2006,21(5):1109-1113.
[10]NAJIA,GHANBAJA J,HUMBERT B,et al.Electroreduction of graphite in LiClO4-ethylene carbonate electrolyte.Characterization of the passivating layer by transm ission electron m icroscopy and Fourier-transform infrared spectroscopy[J].JPower Sources,1996,63(1):33-39.
[11]ZHUANG G R V,ROSSPN.Analysis of the chemical composition of the passive film on Li-ion battery anodes using attenuated total reflection infrared spectroscopy[J].Electrochem Solid State Lett,2003,6(7):A136-A139.
[12]AURBACH D,MARKOVSKY B,SHECHTERA,etal.A comparative study of synthetic graphite and Lielectrodes in electrolyte solutions based on ethylene carbonate dimethyl carbonate mixtures[J].JElectrochem Soc,1996,143(12):3809-3820.
[13]VERMA P,MAIRE P,NOVÁK P.A review of the features and analyses of the solid electrolyte interphase in Li-ion batteries[J].Electrochim ica Acta,2010,55:6332-6341.
[14]AURBACH D,LEVIMD,LEVIE,etal.Failure and stabilization mechanisms of graphite electrodes[J].Journal of Physical Chem istry,1997,101(12):2195-2206.
[15]ZABAN A,AURBACH D.Impedance spectroscopy of lithium and nickelelectrodes propylene carbonate solutions of different lithium salts:A comparative study[J].JPower Sources,1995,54:289-295.
