血必净注射液中芍药苷的降解动力学研究
2014-04-11蒲位凌任晓亮邱喜龙张慧杰戚爱棣
蒲位凌, 任晓亮, 邱喜龙, 张慧杰, 戚爱棣
(天津中医药大学, 天津 300193)
血必净注射液中芍药苷的降解动力学研究
蒲位凌, 任晓亮*, 邱喜龙, 张慧杰, 戚爱棣
(天津中医药大学, 天津 300193)
目的 研究芍药苷 (Paeoniflorin) 在血必净注射液及水溶 液中, 不同 pH、 温 度下降解的 动力学规律。 方 法
芍药苷; 血必净注射液; pH; 温度; 降解动力学
血必净注射液是在中医药理论的指导下,经现代制剂工艺精制开发的中药复方注射液。该药由丹参、红花、川芎、当归和赤芍五味中药组成,临床上常与抗生素联用,治疗脓毒症及多器官功能障碍综合症[1-2]。 有文献报道其与炎症靶点 COX-2、 5-LOX、 IKK-2 之间存在较好的结合和抑制效应[3]。 有文献报道, 其对神经系统[4]、 免疫系统[5]、心血管系统[6]都有调节作用。 鲍天冬等[7]对芍药苷的体内药动学研究表明其在大鼠体内属于线性药动学过程。芍药苷为中药赤芍的有效成分之一[8], 也是血必净注射液中具有抗炎作用的活性成分之一,芍药苷量受产地、加工方法等多种因素的影响[9]。 冀兰鑫等[10]测定了血必净注射液中的11种主要成分, 其中芍药苷含有量较高。 本实验从化学反应动力学角度对比了芍药苷在血必净注射液中和水溶液中的降解规律,为完善该注射液的质控方法和改进剂型稳定性提供依据。
芍药苷为一种蒎烷单萜苷类物质,具有抗炎保肝的作用[11], 化学结构如图 1。 芍药苷结构中酯键、 糖苷键和缩醛结构,可能被酸或碱催化分解,即不稳定基团。有研究表明, 芍药苷在碱性及高温条件下不稳定[12-13]。 陈剑平[14]等研究表明芍药苷在不同制剂工艺因素下稳定性不同,加热温度及时间是影响芍药苷量的主要因素。因此对其稳定性的研究就较为重要,进而有利于血必净注射液的质量控制研究。
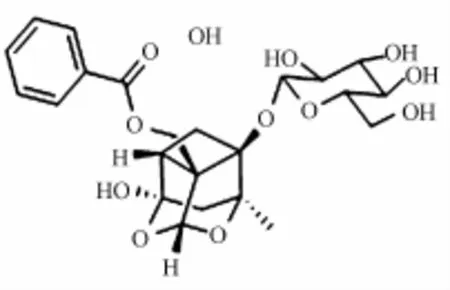
图1 芍药苷结构
1 仪器与试药
SHIMADZU高 效 液 相 色 谱 仪 ( 日 本 岛 津), SPD-20A UV-VIS 检 测 器; BT1250D分 析 天 平 (Sartorius公司); HH-8S 数显恒温水浴锅 ( 金坛市盛蓝仪器制造有限公司); DELTA 320 pH计 (瑞士 METTLER TOLEDO公司)。
血必净注射液 (天津红日药业股份有效公司, 规格为每支 10mL, 批号 1205301); 芍药苷对照品 (天津中新药业研究中心, 纯度≥98%); HPLC分析用乙腈为色谱纯(Sigma公司); 娃哈哈纯净水; 氢氧化钠、 碳酸钠、 浓盐酸均为分析纯。
2 方法与结果
2.1 分析方法的建立 Waters SymmetryTMRP18色谱柱 (4.6 mm×150 mm, 5 μm); 流动相为乙腈 (A)-水 (B) 梯度洗脱 (见表 1); 体积流量 1 mL/min; 柱温为室温; 检测波长 230 nm[15]; 进样量 10 μL。 其色谱图见图 2。
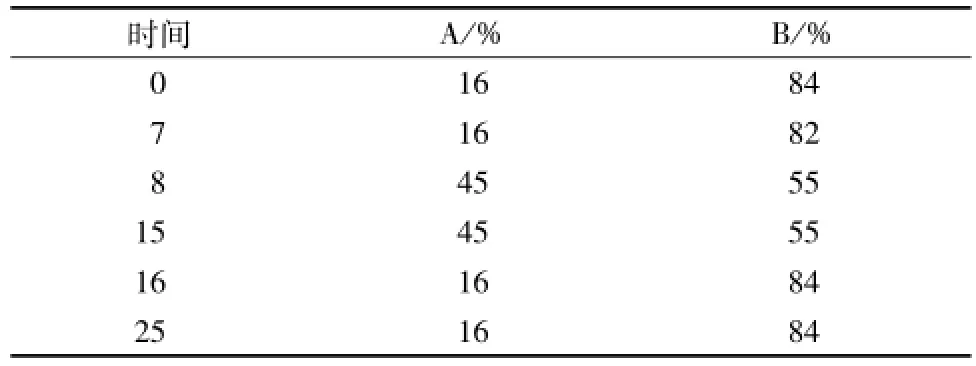
表1 梯度洗脱条件
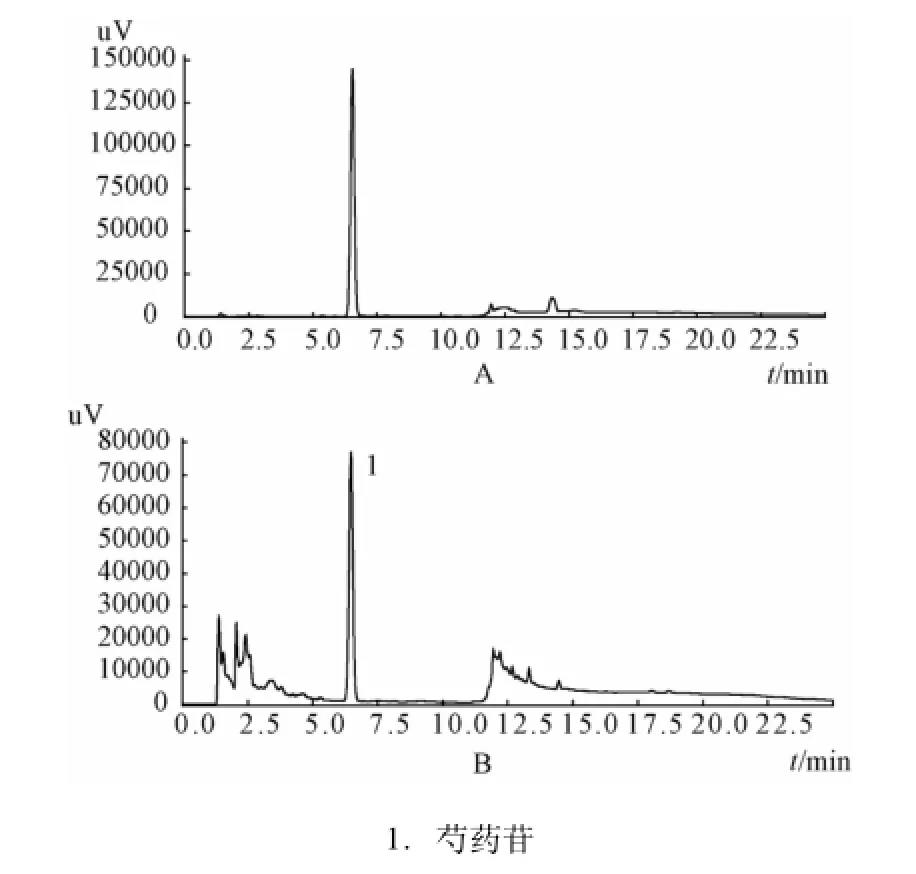
图2 芍药苷对照品 (A) 和血必净注射液(B) 的 HPLC色谱图
2.1.1 线性关系试验 精确称取 10.82mg芍药苷于 10mL棕色瓶中, 以纯水定容, 配制成质量浓度为 1.082 mg/mL的芍药苷贮备液。精密量取对照品贮备液适量,制得质量浓度分别为 5.41、 10.82、 21.64、 43.28、 64.92、 86.56、108.20 μg/mL, 置于 5 mL棕色量瓶中, 摇匀, 按 “2.1”项下的色谱条件, 将上述 7 份对照品溶液分别进样 10 μL,以峰面积 (Y) 为纵坐标, 质量浓度 (X, μg/mL) 为横坐标进行线性回归, 得回归方程:Y=1.416 4 ×104X-1 756,r=0.999 8。 结果表明, 芍药苷在 5.41 ~108.20 μg/mL范围内线性关系良好。
2.1.2 精密度试验 取 “2.1.1” 项下质量浓度为 21.62 μg/m L的对照品溶液, 重复进样 6 次, 记录峰面积, 计算得 RSD值为 0.5%。 表明仪器及进样精密度良好。
2.1.3 重复性试验 取芍药苷对照品贮备液 6 份, 分别用去离子水稀释至 21.64 μg/mL, 进样测定。 结果芍药苷RSD为 1.0%, 表明方法重复性良好。
2.1.4 加样回收率试验 精密量取芍药苷贮备液 130 μL和 100 μL血必净注射液于 5 mL棕色量瓶中, 涡旋混匀,以纯水定容至刻度。 平行配制6 份, 分别取上述溶液10 μL进 HPLC测定, 记录峰面积, 通过外标法计算, 得平均加样回收率为 99.86%, RSD为 1.0%, 见表 2。

表 2 加样回收率试验 (n=6)
2.2 芍药苷水溶液在不同环境下的稳定性研究
2.2.1 不同 pH的缓冲液及芍药苷贮备液的配制 用适量浓 HCl、 Na2CO3及 NaOH溶液配制 pH 1 至 pH 13 的一系列缓冲液。 另外, 将10 mL棕色量瓶用消毒酒精灭菌后, 精确称取 11.07mg芍药苷于量瓶中, 以纯水定容, 配制成质量浓度为 1.107 mg/mL的芍药苷贮备液。
2.2.2 芍药苷在不同 pH下的稳定性研究 取芍药苷贮备液 275 μL, 置于经酒精灭菌 5 mL的棕色量瓶中, 用一系列缓冲溶液分别定容至刻度,涡旋混匀,得到芍药苷在不同 pH条件下的样品溶液, 分别用 HPLC测定溶液中芍药苷的初始质量浓度 (C0)。 将样品溶液密封并于室温条件下放置,间隔一定的时间对样品取样,测定溶液中芍药苷的剩余质量浓度 (Ct)。 按照上述方法重复实验一次。 以芍药苷剩余质量浓度的对数 [ln(Ct/C0)] 对时间 (t) 作图,见图3。
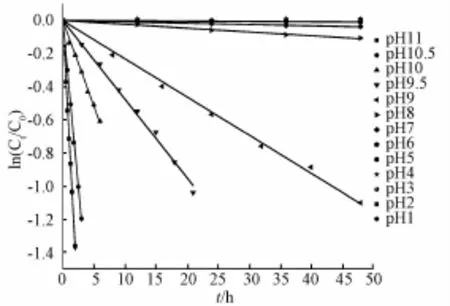
图 3 在不同 pH条件下芍药苷在水溶液中相对剩余质量浓度对数 [ln(Ct/C0)] 与时间 t关系图
将测定结果进行拟合,拟合结果可得芍药苷的降解过程符合一级动力学,其相关动力学方程、降解速率常数(k) 等见表 3。
pH与 lnk 的关系作图。 由图 3 可知, 芍药苷水溶液在酸性条件 (pH2 ~6) 下较稳定, pH1 中有极缓慢的降解,在中性和碱性条件下不稳定。 当 pH>9 后, 降解速率明显加快。
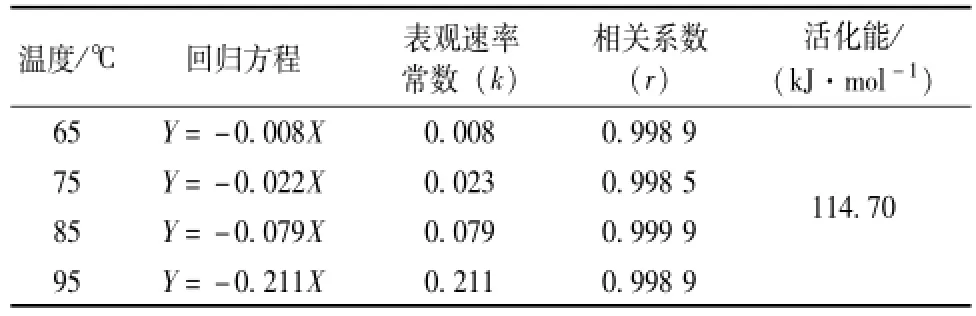
表3 在不同温度下芍药苷降解动力学曲线拟合结果
2.2.3 芍药苷在不同温度下的稳定性研究 移取 275 μL芍药苷贮备液置于 5 mL灭菌量瓶中, 以超纯水定容,混匀, 制得样品溶液, 并分别用 HPLC测定溶液中芍药苷的初始质量浓度 (C0)。 将样品溶液密封, 分别置于温度为65、 75、 85、 95 ℃的恒温水浴锅中, 间隔一定的时间对样品取样, 测定溶液中芍药苷的残余质量浓度 (Ct)。 按照上述方法重复实验一次。 以芍药苷剩余质量浓度的对数 [ln (Ct/C0)] 对时间 (t) 作图, 见图 4。
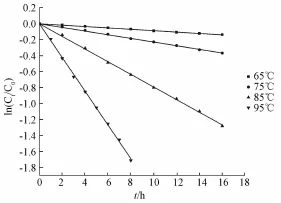
图4 芍药苷在不同温度下相对剩余质量浓度对数值[ln Ct/C0] 与时间 (t) 关系图
通过对芍药苷在水溶液中在不同温度下降解得到的拟合曲线方程可知其表观速率常数 k, 并根据阿仑尼乌斯方程 ln k=ln A-Ea/RT, 可计算其活化能, 结果见表 3。 结果表明,芍药苷在水溶液中的降解反应速率随温度的升高而加快,该反应呈现一级动力学规律,反应的活化能较高,表明芍药苷在中性水溶液中较为稳定。
2.3 芍药苷在血必净注射液中的稳定性研究
2.3.1 血必净注射液中的芍药苷在不同 pH下的稳定性研究 用适量浓 HCl、 Na2CO3及 NaOH溶液配制 pH1 至 pH13的一系列缓冲液。 取血必净注射液 200 μL, 置于经酒精灭菌5 mL的棕色量瓶中, 用一系列缓冲溶液分别定容至刻度, 涡旋混匀, 得到注射液在不同 pH条件下的样品溶液,分别用 HPLC测定溶液中芍药苷的初始质量浓度 (C0)。 将样品溶液密封并于室温条件下放置,间隔一定的时间对样品取样, 测定溶液中芍药苷的剩余质量浓度 (Ct)。 按照上述方法重复实验一次。 以芍药苷剩余质量浓度的对数 [ln (Ct/C0)] 对时间 (t) 作图, 见图 5。 pH与 ln k的关系见图 6。 根据数据可知注射液中芍药苷在碱性和强酸 (pH 1)环境不稳定, 在酸性 (pH 2 ~6) 条件下稳定。
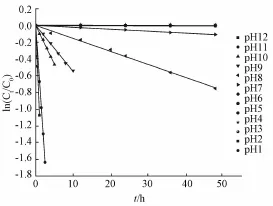
图5 不同 pH条件下芍药苷在血必净注射液中相对剩余质量浓度对数值 [ln(Ct/C0)] 与时间关系图

图6 在不同溶液中芍药苷的降解速率常数 (ln k) 的比较
2.3.2 血必净注射液中的芍药苷在不同温度下的稳定性研究 移取 200 μL血必净注射液于 5 mL灭菌量瓶中, 以超纯水定容, 混匀, 制得样品溶液, 并分别用 HPLC测定注射液中芍药苷的初始质量浓度 (C0)。 将样品溶液密封,分别置于温度为 65、 75、 85、 95 ℃的恒温水浴锅中, 间隔一定的时间对样品取样,测定溶液中芍药苷的残余质量浓度 (Ct)。 按照上述方法重复实验一次。 由不同时间对芍药苷剩余质量浓度的对数 [ln(Ct/C0)] 对时间 (t) 作图,见图7。结果表明, 芍药苷在血必净注射液中的降解反应速率随温度的升高而加快,该反应呈现一级动力学规律,反应的活化能较高, 见表 4, 表明芍药苷在血必净注射液中较为稳定。
2.4 各 pH条件下的半衰期和有效期预测

图7 在不同温度下芍药苷在血必净注射液中相对剩余质量浓度 对 数 值 [ ln( Ct/C0)] 与时 间 关系图
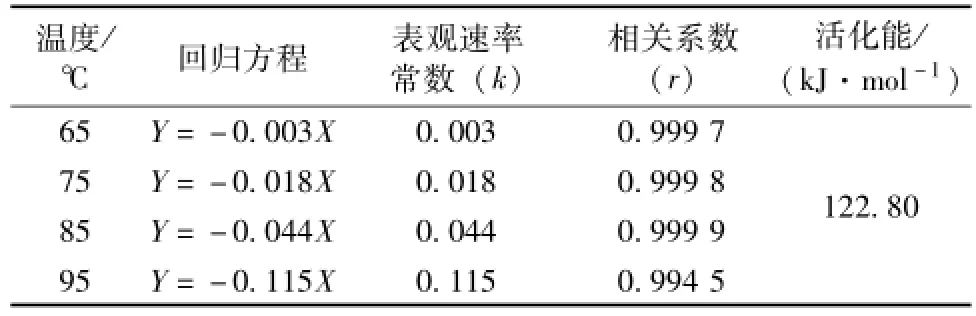
表4 在不同温度下注射液中芍药苷降解动力学曲线拟合结果
芍药苷分别在水溶液和血必净注射液中不同 pH下降解,测得两种介质中芍药苷的相对剩余含量相比较,根据一级反应速率方程 ln(C0/Ct)=kt, 计算降解速率常数 k、有效期 t0.9和半衰期 t0.5, 如表 5。 芍药苷在不同溶液中降解速率 ln k对 pH作图。 结果表明, 芍药苷在水溶液和血必净注射液中的降解趋势一致,在注射液中的稳定性稍高于水溶液。
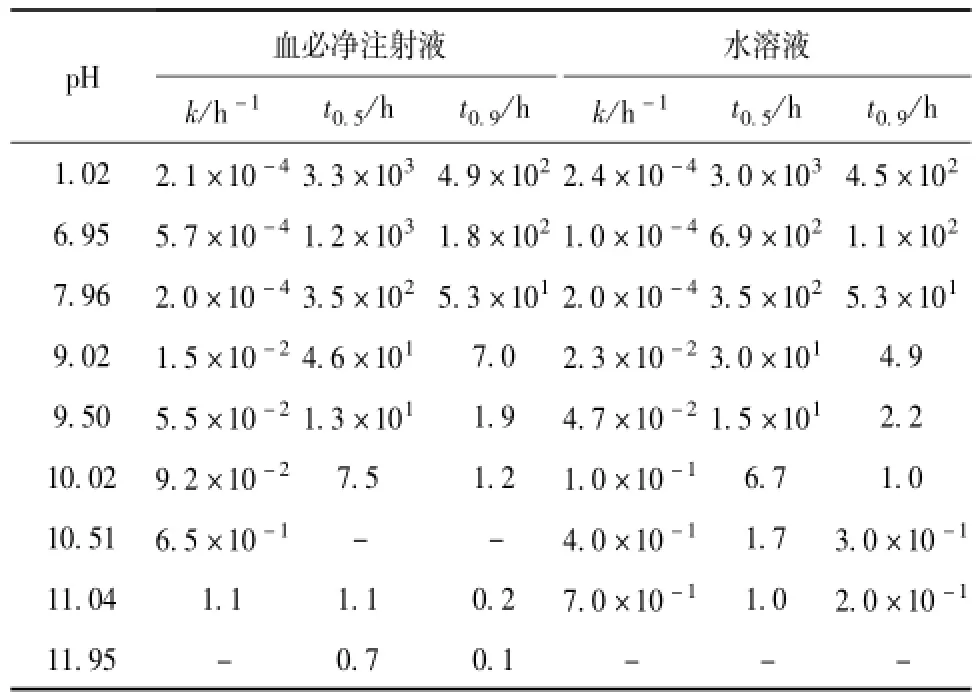
表 5 在不同 pH溶液中芍药苷试验结果的比较
2.5 各温度下半衰期及有效期预测 芍药苷分别在水溶液和血必净注射液中不同温度 (65, 75, 85, 95 ℃)下降解,测得两种介质中芍药苷的相对剩余质量浓度相比较, 根据公式 t0.5=ln2/k和 t0.9=0.105 4/k预 测 有 效期 t0.9和半衰 期 t0.5, 如 表 6 。 芍 药 苷 在 不 同 溶 液 中 降 解速率 ln k对 1/T作图 ( 图 8) 。 结果表明, 芍药苷在水溶液和血必净注射液中的降解趋势一致,在注射液中的稳定性稍高于水溶液中。

表6 在不同温度下芍药苷试验结果的比较

图 8 温度 (1/T) 与芍药苷降解速率常数 (ln k) 之间的关系
3 结论与讨论
3.1 实验结果表明, 在加热和碱性条件下, 芍药苷的降解属于一级动力学反应。 另外, 在强酸条件下 (pH1), 芍药苷在室温条件下也有很缓慢的降解,推测可能是由于酸碱降解机理不同造成。通过对比芍药苷在水溶液和血必净注射液中的降解速度可知,二者降解趋势大体一致,但芍药苷在血必净注射液中比在水溶液中稳定,即制剂水平下芍药苷较稳定。本实验为芍药苷的使用、贮存及制剂研究和质量控制提供了依据。
3.2 在 pH1 ~13 一系列的缓冲溶液体系下, 当 pH大于 12后, 降解过快, 故本实验结果中 pH的上限为: 水溶液中pH为 11, 注射液中为 12。 芍药苷在 pH2 ~6 的条件下稳定, 故在图表中未显示 pH2 ~6 的数据结果。 另外, 为准确表征其降解速率变化较快的区间,实验中在降解速度变化较大的 pH区间进一步缩小 pH间隔以更精确的描绘降解速率随 pH变化的趋势。
3.3 芍药苷为蒎烷型双环单萜苷, 其中有酯键、 苷键及缩醛结构。酯键在碱催化下较易发生水解反应;糖苷键中的苷键原子在酸性环境中易被质子化而裂解;缩醛结构在酸性条件下也易断裂。在对其降解产物进行梯度洗脱,发现其中有几种新物质出现,初步判定其为降解产物。其降解产物及降解机理需进一步实验确定。
3.4 波长及流动相选择 考虑分析时间及分离效果等因素, 采用乙腈-水为流动相, 由于注射剂成分较复杂, 采用梯度洗脱并用高比例乙腈将干扰成分全部洗脱。芍药苷的最大吸收波长为 230 nm, 在此波长下, 芍药苷响应值高,而且在注射剂中的选择性高,其他成分不干扰芍药苷测定,故选择 230 nm为测定波长。
[ 1 ] 王金达, 雪 琳.细菌、 内毒素、 炎性介质并治——治疗重症脓毒病的新对策[J].中国危重病急救医学, 1998, 10 (6):323.
[2] 高红梅,常文秀,曹书华.“血必净” 注射液对内毒素刺激的内皮细胞的影响[J].中国急救医学, 2005, 25(6):437.
[3] 马世堂,刘培勋,龙 伟,等.血必净抗炎作用药效物质基础和多靶点作用效应[J].物理化学学报, 2009, 25(10): 2080-2086.
[ 4 ] Chang Yan, Zhang Lei, Wang Chun, etal.Paeoniflorin inhibits function of synoviocytes pretreated by rIL-1α and regulates EP4receptor expression [ J] .J Ethnopharmacol, 2011, 137 (3):1275-1282.
[ 5 ] 孙丽荣, 曹 雄, 侯凤青, 等.芍药苷研究进展[J].中国中药杂志, 2008, 33(18):2028-2032.
[ 6 ] Lin Jingrui, Bi Kaishun, Wang Lingzhi, et al.Inhibitory Effects of Paeonidlorin on ACE Activity in Vitro[ J] .Mode Tradit Chin Med Mater Med, 2009 , 11(2):249-252.
[ 7 ] 鲍天冬, 张英丰, 李玉洁, 等.LC-MS 研究炒白芍提取物中芍药苷在大鼠体内的药代动力学[J].中国中药杂志,2010, 35(9):1193-1196.
[ 8 ] 杨媛媛, 周 刚, 马晓康, 等.赤芍的研究进展[J].医药导报, 2008, 27(1):67-69.
[9] 吕 华,郭兰萍.不同因素对白芍中芍药苷含量的影响研究进 展 [ J].中 国 医 院 药 学 杂 志, 2012, 32(20): 1643-1645.
[10] 冀兰鑫, 黄 浩, 姜 民, 等.HPLC测定血必净注射液内11 种主要 成分 [ J].中 国 中 药 杂志, 2010, 35(18): 2395-2398.
[11] 全国中草药会编编写组.全国中草药汇编: 上册[M].2版.北京: 人民出版社, 2000:290.
[12] 姚仲青, 朱 虹, 姚海峰.温度及 pH对赤芍总苷稳定性的影响[J].时珍国医国药, 2006, 17(7):1214-1215.
[13] 闫兴丽, 张建军, 李小燕, 等.温度对白芍药材、 白芍提取物及乾坤清颗粒成品中芍药苷含量稳定性的影响[J].中草药, 2003, 34(2):131-133.
[14] 陈剑平, 林荣锋, 张惜强, 等.滋肾宁神胶囊中芍药苷在制剂工艺中的热稳定性考察[J].中成药, 2010, 32(5):767-769.
[15] 李中娥.HPLC法同时测定妇科分清丸中阿魏酸和芍药苷[J].中成药, 2012, 34(3):487-489.
927.11
:B
:1001-1528(2014)02-0404-05
10.3969/j.issn.1001-1528.2014.02.045
2013-02-05
国家 自 然 科 学 基 金 青 年 基 金 项 目 (81102732); 教 育 部 高 等 学 校 博 士 学 科 点 专 项 科 研 基 金 新 教 师 基 金 项 目(20111210120006)
蒲位凌 (1988—) , 女, 硕士生, 研究方向: 药物分析。 Tel:15202206313, E-mail:linlin8229@163.com
*通信作者: 任晓亮 (1980—) , 男, 研究方向: 药物分析。 Tel:(022)59596221, E-mail:xiaoliang-ren@sina.com
采用高效液相色谱法 (HPLC) 考察不同 pH和温度对芍药苷稳定性的影响, 利用化学反应动力学模型及 Arrhenius公式分析芍药苷在不同条件下的降解规律并计算降解反应动力学参数。结果 芍药苷在碱性和加热时降解较快,符合一级动力学规律, 碱性条件下随pH升高, 降解速度明显增加。 计算得芍药苷在水溶液和血必净注射液中降解活化能分别为 114.70 kJ/mol和 122.80 kJ/mol。 结论 芍药苷在碱性和强酸性条件下不稳定。 相同条件下, 芍药苷在血必净注射液中的稳定性都要高于其水溶液。
