甲基绿探针吸收光谱法测定安乃近
2014-03-26谭建红
谭建红,黄 惟,江 虹
(长江师范学院 化学化工学院,重庆 408100)
安乃近(ANG)是一种重要的解热镇痛类药物,由氨基比林和亚硫酸钠结合得到,在临床上广泛用于感冒、头痛、发热、肌肉关节痛、牙痛、痛经、风湿及类风湿关节痛等的治疗,其解热镇痛效果快而强,使用方便,价格低廉,优于其他解热镇痛药。目前,测定安乃近的方法主要有滴定法[1]、高效液相色谱法[2-5]、电化学分析法[6-8]、紫外分光光度法[9-10]、红外光谱法[11]、荧光分析法[12]、化学发光法[13-15]等。这些方法使用仪器或较贵不易普及或操作麻烦费时、灵敏度较低等,不适用急检需要。本实验在碱性条件下,以甲基绿(MEG)作探针,建立了检测安乃近的吸收光谱法,迄今未见文献报道。实验发现,安乃近与甲基绿反应后的生成物能使溶液颜色产生褪色现象,在可见光区出现3个明显的褪色峰,最大和次大褪色波长分别位于670 nm和424 nm,表观摩尔吸光系数分别为1.82×104L/(mol·cm)和1.50×104L/(mol·cm),在此两波长处,安乃近在一定浓度范围内与吸光度的绝对值呈良好的线性关系,服从比尔定律,能用于安乃近的定量分析。该法用于实际样品测定,结果满意。
1 实验
1.1 仪器与试剂
仪器:U-3010型紫外-可见分光光度计(日本,日立公司);S20K型pH计。
试剂:安乃近(重庆药检所提供)标准溶液(1.0×10-4mol/L),冰箱中4 ℃保存。甲基绿(MEG,中国医药(集团)上海化学试剂公司)溶液(1.0×10-3mol/L)。三羟甲基氨基甲烷(Tris)-盐酸缓冲溶液为0.1 mol/L盐酸溶液和0.2 mol/L Tris混合而成,用酸度计测定配成pH 3.0~9.8的系列缓冲溶液。试剂均为分析纯,实验用水为超纯水。
1.2 实验方法
于10 mL具塞比色管中,依次加入适量的1.0×10-4mol/L安乃近标准溶液,2.0 mL、pH为9.60的Tris-HCl 缓冲溶液和 3.0 mL、1.0×10-3mol/L的甲基绿溶液,用水稀释至刻度,摇匀后室温下放置20 min,以试剂空白作参比,用1 cm 比色皿在670 nm和424 nm波长处测定溶液的吸光度A。
2 结果与讨论
2.1 吸收光谱
测得的溶液的吸光度曲线见图1。
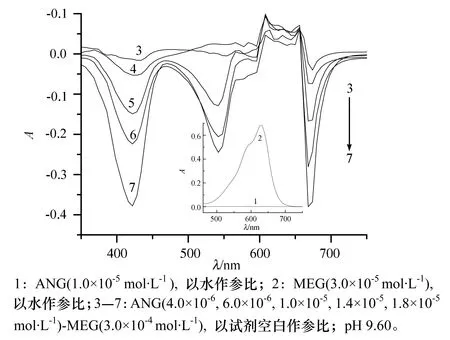
图1 安乃近溶液吸收光谱
从图1可见,安乃近在可见光区几乎无吸收,甲基绿在可见光区产生较强吸收,其最大吸收波长λmax= 630 nm,A=0.668;在碱性条件下,安乃近与甲基绿反应生成具有3个负吸收峰的络合物,其负吸收波长分别位于 424 nm、542 nm和670 nm,从曲线3—7可以看出,最大负吸收波长为670 nm(红移40 nm)和次大负吸收波长为424 nm(紫移206 nm) 处,安乃近在一定浓度范围内,其吸光度的绝对值与浓度呈正比关系,服从比尔定律;而在542 nm处,安乃近与吸光度之间无线性关系。由此可知,在670 nm 和424 nm 处可用于安乃近的定量分析。
2.2 溶液酸度
室温下,考察了BR、Tris-HCl缓冲溶液对体系络合反应的影响。结果表明:在pH为7.2~9.8的Tris-HCl 条件下,体系有较大的灵敏度,实验用pH为9.60 的Tris-HCl 缓冲溶液,用量以2.0 mL 为宜。
2.3 染料用量
室温下,考察了不同用量的1.0×10-3mol/L MEG 溶液对体系灵敏度的影响.结果表明,MEG的适宜用量是2.7~3.2 mL,实验用 3.0 mL、1.0×10-3mol/L的MEG 溶液。
2.4 试剂加入顺序
室温下,考察了ANG、MEG及pH为9.60 的Tris-HCl 溶液在不同加入顺序时对体系吸光强度的影响。结果表明:按ANG、Tris-HCl、MEG的加入顺序配制溶液,生成的络合物在424 nm和670 nm处其吸光度的绝对值较大,实验选用该加入顺序。
2.5 反应时间
考察了在670 nm处不同时间对体系灵敏度的影响,结果表明:20 min后吸光度值趋于平稳,稳定时间可达1 h以上,实验选在室温下20 min后测定。
2.6 干扰实验
室温下,670 nm 处,考察了药物制剂中常见辅料物质对测定安乃近含量的干扰情况。结果表明,100倍的葡萄糖、蔗糖、麦芽糖、乳糖、NaCl、KCl及60倍的L-色氨酸、L-亮氨酸、L-组氨酸、甘氨酸、谷氨酸,20倍的淀粉、利福平、麦迪霉素、红霉素、罗红霉素等对安乃近的测定均无干扰。
2.7 标准曲线
按实验方法配制系列标准溶液(浓度为c)并扫描吸收光谱,作A-c标准曲线。得到的一元线性回归方程、相关系数、线性范围及灵敏度等见表1。

表1 标准曲线相关参数
2.8 样品测定
取安乃近片3粒,用水溶解后过滤,转入1 000 mL容量瓶中,稀释至刻度,摇匀。取安乃近注射液和安乃近滴鼻液各1支,分别将其内容物置于500 mL 容量瓶中,用水稀至刻度,摇匀。取前述稀释液各1.0 mL,分别置于100 mL容量瓶中,用水稀释至刻度,摇匀,安乃近片待测液记为1#、安乃近注射待测液记为2#、安乃近滴鼻待测液记为3#。取各待测液1.0 mL,分别在670 nm波长下,按实验方法各平行测定6次,同时作加标回收实验,结果见表2。

表2 样品浓度分析及回收结果
[1] 中华人民共和国药典委员会.中华人民共和国药典(第二部)[M].北京:中国医药科技出版社,2010:286.
[2] 赵纯玉,饶伟文,唐文翠.安乃近片的HPLC测定法研究[J].中国药品标准,2009,10(3):233-236.
[3] 汪灿,刘雁鸣,汪文涛,等.HPLC法测定安乃近片的含量[J].中国药品标准,2006,7(3):68-70.
[4] 李秀梅.反相HPLC 法测定安乃近中的去4-N-去甲基安乃近[J].药物分析杂志,2006,26(3):406-408.
[5] 梁选革,张春燕.HPLC测定安乃近片中的安乃近和4-N-去甲安乃近[J].华西药学杂志,2008,23(2):211-213.
[6] 张艳,何晓英,李容,等.安乃近在蒙脱土修饰电极上的电化学行为及测定[J].分析科学学报,2010,26(1):75-78.
[7] 梁述忠.恒电流库仑分析法测定维生素 C等药物[J].理化检验:化学分册,2005,41(9):671-673.
[8] 吴旭刚,何家香,罗杨.电位法快速测定复方制剂中安乃近含量[J].中国兽药杂志,2003,37(3):51-52.
[9] 李传响,陆国斌,陈欢兰.紫外分光光度法测定安乃近片的含量[J].安徽医药,2003,7(4):301-302.
[10] 马卫兴,贾海红,方剑慧,等.安乃近的Fe(Ⅲ )-磺基水杨酸分光光度测定[J].淮海工学院学报,2003,12(2):39-42.
[11] 范常龙.安乃近片近红外定量分析模型的建立[J].荆楚理工学院学报,2010,25(9):36-37,40.
[12] 甘晓娟,刘绍璞,刘忠芳,等.某些芳香族氨基酸作探针荧光猝灭法测定安乃近及其代谢产物[J].化学学报,2012,70(1):58-64.
[13] 何云华,吕九如,张红鸽,等.分子印迹-化学发光分析法测定安乃近[J].高等学校化学学报,2005,26(4):642-646.
[14] 张红鸽,祝兴华,何云华.锰 (Ⅳ) -安乃近-甲醛化学发光体系的研究[J].分析试验室,2005,24(1):5-7.
[15] 张尼,宋正华,孙文超.流动注射化学发光测定尿液和血清中痕量安乃近[J].药物分析杂志,2004,24(5):547-550.
