电解剥离-生物质酸浸回收废旧锂电池
2014-03-18徐筱群满瑞林孙祖眉
徐筱群,满瑞林,张 建,刘 琦,徐 娟,孙祖眉
(中南大学 化学化工学院 有色金属资源化学教育部重点实验室,长沙 410083)
锂离子电池是目前广泛应用于手机、手提电脑、玩具等各种便携式电器中的可充电动力电池[1],随着这些电池或电器的报废,将产生大量废旧锂离子电池,研究这些废旧锂电池的综合回收处理具有较大的经济和环保价值。常规的锂离子电池一般含10%~15%的 钴[2-3]、10%~15%的铜、3%~7%的铝、20%~25%的铁以及0.10%~0.3%(质量分数)的锂等有价金属。
废旧锂离子电池,一般采用手工拆解和剥离外 壳。而壳体内部以钴的回收价值最高,因此,当前研究一般围绕在由涂覆于铝箔上钴酸锂正极材料的处理 上[4-10]。由于正极活性物质钴酸锂与铝箔粘接紧密,不易分离,常规的处理方法是将活性物质钴酸锂以及铝箔混在一起用硫酸/过氧化氢(还原剂)加热浸出,此时铝箔溶入溶液。传统分离钴铝的方法是用碱调节pH使Al成为Al(OH)3分离,但回收的Al(OH)3产品质量和本身价值均不高,且过滤大体积絮状Al(OH)3较为困难,更重要的是絮状Al(OH)3夹带造成钴的损失。为此,有学者提出采用有机溶剂溶解剥离[11]或采用高温真空热解粘合剂[12],使铝箔与活性物质LiCoO2分离回收,但有机溶剂溶解剥离需采用和消耗大量的有机溶剂,多数有机溶剂易挥发且容易对环境产生污染。而高温真空热解粘土剂采用保护气氛高温煅烧,其设备和温度控制等方面存在许多问题。对电池材料的酸浸过程,学者们普遍采用硝酸、盐酸和硫酸,又以硫酸浸出效果最好。但硫酸体系需要以双氧水为还原剂,否则浸出率很低。双氧水在酸性加热条件易自分解,利用率低,且过程剧烈,易造成事故。为避免这些问题,本文作者提出电解剥离-生物质酸浸新工艺。该工艺以正极材料为阴极,铅板为阳极,在较低酸度下进行电解,由于铝箔受到阴极保护[13],外加电流提供电子以及电解产生新生态氢用于钴的还原溶解,在铝箔不被溶解或尽可能少被溶解的同时,实现正极材料LiCoO2与铝箔的剥离。对于电池渣,采用生物质秸秆,硫酸酸浸剩余的钴。此工艺可以以铝箔的形式回收金属铝,且不用双氧水作还原剂,既经济又安全。
1 实验
1.1 实验原料
本研究所用废旧锂电池来源于湖南某电池回收厂,通过拆解得到电池外壳与电池芯。将电池芯分离得到锂电池正极条、负极条与隔膜。通过大量的拆解电池过程发现,由于电池损耗严重,部分正极粉粘在聚偏氟乙烯隔膜上,而单纯的水洗不能实现电池粉从隔膜上的分离。正极条是由90%LiCoO2活性物质、7%~8%乙炔黑导电胶和3%~4%有机粘结剂涂覆于铝箔上。本文作者即对废旧锂电池中的正极条进行处理,以期高效回收钴资源。所用生物质为莜麦秸秆,将其粉碎,过筛得到直径小于150 μm的麦秆粉。
1.2 实验方法
由于电池条具有良好的导电性,本研究采用电解剥离浸出的方法,实现LiCoO2活性物质与铝箔的分离,即以废锂电池正极条为阴极,铅板为阳极,溶有柠檬酸的稀硫酸溶液为电解液。在一定电流密度下,电解15~30 min,活性物质从铝箔上脱落掉入溶液中。过滤,得到电解液与电池渣。铝箔由于阴极保护得到大部分回收。 电极反应方程式为
阴极:

阳极:
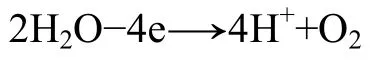
由于铝箔表面部分已被氧化为氧化铝,失去了阴极保护能力,因此,在电解过程中,会有少量的铝浸入电解液中。为了净化电解液,采用P204萃取回收电解液中的铝,萃余液中钴的纯度得以提高。
将电解剥离得到的电池渣采用生物质酸浸处理,即以莜麦秸秆粉为还原剂,硫酸酸浸电池渣中的钴,过滤得到钴浸出液。将电解净化液与生物质酸浸钴液一并采用草酸沉钴,以得到草酸钴产品。具体工艺流程如图1所示。
1.3 分析检测方法
溶液中钴的测定采用亚硝基红盐分光光度法测定,溶液中的COD采用重铬酸钾快速测定法进行定量分析[14]。采用红外仪对麦秆及所得草酸钴进行定性分析,对电解剥离得到的电池渣及草酸钴的晶格结构进行XRD测试分析。
2 结果与分析
2.1 电解剥离浸出过程
在20 g/L硫酸、18 g/L柠檬酸的电解液中,电流密度200 A/m2,以废旧锂电池正极条为阴极,电解剥离20~30 min,LiCoO2正极材料从铝箔上剥离,部分钴被还原浸出,而铝箔由于阴极保护作用得到大部分回收,只有少部分氧化铝溶入电浸液中。
图2所示为时间对电解剥离浸出和电流效率的影响。通过图2可以看出,随着电解时间的增长,钴的浸出率逐渐增大,当电解时间为30~50 min时,钴浸出率变化不大,电流效率则随着时间的延长而逐渐降低;当电解时间为10 min时,钴浸出率达到30%,电流效率接近100%,但是并未实现LiCoO2正极材料从铝箔上剥离。通过大量的实验发现,正极条一般在20~30 min从铝箔上发生剥离,此时,钴浸出率达到50%左右,电流效率亦有70%。
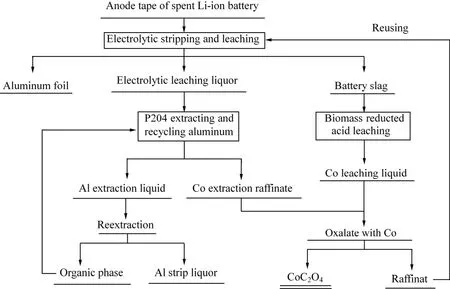
图1 电解剥离-浸出工艺流程图Fig.1 Flow diagram of electrolytic stripping-leaching process

图2 时间对电解剥离浸出和电流效率的影响 Fig.2 Influence of time on electrolytic stripping leaching and current efficiency

图3 电解剥离的电池渣的XRD谱 Fig.3 XRD pattern of battery slag by electrolytic stripping
图3 所示为电解剥离电池渣的XRD谱。通过XRD 测试发现,电解浸出剥离得到的电池渣与标准钴酸锂的峰位近似,表明得到的渣中的钴仍以钴酸锂的形式存在。
2.2 麦秆粉酸浸电池渣
以2 mol/L硫酸为浸出液,1 g电池渣加入0.5~0.7 g麦秆粉,固液比为1:5~1:10 (g/mL),在80~90℃反应1~2 h,钴的浸出率达到98%以上。浸出液中Co2+的浓度为30 g/L,而COD含量达到6~8 g/L。通过实验发现,浸出液中的COD有利于钴的浸出。因此,为了尽可能充分利用溶液中的硫酸与降低浸出液中COD值,本研究提出三级浸出工艺。
称取一定质量麦秆粉于2 mol/L硫酸溶液中,液固比控制在100:7,经90 ℃反应2 h,过滤得到酸浸原液。在三级酸浸电池渣中,每级反应控制液固比为10,经90 ℃反应2 h,生物质三级酸浸各级数据如表1 所列。
从表1可以看出,三级浸出液较一级浸出液,COD值大幅下降,而钴的浓度却大幅增高。COD值降低方便后期废水处理,而钴浓度的提高则有利于钴的回收处理。因此,两级或三级工艺可充分利用浸出液中的COD及硫酸。
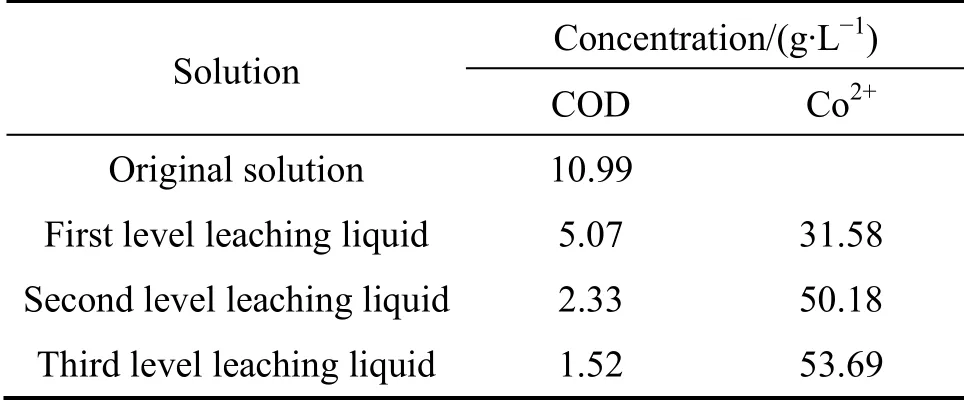
表1 生物质三级酸浸电池渣 Table1 Process of triple biological acid leaching battery slag
图4所示为莜麦麦秆粉酸浸前后渣的红外光谱。分析发现,酸处理麦秆粉前后,官能团没有明显的变化。表2所列为麦秆粉的红外光谱解析。从表2分析可知,莜麦麦秆粉中含有丰富的醇或酚羟基、不饱和碳链等官能团。通过现有研究发现,燕麦中富含多酚类物质、维生素E、甾醇、羟基脂肪酸等抗氧化物 质[16],麦秆中的抗氧化物质虽没有麦粉中的丰富,其中的纤维素、果胶以及水溶性酚类、羟基脂肪酸等亦 可替代双氧水起到还原作用。

图4 莜麦麦秆粉酸浸前后渣的红外光谱 Fig.4 FTIR spectra of naked oats straw powder before and after acid treatment
2.3 P204除铝净化电解钴液
P204作为一种酸性含磷金属离子萃取剂,对金属具有较强的萃取能力,且已用于从混合金属溶液中萃取铝[17]。P204萃取剂组成为15% P204+80% 磺化煤油+5% TBP(体积分数),皂化率20%。萃取实验在室温下进行,相比为1,萃取5 min,以电解浸出液为原料液,考察pH值对P204萃取除杂的影响,其结果如图5所示。由图5可看出,随着pH的升高,铝的萃取率逐渐增大,当pH>2.6时,铝的萃取率可以达到90%以上,但此时,原料液中的钴也开始进入到有机相,并随着pH值的升高,钴的萃取率也逐渐增大。因此,实验选择控制萃取pH值为2.6,此时铝的一次 萃取率为90.2%,而钴全留在萃余液中。

图5 pH值对P204萃取浸出液的影响 Fig.5 Influence of pH on P204 extracting leaching liquor

表2 麦秆粉的红外光谱解析[15] Table2 Infrared spectrum analysis of straw powder[15]
控制萃取平衡的pH值为2.6,将电解浸出液进行多次错流萃取,萃取结果如表3所列。由表3可以看出,电解浸出液经过两次错流萃取后,萃余液中Al3+的含量可以降到0.4 mg/L,而Co2+未有损失,实现电解浸出液的净化除铝。
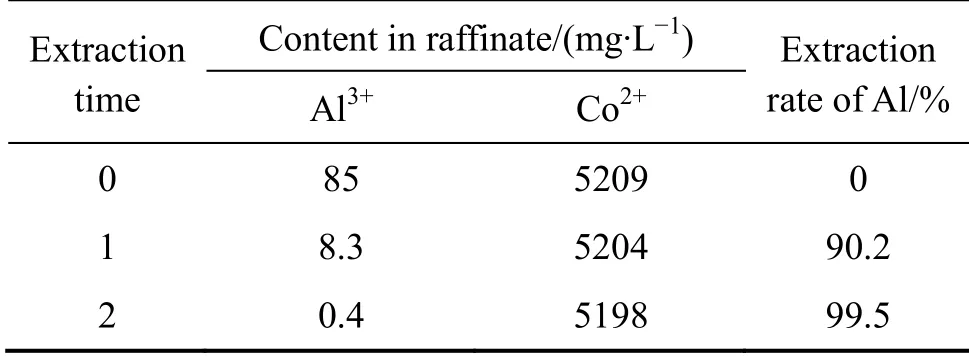
表3 P204错流萃取实验结果 Table3 P204 cross-flow extraction results
2.4 草酸沉钴
较氢氧化钠沉钴相比,草酸沉钴可在低pH值下进行。调节溶液pH为2,保持,于50 ℃下反应1 h,过滤得到草酸钴产品,在80 ℃条件下干燥。钴的沉淀率达到92.46%,而滤液pH值为0.2,其酸度已达到电解剥离浸出工艺所需酸度,可循环使用滤液。
通过草酸沉钴得到的草酸钴与标准样品的红外光谱进行对比(见图6),产品在680 cm-1位置出现了裂峰,可能与草酸钴的晶型结构有关,其他峰位置与纯品近乎一致,无杂峰出现,说明草酸沉钴可以得到纯草酸钴产品,且溶液中的COD通过干燥烘干,并未残留于产品中,但可能对草酸钴的晶型有影响。
2.5 电池材料的制备
为研究所得草酸钴晶型对电池材料制备的影响,采用高温固相法将其与Li2CO3按n(Co2+):n(Li+)=1在玛瑙研钵中充分研磨后转移至马弗炉中焙烧处理。首先在650 ℃下预焙烧5 h,然后再于850 ℃下焙烧5 h, 冷却至室温,研磨成粉,制备得LiCoO2正极材料。对该材料进行XRD检测,并分析材料的晶格参数,与市场样品的性能进行比较。

图6 草酸钴产品的红外光谱 Fig.6 FTIR spectra of cobalt oxalate:(a) Pure CoC2O4; (b) CoC2O4 with COD
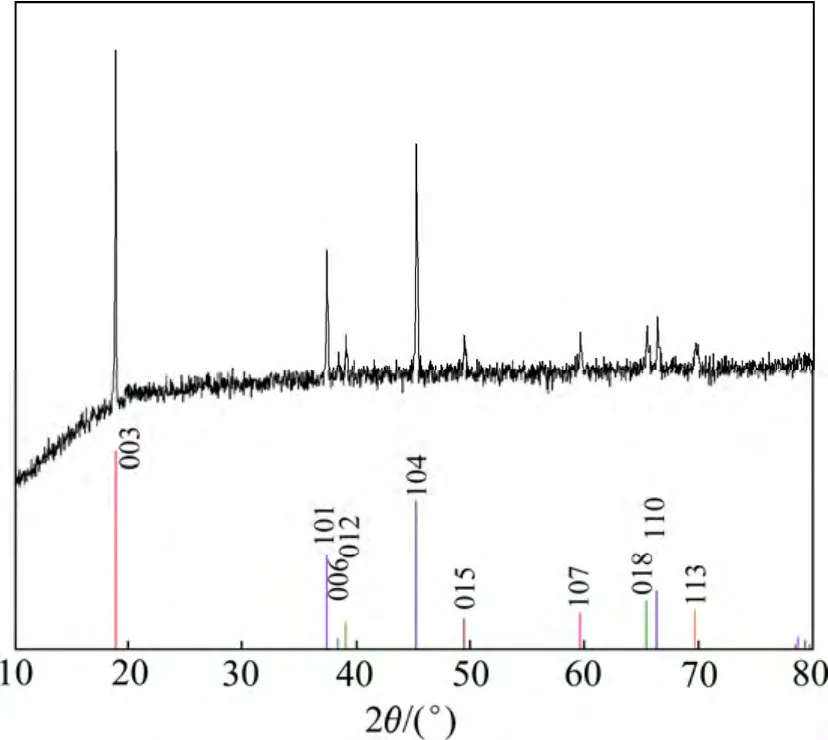
图7 LiCoO2电池材料XRD谱 Fig.7 XRD pattern of LiCoO2 battery material

表4 钴酸锂的晶格参数 Table4 Lattice parameters of LiCoO2
图7所示为LiCoO2电池材料XRD谱。表4所列为钴酸锂的晶格参数。通过对图7以及表4分析发现, 本研究制备的电池材料峰型尖锐、无杂峰,其晶格参数高于国产常规钴酸锂的,尤其是c/a指标,高于日本18650型钴酸锂的。从(003)、(006)、(104)等特征峰强度分析,制备的材料的强度接近国产常规钴酸锂的。综上所述,采用本研究中的方法所制得草酸钴可用作制备电池材料。
3 结论
1) 采用电解剥离工艺,短时间实现电池材料与铝箔的分离。同时,钴在低酸度条件下其浸出率达到50%,电流效率达到70%以上。
2) 采用生物质秸秆硫酸体系浸出电池渣,钴的浸出率达到99%以上。且通过两级、三级浸出工艺,浸出液中的酸与COD得到充分利用。
3) 对浸出的钴采用草酸沉淀,通过红外测试发现,生物质浸出液中的COD对产品没太多影响。
4) 将CoC2O4与纯品Li2CO3高温固相制备锂离子电池材料,对LiCoO2进行XRD分析并计算晶格参数发现,制备出的电池材料具有较好的放电性能。
[1] 郭炳焜,徐 徽,王先友. 锂离子电池[M]. 长沙:中南大学出版社. 2002.
GUO Bing-kun,XU Hui,WANG Xian-you. Lithium ion battery[M]. Changsha:Central South University Press,2002.
[2] FOUAD O A,FARGHALY F I,BAHGAT M. A novel approach for synthesis of nanocrystalline γ-LiAlO2from spent lithium-ion batteries[J]. Journal of Analytical and Applied Pyrolysis,2007,78(1):65-69.
[3] LEE C K,RHEE K I. Preparation of LiCoO2from spent lithium-ion batteries[J]. Journal of Power Sources,2002,109(1):17-21.
[4] FERREIRA D A,PRADOS L M Z,MAJUSTE D,MANSUR M B. Hydrometallurgical separation of aluminium,cobalt,copper and lithium from spent Li-ion batteries[J]. Journal of Power Sources,2009,187(1):238-246.
[5] PAULINO J F,BUSNARDO N G,AFONSO J C. Recovery of valuable elements from spent Li-batteries[J]. Journal of Hazardous Materials,2008,150(3):843-849.
[6] WANG Rong-chi,LIN Yu-chuan,WU She-huang. A novel recovery process of metal values from the cathode active materials of the lithium-ion secondary batteries[J]. Hydrometallurgy,2009,99(3/4):194-201.
[7] DORELLA G,MANSUR M B. A study of the separation of cobalt from spent Li-ion battery residues[J]. Journal of Power Sources,2007,170(1):210-215.
[8] LI Li,GE Jing,WU Feng,CHEN Ren-jie,CHEN Shi,WU Bo-rong. Recovery of cobalt and lithium from spent lithium ion batteries using organic citric acid as leachant[J]. Journal of Hazardous Materials,2010,176(1/3):288-293.
[9] XU Jin-qiu,THOMAS H R,FRANCIS R W,LUM K R,WANG Jing-wei,LIANG Bo. A review of processes and technologies for the recycling of lithium-ion secondary batteries[J]. Journal of Power Sources,2008,177(2):512-527.
[10] SAEKI S,LEE J,ZHANG Q W,SAITO F. Co-grinding LiCoO2with PVC and water leaching of metal chlorides formed in ground product[J]. International Journal of Mineral Processing,2004,74(S):s373-s378
[11] CONTESTABILE M,PANERO S,SCROSATI B. A laboratory-scale lithium-ion battery recycling process[J]. Journal of Power Sources,2001,92(1/2):65-69.
[12] SUN Liang,QIU Ke-qiang. Vacuum pyrolysis and hydrometallurgical process for the recovery of valuable metals from spent lithium-ion batteries[J]. Journal of Hazardous Materials,2011,194:378-384.
[13] 徐晓刚. 化工腐蚀与防护[M]. 北京:中国石化出版社,2009.
XU Xiao-gang. Chemical corrosion and protection[M]. Beijing:Chinese Petrochemical Press,2009.
[14] 魏海娟,黄继国,贾国元,许文峰. 一种快速测定化学需氧量(COD)的方法[J]. 环境科学与技术,2006,29(1):45-46.
WEI Hai-juan,HUANG Ji-guo,JIA Guo-yuan,XU Wen-feng. A method to rapid measure chemical oxygen demand[J]. Environmental Science & Technology,2006,29(1):45-46.
[15] PANDEY K K,PITMAN A J. FTIR studies of the changes in wood chemistry following decay by brown-rot and white-rot fungi[J]. International Biodeterioration & Biodegradation,2003,52(3):151-160
[16] 汪海波,谢笔钧,刘大川. 燕麦中抗氧化成分的初步研究[J]. 食品科学,2003,24(7):62-67.
WANG Hai-bo,XIE Bi-jun,LIU Da-chuan. Preliminary studies of antioxidant in oats[J]. Food Science,2003,24(7):62-67.
[17] DEBASISH M,KIM H I,NAM C W,PARK K H. Liquid-liquid extraction of aluminium(Ⅲ) from mixed sulphate solutions using sodium salts of Cyanex 272 and D2EHPA[J]. Separation and Purification Technology,2007,56(3):311-318.
[18] KIM D S,SOHN J S,LEE C K. Simultaneous separation and renovation of lithium cobalt oxide from the cathode of spent lithium ion rechargeable batteries[J]. Journal of Power Sources,2004,132 (1/2):145-149.
