柱前衍生化反相高效液相色谱法测定大鼠血浆中牛磺酸的含量及其药动学研究
2014-03-07岳山岚帅淑平王吉琳赵一凡杨俊毅
岳山岚,王 维,帅淑平,王 静,王吉琳,赵一凡,杨俊毅
(四川大学华西药学院,四川 成都 610041)
柱前衍生化反相高效液相色谱法测定大鼠血浆中牛磺酸的含量及其药动学研究
岳山岚,王 维,帅淑平,王 静,王吉琳,赵一凡,杨俊毅
(四川大学华西药学院,四川 成都 610041)
建立一种测定大鼠血浆中牛磺酸含量的柱前衍生化-高效液相色谱法,并将其应用于牛磺酸在大鼠体内的药动学研究。采用柱前衍生化高效液相色谱法,以2,4-二硝基氟苯(DNFB)为衍生化试剂,以KH2PO3缓冲液(pH 7.0):乙腈∶水(70∶15∶15,v/v)为流动相,经C18色谱柱(250mm×4.6mm×5μm)分离,柱温30℃,流速1.0mL/min,进样量为20μL,牛磺酸衍生物的紫外检测波长为360nm,并以DAS2.0计算其药动学参数。大鼠血浆中牛磺酸在1.29~1 287.5 μg/mL质量浓度范围内线性关系良好,r=0.999 9,最低定量限1.29 μg/mL,主要药动学参数t1/2为(3.747±1.430)h,Cmax为(949.573±192.967)μg/mL,Tmax为(1.000±0.000)h,AUC0-t为(2862.168±565.917)(mg/L)/h。该法简单、经济、灵敏,适用于牛磺酸血药浓度测定及药动学研究。
牛磺酸;高效液相色谱法;柱前衍生化;药动学
0 引 言
牛磺酸(taurine)又名牛胆碱、牛胆素,是存在于人及动物体内的一种非蛋白游离氨基酸[1]。牛磺酸具有广泛的生理药理作用[2-3],临床上用于治疗支气管炎,急慢性肝炎,高血压等疾病,大多为口服制剂[4]。牛磺酸本身没有紫外吸收,因此无法使用常规的高效液相色谱法(HPLC)对其浓度进行检测。国内外文献中关于牛磺酸浓度的测定方法主要有氨基酸自动分析仪法[5]、液相色谱-质谱联用法(LCMS)[6]、柱后衍生化法[7]、柱前衍生化法[8]、薄层扫描法[9]等。其中,LCMS法、柱后衍生化法、氨基酸自动分析仪法存在对检测仪器要求较高,且检测费用昂贵,不适用于大批量样品检测分析的缺陷;而薄层扫描法在操作过程中影响因素太多。柱前衍生化为将样品在进样前进行衍生化反应,可以相对自由地选择反应条件,不存在反应动力学的限制;衍生化的副产物可进行预处理以降低或消除其干扰;允许多步反应的进行,有较多的衍生化试剂可选择。2,4-二硝基氟苯(DNFB)作为一种衍生化试剂,与牛磺酸在碱性条件下发生衍生化反应:

生成的牛磺酸衍生物具有紫外吸收,可用于检测分析。本研究旨在建立一种简单、经济且具有足够灵敏度的柱前衍生化-高效液相色谱法,以测定生物样品中牛磺酸的浓度,并应用于牛磺酸的临床前药动学研究。
1 材 料
1)仪器。LC-10AT高效液相-泵(SHIMAZU,日本);CTO-10Asvp高效液相-柱温箱(SHIMAZU,日本);B-220恒温水浴锅(上海雅荣生化仪器设备有限公司);ZP-200振荡器(江苏太仓市实验设备厂);TGL-16高速离心机(上海安亭科学仪器厂);SIMENS低温冰箱(美国Thermo公司);AUW 120D电子天平(SHIMAZU,日本);DW-FL 270低温冰箱(中科美菱)。
2)药物和试剂。牛磺酸(潜江永安药业股份有限公司,批号:20110424,纯度:99%);牛磺酸对照品(纯度>99%,Sigma公司);2,4-二硝基氟苯(DNFB)(日本东京化成工业株式会社);磷酸二氢钾、氢氧化钠、碳酸氢钠为分析纯;乙腈为色谱纯,水为超纯水。
3)实验动物。健康SD大鼠,雌雄各半,四川大学动物实验中心提供,许可证号:SCXK(川)2009-09。
2 方法与结果
2.1 色谱条件
Kromasil C18色谱柱(250mm×4.6mm×5μm),流动相为KH2PO3缓冲液(pH 7.0)∶乙腈∶水(70∶15∶15,v/v),流速1.0 mL/min,柱温30℃,检测波长360nm,进样量20μL。
2.2 牛磺酸标准溶液的配制
取牛磺酸对照品约1g,精密称定,置于100 mL容量瓶中,加纯水溶解并稀释至刻度,混匀,得质量浓度为0.010 3 g/mL的牛磺酸储备液。精密吸取储备液适量,用水稀释,得质量浓度分别为2.575,5.15,25.75,103,257.5,1030,2060,2575μg/mL的牛磺酸系列标准溶液。
2.3 血浆的制备
取SD大鼠5只,实验前禁食12h,按0.9g/kg剂量单次口服灌胃牛磺酸,在给药过程中保证SD大鼠服药完全,分别于给药前和给药后0.033,0.083,0.25,0.5,1,2,3,5,7,9,12,24h尾静脉采血0.5 mL,血样置肝素化采血管中,8 000 r/min离心5min,分离血浆,于-40℃冰箱储存待测。
2.4 血浆样品的处理
取200μL血浆样品,加纯水100 μL,涡旋混合30 s,加乙腈500 μL,涡旋3 min,12 000 r/min离心5min,取上清液500μL于5mL容量瓶中,加NaHCO3溶液(0.5 mol/L,pH9.0)500 μL,再加入1.0%(v/v)的2,4-二硝基氟苯乙腈溶液100μL,避光80℃水浴加热1h,取出,用KH2PO3缓冲液(pH7.0)稀释至刻度,取20μL进样。
2.5 方法学验证
2.5.1 方法的专属性
在本实验所采用的HPLC条件下,2,4-二硝基氟苯的出峰时间在7.6 min,牛磺酸衍生物的出峰时间在13.5 min,峰形良好,与衍生化试剂分离良好,空白血浆样品无明显内源性杂质峰干扰测定;本方法具有较高的特异性,能准确测定血浆中的牛磺酸的质量浓度,灵敏度较高,如图1所示。
2.5.2 标准曲线制备
精密吸取空白SD大鼠血浆200μL,置于1.5mL离心管中,分别加2.2的牛磺酸系列标准溶液100μL,得到牛磺酸质量浓度分别为1.29,2.58,12.88,51.5,128.75,515,1030,1287.5μg/mL的标准血浆样品,除不加纯水100μL外,其余按2.4方法操作,记录色谱图。计算牛磺酸衍生物峰面积ATau和空白血浆中牛磺酸衍生物峰面积AKB的差值y,采用SPSS 13.0统计学软件,以y值对血药浓度C作加权直线回归计算,得线性回归方程y=2 218.381×C+7 653.674,r=0.9999,在1.29~1287.5μg/mL质量浓度范围内线性关系良好,结果见图2。
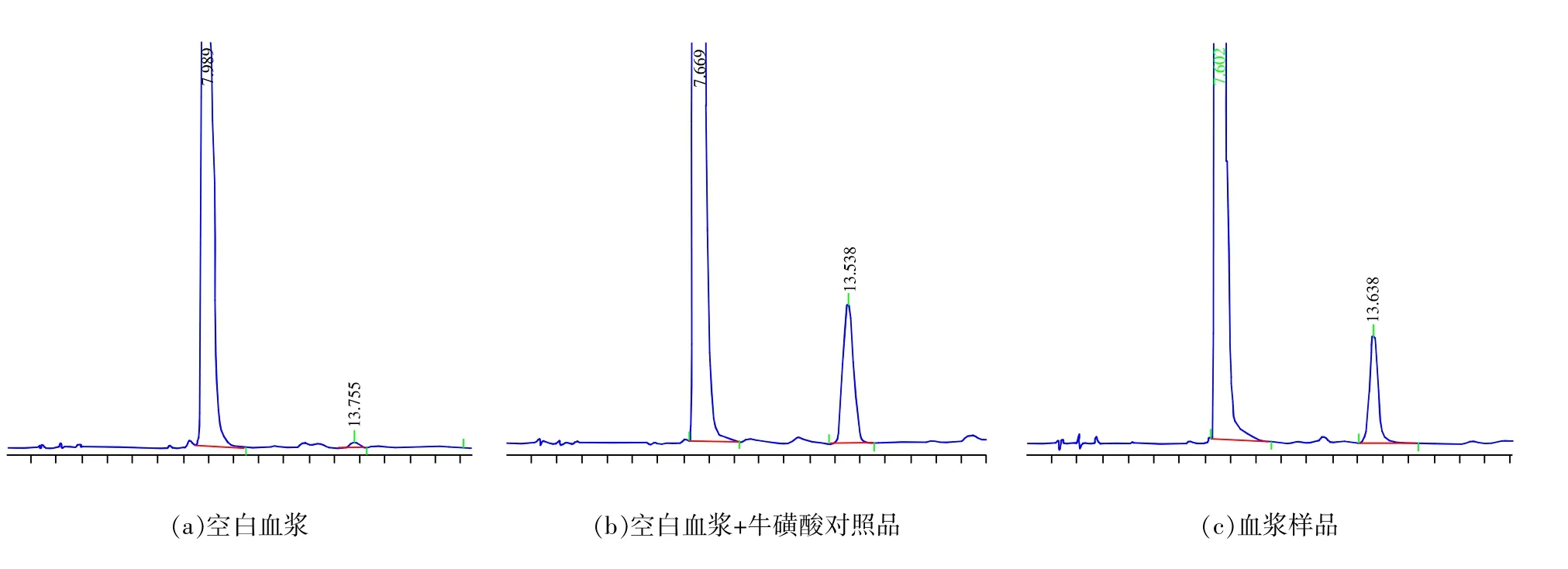
图1 牛磺酸衍生物与衍生化试剂色谱图
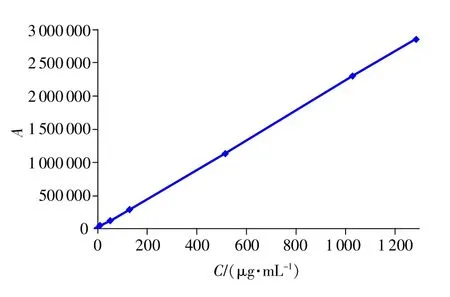
图2 牛磺酸血浆样品标准曲线
2.5.3 定量下线的确定
取空白血浆200 μL,制备含牛磺酸质量浓度为1.29 μg/mL的标准血浆样品(n=5),除不加纯水100μL外,其余按2.4方法操作。记录色谱图,计算牛磺酸衍生物峰面积ATau和空白血浆中牛磺酸衍生物峰面积AKB的差值y,根据标准曲线计算实测质量浓度,得其回收率为108.38%±7.24%。按上述条件测得牛磺酸在血浆中的定量下限为1.29μg/mL。
2.5.4 准确度和精密度试验
取空白血浆200μL,制备低、中、高浓度分别为2.58,128.75,1 030 μg/mL的含药血浆样品(n=5),除不加纯水100μL外,其余按2.4方法操作。连续制备3个分析样品,记录色谱图,计算牛磺酸衍生物峰面积ATau和空白血浆中牛磺酸衍生物峰面积AKB的差值y,根据标准曲线计算实测质量浓度及准确度、批内和批间精密度。结果低、中、高3种浓度样品回收率在98.45%~109.27%之间,批内及批间RSD均≤5.0%。
2.5.5 样品稳定性考察
取空白血浆200μL,制备浓度分别为2.58,128.75, 1030μg/mL的含药血浆样品(n=5),按2.4方法操作后,室温放置0,10,24h后再测定,记录样品峰面积,计算实测质量浓度,并与0h测定结果进行比较。结果表明,牛磺酸血浆样品在处理后室温放置至少能稳定24h。
2.6 药动学研究
取SD大鼠5只,实验前禁食12h,按0.9g/kg剂量单次口服灌胃给予牛磺酸,在给药过程中保证SD大鼠服药完全,分别于给药前和给药后0.033,0.083,0.25,0.5,1,2,3,5,7,9,12和24 h尾静脉采血0.5 mL,血样置肝素化采血管中,8000r/min离心5min,分离血浆,于-40℃冰箱储存。按2.4方法操作后,在本实验条件下测定。根据测定结果绘制牛磺酸的平均血药浓度-时间曲线,见图3。
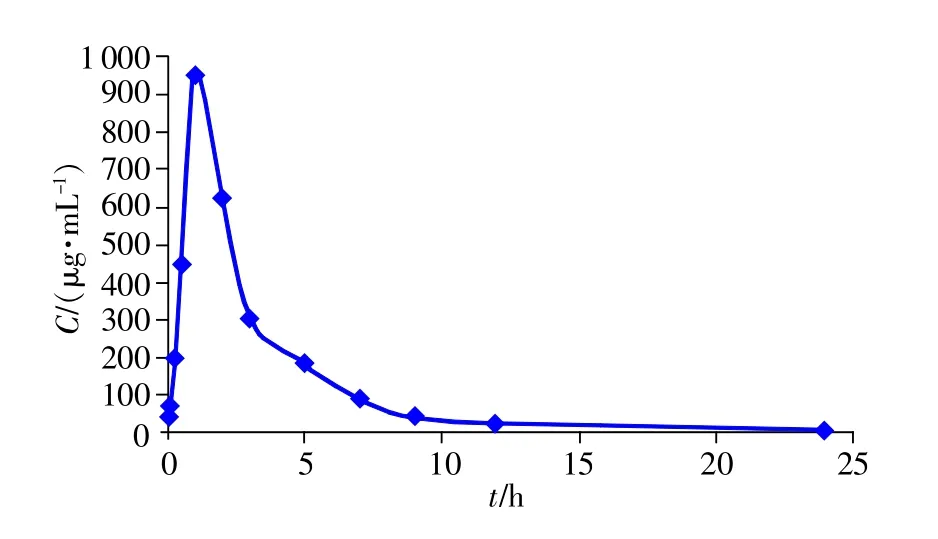
图3 牛磺酸平均血药浓度-时间曲线
采用药动学软件DAS 2.0计算主要药动学参数,根据二室模型依赖性参数估算方法,计算SD大鼠口服牛磺酸后的药动学主要参数,AUC0-t为(2862.168± 565.917)(mg/L)/h,Cmax为(949.573±192.967)μg/mL,Tmax为(1.000±0.000)h,t1/2为(3.747±1.430)h,结果见表1。
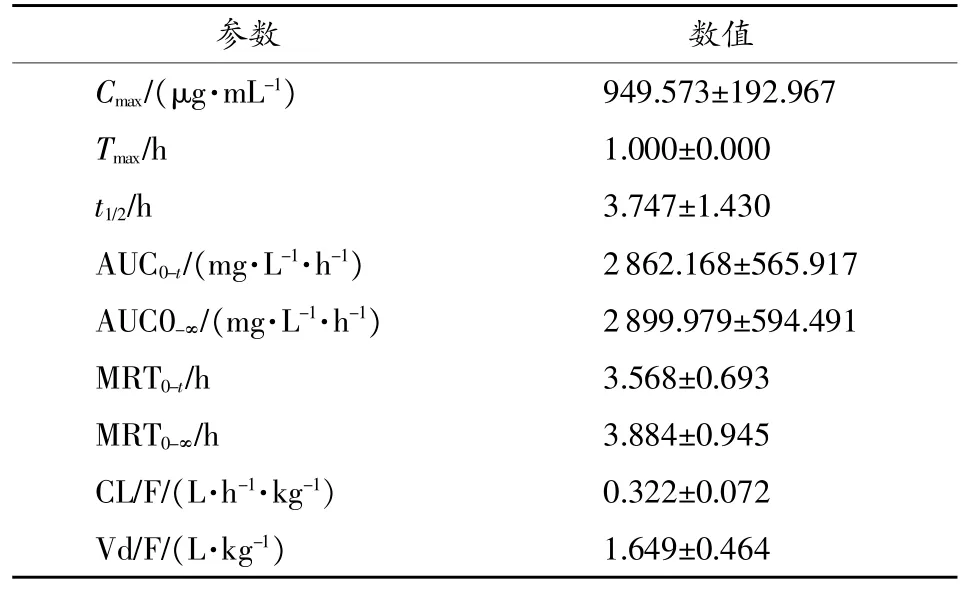
表1 牛磺酸药动学参数
3 讨 论
牛磺酸本身没有紫外吸收,须经衍生化后方能通过紫外检测进行含量测定。因此衍生化试剂的选择尤其重要,常用的衍生化试剂有邻苯二甲醛(o-phthaldialdehyde,OPA),丹磺酰氯(dansylchloride)和2,4-二硝基氟苯(2,4-dinitrofluorobenzen,DNFB)等,用邻苯二甲醛配制的OPA试液可使牛磺酸在短时间内衍生化,但衍生化产物稳定性差,要求检测迅速,故更适用于柱后衍生化检测,且因其不稳定性对操作要求较高。而丹磺酰氯做衍生试剂易产生副产物,干扰测定。本实验选用DNFB作为衍生化试剂,以桑格反应(Sanger reaction)为基础,在弱碱性,避光,80℃条件下,DNFB与牛磺酸的α-氨基发生反应,生成黄色的2,4-二硝基苯牛磺酸,这种衍生化产物结构稳定,不易水解,且过量的DNFB的色谱峰对牛磺酸含量测定无干扰,衍生化及HPLC检测过程操作简单,快速,重现性好;另本方法的定量下限为1.29μg/mL,小于最新报道的使用相同衍生化方法后检测所得的定量下限值3.00μg/mL[10]。且与报道中的梯度洗脱法相比,在两法均能使牛磺酸衍生物与其他物质有效分离的前提下,本方法中使用的等度洗脱具有重现性好、精密度高的优点,可广泛应用于牛磺酸生物样本的分析。
本研究考察了衍生化试剂(DNFB)的用量(100,200μL)、衍生化反应时间(35,40,45,50,55,60min)及反应温度(60,70,80℃)。结果表明当衍生化试剂(DNFB)用量为100μL,在避光条件下80℃反应1h后衍生化效率最高。在此条件下,DNFB与牛磺酸生成的衍生物室温下放置24h仍然稳定。
4 结束语
本实验选用2,4-二硝基氟苯(2,4-dinitrofluorobenzen,DNFB)作衍生化试剂建立的柱前衍生化-高效液相色谱法操作简单,经济成本低,重复性好,可成功地用于大鼠血浆中牛磺酸的含量测定。将其应用于牛磺酸在大鼠体内的药动学研究后得到的主要药动学参数Cmax为(949.573±192.967)μg/mL,Tmax为(1.000±0.000)h,t1/2为(3.747±1.430)h,AUC0-t为(2862.168±565.917)(mg/L)/h。本研究结果可为牛磺酸的进一步药动学研究提供参考。
[1]Musio R,Sciacovelli O.Detection of taurine in biological tissues by 33S NMR spectroscopy[J].Journal of Magnetic Resonance,2001,153(2):259-261.
[2]Parildar K H,Mehmetcik G,Özdemirler E G,et al. Effect of taurine treatment on pro-oxidant-antioxidant balance in livers and brains ofold rats[J].Pharmacological Reports,2008(60):673-678.
[3]Militante J D,Lombardini J B.Treatment of hypertension with oral taurine:experimental and clinical studies[J]. Amino Acids,2002,23(4):381-393.
[4]王文乐,赵小燕,聂秀芹,等.牛磺酸的临床应用[J].现代医药卫生,2005,21(23):3332-3333.
[5]王洪健,周兴起,冯志强,等.氨基酸自动分析仪测定食品中牛磺酸的方法建立[J].现代食品科技,2012,28(3):348-350.
[6]Yu Y,Zheng X,Bian T,et al.Development and application of a LC-MS/MS assay for the simultaneous quantification of edaravone and taurine in beagle plasma[J]. Journal of Separation Science,2013,36(24):3837-3844.
[7]张彤,山广志,余立.柱后衍生HPLC法测定牛磺酸颗粒的含量[J].中国新药杂志,2010(4):340-342.
[8]蒲秋易,张一竹,张二云,等.柱前衍生化高效液相色谱法测定全蝎中游离牛磺酸的含量[J].中国新药杂志,2013,22(2):230-234.
[9]郭丽仪.薄层扫描法测定人体血液中牛磺酸的含量[J].中草药,2001,32(3):217-218.
[10]赵宏涛,黎云燕.牛磺酸在大鼠体内的药代动力学[J].天津医科大学学报,2013,19(4):341-344.
Determination of taurine in rat plasma by RP-HPLC with pre-column derivatization and its pharmacokinetic study
YUE Shan-lan,WANG Wei,SHUAI Shu-ping,WANG Jing,WANG Ji-lin,ZHAO Yi-fan,YANG Jun-yi
(School of Pharmacy,Sichuan University,Chengdu 610041,China)
To develop a HPLC method with pre-column derivatization for the determination of taurine in rat plasma and its application to the pharmacokinetic study after oral administration of taurine.The concentration of taurine in plasma was determined by a HPLC method with precolumn derivatization,and 2,4-dinitrofluorobenzene(DNFB)was used as a derivatization reagent. Chromatographic separation was performed on an C18 column(250 mm×4.6 mm×5μm),the mobile phase was consisted of KH2PO3buffer solution∶acetonitrile∶water(70∶15∶15,v/v)at a flow rate of 1.0 mL/min,the column temperature was at 30℃ and injection volume was 20 μL.The taurine derivative wasdetected by measuring the UV absorbance at360 nm.The pharmacokinetic parameters were calculated with the DAS2.0 software.Results:the calibration curve of taurine was linear(r=0.999 9)in the range of 1.29~1287.5 μg/mL.The limit of quantitation was 1.29 μg/mL,and the key pharmacokinetic parameters were t1/2(3.747±1.430)h,Cmax(949.573±192.967)μg/mL,Tmax(1.000±0.000)h,AUC0-t(2 862.168±565.917)(mg/L)/h.The method is simple,economic and sensitive,which can be successfully applied for the determination of taurine in plasma and its pharmacokinetic studies in rats.
taurine;HPLC;pre-column derivatization;pharmacokinetics
R914;TQ460.7+2;O657.7+2;O623.84
:A
:1674-5124(2014)06-0056-04
10.11857/j.issn.1674-5124.2014.06.015
2013-12-01;
:2014-01-24
岳山岚(1988-),女,四川阆中市人,硕士研究生,专业方向为临床用药的药动学基础研究。
