银杏叶复方制剂对小鼠急性毒性和细胞毒性研究
2014-01-16李焰林香燕张继欣尹会方
李焰,林香燕,张继欣,尹会方
(1.龙岩学院生命科学学院,福建龙岩 364000;2.福建省高校预防兽医学重点实验室,福建龙岩 364000)
银杏叶复方制剂对小鼠急性毒性和细胞毒性研究
李焰1,2,林香燕1,张继欣1,尹会方1,2
(1.龙岩学院生命科学学院,福建龙岩 364000;2.福建省高校预防兽医学重点实验室,福建龙岩 364000)
文章旨在研究银杏叶复方制剂对小鼠急性毒性和细胞毒性的影响,以确保临床用药安全。结果表明,①急性毒性试验以半数致死量(LD50)和最大耐受量(MTD)为指标,用40 g·kg-1体重剂量的银杏叶复方制剂灌胃,7 d后小鼠未发生死亡,再在小鼠可接受的最大容积下,给小鼠灌服日累积剂量为120 g·kg-1体重的银杏叶复方制剂进行MTD试验,7 d后处死观察其病理变化。②分别用形态学观察法和MTT法进行细胞毒性试验,用细胞维持液将100 g·L-1银杏叶复方制剂原液稀释成2-n(n为1~8)8个稀释度,测试银杏叶复方制剂在鸡胚成纤维细胞(CEF)的体外培养中的最大安全质量浓度(TC0)。结果表明,银杏叶复方制剂LD50>40 g·kg-1体重,MTD>120 g·kg-1体重,小鼠无一例出现死亡,剖检未见明显肉眼可见的病理变化,说明药物毒性很小,临床使用安全。在形态学观察法中,银杏叶复方制剂在高浓度时未表现细胞毒性,在MTT法中银杏叶复方制剂对CEF的最大安全质量浓度为0.78 g·L-1。
银杏叶复方;小鼠急性毒性;鸡胚成纤维细胞;细胞毒性
目前畜禽生产中普遍存在长期大量滥用抗生素、不合理疫苗接种、应激、病原微生物感染等问题,导致畜禽免疫功能下降、生产性能降低、引发毒副作用和药物残留,引发的食品安全问题屡见不鲜。因此,研究开发特性确定、高效、稳定、无毒、无污染和无残留的理想免疫增强剂将是对畜禽抗御疾病及增强体质具有重要意义。天然植物性免疫增强剂具有无残留、安全和免疫功效显著等优点[1]。本试验前期研究,利用银杏叶与党参、黄芪、白术等中草药配制成银杏叶复方制剂,研究银杏叶复方制剂对预防试验性脾虚证小鼠各种生理机能的影响,结果表明银杏叶复方制剂具有提高脾虚小鼠消化酶活性、促进肠道吸收功能和抗疲劳作用[2-3];对脾虚证模型小鼠的免疫功能研究表明,脾虚小鼠存在神经一内分泌一免疫网络之间的调节失衡,最终引起脾虚时机体免疫功能低下,经银杏叶复方制剂治疗后上述免疫失调现象得到明显改善[4]。本试验所用的银杏叶复方制剂在前期研究的基础上[2]增加砂仁和陈皮,用水煮醇提法配制而成。为确保临床用药安全,本试验对该复方进行急性毒性、最大耐受量及细胞毒性的研究,急性毒性和最大耐受量试验选用小鼠作为研究对象,细胞毒性试验采用鸡胚成纤维细胞(CEF),分别用形态学观察法和MTT两种方法,将银杏叶复方制剂与CEF体外共培养,检测银杏叶复方制剂的细胞毒性,测定银杏叶复方制剂在CEF培养体系中的细胞安全浓度,评价其药物毒性,为进一步研究银杏叶复方制剂的药效及药理研究奠定基础。
1 材料与方法
1.1 材料
1.1.1 试验药物
银杏叶干粉由长沙博健生物科技有限公司提供,产品标准号:Q/ADPG001-2008;黄芪、党参、茯苓、白术、陈皮、砂仁购自福建紫金医药连锁有限公司,质量符合中华人民共和国兽药典(2005版)标准。银杏叶复方制剂制备方法参照前期研究结果,制得每mL含有1 g生药的药液[2],为急性毒性试验用。体外细胞毒性试验前将药液浓度调整至100 g·L-1,0.22 μm滤膜过滤除菌,按2-n倍比稀释(n为1~8),用细胞维持液分别稀释成:50 g·L-1(2-1)、25 g·L-1(2-2)、12.5 g·L-1(2-3)、6.25 g· L-1(2-4)、3.12 g·L-1(2-5)、1.56 g·L-1(2-6)、0.78 g· L-1(2-7)、0.39 g·L-1(2-8)共8个稀释度。
1.1.2 试验动物
6周龄清洁级KM种小鼠,雌性,体质量23~26 g,购自上海斯莱克实验动物有限公司,合格证编号2007000502350。
1.1.3 鸡胚成纤维细胞(CEF)
10日龄鸡胚,检查正常后,按常规方法处理鸡胚并经胰蛋白酶消化后,以10%小牛血清的RPMI 1640调整细胞密度5×108个·L-1[5]。
1.1.4 试剂
细胞生长液:含10%小牛血清(山东赛恩斯科技有限公司产品)的RPMI 1640培养液(HyClone公司);细胞维持液:基本同细胞生长液,但小牛血清浓度均减至2%;D-Hanks'缓冲液常规配制;MTT(四甲基偶氮唑盐,上海捷瑞生物工程公司),用生理盐水配制成5 g·L-1溶液。
1.1.5 仪器
3111型CO2恒温培养箱(Thermo公司);TH4-200型荧光倒置显微镜(购自日本OLYMPUS公司);酶标仪(购自Thermo公司);SW-CJ-1FB型超净工作台(购自苏州净化设备有限公司);96孔细胞培养板(Corning Incorporated,USA)。
1.2 方法
1.2.1 银杏叶复方制剂对小鼠的急性毒性试验
1.2.1.1 小鼠一般症状观察以及半数致死量(LD50)测定方法
预试验找出0和100%估计致死量。试验取清洁级KM小鼠48只,平均随机分成4组,第1~3组为不同剂量组,第4组为对照组。试验前禁食12 h,1次性灌胃给药,给药浓度分别为0.25、0.50和1.00 g·mL-1,对照组灌服生理盐水,各组给药量均为0.40 mL·10 g-1,给药后连续观察7 d,注意观察小鼠的行为活动、饮食及精神状况,详细记录中毒症状、中毒时间、中毒持续时间以及动物死亡时间。改良寇氏法计算LD50[6]。
1.2.1.2 小鼠最大耐受量(MTD)测定
取清洁级KM小鼠20只,采用1 g·mL-1浓度的药物,0.4 mL·10 g-1(为体重20 g小鼠的最大给药剂量)灌胃,1日给药3次,每8 h一次(累积折合日用药量为120 g·kg-1体重)。第3次给药后2 h喂食,连续观察7 d。第7天全部小鼠脱颈处死,剖检,记录心、肝、脾、肺、肾的病理变化[7]。
1.2.2 银杏叶复方制剂体外细胞毒性测定
1.2.2.1 形态学观察法以及最大安全质量浓度(TC0)的判断标准
分别在96孔细胞培养板的各试验孔加入5× 108个·L-1CEF 100 μL及各稀释度药物100 μL,每一浓度重复4孔,同时设4孔不加药物但加5×108个·L-1CEF 100 μL和100 μL细胞维持液作为细胞对照,另设4孔加200 μL细胞维持液作为空白对照。5%CO2、37℃培养24、48和72 h后观察细胞生长情况,判定药物对细胞贴壁的影响,结果记录为4个平行孔的平均值,以“+”、“-”表示。药物的安全质量浓度应是对未贴壁的CEF无影响的最小药物稀释度。选择对CEF贴壁没有损伤的最低稀释度为本试验受试药物的最大安全质量浓度(TC0)。判断结果标准如下[8]:
“+++++”表示细胞生长最好,细胞折光性良好,全部贴壁,无空隙;“++++”表示细胞生长较好,细胞基本贴壁,基本无空隙;“+++”表示细胞生长一般,细胞贴壁少,有较多空隙和极少圆细胞;“++”表示细胞生长较差,有大量圆细胞和空隙;“+”表示细胞生长很差,基本为圆细胞,极少贴壁细胞;“-”表示细胞生长极差或无细胞生长,全部为未贴壁圆细胞或细胞破碎不完整或轮廓不清无明显可见的细胞。
1.2.2.2 MTT法以及最大安全质量浓度(TC0)的判断标准
待CEF长成均匀单层后,弃去细胞生长液,由高到低加入不同浓度的药物,每孔50 μL,每个质量浓度重复4孔,同时以相应的同体积培养液代替,药液正常细胞对照组和培养液空白对照组各4孔,继续培养。加药后每隔12 h观察1次细胞单层完好程度,培养44 h后每孔加入MTT 100 μL,4 h后弃MTT上清液,加二甲基亚砜(DMSO)溶解液150 μL,30 min后用酶标仪测定每孔的A570nm值。取4个平行孔的平均A值,计算细胞破坏百分率。
破坏率(%)=[(A细胞组-A给药组)/(A细胞组-A空白组)]×100%[8]
选择与细胞对照组A570nm值差异不显著的细胞,细胞破坏率小于5%的药物最大质量浓度为该药最大安全质量浓度(TC0)。复方制剂组的A570nm值显著大于细胞对照组时,表明该药显著促进细胞生长[9]。
1.3 统计分析
数据用SPSS16.0软件统计,进行One-Way ANOVA分析和Duncan's氏多重比较,结果以平均值±标准差表示。
2 结果与分析
2.1 银杏叶复方制剂LD50的测定
各组小鼠根据表1中不同剂量一次性灌胃给药。刚灌完药时,小鼠精神沉郁、被毛耸立、扎堆,6 h后开始活动,12 h后开始恢复饮水采食,1周后观察小鼠无一死亡,活动、饮食及精神状况等均无异常。结果表明,当银杏叶复方制剂LD50>40 g·kg-1体重,药物毒性很小,临床使用安全(见表1)。
2.2 小鼠最大耐受量(MTD)测定
经MTD测定,连续观察7 d发现各组小鼠全部存活,精神、食欲与对照组相比无差别,剖检观察小鼠各内脏器官均无明显病理变化,表明小鼠对该复方制剂的MTD在120 g·kg-1体重以上。
2.3 形态学观察法测定结果
银杏叶复方制剂对CEF的影响见表2和图1~6。CEF只贴壁生长繁殖,是由其细胞特性决定及试验过程加入血清贴壁因子所致。添加不同药物浓度的CEF在培养24 h后均贴壁完全,生长良好,与细胞对照组生长趋势一致。72 h时药物浓度达最高稀释度50 g·L-1时也不影响CEF贴壁,1~8孔细胞长势与细胞对照组相比无差别,空白对照组无细胞生长。结果表明,用形态学观察法测定该复方制剂对CEF的最大安全质量浓度(TC0)>50 g·L-1,说明该药物高浓度时未表现细胞毒性。
2.4 MTT法测定结果
MTT法48 h测定结果见表3。由表3可知,当药物浓度低于3.12 g·L-1时,各孔吸光度值与细胞对照组无显著差异(P>0.05),药物浓度在0.78和0.39g·L-1时,细胞破坏率为负值,且随药物浓度的降低,吸光度值成上升趋势,活细胞率提高,说明在此浓度范围内药物对CEF无明显的细胞毒性;当药物浓度高于6.25 g·L-1时,各孔吸光度值显著低于细胞对照组(P<0.05),且随药物浓度的增加,吸光度值明显下降,活细胞率减少,说明药物在高浓度范围内对细胞具有不同程度的毒性作用,随着药物浓度的增加毒性显著增强。结果表明,MTT法测定该复方制剂对CEF的最大安全质量浓度(TC0)是0.78 g·L-1。
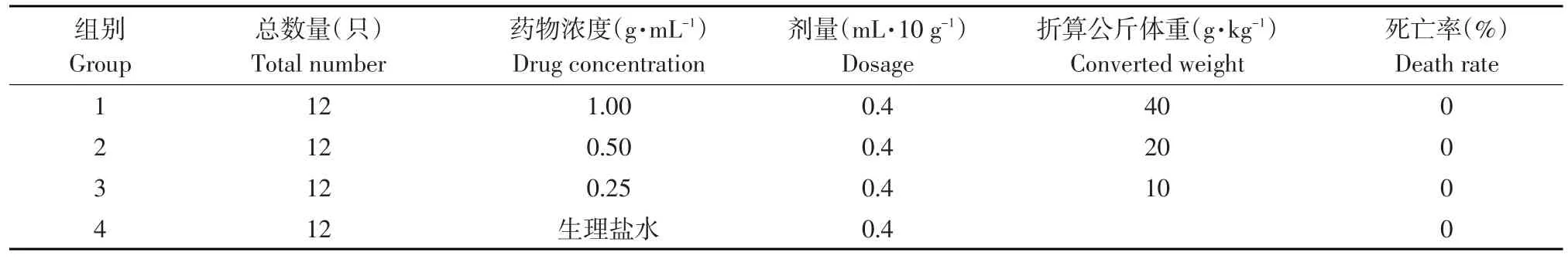
表1 银杏叶复方制剂LD50Table 1 Oral LD50of Ginkgo biloba compound

表2 不同药物终浓度对CEF贴壁的影响Table 2 Effect on adherent CEF of the different concentrations(g·L-1)

图1 银杏叶复方制剂对鸡胚成纤维细胞(CEF)24 h贴壁的影响(×20)Fig.1 Effect of adherent CEF of Ginkgo biloba compound in 24 h(×20)
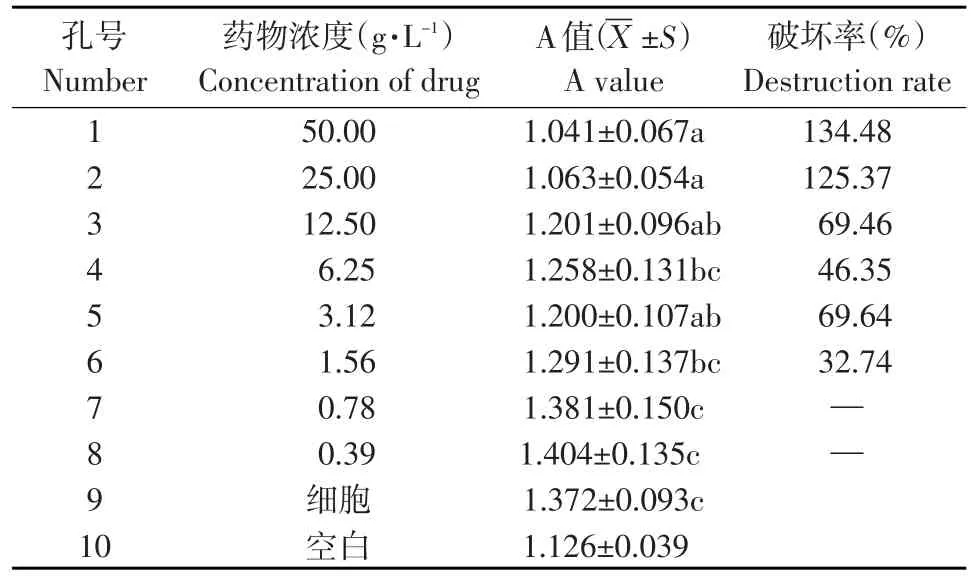
表3 银杏叶复方对鸡胚成纤维细胞毒性测定结果Table 3 Cytotoxicity of Ginkgo biloba compound on chick embryo fibroblast
3 讨论与结论
3.1 银杏叶复方制剂的急性毒性试验
刘翠艳以黄芪、白术、防风、茯苓等配制成中药免疫增强剂,试验发现小鼠以40 g·kg-1体重灌胃给药,无小鼠死亡,无法测定LD50,即LD50在40 g·kg-1体重以上;经MTD测定,小鼠对该复方制剂的MTD在120 g·kg-1体重以上[7],与本试验结果一致,表明银杏叶复方制剂毒性很低。按照毒性分级标准,可认为该制剂在短期内使用安全。
3.2 银杏叶复方制剂体外细胞毒性测定
目前国内外一般使用MTT法和形态学观察法对药物的细胞毒性进行分析。形态学观察法检测药物毒性最为常用,在显微镜下逐日观察细胞形态变化,药物浓度高对细胞有毒性时细胞会变圆,固缩性坏死甚至脱落,但此法主观性强,需要经验且耗时。目前MTT[3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐]比色法在体外肿瘤细胞化疗药敏试验的应用越来越广泛,成为评价药物安全的重要指标,检测原理为活细胞线粒体中的琥珀酸脱氢酶能使外源性MTT还原为水不溶性的蓝紫色结晶甲瓒并沉积在细胞中,而死细胞无此功能。二甲基亚砜(DMSO)能溶解细胞中的甲瓒,用酶联免疫检测仪在一定波长处测定其光吸收值,可间接反映活细胞数量,此法优点是灵敏度高、经济。本试验分别采用形态学观察和MTT两种方法,比较两种方法测定的效果,综合两种方法的测定结果以确定药物的最大安全浓度,结果表明:①用形态学观察法观察银杏叶复方制剂对CEF的贴壁程度,高浓度时银杏复方制剂并不抑制细胞生长,不呈现细胞毒性,细胞贴壁且贴壁效果与细胞对照组无明显差异。②在MTT法中,在一定的浓度范围内,随着药物浓度的降低,吸光度值增大,细胞破坏率减小。③用MTT法得到银杏叶复方制剂对CEF的最大安全浓度(TC0)是0.78 g·L-1,而在形态学观察法中药物的最大浓度(TC0)达50 g·L-1时也在安全浓度范围内,表明形态学观察法主观性强,容易对试验结果产生较大误差,而MTT法相对简单直观、准确性更高,此结果可为后续体外免疫药理学研究提供理论依据。
银杏叶复方制剂LD50>40 g·kg-1体重,MTD>120 g·kg-1体重,说明药物毒性很小,临床使用安全。在形态学观察法中银杏叶复方制剂在高浓度时未表现细胞毒性,在MTT法中银杏叶复方制剂对CEF的最大安全质量浓度为0.78 g·L-1。
[1]高庚渠,马威,陈博,等.中草药免疫增强剂在养禽生产中的应用[J].河南畜牧兽医,2010,31(8):8-10.
[2]李焰,王华,周孝琼,等.银杏叶复方对实验性脾虚证模型小鼠消化酶活性和抗氧化性能的影响[J].中国畜牧杂志,2010,46(21): 52-55.
[3]李焰,杨小燕,黄其春,等.银杏叶复方对脾虚证小鼠肠道推进功能、抗疲劳和抗氧化作用的影响[J].安徽农业大学学报,2012, 39(2):170-173.
[4]李焰,杨小燕,黄其春,等.银杏叶复方对脾虚证小鼠细胞因子、免疫球蛋白和血浆内种神经肽含量的影响[J].东北农业大学学报,2012,43(6):82-87.
[5]赵晓娜,牛家强,胡元亮,等.十二种藏药对鸡胚成纤维细胞的安全浓度和生长的影响[J].中国兽医学报,2009,29(4):511-513.
[6]王月华,杨海光,李莉,等.昂单斯琼杂质的小鼠急性毒性和细胞毒性研究[J].中国药物警戒,2012,9(12):707-709.
[7]刘翠艳.兽医中药免疫增强剂的筛选试验及其药理学研究[D].泰安:山东农业大学,2007:46-56.
[8]刘翠艳,赵宏坤,韩春杨.中药免疫调节剂体外细胞毒性测定[J].山东农业大学学报:自然科学版,2007,38(2):225-229.
[9]赵晓娜,牛家强,胡元亮,等.十二种藏药对鸡胚成纤维细胞的安全浓度和生长的影响[J].中国兽医学报,2009,29(4):511-513.
Study on acute toxicity in mice and cytotoxicities ofGinkgo biloba compound
LI Yan1,2,LIN Xiangyan1,ZHANG Jixin1,Yin Huifang1,2(1.School of Life Science of Longyan University,Longyan Fujian 364000,China;2.Key Laboratory of Preventive veterinary medicine,Educational Commission of Fujian Province;Longyan Fujian 364000,China)
Study the acute toxicity in mice and cytotoxicities ofGinkgo bilobacompound to make sure the safety of clinical application.①The half lethal dose(LD50)and the maximum tolerance dose (MTD)were the indexes in the acute toxicity test.The mice were givenGinkgo bilobacompound through intragastric administration at the dose of 40 g·kg-1·W.The mice were still alive after 1 week, then they were given the compound at the dose of 120 g·kg-1·W.everyday at the condition of the most tolerant dose.After 1 week,the mice were killed to observe the pathological change.②The cytotoxicity tests were carried out by the morphology observation and the MTT assay.100 g·L-1ofGinkgo biloba compound was diluted into 2-n(n is from 1 to 8)with the cell maintenance medium,to test the most safety concentration(TC0)ofGinkgo bilobacompound on chick embryo fibroblast(CEF).The results showed that the acute toxicity ofGinkgo bilobacompound was very low.The LD50and MTD was above 40 g·kg-1·W.and 120 g·kg-1·W.,respectively.The mice were still alive and had no pathological change.According to the toxicity level standard,the short period use of compound was safe.Ginkgo biloba compound did not exhibit cytotoxicity at high concentrations in the morphology observation.The TC0of Ginkgo biloba compound was 0.78 g·L-1in the MTT assay.
Ginkgo biloba compound;mice acute toxicity;chick embryo fibroblast;cytotoxicity
S792.95;S816.79
A
1005-9369(2014)08-0079-05
2014-02-11
福建省科技厅自然科学基金项目(2012J01142);福建省科技厅科技计划重点项目(2011N0024)
李焰(1968-),女,教授,硕士.研究方向为饲料添加剂。E-mail:tina680605@tom.com
时间2014-7-18 14:58:44[URL]http://www.cnki.net/kcms/detail/23.1391.S.20140718.1458.004.html
李焰,林香燕,张继欣,等.银杏叶复方制剂对小鼠急性毒性和细胞毒性研究[J].东北农业大学学报,2014,45(8):79-83.
Li Yan,Lin Xiangyan,Zhang Jixin,et al.Study on acute toxicity in mice and cytotoxicities ofGinkgo bilobacompound[J]. Journal of Northeast Agricultural University,2014,45(8):79-83.(in Chinese with English abstract)
