奈达铂或顺铂联合调强放疗治疗鼻咽癌的随机对照研究
2013-10-10张立新汪宏斌孙国贵董桂兰刘卫东
张立新 汪宏斌 孙国贵 董桂兰 刘卫东
绝大多数中晚期鼻咽癌同步放化疗的临床研究表明,这种治疗模式能显著提高中晚期鼻咽癌患者的临床疗效,同时毒副反应也明显增加。随着放疗技术及放射生物学发展,肿瘤的局部控制率明显提高,而远处转移已成为中晚期鼻咽癌治疗失败的主要原因。寻找高效低毒、且与放疗毒性不相叠加的化疗药物,从而不明显增加治疗相关毒副反应是中晚期鼻咽癌同步放化疗综合治疗的主要方向。
1 资料与方法
1.1 一般资料 2009年1月至2011年1月,共有75例Ⅲ、Ⅳ期鼻咽癌初治患者入组。采用随机数字表,将62例患者随即分为NR组和DR组,每组32例。NR组中男23例,女9例;平均年龄(45±11)岁;DR组中男22例,女10例;平均年龄(45±10)岁。2组患者的临床资料比较,差异无统计学意义(P>0.05)。见表1。

表1 2组鼻咽癌患者一般情况比较 例
1.2 入组标准 (1)经组织病理学确诊的鼻咽癌初治患者;(2)按照中国鼻咽癌临床分期工作委员会通过的鼻咽癌2008分期标准,均为Ⅲ期~Ⅳa期;(3)年龄23~65岁;(4)无远处转移,心、肺、肝、肾正常功能;(5)Karnofsky评分≥70;(6)至少有一个单径可测量的病灶(≥10 mm);(7)患者签署放化疗同意书。
1.3 治疗方法 治疗组:从开始调强放疗第1天开始,奈达铂30 mg/m2,每周1次,共5周。对照组:从开始调强放疗第1天开始,顺铂30 mg/m2,每周1次,共5周。比较2组的疗效和急性不良反应。2组患者化疗前常规应用止吐药5-HT3受体拮抗剂;疗中出现血白细胞和血小板减少者给予粒细胞集落刺激因子和白介素-Ⅱ治疗。重组人表皮生长因子外用溶液(金因肽)处理Ⅱ度以上口腔黏膜及颈部皮肤反应。
1.4 疗效评价及不良反应观察 每周复查血常规1次,每周检查口咽黏膜、鼻咽部及颈部皮肤及淋巴结2次,每次化疗前复查肝肾功能,治疗前、治疗结束后结束后1个月全面体格检查。鼻咽原发灶检查采用鼻咽间接镜、鼻咽光导纤维镜及鼻烟CT或鼻烟MRI检查评价疗效。毒副反应采用WHO毒性分级标准0~Ⅳ级。
1.5 评价标准 患者每周复查血常规、每两周复查生化常规及体检,并于第5周末行MRI检查。填写临床观察表,对急性不良反应记录并处理,按实体瘤评价标准(RECIST)评价疗效。分为完全缓解(CR)、部分缓解(PR)稳定(SD)和疾病进展(PD),有效率为CR+PR。
1.6 统计学分析 应用SPSS 13.0统计软件,计数资料采用χ2检验及Fisher精确检验,P<0.05为差异有统计学意义。
2 结果
2.1 2组疗效比较 治疗后鼻咽原发性及颈部淋巴结消退情况2组比较差异无统计学意义(P>0.05)。见表2。
2.2 2组不良反应比较 2组患者的白细胞、血小板、谷丙转氨酶、水平检测无明显差异(P>0.05),Ⅲ度急性口腔黏膜炎Ⅲ度颈部皮肤反应、体重下降的发生率比较,亦无明显统计学意义(P >0.05)。见表3。

表2 2组治疗后鼻咽原发灶及颈部淋巴结消退情况
3 讨论
鼻咽癌对放射线高度敏感,化疗亦有较高有效率,早期患者预后好。而70%患者在诊断时已是局部晚期,单纯放疗效果差,晚期鼻咽癌患者单纯放射治疗的5年生存率为50% 左右,同步放化疗的5年生存率为70% 左右[1-5]。治疗失败者中局部复发和远处转移各占一半。在比较同步放化疗和单纯放疗的研究中,Chan等[6]PWHQEH-94临床研究亚组分析发现同步放化疗对于T3-4期患者效果明显,而T1-2期患者却没有从中获益。新辅助化疗在局部晚期鼻咽癌综合治疗中的作用已基本被否定[7],而辅助化疗在鼻咽癌治疗中也未能降低远处转移率和提高生存率[8]。
调强放疗技术在保护周围正常器官的同时使病变部位达到根治剂量成为可能。2006年以来,给予肿瘤原发灶及转移淋巴结70~74 Gy,高危淋巴引流区60~66 Gy,预防照射区50~54 Gy的照射剂量已形成共识。治疗局部晚期鼻咽癌所面临的最大挑战是如何防止远处转移。同步放化疗可增加放射治疗的敏感性、减少远处转移[9],多数学者尝试通过同步放化疗来提高鼻咽癌的局部控制率和生存率、降低远处转移率。现有研究结果表明,同步放化疗能够显著提高肿瘤的局部控制率(同步放化疗后CR率为67%~85%)和患者的总生存率(5年无进展生存率为60%)[10-13]。越来越多的Ⅲ期临床实验已证实,同步放化疗可使局部晚期NPC的5年生存率从原来的50%提高到70%。
然而,Psyrri等[14]经长期随访的结果显示:同步放化疗用于头颈部鳞癌:急性毒性反应和治疗结束3年后的晚期毒性反应均显著高于单纯放疗(P<0.01)。国内同步放化疗Meta分析结果显示同步放化疗可以减少远处转移率并提高生存率,同步放化疗远处转移率是单纯放疗的0.44倍;1、3、5总生存率分别是单纯放疗的2.00倍、2.31倍、2.37倍。但毒副反应发生率也明显增加,3/4度白细胞减少、胃肠道反应、口腔黏膜反应分别是单纯放疗的 10.27 倍、6.34 倍、2.06 倍[15]。
黄晓东等[16]鼻咽癌同步放化疗耐受性研究发现泰素和顺铂在急性并发症方面有所不同,泰素组患者黏膜炎和皮肤炎较重,而顺铂则骨髓抑制较为明显,均不是很理想的同步治疗药物。因此应筛选新型的毒副作用低的药物进行同步放化疗,在提高疗效的同时,不增加患者的急性毒副反应。王凯等[17]研究发现与每周顺铂同步放化疗相比,3周方案的化疗并发症有所增加,化疗依从性差,但未影响放疗的进行。
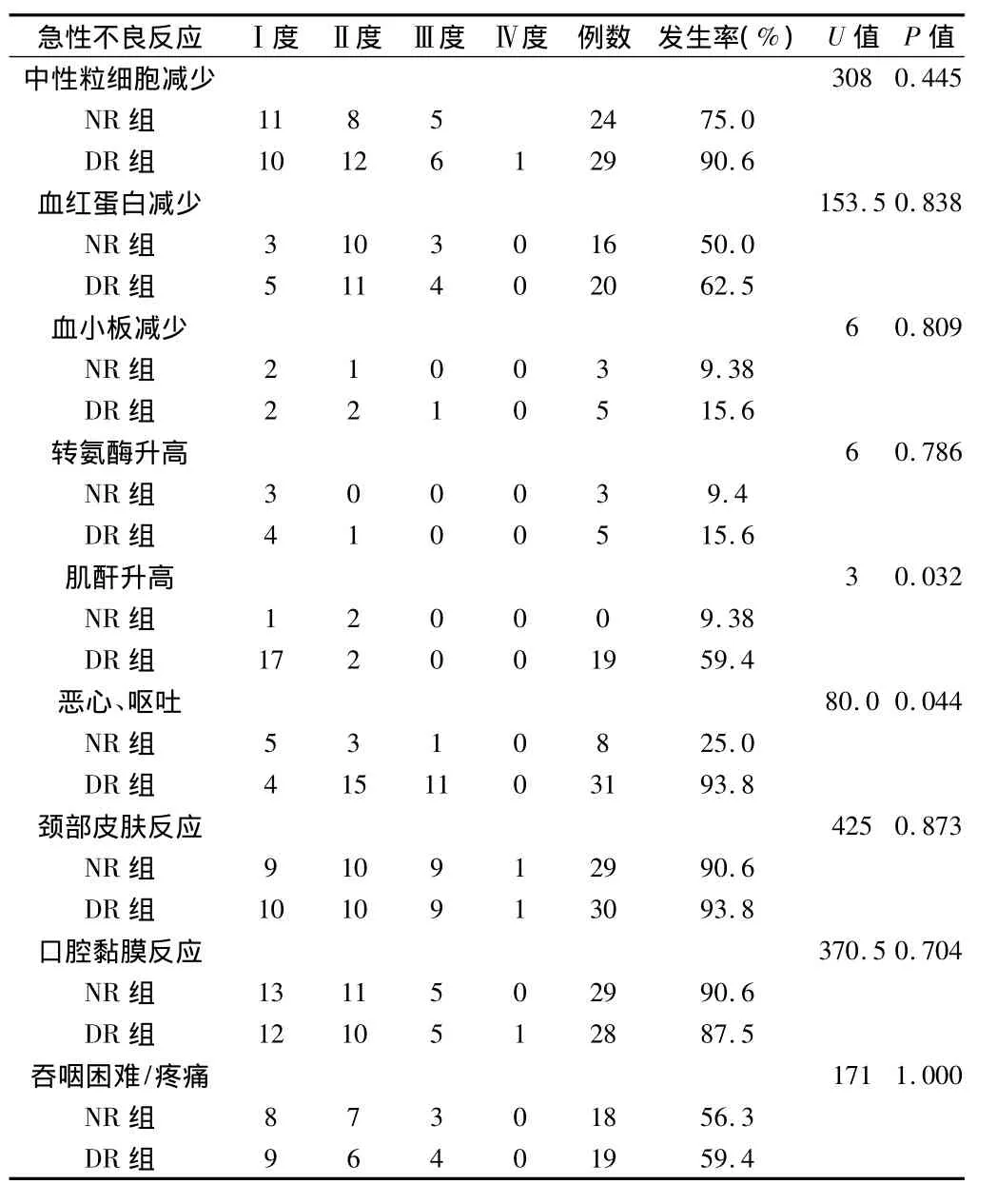
表3 2组鼻咽癌患者同步放化疗不良反应比较n=32,例
奈达铂(CDGP)是日本研发的第二代钵类化合物,其研发目的在于降低使用顺铂(CDDP)相关联的肾毒性。其作用机理是与DNA结合而抑制DNA复制,产生抗肿瘤活性。奈达铂水溶性比顺铂高10倍,并且胃肠道反应和肾毒性均明显低于顺铂,临床上已广泛用于头颈癌、肺鳞癌、食管癌、卵巢癌和宫颈癌等,在晚期宫颈癌奈达铂同步放化疗近期有效率为100%[18,19]。
余忠华等[20]应用每周小剂量奈达铂或顺铂同步放化治疗局部晚期鼻咽癌的近期有效率分别为73.33%和76.67%,差异无统计学意义(P>0.05)。庞丹梅等[21]将奈达铂单药用于局部晚期鼻咽癌同步放化疗与顺铂加5-氟尿嘧啶联合方案同步放化疗比较疗效相近似,总生存率、局部控制率及无复发生存率均无统计学差异(P>0.05),奈达铂单药在恶心、呕吐、口腔黏膜反应较轻。
本研究中对奈达铂单药用于局部晚期鼻咽癌同步放化疗,并与CDDP单药同步放化疗的近期疗效及急性毒副反应对比观察。肿瘤放疗剂量50Gy时鼻咽病灶消退率(P>0.05)、颈部淋巴结转移灶消退率(P>0.05),全程放疗结束后3个月鼻咽病灶消退率(P>0.05)、颈部淋巴结转移灶消退率(P>0.05)2组均无统计学差异。2组毒副反应比较:NR vs DR皮肤反应、黏膜反应、吞咽困难/疼痛、中性粒细胞减少、恶心呕吐、贫血、血小板减少。恶心呕吐、血肌酐升高DR组均较NR组明显(P<0.05)。
同步放化疗用于局部晚期鼻咽癌的理论基础是:(1)化疗的细胞毒作用使肿瘤缩小并使肿瘤细胞周期同步化,改善肿瘤细胞乏氧,起放疗增敏作用。(2)干扰或抑制肿瘤细胞亚致死性损伤的修复,与放疗起协同作用。(3)消灭亚临床转移灶[22,23]。
依据上述理论每周一次奈达铂或顺铂能更好地起增敏作用,本研究中2组在近期疗效方面无统计学差异,而奈达铂单药同步放化疗毒副作用较低,患者耐受性好。所以,同步放化疗可采用奈达铂单药每周一次方案,而奈达铂每周的具体剂量和长期疗效需要进一步研究。
1 Wee J,Tan EH,Tai BC,et al.Randomize d trial of radio-therapy versus concurrent chemoradiothe rapy followed by adjuvant chemotherapy in patients with American Joint Committee on Cancer/Interna tional Union against cancer stageⅢandⅣnasopharyngeal cancer of the endemic variety.JClin Oncol,2005,23:6730-6738.
2 Langendijk JA,Lee mans ChR,Buter J,et al.The additional value of chemotherapy to radiothera py in locally advanced nasopharyngeal carcinoma:a meta-analysis of the published literature.J Clin Oncol,2004,22:4604-4612.
3 Kwong DL,Sham JS,Au GK,et al.Concurrent and adjuvant chemotherapy for nasopharyngeal carc inoma:afactorial study.J Clin Oncol,2004,22:2643-2653.
4 Lin JC,Jan JS,Hsu CY,et al.Phase Ⅲ study of concurrent chemoradiotherapy versus radiotherapy a lone for advanced nasopharyngeal carcinoma:positive effect on over-all and progression-free survival.JClin Oncol,2003,21:631-637.
5 Chau DT,Ma J,Sham JST,et al.Long-term survival after cisplatin-based induction che motherapy and radiotherapy for nasopharyngeal carcinoma:A pooled data analysis of two phase Ⅲ Trials.J Clin Oncol,2005,23:1118-1124.
6 Chan AT,Leung SF,Ngan RK,et al.Overall survival after concurrent cisplatin-radiotherapy compared with radiotherapy alone in locoregionally advanced nasopharyngeal carcinoma.J Natl Cancer Inst,2005,97:536-539.
7 Geare FB,Glisson BS,Sangguineti G,et al.Induction chemotherapy follow by radiotherapy alone in patients with advance nasopharyngeal carcinoma:results of matched cohort study.Cancer,1997,79:1279-1286.
8 Rossi A,Molinari R,Boracchi P,et al.Adjuvant chemotherapy with vincristine,cyclophosphamide,and doxorubicin after radiotherapy in local-regional nasopharyngeal cancer:results of a 4-year multicenter randomomized study.J Clin Oncol,1988,6:1401-1410.
9 Wolden SL,Zelefsky MJ,Kraws DH,et al.Accelerated concomitant boot radiotherapy and chemothe rapy for advanced nasopharyngeal carcinoma.J Clin Oncol,2001,19:1105-1110.
10 Langendijk JA,Leemans CR,Buter J,et al.The additional value of chemotherapy to radiotherapy in locally a dvanced nasopharyngeal carcinoma:a meta-analysis of the published literature.J Clin Oncol,2004,22:4604-4612.
11 Lee AW,Lau WH,Tung SY,et al.Preliminary results of a randomized study on the rapeutic gain by concurrent chemotherapy for regionallyadvanced nasopharyngeal carcinoma:NPC-9901 Trial by the Hong Kong Nasopharyngeal Cancer Study Group.J Clin Oncol,2005,23:6966-6975.
12 Lin JC,Jan JS,Hou CY,et al.PhaseⅢstudy of concurrent chemoradiotherapy versus radiotherapy a lone for advanced nasopharyngeal carcinoma:positive effect on over-all and progression-free survival.J Clin On-col,2003,21:631-637.
13 Cooper JS,Lee H,Torrey M,et al.Improved outcome secondary to concurrent chemoradiotherapy for a dvanced carcinoma of the nasopharynx:preliminary corroboration of the intergroup experience.Int JRadiat Oncol Biol Phys,2000,47:861-866.
14 Psyrri A,Kwong M,DiStasio S,et al.Cisplatin,fluorouracil,and leucovorin induction chemotherapy followed by concurrent cisplatin chemoradiotherapy for organ preservation and cure in patients with advanced head and neck cancer:long-term follow-up.J Clin Oncol,2004,22:3061-3069.
15 邹长林,景钊,张薛榜,等.中晚期鼻咽癌同期放化疗疗效的Meta分析.温州医学院学报,2008,38:237-240.
16 黄晓东,易俊林,高黎,等.鼻咽癌同步放化疗耐受性研究.肿瘤学杂志,2007,13:367-371.
17 王凯,易俊林,高黎,等.三周方案顺铂同步放化疗治疗晚期头颈部肿瘤的耐受性.肿瘤学杂志,2006,12:251-253.
18 李继东,王舒,肖永久,等.国产奈达铂联合吉西他滨治疗晚期非小细胞肺癌.实用医学杂志,2008,24:811-812.
19 程晓伟,杨宇星,俞小元.顺铂与奈达铂同步放化疗治疗中晚期宫颈癌的临床研究.肿瘤,2011,7,31:662-664.
20 余忠华,王镇南.每周小剂量奈达铂或顺铂同步放化疗治疗局部晚期鼻咽癌的近期疗效观察.中华医学会放射肿瘤治疗学分会六届二次暨中国抗癌协会肿瘤放疗专业委员会二届二次学术会议论文集.
21 庞丹梅,邓燕明,卫光宇.局部晚期鼻咽癌同步放化疗单药与联合方案的疗效对比.实用医学杂志,2010,26:76-78.
22 王小军,张建,郭琳琅,等.阿司匹林增强鼻咽癌细胞放射敏感性的研究.实用医学杂志,2009,25:1186-1188.
23 殷蔚伯,谷铣之主编.肿瘤放射治疗学.第1版.北京:中国协和医科大学出版社,2003.369-381.
