槲皮素锑的制备*
2013-07-19郑赛飞渠文涛翟广玉
郑赛飞, 渠文涛, 翟广玉,**
(1.郑州大学 护理学院,河南 郑州 450052;2.郑州大学 药学院 ,河南 郑州 450052)
槲皮素锑的制备*
郑赛飞1, 渠文涛2, 翟广玉1,2**
(1.郑州大学 护理学院,河南 郑州 450052;2.郑州大学 药学院 ,河南 郑州 450052)
以槲皮素与三氯化锑为原料制备槲皮素锑配合物,研究合成槲皮素锑的最佳反应条件。试验分别考察了温度、pH及反应时间对槲皮素锑收率的影响,并通过紫外光谱、红外光谱对槲皮素锑进行了表征。结果显示:槲皮素与三氯化锑在甲醇溶液中,在pH=8.6的室温条件下反应2h收率最高,达到62%。
槲皮素;槲皮素锑;配合物;合成
前 言
槲 皮 素 [3,3',4',5,7- 五羟基 黄 酮 ,CAS:117-39-5]是天然存在的黄酮醇类化合物,由两个苯环(A环和B环)和一个吡喃酮连接组成,属于苯并吡喃酮(γ)衍生物。槲皮素广泛分布在人们的日常饮食中,如洋葱、番茄等蔬菜[1];苹果、柑橘等水果[2];田七、银杏等中草药[3];茶叶、可可粉等饮料[4]中。槲皮素具有广泛的生物活性及药理活性,如抗氧化[5~6]、抗肿瘤[7]、抗炎[8]、抗病毒[9]、保护心脏[10]等。近年来,槲皮素及其衍生物已成为药物化学研究的一个热点[11]。

图1 槲皮素的化学结构Fig.1 The chemical structure of quercetin
锑及其化合物的用途广泛。三氧化锑具有阻燃性,是很好的防火材料。家庭使用的沙发,窗帘,地毯等常常喷涂三氧化锑作为阻燃涂料。三氧化锑还是优良的白色颜料,广泛用于陶瓷、橡胶、油漆、玻璃、纺织及化工产业。然而,由于自然过程及人类活动的影响,环境中的锑污染也日益严重。锑是一种有毒的重金属,环境中的锑可能会通过饮食、呼吸、皮肤接触等各种途径进入人体,从而对人类的健康构成潜在的威胁。因此,人类应当对环境中的重金属污染予以高度重视[12]。
螯合治疗是减缓重金属中毒的首选疗法[6]。螯合剂能与引起中毒的重金属离子牢固地结合成螯合物,从体内排泄出去,达到解毒的目的。由于槲皮素的强配位氧原子及合适的空间构型,易与金属离子结合成稳定的螯合物,是一种有良好的金属离子螯合配体。经常食用一些富含槲皮素等黄酮类的食物,如苹果、洋葱、茶叶、银杏、荞麦等,可清除体内的自由基,使机体免受自由基的损伤,对降低人体内重金属离子的含量也起着重要的作用[13]。
作者研究发现,槲皮素与锑离子在室温下很容易生成槲皮素锑配合物。本文探讨了合成槲皮素锑的最佳条件,槲皮素锑的生物学活性正在研究中。
1 实验部分
1.1 仪器和试剂
UV-2550型紫外-可见分光光度计(日本岛津公司);iS10 FT-IR型红外光谱仪(美国尼高力,KBr压片);RE-52AA型旋转蒸发仪(上海亚荣生化仪器厂);85-2型恒温磁力搅拌器(上海司乐仪器有限公司)。槲皮素(97%,上海晶纯试剂有限公司),三氯化锑(AR,国药集团化学试剂有限公司),甲醇钠(AR,天津科密欧化学试剂有限公司),其它试剂均为分析纯。
1.2 槲皮素锑的制备
[6]方法并有所改进。取槲皮素(1mmol,0.3020g),放入50mL的圆底烧瓶,加入25mL甲醇,搅拌15min至完全溶解,溶液为浅黄绿色。用适量甲醇钠调节至pH=8.6,加入无水三氯化锑(1mmol,0.2282g),溶液的颜色转变为桔黄色。常温下反应2h,薄层层析(TLC)监测反应进程。反应结束后,过滤,滤液旋蒸浓缩,得深棕黄色固体。用甲醇/水(1:3)洗涤固体3次,放入真空干燥箱干燥,即得到槲皮素锑,收率62%。
2 结果与讨论
2.1 反应温度对配合物生成的影响
从参考文献看,槲皮素金属配合物的制备大部分在60℃左右反应。作者从室温(25℃)每隔5℃做一个试验,并采用TLC监测反应进程。实验结果显示,反应温度对槲皮素锑的收率影响并不大。即室温反应与加热反应,槲皮素锑的收率都是在60%左右。所以作者选择在常温下制备槲皮素锑配合物。
2.2 反应pH值对配合物生成的影响
槲皮素具有较高的超离域度,完整的大π键共轭体系,强配位氧原子与合适的空间构型,是金属离子的良好螯合配体,可作为Lewis碱与作为Lewis酸的金属离子进行酸碱螯合反应。但是,由于槲皮素本身分子内氢键的作用,使其供电子能力减弱,加入碱可破坏其氢键。目前,文献中常用的碱有:氢氧化钠、氢氧化钾、氨水、甲醇钠、乙醇钠、醋酸钠、碳酸钠、碳酸钾、碳酸氢钠等。在考虑到反应产物的纯化等问题后,我们采用甲醇钠调溶液的pH值,每隔0.2pH单位为一个实验,我们分别试验了pH=7.2~10.0共15个试验,实验结果发现,pH=8.6时,收率最高。
2.3 反应时间对配合物生成的影响
反应时间的长短,直接影响反应进行的程度。作者从0.5h开始,每隔30min,做一个试验,从0.5~5.0h,采用TLC监控反应进程,实验结果如表1所示。

表1 反应时间对收率的影响Table 1 The effects of reaction time on the yield
从上表可以看出,反应在2h时,收率较高。再延长反应时间,收率变化不大。

图2 薄层层析图Fig.2 The thin-layer chromatography
从图2 TLC可以清楚的看出,在0.5h时,大部分原料还没有反应,从TLC上可以清楚的看到,产物很少;1.5h时,原料槲皮素还有一部分没有反应。在2h时,原料槲皮素已经完全转变成产物槲皮素锑。再延长反应时间,收率变化不大。故作者把反应时间控制在2h。
2.4 紫外光谱分析
槲皮素的紫外光谱两个特征吸收峰分别为:带II为 255nm,带 I为 375 nm。

图3 槲皮素和槲皮素锑的紫外光谱Fig.3 The UV spectrum of quercetin and quercetin-Sb complex
比较槲皮素与槲皮素锑的紫外线光谱发现。槲皮素形成配合物后,特征吸收峰发生了红移,这可能是由于形成配合物后,共轭体系扩大所致。带I从375nm移到426nm,红移了51nm。带II从255 nm移到280 nm,红移了25 nm。这说明槲皮素与锑离子形成了配合物,共轭体系增大,导致紫外光谱发生红移。
2.5 红外光谱分析
槲皮素分子主要官能团红外吸收峰分别是:羟基 υ-OH3408.74cm-1;υC=O1663.10cm-1;苯环骨架振动频率 υC=C1610.89cm-1,1168.97cm-1,1014.70cm-1。
槲皮素锑配合物主要官能团红外吸收峰分别是:羟基 υ-OH3385.65cm-1;υC=O1651.57cm-1;苯环骨架振动频率 υC=C1595.53cm-1,1166.63cm-1,1010.04cm-1。

图4 槲皮素的红外光谱Fig.4 The IR spectrum of quercetin
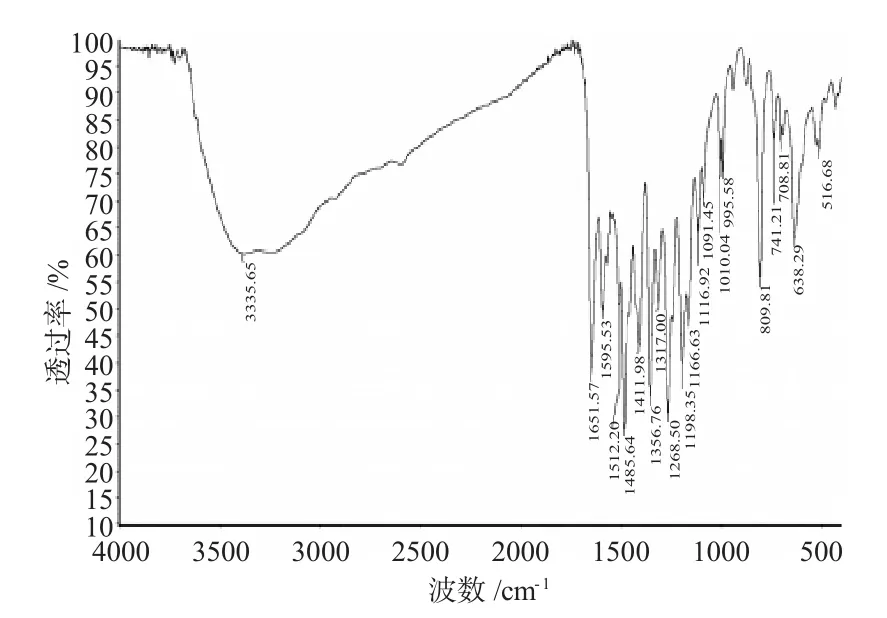
图5 槲皮素锑的红外光谱Fig.5 The IR spectrum of quercetin-Sb
通过上图数据比较可以发现:
(1)槲皮素的υ-OH3408.74cm-1,在配合物中移动到3385.65cm-1处,峰变得较宽,说明在形成配合物时的碱性条件下,酚羟基解离为离子所致。
(2)槲皮素的 υ(C=O)出现在 1663.10cm-1,当形成配合物后该振动频率是1651.57cm-1,羰基的吸收峰红移了12cm-1,这说明配合物在羰基处形成了配位键[10]。
(3)槲皮素中苯环的特征吸收峰分别是:1610.89cm-1、1168.97cm-1、1104.70cm-1。在配合物中苯环的特征吸收峰分别是:1595.53cm-1、1166.63cm-1、1010.04cm-1。数值基本上没有发生变化,这说明形成配合物后,对苯环的结构并没有破坏。
(4)υ(Sb-O)伸缩振动峰在 638.29cm-1的出现,说明了金属配位键的形成[10],而槲皮素没有此峰。
3 结论
槲皮素与三氯化锑在甲醇溶液中,可以生成槲皮素锑配合物。在pH=8.6,室温(25℃)条件下反应2h时收率最高。通过紫外光谱和红外光谱对槲皮素锑进行了表征。槲皮素既是天然的自由基清除剂,又是良好的金属离子螯合剂,且在常温下即可生成槲皮素锑,这提示人们:在日常生活中,多食用富含槲皮素的食物(如葡萄、苹果和洋葱等),一方面可以有效地清除体内多余的自由基,另一方面还可以促进体内重金属离子的排出,这还表明了开发此类保健食品具有重要意义。
参考文献:
[1]LEE J,MITCHELL AE.Pharmacokinetics of Quercetin Absorption from Applesand Onions in Healthy Humans[J].JAgric Food Chem.,2012,60(15):3874~3881.
[2]LEE J,MITCHELL AE.Quercetin and Isorhamnetin Glycosides in Onion(Allium cepa L.):Varietal Comparison,Physical Distribution,Coproduct Evaluation,and Long-Term Storage Stability[J].JAgric Food Chem.,2011,59(3):857~863.
[3]SULTANA B,ANWAR F.Flavones(kaempeferol,quercetin,myricetin)contents of selected fruits,vegetables and medicinal plants[J].Food Chem.,2008,108:879~884.
[4]SHAHIDIF,MCDONALD J,CHANDRASEKARA A,et al.Phytochemicals of foods,beverages and fruit vinegars:Chemistry and health effects[J].Asia Pac JClin Nutr.,2008,17:380~382.
[5]BOOTSAW,HAENEN GR,BAST A.Health effects of quercetin:From antioxidant tonutraceutical[J].Eur JPharmacol.,2008,585:325~337.
[6]DEHGHAN G,KHOSHKAM Z.Tin(II)-quercetin complex:Synthesis,spectral characterisation and antioxidant activity[J].Food Chem.,2012,131(2):422~426.
[7]SPAGNUOLO C,RUSSOM,BILOTTO S,et al.Dietary polyphenols in cancer prevention:the example of the flavonoid quercetin in leukemia[J].Ann N Y Acad Sci.,2012,1259(1):95~103.
[8]CHOISJ,TAIBH,CUONG NM,et al.Antioxidative and antiinflammatory effect of quercetin and its glycosides isolated from mampat(Cratoxylum formosum)[J].Food Science and Biotech -nology,2012,21(2):587~595.
[9]GANESAN S,FARIS AN,COMSTOCK AT,et al.Quercetin inhibits rhinovirus replication in vitro and in vivo[J].iral Research,2012,94(3):258~271.
[10]KHOO K,WHITE CR,POZZO ML,et al.Dietaryfl avonoid quercetinstimulatesvasorelaxation inaortic vessels[J].FreeRadic Biol Med.,2010,49:339~347.
[11]DOLATABADI JE.Molecular aspects on the interaction of quercetinand itsmetalcomplexeswith DNA[J].Int JBiolMacromol.2011,48(2):227~233.
[12]何孟常,万红艳.环境中锑的分布、存在形态及毒性和生物有效性[J].化学进展,2004,16(1):131~135.
[13]GORDON MH.Significance of Dietary Antioxidants for Health[J].Int JMol Sci.,2012,13:173~179.
Preparation of Quercetin Antimony
ZHENG Sai-fei1,QUWen-tao2 and ZHAIGuang-yu1,2(1.College of Nursing,Zhengzhou University,Zhengzhou 450052,China;2.College of Pharmacy,Zhengzhou University,Zhengzhou 450001,China)
A quercetin antimony complex was synthesized from the raw material quercetin and antimony trichloride,and the optimal reaction conditions for synthesizing quercetin antimony were investigated.The effects of temperature,pH value,and reaction time on the yield of quercetin antimony were studied,and the prepared quercetin antimony was characterized by UV and IR spectroscopy.The results showed that the highest yield which was 62%was obtained under the conditions as follows:the quercetin and antimony trichloride was stirred for 2h in methanol solution which pH=8.6 at room temperature.
Quercetin;quercetin antimony;complex;synthesis
TQ 710.6
A
1001-0017(2013)01-0047-03
2012-08-22 *基金项目:郑州大学大学生创新创业训练计划项目(编号:2011CXSY164)
郑赛飞(1990-),女,河南淅川人,本科生,研究方向:药物化学。
*通讯联系人:翟广玉,男,教授,硕士生导师。
