硫酸盐熔融反应法从钛铁矿中提取钛的研究*
2013-04-07陈科云张德拉张永明徐树英
陈科云,张德拉,2,张永明,2,徐树英,2,3
(1.海南大学材料与化工学院,海南海口570228;2.海南大学,海南省石油化工产品检测技术重点实验室;3.天津大学化工学院)
硫酸盐熔融反应法从钛铁矿中提取钛的研究*
陈科云1,张德拉1,2,张永明1,2,徐树英1,2,3
(1.海南大学材料与化工学院,海南海口570228;2.海南大学,海南省石油化工产品检测技术重点实验室;3.天津大学化工学院)
摘要:以海南万宁的钛铁矿和硫酸铵为主要原料,通过熔融反应法使钛铁矿中的钛转化为易溶于稀酸的硫酸氧钛,用稀硫酸浸取,达到提高钛浸取率的目的。考察了硫酸铵加入量、焦硫酸钾加入量、反应温度、稀硫酸浸取浓度对钛浸取率的影响。实验结果表明:硫酸铵和焦硫酸钾的加入量、反应温度对钛浸取率的影响较大。提高钛浸取率的最佳条件为:m(钛铁矿)∶m(硫酸铵)∶m(焦硫酸钾)=1∶6∶0.5,反应温度为450℃,保温时间为30 min,稀硫酸浸取浓度为2.32 mol/L,在此条件下钛的浸取率达到96.82%。
关键词:钛铁矿;二氧化钛;硫酸铵;浸取率
中国是世界上钛资源储量最丰富的国家之一。目前国内外对钛的提取做了大量研究。杨轩等[1]以NaOH盐熔反应分解高钛渣;王思佳等[2]以(NH4)2SO4熔融法分解高钛渣;王强等[3]以熔盐法处理富钛渣;Liu Yumin等[4]、Zhang Yongjie等[5]以NaOH亚熔盐分解高钛渣;熊雪良等[6]在预氧化条件下以质量分数为20%的盐酸分解钛铁矿,但这些方法均存在不同程度的环境污染问题。本研究是硫酸盐与钛铁矿加热熔融反应法生产金红石型钛白粉新工艺中的第一道工序。
1 材料与设备
1.1实验材料
主要原料:海南万宁矿区钛铁矿,钛铁矿的化学分析结果为:w(TiO2)=49.33%,w(Fe2O3)=10.63%, w(FeO)=35.76%,w(MgO)=0.20%,w(CaO)=0.79%,w(Al2O3)=1.05%,w(SiO2)=0.7%,w(MnO)=1.514%,w(其他)=0.026%。
试剂:硫酸铵、焦硫酸钾、浓硫酸、铁屑,均为分析纯。
1.2实验设备仪器
GZX-9070MBE数显鼓风干燥箱;LJM5-LJM50L立式搅拌磨;GM-0.50真空抽滤机;SYP1023马弗炉;DF-101S集热式恒温加热磁力搅拌器。
2 实验方法及其原理
2.1实验方法
将钛铁矿用立式搅拌磨研磨至51~63 μm;取10 g钛铁矿与(NH4)2SO4和K2S2O7按实验设定的比例混合均匀,装入坩埚中;在马弗炉中加热至设定的温度进行反应,保温30 min[7],得到多孔状固体;冷却后将多孔状固体研碎装入样品袋进行编号;研碎的固体加入三口烧瓶内,按计算的液固比加入稀硫酸混合均匀,在设定温度下恒温搅拌、浸取,加铁屑还原;过滤得到滤液和残渣;对浸出的钛液进行分析测量。
加热熔融过程中,K2S2O7约在325℃开始熔融,与钛铁矿中的相应物质发生反应,并分解释放出SO3[8];(NH4)2SO4在250℃左右开始分解为氨气和硫酸氢铵[7],然后硫酸氢铵与钛铁矿中的金属氧化物反应[2]。同时,用导管将氨气和三氧化硫气体从马弗炉内导出,并通入相应的吸收液中,避免氨气、三氧化硫气体污染大气。
2.2实验反应原理
钛铁矿、硫酸铵、焦硫酸钾在煅烧条件下的主要反应方程式如下:
硫酸铵反应方程式:
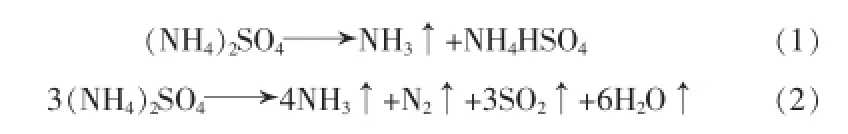
混合物中金属氧化物反应方程式:
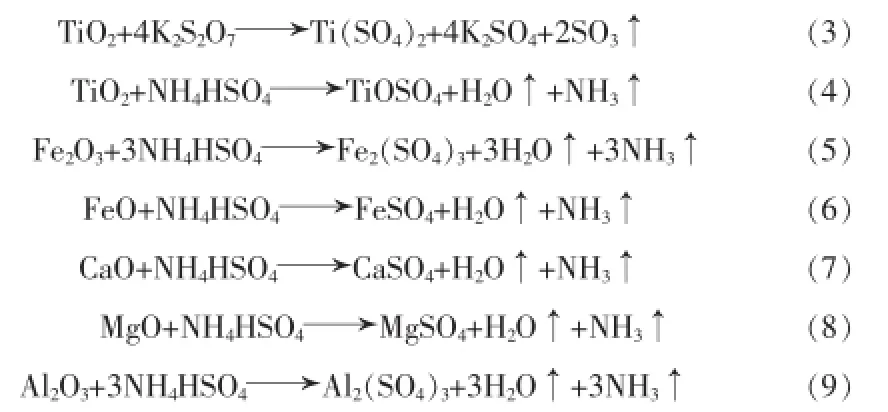
K2S2O7的熔点约为325℃,根据物理化学原理,低熔点物质的存在可使反应体系中存在更多的液相,促进原料更充分地接触,反应更加完全;另外,从化学反应理论上看,(NH4)2SO4和K2S2O7均可以发生类似的反应,达到溶出钛的目的,但考虑到K2S2O7的单位价格远高于(NH4)2SO4,且K2S2O7与钛铁矿的反应产物为K2SO4,其在水中的溶解度明显低于(NH4)2SO4在水中的溶解度,不便于浸取,故选用(NH4)2SO4和K2S2O7二者的混合物,并以(NH4)2SO4为主要反应物,K2S2O7为辅助反应物。
2.3分析测试
分析浸取钛液中二氧化钛的含量。总Ti的测试采用Al片还原法,将Ti4+还原成Ti3+,反应后钛液中Ti3+直接用高铁盐氧化还原滴定法测定。钛铁矿经反应后加稀硫酸浸取,其中绝大部分钛转入溶液中成为可溶性钛盐。溶液中的可溶性钛盐总量(以TiO2计)占所投钛铁矿中所含钛总量(以TiO2计)的分数,叫做浸取率[8]。
溶液中总钛含量的测定公式为:
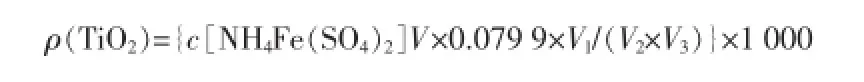
式中:ρ(TiO2)为二氧化钛的质量浓度,g/L;V为消耗硫酸高铁铵溶液的体积,mL;V1为容量瓶体积,mL;V2为取稀释后试液的体积,mL;V3为取原始浓溶液的体积,mL;c[NH4Fe(SO4)2]为硫酸高铁铵溶液的浓度,mol/L;0.079 9为二氧化钛的摩尔质量,kg/mol。
3 结果与讨论
3.1K2S2O7加入量对钛浸取率的影响
将钛铁矿、(NH4)2SO4和K2S2O7分别以质量比为1∶6∶2、1∶6∶1、1∶6∶0.5、1∶6∶0混合均匀,在马弗炉中升温至350℃,并保温30 min,加入3.72 mol/L稀硫酸在70℃下恒温搅拌浸取,根据实验结果选择最优的K2S2O7加入量。实验结果为:m(钛铁矿)∶m[(NH4)2SO4]∶m(K2S2O7)=1∶6∶0时,钛浸出率为80.79%;m(钛铁矿)∶m[(NH4)2SO4]∶m(K2S2O7)=1∶6∶0.5时,钛浸出率为89.26%;m(钛铁矿)∶m[(NH4)2SO4]∶m(K2S2O7)=1∶6∶1时,钛浸出率为90.92%;m(钛铁矿)∶m[(NH4)2SO4]∶m(K2S2O7)=1∶6∶2时,钛浸出率为93.60%。可以看出,钛浸取率随K2S2O7加入量的增加迅速升高并逐渐趋于缓和。这是因为低熔点、低黏度组分的含量达到一定量后,体系的熔化温度和黏度基本趋于恒定,其加入量的增加对体系的熔化温度和黏度影响不大,进而对熔融反应速率影响不大。从节省原料和资金的角度考虑,选择m(钛铁矿)∶m[(NH4)2SO4]∶m(K2S2O7)为1∶6∶0.5。
3.2(NH4)2SO4加入量对钛浸取率的影响
根据钛铁矿中各种氧化物的含量和式(1)及式(4)~式(9),可计算出硫酸铵过量系数为0时,钛铁矿与硫酸铵的质量比为1∶2.0左右,但低熔点NH4HSO4的挥发和分解容易造成反应进行得不完全,故应提高(NH4)2SO4的加入量。将钛铁矿与(NH4)2SO4和K2S2O7分别以1∶4∶0.5、1∶5∶0.5、1∶6∶0.5、1∶8∶0.5的质量比混合均匀,在马弗炉中升温至350℃,并保温30 min,加入3.72 mol/L稀硫酸在70℃下恒温搅拌浸取,根据实验结果选择最优的(NH4)2SO4加入量。实验结果为:m(钛铁矿)∶m[(NH4)2SO4]∶m(K2S2O7)=1∶4∶0.5时,钛浸出率为73.16%;m(钛铁矿)∶m[(NH4)2SO4]∶m(K2S2O7)=1∶5∶0.5时,钛浸出率为75.82%;m(钛铁矿)∶m[(NH4)2SO4]∶m(K2S2O7)= 1∶6∶0.5时,钛浸出率为89.26%;m(钛铁矿)∶m[(NH4)2SO4]∶m(K2S2O7)=1∶8∶0.5时,钛浸出率为92.31%。可以看出,随着(NH4)2SO4加入量的增大,钛的浸取率逐渐升高并趋于缓和,m(钛铁矿)∶m[(NH4)2SO4]∶m(K2S2O7)为1∶6∶0.5时,钛浸取率基本达到了实验预设的目标。为节省原料,故选择钛铁矿与(NH4)2SO4和K2S2O7的质量比为1∶6∶0.5。
3.3反应温度对钛浸取率的影响
将钛铁矿与(NH4)2SO4和K2S2O7以1∶6∶0.5的质量比混合均匀,分别加热到350、400、450、500℃,保温30 min,加入3.72 mol/L稀硫酸在70℃下恒温搅拌浸取,根据实验结果选择最优的实验温度。实验结果为:反应温度为350℃时,钛浸取率为90.55%;反应温度为400℃时,钛浸取率为93.86%;反应温度为450℃时,钛浸取率为95.44%;反应温度为500℃时,钛浸取率为42.39%。可知,温度从350℃升高到500℃时,钛的浸取率先逐渐提高后迅速降低。根据Vant Hoff经验理论和Arrhenius公式可以对此作出解释:当温度升高时,分子运动速度加快,反应体系的黏度降低,原料接触面积变大,进而使反应速率明显加快[9],但温度过高时,将破坏原有的反应组分。当温度从350℃升高到450℃时,浸取率逐渐升高并达到最大值;当温度达到500℃时,浸取率迅速变小,说明该温度下组分发生了改变。从动力学上讲,反应体系中存在非水溶性、高熔点、高黏度物质(如硫酸钙和二氧化硅),对原料的熔融有不利影响,一定程度上对钛的熔解产生障碍,从而使反应速率降低;从热力学上看,TiOSO4对热不稳定,温度过高时水溶性物质TiOSO4开始分解为TiO2,使钛的浸取率难以提高。因此,从实验数据分析,可以确定450℃为该条件下的最佳反应温度。
3.4稀酸浸取浓度对钛浸取率的影响
将钛铁矿与(NH4)2SO4和K2S2O7以1∶6∶0.5的质量比混合均匀,在马弗炉内加热到450℃,保温30min。冷却后得到青灰色的多孔状固体,将块状固体进行研碎后按比例加稀硫酸混合,分别加入浓度为1.09、2.32、3.72 mol/L的稀硫酸,在70℃下恒温搅拌浸取,根据实验结果选择最佳的稀酸浸取浓度。实验结果为:硫酸浓度为1.09 mol/L时,钛的浸取率为92.08%;硫酸浓度为2.32 mol/L时,钛的浸取率为96.82%;硫酸浓度为3.72 mol/L时,钛的浸取率为97.19%。可以看出,硫酸浓度从1.09 mol/L升高到3.72 mol/L时,钛的浸取率逐渐提高并趋于稳定;硫酸浓度为2.32 mol/L时,钛的浸取率达到96%的实验目标。为节省原料及对稀酸进行综合利用,故在此条件下,选择最佳的稀硫酸浸取浓度为2.32 mol/L。
4 结论
1)硫酸盐熔融反应法作为生产金红石型钛白粉新工艺中的第一道工序,对降低钛铁矿的煅烧活化温度,提高钛的浸取率是可行的。2)随(NH4)2SO4和K2S2O7加入量的增加,钛浸取率增加然后趋于缓和。虽然K2S2O7的加入对钛浸取率的影响没有(NH4)2SO4明显,但有低熔点的K2S2O7存在,可使反应体系中存在更多的液相,促进原料更充分地接触,反应更加完全。3)(NH4)2SO4与K2S2O7的加入量和反应温度对钛浸取率的影响较大,选择最佳的工艺条件为:钛铁矿、(NH4)2SO4和K2S2O7的质量比为1∶6∶0.5,反应温度为450℃,保温时间为30 min,稀硫酸浸取浓度为2.32 mol/L,在此条件下钛的浸取率为96.82%。
参考文献:
[1]杨轩,薛天艳,王丽娜,等.碱法钛白粉生产工艺中硫酸钛溶液的制备和水解[J].湿法冶金,2010,29(4):277-281.
[2]王思佳,张悦,薛向欣,等.硫酸铵熔融反应法从含钛高炉渣中回收钛[J].化工学报,2012,63(3):991-995.
[3]王强,张庆武.熔盐法处理富钛渣制备金红石型TiO2[J].应用化工,2008,37(2):140-141.
[4]Liu Yumin,Qi Tao,Zhang Yi.A novel way to synthesize potassium titanates[J].Mater.,Lett.,2006,60(2):203-205.
[5]Zhang Yongjie,Qi Tao,Zhang Yi.A novel preparation of titanium dioxide from titanium slag[J].Hydrometallurgy,2009,96(1/2):52-56.
[6]熊雪良,欧阳红勇,杨智,等.预氧化对钛铁矿结构及其产物金红石的影响[J].钛工业进展,2010,27(5):40-43.
[7]刘科伟,陈天朗.硫酸铵的热分解[J].化学研究与应用,2002,14(6):737-738.
[8]陈朝华.钛白粉生产技术问答[M].北京:化学工业出版社,1998:255-256.
[9]张悦,杨合,王丽,等.用含钛高炉渣制备肥料[J].东北大学学报:自然科学版,2010,31(8):1161-1164,1169.
联系方式:xushuying1980@163.com
中图分类号:TQ134.11
文献标识码:A
文章编号:1006-4990(2013)10-0011-03
收稿日期:2013-04-20
作者简介:陈科云(1989—),男,本科,从事无机材料研究。
通讯作者:徐树英
*基金项目:海南省自然科学基金项目(512109);海南大学2012年本科生创新科研课题(HDCX2012025)。
Research on extracting titanium from ilmenite by sulfate melting reaction
Chen Keyun1,Zhang Dela1,2,Zhang Yongming1,2,Xu Shuying1,2,3
(1.School of Materials and Chemical Engineering,Hainan University,Haikou 570228,China;
2.Key Laboratory of Petrochemical Product Detecting Techniques of Hainan Province,Hainan University;
3.School of Chemical Engineering,Tianjin University)
Abstract:For the purpose of increasing the titanium leaching rate,the titanium in ilmenite was firstly transformed into titanyl sulfate,which was easy to dissolve in dilute acid,by the sulfate melting reaction method,with the ilmenite from Wanning,Hainan Province and(NH4)2SO4as the main raw materials,and then leaching with dilute sulfuric acid.Effects of the added amounts of(NH4)2SO4and K2S2O7,reaction temperature,and leaching concentration of dilute sulfuric acid on the titanium leaching rate were investigated.Experimental results showed that the added amounts of(NH4)2SO4and K2S2O7,and the reaction temperature had a greater impact on the titanium leaching rate.The optimum conditions of enhancing the titanium leaching rate were as follows:the mass ratio of ilmenite,(NH4)2SO4,and K2S2O7was 1∶6∶0.5,the reaction temperature was 450℃,the holding time was 30 min,and the concentration of dilute sulfuric acid was 2.32 mol/L.The leaching rate of titanium reached 96.82%under the above optimum conditions.
Key words:ilmenite;titanium dioxide;ammonium sulfate;leaching rate
