磷脂酰聚乙二醇单甲醚的合成及其自组装纳米胶束的研究
2012-12-31刘天军
武 莉 陈 静 刘天军
(中国医学科学院北京协和医学院生物医学工程研究所,天津生物医学材料重点实验室,天津 300192)
引言
磷脂是细胞膜的构筑材料,具有很好的生物相容性和成膜性,可以形成囊泡和胶束,在药用辅料方面有着广泛的应用。然而,磷脂分子量较小,形成的囊泡和胶束稳定性不够,作为长循环和缓释材料的应用方面受到很大的限制。目前的解决办法是在其中加入含有长循环的组分:聚乙二醇、多聚糖、环糊精等成为长循环磷脂,以提高磷脂胶束或胶囊的稳定性[1]。从化学结构相似相溶的原理出发,外加结构与磷脂最为相似的组分应该具备很好的互溶性,从理论上讲对其结构改善也应最好。因而含有磷脂组分的高分子或大分子体系的研究受到人们的广泛重视,将磷脂接枝于高分子骨架或侧链上形成高分子化磷脂(mPEG-磷脂)便是在该背景下的研究。聚乙二醇(PEG)是一种中性、无毒、具有生物相容性的亲水性聚合物,在药物制剂方面有着广泛的应用[1],而磷脂是生物膜的组成成分,具有良好的生物降解性和生物兼容性[2],将聚乙二醇(PEG)和磷脂相结合制备两亲性聚合物可以兼顾其良好的生物相容性和长循环的目的。实践证明PEG衍生化磷脂作为药用辅料具有较好的应用价值,可以有效提高药物的长循环特性[3-6],特别是用于抗肿瘤药物载体,可以延长肿瘤组织药物作用时间,有效抑制肿瘤生长,增强药效[7-8]。
目前主要以聚乙二醇磷脂酰乙醇胺(PEG-PE)应用较多[9],是在体内可降解并经美国食品药品管理局(FDA)批准的可用于人体的药物载体材料,PEG-PE纳米胶束可有效携载它莫西芬、紫杉醇和地喹氯铵等多种水溶性差的抗肿瘤药物,且显示了较高的抗肿瘤效果[10],但多为进口,价格昂贵,在一定程度上制约了其广泛的应用。因此,开发新型的PEG衍生化磷脂至关重要。
本研究制备了新型PEG衍生化磷脂——磷脂酰聚乙二醇单甲醚(mPEG-磷脂),通过自组装形成纳米胶束后进行透析分离纯化,并进行了MS、1HNMR等结构表征。通过溶剂挥发法制备mPEG-磷脂胶束,并通过荧光探针法、扫描电子显微镜、透射电子显微镜和粒度及电位分析仪等对其性能进行了研究。
1 材料和方法
1.1 材料
直接进样质谱仪(ESI-MS)(Trace DSQ,热电菲尼根公司,美国)、核磁共振谱仪(300 MHz)(Mercury,Varian公司,美国)、扫描电镜(JSM-6700F,JEOL公司,日本)、透射电镜(JEM-100CXⅡ,JEOL公司,日本)、粒度仪(Zetasizer Nano ZS,Malvern公司,英国)、荧光分光光度计(F-4500,HITACHI公司,日本)、载氯化钯的树脂(本室合成)、二异丙基乙胺(DIPEA)、化学纯,河南四方化工有限公司、三氯氧磷(分析纯,天津大学科威公司)、聚乙二醇单甲醚(mPEG)(分析纯,广州市靖诚贸易有限公司)、其它试剂均为分析纯。
1.2 方法
1.2.1 1,2-十六酰基(十四酰基、十二酰基)甘油二酯(1、2、3)的合成
图1为1,2-十六酰基(十四酰基、十二酰基)甘油二酯的合成路线。载氯化钯的树脂加入到反应斧中用氢气还原,然后加入3-苄基-1,2-十六酰基(十四酰基、十二酰基)甘油二酯100 g、二氯甲烷溶解,密封。从反应釜的出料口通入氢气,放气到2.02×105Pa,重复3次,关闭放气阀,再通入H2,350 r/min搅拌,待压力降到10×105Pa后,再补加到15×105Pa,待压力不再降低时即可。反应完毕,放出未反应的H2,打开反应斧,过滤,滤液旋干,得粗品。用三氯甲烷/石油醚重结晶,得目标产物。

图1 1,2-十六酰基(十四酰基、十二酰基)甘油二酯的合成路线Fig.1 Synthetic route of 1,2-palmitoyl-diacylglycerol,1,2-tetradecanoyl-diacylglycerol or 1,2-Lauroyldiacylglycerol
1.2.2 磷脂酰聚乙二醇单甲醚(4-15)的合成
图2为磷脂酰聚乙二醇单甲醚的合成路线。氮气保护下,将甘油二酯的干燥四氢呋喃溶液于0℃滴加到DIPEA和三氯氧磷的干燥四氢呋喃溶液中,继续搅拌2 h,0℃下继续滴加聚乙二醇单甲醚和吡啶的干燥四氢呋喃溶液,室温反应6 h。过滤,向滤液中加入与三氯氧磷等量的水,搅拌1~2 h,蒸干溶剂,得固体,乙醚沉降得磷脂酰聚乙二醇单甲醚粗品。磷脂酰聚乙二醇单甲醚粗品在水中搅拌成胶束后透析,旋干水,即得到白色产物。
1.2.3 磷脂酰聚乙二醇单甲醚胶束的制备
磷脂酰聚乙二醇单甲醚溶于二氯甲烷,在1 000r/min搅拌下滴入蒸馏水中,滴加完毕后再搅拌6 h,常温下挥去二氯甲烷,离心,上清液过微孔滤膜,即得磷脂酰聚乙二醇单甲醚胶束。
1.2.4 临界胶束浓度(CMC)的测定
采用芘探针荧光法测定两亲性磷脂酰聚乙二醇单甲醚的临界胶束浓度。准确称取一定量的磷脂酰聚乙二醇单甲醚,配制浓度为5×10-4mol/L的水溶液。并稀释成不同浓度的磷脂酰聚乙二醇单甲醚溶液;以水、乙腈、丙酮、甲醇及正丁醇为溶剂配制终浓度为2×10-6mol/L的芘溶液。分别向10 mL容量瓶中加入0.1 mL芘的丙酮溶液,挥干丙酮。分别取10 mL配好的磷脂酰聚乙二醇单甲醚的水溶液,加到容量瓶中使芘的终浓度达到2×10-6mol/L,振荡使溶液均匀,为了平衡芘与胶束,混合液在65℃水浴中加热3 h,再室温放置1天。激发波长为335nm测定芘探针在不同极性溶剂中的荧光光谱,测定不同浓度的待测液在373和384 nm两峰的荧光强度,以浓度为X轴,I384/I373为Y轴作图,由曲线的突变点确定磷脂酰聚乙二醇单甲醚的CMC值。

图2 磷脂酰聚乙二醇单甲醚的合成路线Fig.2 Synthetic route of Diacylglyceryl-Phosphatidyl-O-Methoxy(Polyethylene glycol)
1.2.5 胶束粒径、粒径分布及Zeta电位的测定
磷脂酰聚乙二醇单甲醚溶解于二氯甲烷中,在1 000 r/min搅拌下滴入蒸馏水中,滴加完毕后再搅拌6 h,常温下挥去二氯甲烷,离心,上清液过微孔滤膜,采用Zeta PALS-亚微米粒度及电位分析仪测定胶束的粒径、粒径分布以及Zeta电位。普鲁兰多糖、二糖及单糖的水溶液浓度以糖的羟基数与PEG的氧个数的mol比分别为:1∶4,1∶2,1∶1,2∶1,4∶1。
同法测定不同浓度氯化钠、葡萄糖水溶液中的胶束粒径及离子浓度对胶束粒径的影响。
同法测定不同浓度普鲁兰多糖、二糖及单糖中的胶束粒径及离子浓度对胶束粒径的影响。
1.2.6 胶束的形貌表征
用扫描电子显微镜(SEM)和透射电子显微镜(TEM)观察胶束的形貌。
2 结果与讨论
2.1 3种1,2-十六酰基(十四酰基、十二酰基)甘油二酯的合成和结构分析
研究中合成了3种磷脂分子,包括:产物 A :1,2-十六酰基甘油二酯(1)、产物 B :1,2-十四酰基甘油二酯(2)和产物C:1,2-十二酰基甘油二酯(3)。
产物A的产率为 7 0%,熔点:67~68℃。1HNMR(300MHz,CDCl3):σ 0.88(t,6 H),1.20~1.25(br.s,48 H),1.57~1.62(m,4 H),2.02~2.06(t,1 H),2.30~2.37(m,4 H),3.71~3.75(d,2 H),4.20~4.34(m,2 H),5.06~5.10(br.s,1 H)。ESI-MS:m/z 1159为2M+Na峰。产物B的产率为74.5%,熔点:60~61℃。1H-NMR(300MHz,CDCl3):σ0.87(t,6 H),1.20~1.25(br.s,40 H),1.56~1.63(m,4 H),2.02~2.06(t,1 H),2.24~2.34(m,4 H),3.57~3.59(d,2 H),4.15~4.37(m,2 H),5.22~5.25(br.s,1 H)。ESI-MS:m/z 1047为2M+Na峰。产物C的产率为77.8%,熔点:52~53℃。1H-NMR(300MHz,CDCl3):σ 0.88(t,6 H),1.25(br.s,32 H),1.56~1.632m,4 H),2.02~2.06(t,1 H),2.25~2.34(m,4 H),3.58~3.59(d,2 H),4.15~4.37(m,2 H),5.22~5.26(br.s,1 H)。ESI-MS:m/z 935为2M+Na峰。
2.2 磷脂酰聚乙二醇单甲醚(4-15)的合成和结构分析
利用三氯氧磷直接将甘油二酯与聚乙二醇单甲醚直接连接起来,合成PEG衍生化的磷脂。这比传统的用PEG修饰磷脂[11]的方法简单得多,传统的方法是先利用甘油二酯合成磷脂酰乙醇胺(脑磷脂),再利用一个二元酸酐通过酰胺键和酯键把磷脂与聚乙二醇单甲醚连接起来。这两种化合物在结构上相差不多,只是酰胺键和酯键的差别,所合成的磷脂酰聚乙二醇单甲醚中无酰胺键存在,只含有酯键,与磷脂更接近,都含有疏水烷基链和亲水PEG链,自组装成胶束的性能也相似。甘油二酯、聚乙二醇单甲醚和水依次与三氯氧磷上3个氯发生亲核取代反应。醇羟基与三氯氧磷发生取代的能力比较弱,需在碱性条件下反应,由于三氯氧磷上有3个位点可以反应,为了尽可能的控制甘油二酯只与一个位点进行反应,故选择了空间位阻比较大的二异丙基乙胺,与第2个位点反应的时候可以用三乙胺或吡啶[12-13]做催化剂。在反应过程中这些碱与生成的氯化氢结合生成盐酸盐,以沉淀的形式析出。由于在整个过程中磷酰化、PEG酯化与水解三步反应顺次连续进行,因而前两步反应结束后过滤除掉生成的盐,再行水解,可以获得纯净的目标产物。甘油二酯溶于乙醚,而PEG几乎不溶于乙醚,用乙醚沉降即可除去未反应的甘油二酯,但不能分开PEG与PEG-磷脂。PEG-磷脂与PEG在各种溶剂中的溶解性很相近,尝试了多种溶剂,都未能把二者利用溶解性的差异而分开。PEG-磷脂同时含有亲水链段和疏水链段,其自组装性能与单纯PEG不同[14-15],故利用PEG-磷脂的自组装性能,让其在水中自组装成胶束后,用透析法除去未反应的PEG。

表1 磷脂酰聚乙二醇单甲醚(4-15)的产率和结构分析Tab.1 The yields and structural analysis of phosphatidyl polyethylene glycol monomethyl ether(4-15)
2.3 PEG-磷脂胶束的临界胶束浓度(CMC)、粒径及分布
芘单体荧光振动精细结构具有明显的溶剂依赖性,因此常被用作荧光探针来研究聚合物在溶液中的聚集状态[16]。芘是强憎水性探针,在水中的溶解度为2×10-6~3×10-6mol/L。在胶束和其它大分子体系中,芘会更好地溶解在聚集体的憎水区,因此芘被广泛用于聚合物CMC的研究。利用芘探针在不同极性环境中I384/I373值的突变确定CMC值。图3是磷脂酰聚乙二醇单甲醚浓度的对数与芘的I384/I373值的关系图。
从图中看到初始时,随着各磷脂酰聚乙二醇单甲醚浓度的增大,两峰的比值变化很平缓,但当达到某一浓度时,两峰比值有突变现象,再继续增大磷脂酰聚乙二醇单甲醚的浓度,这一比值基本保持不变的趋势。由于在磷脂酰聚乙二醇单甲醚浓度很低时,没有胶束的形成,环境的极性没有明显变化,所以I384/I373值的变化不大。当磷脂酰聚乙二醇单甲醚浓度达到一定数值时,开始有胶束形成,芘探针进入胶束的疏水区,其环境的极性急剧减小,使I384/I373值发生突变。当磷脂酰聚乙二醇单甲醚浓度达到这一值以后,环境极性基本不变化,故I384/I373值基本趋于平缓。经测定得到,各磷脂酰聚乙二醇单甲醚的CMC值见表2。聚合物的CMC值与疏水链段的性质和长度、亲水链段的长度、聚合物分子量等多种因素有关。固定疏水链段时,随着亲水链段PEG的分子量地增加,聚合物的CMC值稍微增大;而固定亲水链段PEG的分子量时,随着疏水链段地越长,聚合物的CMC值稍微减小。
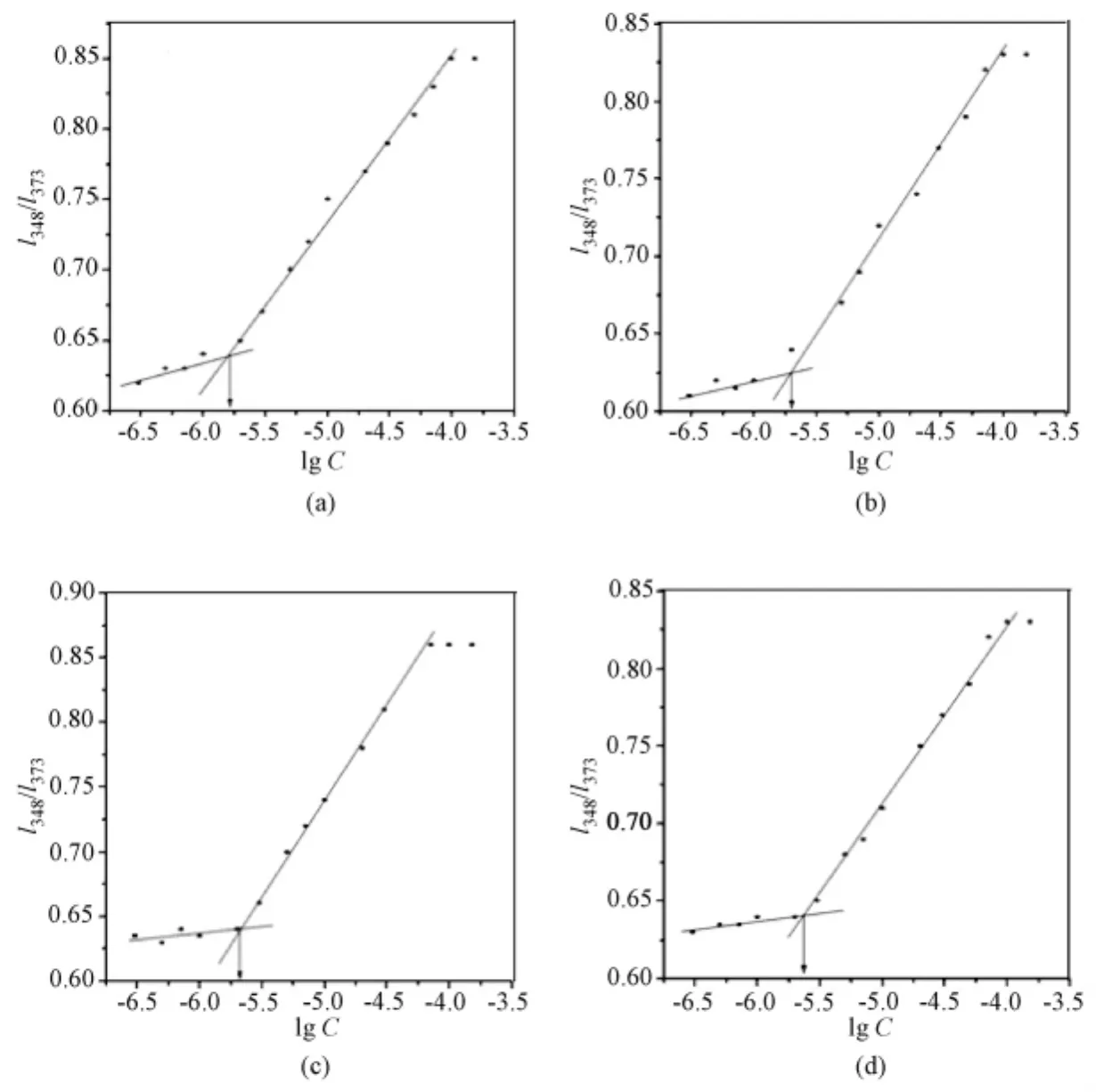
图3 1,2-十六酰基甘油二酯-3-磷脂酰聚乙二醇单甲醚浓度对I384/I373比值的影响。(a)mPEG1-2C16;(b)mPEG2-2C16;(c)mPEG3-2C16;(d)mPEG5-2C16Fig.3 The relationship of fluorescence intensity of I384/I373and the concentration of 1,2-Dipalmitoyl-Glycero-3 Phosphatidyl-O-Methoxy(Polyethylene glycol).(a)mPEG1-2C16;(b)mPEG2-2C16;(c)mPEG3-2C16;(d)mPEG5-2C16
由图4和表2可知,磷脂酰聚乙二醇单甲醚胶束的粒径都集中在100~200 nm。对于同一亲水链段,随着疏水链段的长度改变,所得胶束的粒径并无明显的变化。同样,对于同一疏水链段,亲水链段长度的变化对胶束粒径的影响也不甚明显。
2.4 不同浓度氯化钠、葡萄糖对胶束粒径的影响
由于生理介质中含有NaCl以及不同的单糖、二糖和多糖,它们对于胶束的形态、粒径和稳定性会产生不同的影响,本文探讨了不同浓度氯化钠、葡萄糖二糖对PEG修饰磷脂的胶束粒径及其稳定性的影响。
表3为mPEG1-2C16在不同浓度的氯化钠水溶液中形成胶束的粒径。从图5可知,胶束的粒径随着氯化钠浓度的增大而减小。原因主要有两个方面:一是氯化钠的盐效应有使疏水链段往一起聚集的倾向,因而使疏水链内核变得紧凑,粒径减小;二是小分子氯化钠分散在亲水链段的内部,由于离子效应使亲水外壳也变得紧凑,粒径也减小。

表2 磷脂酰聚乙二醇单甲醚的CMC、粒径及分布Tab.2 CMC and Diameter of Diacylglyceryl-Phosphatidyl-O-Methoxy(Polyethylene glycol)

图4 磷脂酰聚乙二醇单甲醚的粒径与烷基链长短和mPEG分子量的关系图Fig.4 Plots of the diameter vs the length of alkyl chian and the molecular weight of mPEG

表3 不同浓度的氯化钠水溶液中的胶束的粒径Tab.3 Micelle diameter in different concentration of NaCl water solution

图5 胶束的粒径与氯化钠的浓度的关系图Fig.5 Plots of the micelle diameter vsthe concentration of NaCl water solution
表4为mPEG1-2C16在不同浓度的葡萄糖水溶液中形成胶束的粒径。从图6可知,胶束的粒径随着葡萄糖浓度的增加而增大,这可以从两个方面来解释:一是葡萄糖结合于亲水链段之间,由于葡萄糖的分子较大水分子,使亲水外壳变的疏松;二是葡萄糖以氢键结合于胶束的亲水外壳上,随着附着在胶束表面上的葡萄糖的增加,粒径也相应地增大。这两者共同的影响都是使胶束的粒径增大。

表4 不同浓度的葡萄糖水溶液中的胶束的粒径Tab.4 Micelle diameter in different concentration of glucose water solution

图6 胶束的粒径与葡萄糖的浓度的关系图Fig.6 Plots of the micellediametervs the concentration of glucose water solution
2.5 不同浓度多糖、二糖及单糖中的胶束粒径及其对胶束粒径的影响
表5和图7表明,多糖对胶束的粒径影响较大,随着多糖浓度的增加,胶束的粒径明显增大,粒径从200 nm增大到500 nm左右,而在这个浓度范围内,二糖和单糖对胶束粒径的影响都不大,粒径均在200~300 nm。主要原因可能是多糖对胶束的影响为多糖以氢键与亲水链段PEG相结合,缠绕在胶束的外壳上,使粒径增大。基于该实验表明,在生理环境中因为糖、盐以及其它生物大分子的存在,长循环磷脂构成的胶束稳定性与结构会发生显著变化。该问题为缓释或长循环药物制剂的研究设计提供了一些有价值的启迪。
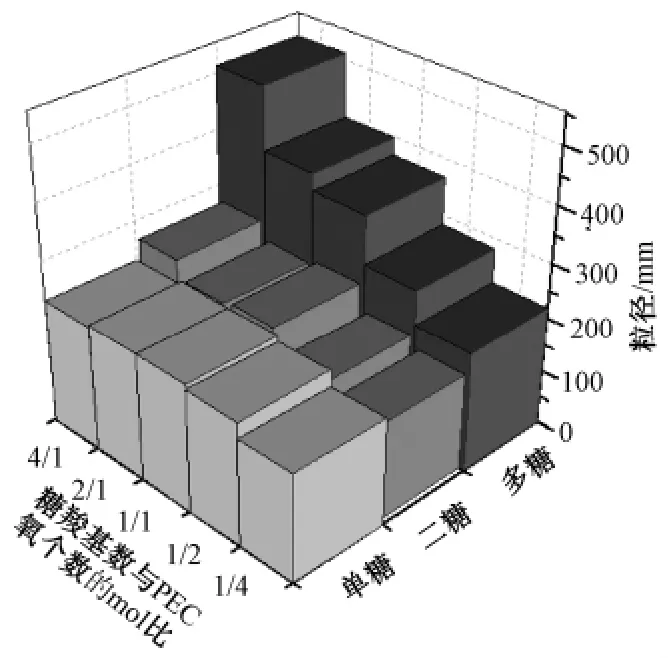
图7 粒径与糖种类和糖浓度的关系图Fig.7 Plots of the diameter vs the concentration of glucose water solution
2.6 胶束的电位
用Zeta PALS-亚微米粒度及电位分析仪测定胶束的电位,结果见表6,所合成的四种磷脂分子形成的胶束,其Zeta电位均约为-38 mV,这与磷脂酰聚乙二醇单甲醚的结构中含有磷羟基是相符的。

表5 不同浓度的葡萄糖水溶液中的胶束的粒径Tab.5 Micelle diameter in different concentration of glucose water solution
2.7 胶束的形貌表征
磷脂酰聚乙二醇单甲醚胶束在透射电子显微镜下观察其形貌,结果如图8(a)和图8(b)所示,从电镜照片可以看到磷脂酰聚乙二醇单甲醚胶束呈球形,平均粒径在200 nm左右,粒子比较均匀,还可以看到核-壳结构。磷脂酰聚乙二醇单甲醚胶束在扫描电子显微镜下观察其形貌,结果如图8(c)所示,从电镜照片可以看到水中磷脂酰聚乙二醇单甲醚胶束呈球形,胶束的平均粒径在100 nm左右,粒子较均匀。

表6 mPEG-磷脂的Zeta电位Tab.6 Zeta Potential of mPEG-phospholipids(a)mPEG1-2C16;(b)mPEG2-2C16;(c)mPEG3-2C16;(d)mPEG5-2C16
3 结论
本研究利用简单的原料,选择甘油二酯与聚乙二醇单甲醚通过三氯氧磷直接相连,合成了12种新的两亲性聚合物磷脂酰聚乙二醇单甲醚,并对各产物进行了MS、HNMR等结构表征。该类聚合物在水中易形成具有明显核-壳结构的球状胶束,粒径在100~200 nm;临界胶束浓度在10-6mol/L,与小分子的表面活性剂相比,CMC值较低,在水中的稳定性增强。同时固定疏水链段时,CMC值随着亲水链段PEG的分子量的增大而增大,而固定亲水链段PEG的分子量时,CMC值随着疏水链段的增长而减小,具有很好的构效关系。在离子效应和氢键效应对胶束的影响方面:随着氯化钠的浓度增加,胶束的粒径减小,随着多糖的浓度增加,胶束的粒径增大。综上,磷脂酰聚乙二醇单甲醚自组装纳米胶束结构稳定,是一种潜在的纳米药物载体。

图8 磷脂酰聚乙二醇单甲醚的TEM和SEM。(a)胶束TEM;(b)单个胶束TEM;(c)胶束 SEMFig.8 TEM and SEM of Diacylglyceryl-Phosphatidyl-O-Methoxy(Polyethylene glycol).(a)TEM of micelles;(b)TEM of a micelle;(c)SEM
[1]Mero A,Schiavon O,Pasut G,et al.A biodegradable polymeric carrier based on PEG for drug delivery[J].Journal of Bioactive and Compatible Polymers 2009,24(3),220-234.
[2]Reddy PD,Swarnalatha D.Recent advances in novel Drug delivery systems[J].Int J Pharm Tech Research,2010,2(3),2025-2027.
[3]Senior J,Delgado C,Fisher D,et al.Influence of surface hydrophilicity of liposomes on their interaction with plasma protein and clearance from the circulation:studies with poly(ethylene glycol)-coated vesicles[J].Biochim Biophys Acta,1991,1062:77-82.
[4]Allen TM,Hansen C,Martin F,et al.A.Liposomes containing synthetic lipid derivativesofpoly(ethylene glycol)show prolonged circulation half-lives in vivo[J].Biochim Biophys Acta,1991,1066:29-36.
[5]Santos ND,Allen C,Doppen AM,et al.Influence of poly(ethyleneglycol)graftingdensityand polymerlength on liposomes:Relating plasma circulation lifetimesto protein binding[J].Biochimi Biophys Acta(BBA)-Biomembranes,2007,1768(6):1367-1377.
[6]Lim SB,Rubinstein I,Önyüksel H.Freeze drying of peptide drugs self-associated with long-circulating,biocompatible and biodegradable sterically stabilized phospholipid nanomicelles[J].2008,356(1-2):345-350.
[7]Huang SK,Lee KD,Hong K,et al.Microscopic localization of sterically stabilized liposomes in colon carcinoma-bearing mice[J].Cancer Res,1992,52:5135-5143.
[8]Wu NZ,Da D,Rudoll TL,et al.Increased microvascular permeability contributes to preferential accumulation of Stealth liposomes in tumor tissue[J].Cancer Res,1993,53:3765-3770.
[9]Torchilin VP,Lukyanov AN,Gao ZG,et al.Polymeric micelles as targetable pharmaceutical carriers[M]//Carrier-Based Drug Delivery,ACS Symposium Series.Washington DC:ACS Publication,2004:120-129.
[10]Lukyanov AN,Gao ZG,Torchilin VP.Micelles from polyethylene glycol/phosph atidylethanol amine conjugates for tumor drug delivery[J].J Control Release,2003,91:97-102.
[11]Sears BD.Synthetic Phospholipid Compounds[P].United States Patent:4534899,1985.
[12]Lindberg J,Ekeroth J,Konradsson P.Efficient synthesis of phospholipids from glycidyl phosphates[J].J Org Chem,2002,67(1):194-199.
[13]Alcaraz ML,Peng L,Klotz P,et al.Synthesis and properties of photoactivatable phospholipid derivatives designed to probe the membrane-associate domains of proteins[J].J Org Chem,1996,61(1):192-201.
[14]Torchilin VP,Levchenko TS,Lukyanov AN,etal.p-Nitrophenylcarbonyl- PEG-PE-liposomes:fast and simple attachment of specific ligands,including monoclonal antibodies,to distal ends of PEG chains via p-nitrophenylcarbonyl groups[J].Biochim Biophys Acta,2001,1511:397-411.
[15]Lundberg BB,Mortimer BC,Redgrave TG.Submicron lipid emulsions containing amphipathic polyethylene glycol for use as drug-carriers with prolonged circulation time[J].Int J Pharm,1996,134:119-127.
[16]Kim IS,Kim SH.Evaluation of polymeric nanoparticles composed of cholic acid and methoxy-poly(ethylene glycol)[J].Int J Pharm,2001,226:23-29.
