电解金属锰制液Mn2+、Fe浸出行为的试验探索
2012-12-31甘昌远
甘昌远
(中信大锰矿业有限责任公司,广西南宁 530028)
在硫酸锰、电解金属锰、电解二氧化锰等产品的工业生产中,Mn2+的浸出和溶液中Fe2+的去除都是一个非常重要的过程。本试验对铁矿粉、碳酸锰粉、还原锰粉进行Mn2+、Fe的浸出行为进行了试验探索,为电解金属锰制液生产Mn2+的浸出和溶液除Fe提供依据,更好地指导我们的生产工作。
1 试验探索
1.1 Fe的浸出行为探索
取铁矿粉(主要物质质量分数:Fe2O351.19%,FeO 0.46%,其它48.36%)10 g溶于100 mL水中,加入4 m L H2SO4(模拟电解金属锰浸出环境的酸浓度),分别在25,50℃下,分别浸出1,2,3 h。实验结果如表1所示。该过程的主要化学反应为:


表1 铁矿粉浸出反应试验结果
在不同的时间、不同的温度下,根据Fe的浸出情况做出Fe的浸出曲线图,如图1所示。

图1 Fe的浸出率曲线
根据实验结果,Fe的浸出率不高,但在反应温度升高后,Fe的浸出率变化较大。反应温度越高,Fe的浸出率也越高。
2.2 M n2+的浸出行为探索
根据某单位的实际情况,实验中主要采用碳酸锰粉(M nCO3)单独浸出、碳酸锰粉与还原锰粉(M nO)混合浸出的方法。该过程主要的化学反应为:

2.2.1 碳酸锰粉单独浸出试验[1-3]
首先对用碳酸锰粉单独浸出时M n2+和 Fe浸出行为进行探索。利用电解金属锰的阳极液作为碳酸锰浸出反应的溶剂。所用的碳酸锰粉和阳极液成份如下:
碳酸锰:Mn 20.29%、Mn2+15.13%、Fe 4.64%
阳极液:Mn2+15.85 g/L、H2SO437.61 g/L
称取碳酸锰粉338 g缓慢加入到2 000 mL的阳极液中,然后再缓慢加入47 mL浓硫酸充分搅拌,分别在25,50℃下浸出。在浸出10,20,30,60,90,120,150,180 min时分别取样分析M n2+和 Fe的浸出情况,结果如表2所示。

表2 碳酸锰粉浸出反应试验结果
根据表2数据,将不同温度下M n2+的浸出情况按时间变量绘制成图,见图2。

图2 Mn2+的浸出曲线
由图2可以发现,Mn2+的浸出在1 h的时候已经基本完成,在50℃的温度下,Mn2+浸出比较快。
根据表2中的数据,同样可得出Fe的浸出曲线图,见图 3。

图3 Fe的浸出曲线
由图3可知,Fe的浸出量不大,随着浸出时间的延长,Fe的浓度随之增加;在50℃下,Fe的浸出量比25℃下高。
2.2.2 碳酸锰粉和还原锰粉混合浸出试验[2-3]
根据我们生产上采用碳酸锰粉和还原锰粉混合浸出的情况,对碳酸锰粉和还原锰粉混合浸出进行了试验。同样用阳极液作为反应溶剂,有关原料的成份如下:
碳酸锰粉:Mn 20.29%、Mn2+15.13%、Fe 4.64%
还原锰粉;Mn 35.59%、Mn4+2.18%、Mn2+30.92%、Fe 9.16%
阳极液:Mn2+15.85 g/L、H2SO437.61 g/L
称取碳酸锰粉190 g缓慢加入到2 000 mL的阳极液中,然后再缓慢加入27 mL浓硫酸充分搅拌,分别在25℃、50℃下浸出。在浸出60 m in后加入已称量好的还原锰粉70 g。在浸出为10,20,30,60,70,80,90,120,150,180 m in时分别取样分析M n2+和Fe的浸出情况,结果如表3所示。
根据表3的数据,将不同温度下Mn2+的浸出情况按时间变量绘制成图,见图4。

1 25℃下;2 50℃下
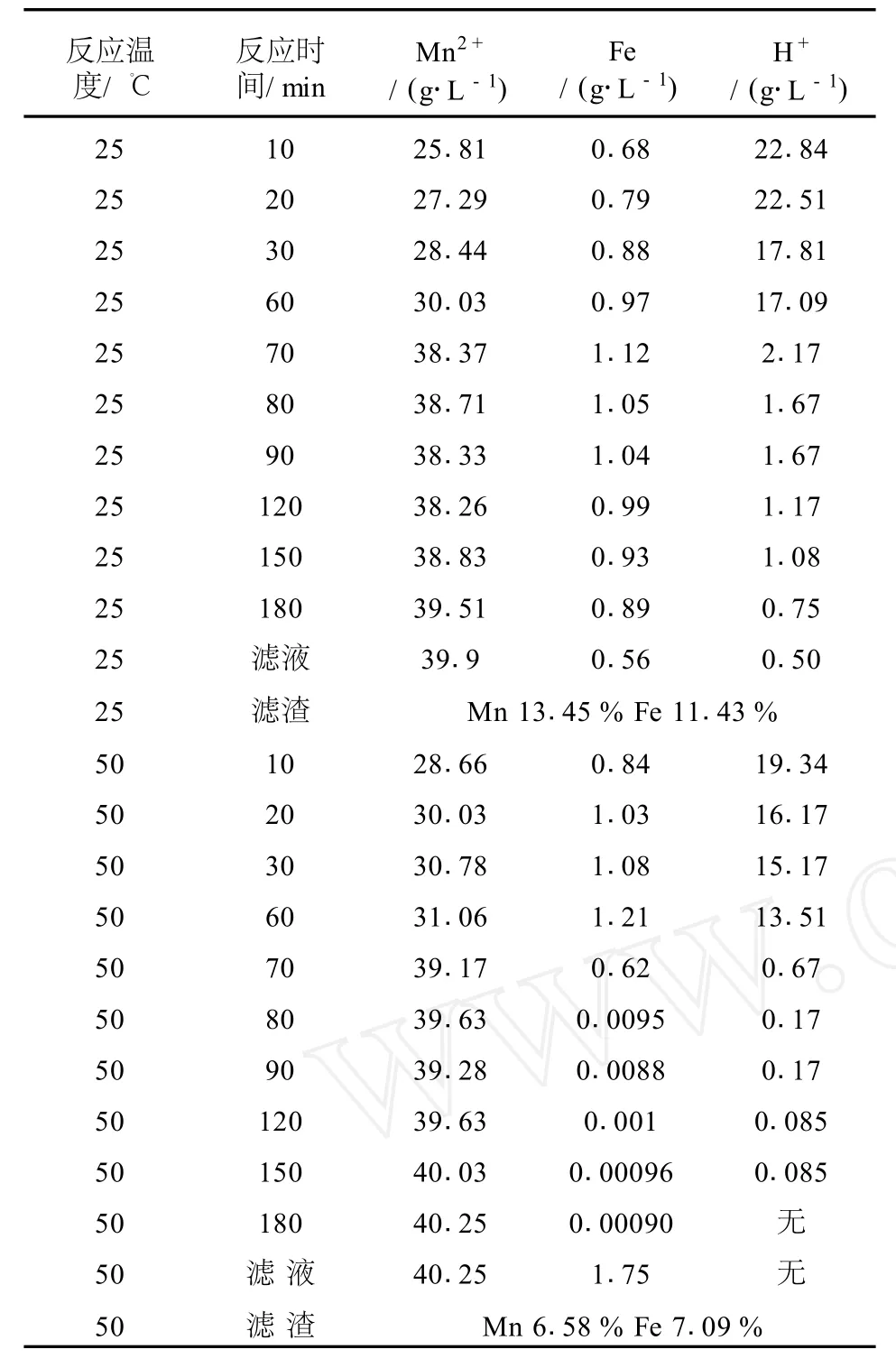
表3 碳酸锰粉与还原锰粉混合浸出反应试验结果
由于是先加碳酸锰粉,硫酸浓度比较大,所以M n2+的浸出较为迅速,60 min的时候碳酸锰粉的M n2+浸出基本完成。还原锰粉的浸出较快,在60~70 min时,M n2+浓度迅速上升,加入10 min后M n2+浓度即达到39 g/L左右,基本上浸出完毕。
根据表3的数据,我们得到Fe的浸出曲线图,见图5。
从图5可以看出,在浸出过程的前60 min,Fe的浸出浓度逐渐升高,当加入还原锰粉后,Fe的浓度逐渐降低。浸出过程中,酸的浓度逐渐减小,再加上还原锰粉中有一定量的MnO2的存在,使浸出的Fe2+氧化为 Fe3+而水解沉淀下来[1-3],从而使的Fe2+浓度降下来。该过程的主要化学反应为:

图5 Fe的浸出曲线

3 结语
1)在电解锰制液的浸出条件下,Fe2O3比较难浸出,铁矿粉中Fe的浸出率不高,因此在碳酸锰的浸出过程中,Fe氧化物较难浸出。
2)碳酸锰粉的浸出过程中,M n2+的浸出较快,在2 h内基本上浸出完全。在实际生产中,为了减少Fe的浸出,降低除Fe工序成本,可适当缩短浸出时间,这样既使M n2+的浸出达到比较好的效果,又降低了Fe的浸出,节省成本。
3)在碳酸锰粉和还原锰粉混合浸出中,先利用大部分的硫酸浸出碳酸锰,再用余酸浸出还原锰粉是可行的,而且在控制一定量的酸的情况下,可使还原锰粉中的一定量的M nO2起到氧化剂的作用,把浸出的Fe2+氧化为Fe3+,从而水解沉淀除去。节省了下一步除Fe的化工锰粉用量,节约成本。
[1]陈家镛.湿法冶金手册[M].北京:冶金工业出版社,2001:1242-1295.
[2]谭柱中,梅光贵,李维健,等.锰冶金学[M].长沙:中南大学出版社,2004:324-334.
[3]丁楷如,余逊贤.锰矿开发与加工技术[M].长沙:湖南科学技术出版社,1992:766-773.
