光催化氧化去除水中新型有机污染物研究进展
2012-08-30王翠彦李梅王洪波崔娅琴
王翠彦,李梅,王洪波,崔娅琴
(山东建筑大学市政与环境工程学院,山东 济南 250101)
0 引言
随着现代合成化工、农药、医药、个人护理品等工业的快速发展,通过各种途径进入水体中的合成有机物数量和种类急剧增加。水中存在的药物、个人护理品,特别是干扰内分泌的化学品统称为新型有机污染物。处理过的污水、地表水、地下水甚至饮用水中已发现都存在这类物质。这些污染物对人体以及生态系统的潜在危害很大,特别是一些内分泌干扰物,会干扰人类和动物的生殖遗传能力,对人类健康和物种繁衍造成严重威胁。常规的水处理工艺以去除传统有机物为主,对新型微量有机污染物的去除有限。因此,探寻高效去除新型污染物技术成为研究热点。高级氧化技术被认为是目前去除难降解有机物的一种有效方法。它可产生氧化能力极强的羟基自由基,将有机物彻底氧化去除。其中,光催化氧化技术因其能耗低、矿化度高、反应条件温和等优点,近年来成为研究的重点。
1 水中新型有机污染物的种类和特点
水环境中存在的新型有机污染物主要有内分泌干扰物、药品和个人护理品两大类。
(1)内分泌干扰物(EDCs),多为人工合成的化学物质,可通过市政污水、工业废水和降水径流带来的农药等途径造成水源污染,并通过接触、饮食等途径进入生物体内,干扰生物体内分泌系统、神经系统、生殖系统的正常运行。EDCs按化学成分不同,分为持久性有机卤化物、农药、类固醇、酞酸酯类、酚类等。水体中EDCs具有以下特点:①多为脂溶性,性质稳定不易降解,生物富集性强。②种类多,浓度低。③危害大,极微量便能引起细胞功能的显著变化[1]。
(2)药物和个人护理品(PPCPs),与人类生产、生活密切相关。人类和牲畜服用的药物以及个人护理品的使用是其进入水体的主要方式。PPCPs包括各种处方药和非处方药(如抗生素、消炎止痛药、降脂药、避孕药、减肥药等),抗菌剂、β-阻滞剂、化妆品等。水体中PPCPs具有以下特点:①多为水溶性,有些带有酸性或碱性的官能团[2]。②具有较强的生物活性、极性和旋光性。③由于个人和畜牧业的大量使用,导致PPCPs形成假性持续性现象[3]。④含量低,不会造成突发性危害。
2 光催化氧化反应机理
光催化氧化技术是一种新型高级氧化技术,多采用半导体金属氧化物为催化剂,以氧气或空气为氧化剂。半导体的能带不连续,在填满电子的低能价带(VB)和空的高能导带(CB)之间存在禁带;当半导体粒子吸收了能量与其带隙能(Eg)相当或超过Eg的光子时,价带电子被激发跃迁至导带,形成高活性光生电子(e-),在价带上产生相应的空穴(h+)[4],形成电子-空穴对的氧化-还原体系,可将多数有机物直接、间接氧化还原。可用作催化剂的半导体材料有 ZnO、TiO2、SnO2、Fe2O3、CdSe、CdS等。由于TiO2的催化活性高、稳定性好、价廉无毒、无二次污染,通常以TiO2作为催化剂。TiO2光催化降解水中有机物的反应过程如下:(1)光生电子空穴分离TiO2-H2O悬浮体系在紫外光照射下,激发产生可自由移动的e-和h+,大部分e-和h+在移动过程中发生复合反应,小部分在电场作用下分离并迁移至TiO2粒子表面;(2)自由基生成 迁移至TiO2粒子表面的h+被表面吸附的H2O、OH-俘获生成羟基自由基·OH;e-被吸附在TiO2粒子表面的溶解氧俘获生成氧自由基·O-2和过羟基自由基·HO2;(3)自由基氧化自由基活性极强,几乎可催化降解所有的有机物,最终矿化生成CO2、H2O等无机小分子物质。其中,自由基的生成是光催化的关键,自由基与有机物的氧化是整个光催化过程的决定步骤[5]。反应式如下所示[6]:
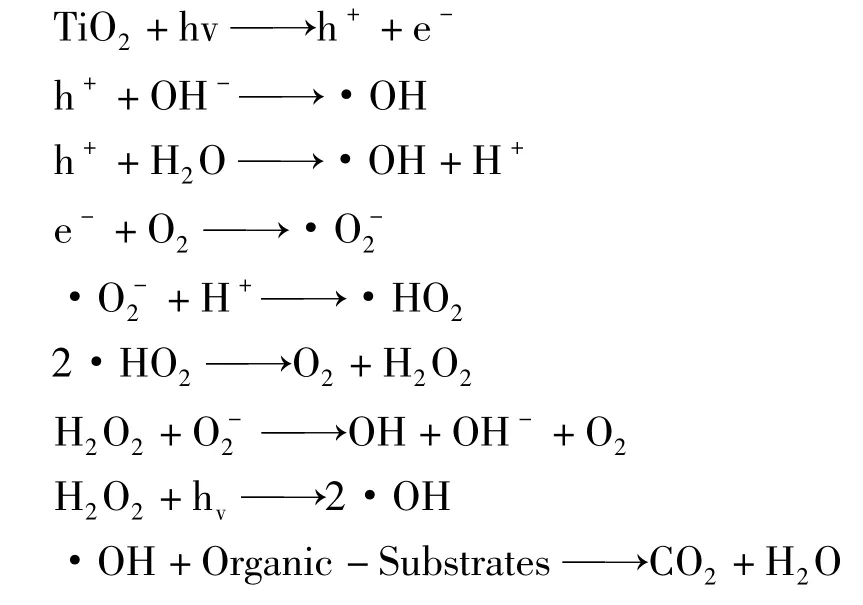
3 光催化氧化去除水中新型有机污染物研究现状
3.1 光催化去除EDCs
3.1.1 持久性有机卤化物
持久性有机卤化物具有潜在致癌性、环境持久性、生物蓄积性等特点,包括有机氯农药(OCPs)(如艾氏剂、狄氏剂、滴滴涕、六六六、氯丹等),多氯联苯(PCBs),二恶英类等。Erick R.Bandala等[7]以日光作光源,TiO2作催化剂处理水中的艾氏剂,发现开始几minTiO2对艾氏剂的吸附作用很强,检测不到水中存在艾氏剂;光照时TiO2表面发生电荷变化,结果艾氏剂发生脱附作用,重新回到水溶液中;加入H2O2促使羟基自由基的产生,可有效降解艾氏剂。张志军等[8]利用中压汞灯作光源,研究了TiO2催化2,3 -二氯代二恶英(DCDD)、1,2,3,7,8-五氯代二恶英(PeCDD)以及八氯代二恶英(OCDD)的光解反应,发现4h后DCCD、PeCDD和OCDD 的降解率分别为87.2%,84.6%和91.2%。
3.1.2 农药
具有内分泌干扰效应的农药除有机氯农药外,还有各种除草剂、杀虫剂和有机磷农药(如敌敌畏、马拉硫磷、久效磷、对硫磷等)。含该类污染物的废水通常毒性大,可生化性差,具有生物累积性特征。Aramendía 等[9]和 Marinas 等[10]均采用 P -25 TiO2为催化剂,分别对除草剂氟草烟和杀虫剂伐虫脒进行了光催化降解研究,如表1所示。
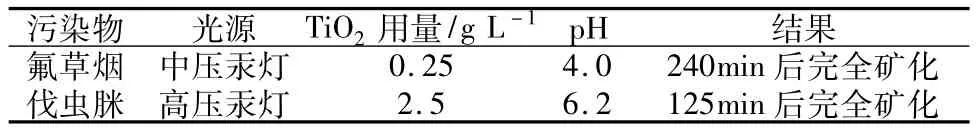
表1 氟草烟和伐虫脒光催化降解比较
研究发现,敌敌畏、马拉硫磷、久效磷、对硫磷等有机磷农药在TiO2光催化降解作用下均可有效脱毒,且降解彻底,最终产物为、Cl-以及CO2等无机物质。
3.1.3 类固醇
类固醇类内分泌干扰物是一种胆固醇合成的生物活性物质,对人体和环境危害很大。典型的类固醇类内分泌干扰物有:雌酮(E1)、17-β-雌二醇(E2)、雌三醇(E3)、乙炔雌醇(EE2)以及孕酮(PROG)。Ohko等[11]以 200W Hg-Xe灯为光源,研究了TiO2光催化降解E2的情况。当TiO2用量为1g/L,反应3h后能将初始浓度为0.272 g/L的E2完全矿化,并发现光催化氧化的起点是E2的酚基,Ohko认为E2光催化氧化后的中间产物不含苯酚环,所以其雌激素活性是可忽略的。李青松等[12]采用间歇式光反应器,以低压汞灯为光源,TiO2为催化剂光催化降解E2。结果表明,对E2的去除效果很好,降解过程符合1级反应动力学模型,降解速率与初始浓度、TiO2用量、溶液pH和光照强度等因素有关。
3.1.4 酞酸酯类(PAES)
PAEs主要用作增塑剂,易通过呼吸和皮肤接触进入人或动物体内,具有类似雌激素的作用。PAEs内分泌干扰物主要有邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二乙酯(DEP)、邻苯二甲酸二丁酯(DBP)以及邻苯二甲酸二辛酯(DEHP)。赵玲等[13]研究了DMP的光催化降解过程,结果表明:当DMP初始浓度为20 mg/L,TiO2用量为70mg/L,反应140 min时DMP的降解率和矿化率分别为95.1% 和62.5%。程沧沧等[14]以125W紫外灯为光源,TiO2薄膜为催化剂,研究了 DEP的光催化降解,发现DEP的降解率随光照时间增加而增大,随DEP初始浓度增加而降低。当TiO2用量为50mg/L、pH值为2.0时,DEP降解效果最好。Chiou等[15]以玻璃珠为载体制备TiO2,光催化降解DBP,结果表明降解过程符合一级动力学方程,在pH 4.5~9时,随pH值增大降解率反而下降,当水样初始浓度为5mg/L时,光照80 min降解率达到75%左右。
3.1.5 酚类
典型的酚类内分泌干扰物包括氯酚类(如双酚A、2,4-二氯苯酚等)和烷基酚类(如壬基酚、辛基酚等)两大类,具有致癌性、潜在的雌激素效应,即使很低的剂量,危害性也很大。Chiang等[16]、Bayarri等[17]和程沧沧等[18]分别进行了含双酚 A、2,4-二氯苯酚以及壬基酚废水的光催化降解研究,如表2所示。
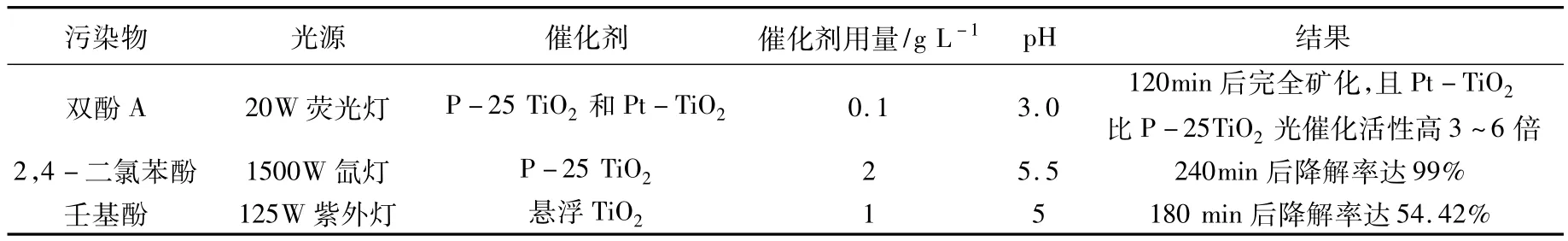
表2 双酚A、2,4-二氯苯酚以及壬基酚光催化降解比较
此外,黄晓明等[19]进行了TiO2光催化降解双酚A的实验研究,发现双酚A在碱性条件下有较好的降解率;随着催化剂用量的增加,紫外光强的增大,双酚A降解程度明显提高。
3.2 光催化去除PPCPs
3.2.1 抗生素
抗生素是一种抑制致病微生物感染的药物。抗生素废水毒性大,难生物降解。典型抗生素污染物有四环素、诺氟沙星、头孢菌素、氯霉素、环丙沙星等。Palominos等[20]、Haque 等[21]和郭佳等[22]分别进行了TiO2光催化降解含四环素、诺氟沙星、头孢曲松钠废水的研究,如表3所示。
Chatzitakisa等[23]采用 P -25 TiO2光催化去除氯霉素,发现反应为假一级反应,符合Langmuir-H inshelwood模型,光照4h后氯霉素可被有效去除,同时可完全脱氯。An等[24]模拟了光催化产生的多种自由基和环丙沙星的反应动力学常数,运用Gaussian函数研究了环丙沙星的光催化降解机理,发现光生空穴和羟基自由基是其光催化降解的主要 途径。
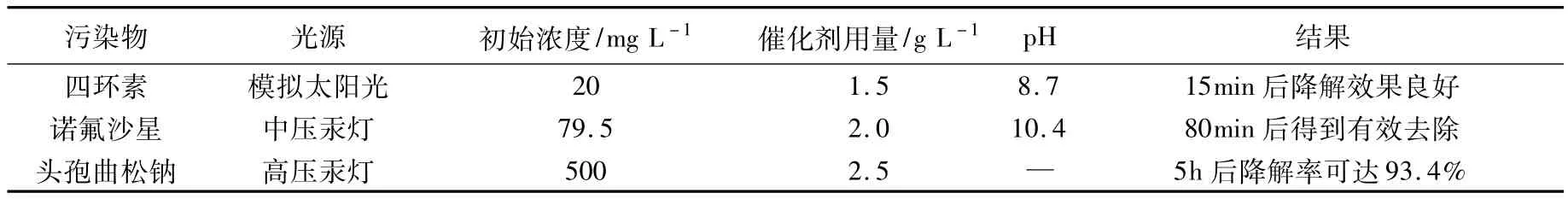
表3 四环素、诺氟沙星以及头孢曲松钠光催化降解比较
3.2.2 消炎止痛药
消炎止痛药具有解热、抗炎、镇痛作用,近年来被大量用作处方药和非处方药,水体中存在较多的这类药物有双氯芬酸、布洛芬、萘普生、阿司匹林等。Perez等[25]以太阳光为光源,进行了双氯芬酸的光催化降解试验研究,发现反应200 min后,初始浓度为43mg/L的双氯芬酸能够被完全降解。Mendez-Arriaga等[26]进行了3种不同中试规模的TiO2/太阳光催化氧化降解布洛芬的试验研究,表明TiO2负载量为0.1~2 mg/L时,布洛芬的降解率为25% ~50%,随着TiO2负载量的增大,降解率成比例升高,且投加H2O2能够进一步提高布洛芬的降解率和TOC去除率。Mendez-Arriaga等[27]对双氯芬酸、萘普生、布洛芬三种物质的钠盐形式进行了光催化降解研究,考察了催化剂量、温度、溶解氧对降解动力学的影响,发现温度只对萘普生的降解有影响,可使其去除率达到99%,而溶解氧可提高萘普生和布洛芬的降解速率。
3.2.3 广谱抗菌剂
广谱抗菌剂普遍存在于个人护理品如化妆品、除臭剂、肥皂和药膏当中。三氯生(TCS)和磺胺嘧啶(SDZ)是典型的广谱抗菌剂。Yu等[28]进行的光催化降解TCS效果实验中发现,光照2h后TCS去除率为80%,延长光照至6h,TCS可被完全降解。Rafqah等[29]对比了不同光催化剂降解TCS的效果,得出P-25 TiO2的催化效果最好,光照1h后,TCS全部被去除,延长光照至25h,TOC去除率可达90%以上。梁凤颜等[30]分别进行了单纯紫外光照和TiO2/UV催化氧化水中磺胺嘧啶(SDZ)的试验,发现单纯紫外光照60min后,SDZ降解率仅为64%;TiO2/UV催化氧化12min时,SDZ降解率可达80%以上,60 min时降解率高达99.9%。
3.2.4 降脂药
目前在水体中检测到的降脂药物有氯贝酸、苯扎贝特、吉非罗齐、非诺贝特酸等。Doll等[31]以氛灯为模拟太阳光源,研究了氯贝酸的光催化降解,发现反应5min后,初始浓度为0.53mg/L的氯贝酸降解率达90%以上。动力学研究还发现氯贝酸的光催化降解率与其初始浓度有关,随浓度增大而降低,且天然有机质的存在会大大降低氯贝酸的降解率。Lambropoulou等[32]以模拟太阳光为光源,TiO2为催化剂,研究了苯扎贝特的光催化降解,发现反应200min后能够将初始浓度为1mg/L的苯扎贝特完全降解,其反应符合假一级动力学。
3.2.5 β-阻滞剂
β-阻滞剂是一种治疗心血管疾病的药物。目前水体中检测到的该类物质主要有阿替洛尔、普萘洛尔、美托洛尔等。Mendana等[33]研究了阿替洛尔的光催化降解机理,发现6种阿替洛尔的单羟基取代物,2种双羟基取代物,6种3羟基取代物,并指出阿替洛尔分子中的芳香环和侧链的断裂是其降解的主要途径。Yang等[34]以普萘洛尔、阿替洛尔、美托洛尔为代表,研究了β-阻滞剂的光催化降解动力学和机理,发现β-阻滞剂光催化降解符合假一级动力学,分子中芳香环个数是影响其光催化降解动力学的重要因素,而侧链的断裂以及羟基自由基对母体化合物的加成是其光催化降解的主要途径。
4 存在的问题及解决方案
我国水体污染形势严峻,水中污染物种类多、成分复杂;特别是一些内分泌干扰物、药物和个人护理品毒性大,含量低,采用传统的生物处理法难以有效去除。而光催化氧化法作为一种典型的高级氧化技术,能降解多种类型的生物难降解和微量有机物,被认为是处理新型有机污染物最有效的方法。而目前对于光催化氧化降解水中新型有机物的研究相对较少,且多停留在实验室研究阶段,要获得大规模应用仍存在一些问题:(1)催化剂易失活且分离回收困难。在光催化氧化反应中电子-空穴对很容易复合,从而使催化剂的活性降低,进而失活。因此减少电子-空穴对的复合是保证TiO2光催化氧化反应有效进行的关键。(2)光源利用率低,工程造价高。实验室研究阶段的光源多为紫外灯,紫外光易被吸收,损失严重,不利于实际工程应用。(3)大型反应器的设计。目前光催化反应器的设计只是停留在小型水处理工艺以及试验阶段,缺乏大型反应器的设计,难以满足工业化发展的需求。为克服这些技术缺陷,可将Pb、Au、Pt等惰性金属负载在催化剂表面,利用金属离子捕获导带中电子,以减少光生电子和空穴的复合,提高催化活性。通过催化剂的掺杂、改性,扩展其对光能的利用范围,使响应波长移至可见光区,提高太阳光能利用率,进而以太阳光代替紫外光,降低工程成本。对现有经济技术指标进一步优化,开发降解水环境中各类EDCs和PPCPs的光催化氧化组合工艺及其集成技术,设计研究实用性强、可长期稳定运行的大型反应器。
[1]武睿.活性炭和膜技术去除水中内分泌干扰物的研究进展[J].工业水处理,2010,30(7):11-14.
[2]Snyder S.A.,Westerhoff P.,Yoon Y.,et al.Pharmaceuticals,personal care products,and endocrinedisruptors in water:Implications for the water industry Environment[J].Engineering Science,2003,20(5):449 -469.
[3]Ternes T.A.,Meisenheimer M.and Mcdowell D.,Removal of pharmaceuticals during drinking water treatment[J].Environmental Science& Technology,2002,36:3855-3863.
[4]张鹏会,王九思,韩迪.TiO2光催化降解有机污染物研究进展[J].化工技术与开发,2009,38(7):51-54.
[5]韦冰心,王亭杰,赵琳,等.二氧化钛颗粒表面的光催化反应过程[J].石油化工,2012,41(2):219-223.
[6]Fujishima A.,Rao N.T.and Tryk A.D.,Titanium dioxide photocatalysis[J].J Photochem..Photobio..C:Photochem Review,2002,1:1-21.
[7]Bandala E.R.,Solar photocatalytic degradation of aldrin[J].Catalysis Today,2002,76(2):189-199.
[8]张志军,包志成.TiO2催化下的氯代二苯并对二恶英光解反应[J].环境化学,1996,15(1):47.
[9]Aramendía M.A.,Marinas A.,Marinas J.M.,et al.Photocatalytic degradation of herbicide fluroxypyr in aqueous suspension of TiO2[J].Catal.Today,2005,101(3 -4):187 -193.
[10]Marinas A.,Guillard C.,Marinas J.M.,et al.,Photocatalytic degradation of pesticide-acaricide formetanate in aqueous suspension of TiO2[J].Appl.Catal.B:Environ,2001,34(3):241-252.
[11]Ohko Y.,Iuchi K.I.,Niwa C.,et al.17Beta-estradiol degradation by TiO2photocatalysis as a means of reducing estrogenic activity[J].Environmental Science and Technology,2002,36(19):4175-4181.
[12]李青松,高乃云,马晓雁,等.TiO2光催化降解水中内分泌干扰物17β- 雌二醇[J].环境科学,2007,28(1):120-125.
[13]赵玲,刘敏,尹平河,等.邻苯二甲酸二甲酯的光催化降解机理[J].环境工程学报,2011,5(6):1273-1277.
[14]程沧沧,付洁媛,岳茜,等.TiO2薄膜光催化降解邻苯二甲酸乙酯的研究[J].环境科学与技术,2005,25(4):39-41.
[15]Chiou C.S.,Shie J.L.,Chang C.Y.,et al.Degradation of dinbutyl Phthalate using Photoreactor paeked with TiO2immobilized on glass beads[J].Journal of Hazardous Materials,2006,137(2):1123-1129.
[16]Chiang K.,Lim T.M.,Tsen L.,et al.,Photocatalytic degradation and mineralization of bisphenol A by TiO2and platinized TiO2[J].Appl.Catal.A:General,2004,261(2):225-237.
[17]Bayarri B.,Giménez J.,Curcó D.,et al.,Photocatalytic degradation of2,4-dichlorophenolby TiO2/UV: Kinetics,actinometries and models[J].Catal Today,2005,101(3 - 4):227-236.
[18]程沧沧,周菊香,万昆,等.TiO2悬浮体系光催化降解壬基酚的研究[J].安全与环境学报,2005,5(2):56-57.
[19]黄晓明,余长亮,熊光胜,等.纳米TiO2光催化氧化降解双酚A研究[J].江西化工,2010,(7):90-94.
[20]Palominos R.A.,Mondaca M.A.,Ana G.,et al.Photocatalytic oxidation of the antibiotic tetracycline on TiO2and ZnO suspensions[J].Catalysis Today,2009,144(1-2):100-105.
[21]Haque M.M.and Muneer M.,Photodegradation of norfloxacin in aqueous suspensions of titanium dioxide[J]..Journal of Hazardous Materials.,2007,145:51 -57.
[22]郭佳,张渊明,杨骏.光催化氧化降解制药废水中头孢曲松钠的研究[J].生态科学,2008,27(6):446- 451.
[23]Chatzitakis A.,Berberidou C.,Paspaltsis I.,et al.,Photocatalytic degradation and drug activity reduction of Chloramphenicol[J].Water Research,2008,42(1 -2):386 -394.
[24]An T.C.,Yang H.,Li G.Y.,et al.Kinetics and mechanism of advanced oxidation processes (AOPs) in degradation of ciprofloxacin in water[J].Applied Catalysis B-Environmental,2010,94(3-4):288-294.
[25]Perez-Estrada L.A.,Maldonado M.I.,Gernjak W.,et al.Decomposition of diclofenac by solar driven photocatalysis at pilot plant scale[J].Catalysis Today,2005,101(3 -4):219 -226.
[26]Mendez-Arriaga F.,Maldonado M I,Gimenez J,et al.Abatement of ibuprofen by solar photocatalysis process:Enhancement and scale up[J].Catalysis Today,2009,144(1/2):112 -116.
[27]Mendze-Arriaga F.,Esplugas S.,Gimenez J.,photocatalytic degradation of non-steroidal anti-inflammatory drugs with TiO2and simulated solar irradiation[J].Water Research,2008,42(3):585-594.
[28]Yu J.C.,Kwong T.Y.,Luo Q.,et al.Photocatalytic oxidation of triclosan[J].Chemosphere,2006,65(3):390 -399.
[29]Rafqah S., WongW. C. P., Nelieu S., etal.Phototransformation of triclosan in the presence of TiO2in aqueous suspension: mechanistic approach[J]. Applied Catalysis B-Environmental,2006,66(1-2):119-125.
[30]梁凤颜,尹平河,赵玲,等.水体中微污染磺胺嘧啶光催化降解行为[J].生态环境学报,2009,18(4):1227-1230.
[31]Doll T.E.,Frimmel F.H.,Kinetic study of photocatalytic degradation of carbamazepine,clofibric acid,iomeprol and iopromide assisted by different TiO2materials——determination of intermediates and reaction pathways[J].Water Research,2004,38(4):955-964.
[32]Lambropoulou D.A.,Hemando M.D.,Konstantinou I.K.,et al.Identification of photocatalytic degradation products ofbezafibrate in TiO2aqueous suspensions by liquid and gas chromatography[J].Journal of Chromatography A,2008,1183(1-2):38-48.
[33]Medana C.,Calza P.,Carbone F.,et al.Characterization of atenolol transformation products on light-activated TiO2surface by high-performance liquid chromatography/high-resolution mass spectrometry[J]. Rapid Communicationsin Mass Spectrometry,2008,22(3):301-313.
[34]Yang H.,An T.C.,LI G.Y.,et al.Photocatalytic degradation kinetics and mechanism of environmental pharmaceuticals in aqueous suspension of TiO2:A case of β-blockers[J].Journal of Hazardous Materials,2010,179(1-3):834-839.
