RP-HPLC法同时测定痛经宁胶囊中4种有效成分
2012-07-26黄文君龙凤荣
黄文君, 龙凤荣, 伍 庆, 乙 引, 洪 江
(1.贵州师范大学,贵州贵阳550001;2.贵州弘康药业有限公司,贵州贵阳550001;3.贵州科学院,贵州贵阳550001)
痛经宁胶囊由白芍、丹参、当归等九味药材组成,具有活血化瘀,行气散寒,调经止痛等功效,用于月经不调,经前、行经期腹痛等[1-2]。目前,对痛经宁胶囊质量标准的研究较少,主要是针对芍药苷的定量测定[3],该方成分复杂多样,单指标难以有效反应制剂质量。丹参活血调经,祛瘀止痛,养血安神,为方中臣药,其水溶性活性成分丹参素理气止痛,原儿茶醛可抑制血小板凝聚,丹酚酸B活血化瘀,通经活络[4-6],均为该制剂有效成分。为了更好的控制痛经宁胶囊的质量,故本实验选择丹参素钠、原儿茶醛、丹酚酸B和芍药苷为检测对象,经过对色谱条件的摸索与优化,建立了RP-HPLC法同时测定痛经宁胶囊中丹参素钠、原儿茶醛、芍药苷、丹酚酸B 4种有效成分。该法简单快速、稳定可靠,为更好的控制该制剂质量提供了依据。
1 仪器与试药
1.1 仪器 Agilent 1200高效液相色谱仪、Agilent色谱工作站 (安捷伦科技有限公司);CH—250超声波清洗仪 (北京创新德超声电子研究所);XS205DU电子分析天平 (梅特勒-托利多)。
1.2 试药 丹参素钠对照品 (批号:110855-200507)、原儿茶醛对照品 (批号:110810-200506)、芍药苷对照品 (批号:110736-200629)、丹酚酸B对照品 (批号:111562-200803)均购于中国药品生物制品检定所。痛经宁胶囊为市售(批号:20110301,20110401,20110801,贵州弘康药业有限公司生产)。甲醇、乙腈为色谱纯,水为超纯水 (自制),其余试剂均为分析纯。
2 方法及结果
2.1 色谱条件 Diamonsil C18色谱柱 (250 mm×4.6 mm,5 μm);流动相为甲醇-乙腈 (2∶1)(A)-0.05%磷酸水溶液 (B),梯度洗脱 (0 min,7%A;15 min,22%A;30 min,31%A;50 min,53%A),体积流量1 mL/min;柱温30℃;检测波长230 nm;进样量10 μL。
2.2 溶液的制备
2.2.1 对照品溶液的制备 精密称取原儿茶醛对照品6.52 mg置10 mL量瓶中,加稀乙醇 (529→1000,下同)稀释至刻度,制成0.652 mg/mL的对照品溶液。精密称取对照品丹参素钠8.78 mg、芍药苷10.41 mg、丹酚酸B 5.72 mg,精密吸取上述原儿茶醛对照品溶液0.5 mL置于同一25 mL量瓶中,加稀乙醇稀释至刻度,制成丹参素钠、原儿茶醛、芍药苷、丹酚酸B质量浓度分别为0.3512 mg/mL、0.01304 mg/mL、0.4164 mg/mL 和0.2288 mg/mL的混合对照品贮备液。精密吸取上述对照品贮备液1 mL于5 mL量瓶中,加稀乙醇稀释至刻度,摇匀,制成丹参素钠、原儿茶醛、芍药苷、丹酚酸 B质量浓度分别为 70.24 μg/mL、2.608 μg/mL、83.28 μg/mL 和 45.76μg/mL 的混合对照品溶液,供定量测定用。
2.2.2 供试品溶液的制备 取痛经宁胶囊内容物,研细,取约0.3g,精密称定,置具塞锥形瓶中,精密加入稀乙醇25 mL,密塞,称定质量,超声处理30 min,放冷,再称定质量,用稀乙醇补足减失的质量,摇匀,滤过,取续滤液,过0.45 μm微孔滤膜,即得。
2.2.3 阴性供试品溶液的制备 参照制剂的工艺过程,按处方比例分别配置不含白芍和丹参的阴性样品,照2.2.2项下方法操作,制备阴性供试品溶液。
2.3 系统适用性试验 精密吸取混合对照品溶液、供试品溶液及阴性样品溶液分别注入高效液相色谱仪,按2.1项下色谱条件进样,记录色谱图,结果丹参素钠、原儿茶醛、芍药苷、丹酚酸B的理论塔板数均不低于10000,与相邻成分达到基线分离,且阴性对照无干扰。对照品、样品与阴性样品的色谱图见图1。
2.4 线性关系试验 分别精密吸取上述混合对照品贮备液0.2、0.5、1.0、1.5、2.0 mL置于5 mL量瓶中,加稀乙醇稀释至刻度,摇匀。按2.1项下色谱条件分别进样,记录色谱图,以峰面积值(Y)对进样量 (X,μg)进行线性回归,得丹参素钠回归方程为 Y =953.53X -2.6216(r=0.9999);原儿茶醛回归方程为 Y=5022.6X+1.8974(r=0.9996);芍药苷回归方程为Y=1285.2X+2.9049(r=0.9998);丹酚酸B回归方程为Y=1995.1X+12.878(r=0.9999)。结果表明,丹参素钠、原儿茶醛、芍药苷和丹酚酸B分别在 0.14048 ~1.4048 μg,0.00522 ~0.0522 μg,0.16656 ~1.6656 μg 和 0.09152 ~0.9152 μg范围内线性关系良好。
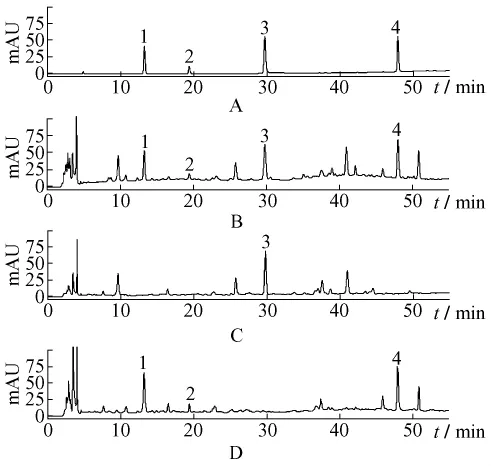
图1 对照品 (A)、样品 (B)、丹参阴性样品 (C)和白芍阴性样品 (D)HPLC色谱图Fig.1 HPLC chromatograms of mixed reference substances(A), sample(B),negative sample without Salviae miltiorrhizae Radix et Rhizoma(C)and negative sample without Paeoniae Radix alba(D)
2.5 精密度试验 精密吸取同一混合对照品溶液,按2.1项下色谱条件连续进样6次,按峰面积计算RSD值,结果丹参素钠、原儿茶醛、芍药苷和丹酚酸B的RSD分别为0.82%、1.43%、0.96%和1.61%。结果表明,仪器精密度良好。
2.6 稳定性试验 取同一供试品溶液,分别在0、2、4、6、8、10 h进样,记录色谱峰面积,结果丹参素钠、原儿茶醛、芍药苷和丹酚酸B峰面积的RSD分别为1.45%、1.26%、0.98%和1.83%,表明供试品溶液在10 h内稳定。
2.7 重复性试验 取同一批号 (20110801)痛经宁胶囊内容物粉末,照2.2.2项下方法操作,平行制备6份供试品溶液,按2.1项下色谱条件进行测定,计算含有量,结果丹参素钠、原儿茶醛、芍药苷和丹酚酸B含有量的RSD分别为1.12%、2.03%、0.76%、1.58%,表明该方法的重复性良好。
2.8 加样回收率试验 精密称取已知含有量的痛经宁胶囊 (批号:20110801)9份,每份约0.15 g,置25 mL量瓶中,分别精密加入上述混合对照品贮备液1.6、2.0、2.4 mL,各平行3份,加稀乙醇适量,超声处理30 min,放冷,用稀乙醇加至刻度,摇匀,滤过,取续滤液,过0.45 μm微孔滤膜,进样测定,计算回收率,结果见表1。
2.9 样品测定 取3批样品,照2.2.2项下方法制备供试品溶液,按2.1项下色谱条件进行测定,记录峰面积,计算各自质量分数,结果见表2。
3 讨论
3.1 检测波长的选择 经紫外-可见分光光度计扫描,丹参素钠分别在207、221、282 nm处有吸收峰,原儿茶醛分别在207、231、280、312 nm处有吸收峰,芍药苷分别在202、230、275 nm处有吸收峰,丹酚酸B分别在206、224、254、286、308 nm处有吸收峰。结合相关文献[7-8],本实验比较了230 nm与280 nm波长下样品的吸收,实验结果表明采用230 nm同时测定4种成分时的响应值和峰形优于采用280 nm测定结果。
3.2 提取条件的选择 由于丹酚酸B的热不稳定性[9],故选择超声提取。丹参素钠、原儿茶醛、芍药苷和丹酚酸B均为水溶性成分,本实验考察了纯水,稀乙醇,95%乙醇,50%甲醇及80%甲醇的提取效果,结果表明,稀乙醇与50%甲醇优于其他溶剂,二者对丹参素钠、原儿茶醛、芍药苷的提取率相当,而稀乙醇对丹酚酸B的提取率高于50%甲醇;进一步试验,以稀乙醇为提取溶剂,分别超声提取20、30、45 min,发现超声提取30 min各组分均可提取完全。故本实验选择稀乙醇作提取溶剂超声提取30 min制备供试品溶液。
3.3 流动相的选择 由于丹参素钠、原儿茶醛、芍药苷和丹酚酸B均为酸性化合物,为改善其拖尾现象,故在流动相中加入酸来改善峰形,而醋酸在230 nm有吸收,容易发生基线的漂移,因此选择加入磷酸,同时结合相关文献资料[10-13],也比较了甲醇与乙腈的分离效果,选择了甲醇-乙腈(2∶1)(A)-0.05%磷酸 (B)系统,经梯度洗脱优化,最终确定了上述最佳流动相。

表1 加样回收率试验结果 (n=9)Tab.1 Results of recovery tests(n=9)
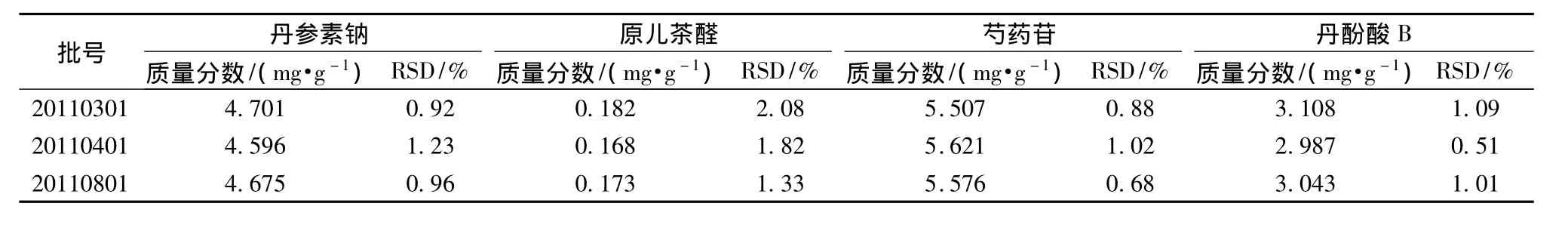
表2 样品测定结果 (n=3)Tab.2 Content determination of samples(n=3)
[1]张金艳,曹永孝,刘 静,等.痛经宁胶囊对雌性幼鼠生殖器官发育的影响及其镇痛抗炎作用[J].中成药,2004,26(7):571-573.
[2]颜利玲.痛经宁胶囊制备工艺的研究[J].湖南中医杂志,2006,22(1):63-24.
[3]江 帆,郭培果,蔡晓静.RP-HPLC测定痛经宁胶囊中芍药苷的含量[J].中国现代应用药学,2010,27(8):741-743.
[4]林 峰,石 杰.丹参活性成分的药效药理作用[J].医学信息,2011,24(6):3813-3814.
[5]李克明,付桂香.丹参中丹酚酸B药理研究进展[J].中日友好医院学报,2008,22(6):366-367.
[6]常新全,丁丽霞.中药活性成分分析手册[M].北京:学苑出版社,2002.
[7]叶晓平,茅仁刚,袁 萍.RP-HPLC法同时测定芝参正肝胶囊中丹酚酸B、葛根素和芍药苷的含量[J].药物分析杂志,2010,30(5):887-890.
[8]魏惠珍,王跃生,吴有根,等.HPLC同时测定冠心丹参胶囊中丹参素、原儿茶醛、丹酚酸B和丹参酮ⅡA的含量[J].中成药,2009,31(1):64-68.
[9]王凤美,李 磊,柳先平,等.丹参药材中丹酚酸B的提取及其HPLC测定[J].现代中药研究与实践,2004,18(1):62-64.
[10]肖 霞,曹俊凯.中药止痛胶囊中芍药苷的HPLC含量测定[J].中国现代药物应用,2011,5(11):72-73.
[11]谭生建,刘 刚,张 华.梯度洗脱HPLC法测定抗栓保心片中芍药苷和丹酚酸B的含量[J].药物分析杂志,2009,29(7):1104-1106.
[12]梁小洁,伍 庆,邹 晶.HPLC同时测定三宝胶囊中原儿茶醛、丹参素钠和丹酚酸B含量[J].贵州师范大学学报,2008,26(4):97-99.
[13]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010.
