HPLC-MS/MS联用技术定量测定人血浆中伊伐布雷定及其代谢产物
2012-02-02贾艳艳鹿成涛丁莉坤陈敏纯李雪晴冯智军文爱东
贾艳艳,鹿成涛,宋 颖,丁莉坤,杨 静,陈敏纯,李雪晴,宋 薇,周 伦,冯智军,文爱东
(中国人民解放军第四军医大学第一附属医院药剂科,陕西 西安710032)
HPLC-MS/MS联用技术定量测定人血浆中伊伐布雷定及其代谢产物
贾艳艳,鹿成涛,宋 颖,丁莉坤,杨 静,陈敏纯,李雪晴,宋 薇,周 伦,冯智军,文爱东
(中国人民解放军第四军医大学第一附属医院药剂科,陕西 西安710032)
为了定量测定人血浆中伊伐布雷定和去甲伊伐布雷定浓度,建立了HPLC-MS/MS联用方法以地西泮为内标,V(甲醇)∶V水(5mM醋酸铵+1%甲酸)=80∶20的混合溶液为流动相,Diamosil C18(150mm×4.6mm,5μm)色谱柱为分析柱,通过电喷雾离子源(ESI),以正离子多反应监测(MRM)方式检测。用于定量分析的离子对分别为m/z469.2→177.1(伊伐布雷定),m/z455.2→177.1(去甲伊伐布雷定),m/z285.1→193.1(地西泮)。伊伐布雷定的标准曲线线性范围为0.101 3~101.3μg/L,定量下限为0.101 3μg/L;去甲伊伐布雷定的标准曲线线性范围为0.085~25.5μg/L,定量下限为0.085μg/L。日内、日间精密度的RSD<15%,平均回收率>75%。
伊伐布雷定;去甲伊伐布雷定;高效液相色谱-串联质谱;血浆药物浓度
盐酸伊伐布雷定是一种减缓心率药,起到减缓窦房结起搏点活动速度的作用,用于治疗慢性稳定型心绞痛。伊伐布雷定常见的不良反应为心动过缓、房室传导1度阻滞、室性期外收缩、头痛、眩晕和视力模糊与其剂量存在依赖性[1-2]。伊伐布雷定在体内经肝药酶代谢成去甲伊伐布雷定,从而发挥减慢心率的作用,是临床常用的药物[3-5],但目前国内暂无伊伐布雷定及其代谢产物体内定量检测方法的研究报道。本试验建立了伊伐布雷定及其代谢产物在人血浆中定量检测的方法,并用于人体药动学研究。
1 试验部分
1.1 主要仪器与装置
6410型高效液相色谱-串联质谱联用仪:美国Agilent公司产品,其中安捷伦1200高效液相色谱系统包括二元输液泵、自动进样器、柱温箱,串联质谱仪为Agilent 6410型三重四极杆串联质谱仪,包含电喷雾离子化源以及串联三重四极杆质谱检测器;色谱工作站:MassHunter数据处理软件,美国Agilent公司产品;FA1004电子天平:上海恒平科学仪器公司产品;Milli-Q Plus纯水器:美国密理博中国有限公司产品;XW-80A微型旋涡混合仪:上海沪西分析仪器有限公司产品;TGL 16G台式离心机:上海安亭科学仪器厂产品;KS康氏振荡器:江苏省金坛市荣华仪器制造有限公司产品。
1.2 主要试剂
盐酸伊伐布雷定对照品(含量99.13%,批号:YF-D01),盐酸去甲伊伐布雷定对照品(含量99.13%,批号:091007):由常州四药制药有限公司提供;地西泮对照品(内标,批号:100294-200602):由中国药品生物制品检定所提供;甲醇,磷酸(色谱纯):美国Fisher公司产品;水:自制纯化水;空白血浆:由第四军医大学第一附属医院提供;实验用水为去离子水,实验室自制。
1.3 HPLC-MS/MS分析条件
1.3.1 色谱条件 色谱柱:迪马公司DIAMOSIL C18(150mm×4.6mm,5μm);流动相:V(甲醇)∶V 水(5mmol/L醋酸铵+0.1%甲酸)=80∶20的混合溶液;流速0.6mL/min;柱温40℃;进样量5μL。
1.3.2 质谱条件 电喷雾离子化源(ESI源),正离子模式检测,多反应监测(MRM)方式,毛细管电压4 000V,驻留时间150ms,干燥气温度325℃,干燥气流速12L/min,雾化气压力345kPa。以多反应监测的质谱扫描方式分析,测定伊伐布雷定,用于定量分析的离子对m/z 469.2→177.1,碰撞电压25eV,裂解电压140 V;去甲伊伐布雷定,用于定量分析的离子对m/z455.2→177.1,碰撞电压23eV,裂解电压140 V;地西泮(内标),用于定量分析的离子对m/z 285.1→193.1,碰撞电压32eV,裂解电压150 V,所得的质谱图示于图1。
1.4 试验步骤
1.4.1 血浆样品的处理 精密量取1mL血浆样品于10mL玻璃离心管中,加入50μL内标溶液(2mg/L地西泮溶液),旋涡30s后混匀,加入4mL乙酸乙酯,涡漩3min,以4 000r/min离心10min。吸取有机层,在30℃水浴中以氮气流吹干,残渣以200μL流动相复溶,以16 000 r/min离心8min,吸取上清液转移至自动进样器样品管中,进样量5μL,进行 LC-MS/MS分析。
1.4.2 标准曲线和质控样品的制备 精密称量11.01mg盐酸伊伐布雷定标准品 (含10.13mg伊伐布雷定标准品),置于10mL棕色容量瓶中,用甲醇定容,得伊伐布雷定浓度为1.013 g/L,作为储备液备用,然后用空白血浆依次稀释配制 成 浓 度 为 0.101 3、0.303 9、1.013、3.039、10.13、30.39、101.3μg/L的标准含药血浆。按照1.4.1方法进行处理并测定。同样步骤再次配制浓度为0.202 6、5.065、75.975μg/L的质控样品。
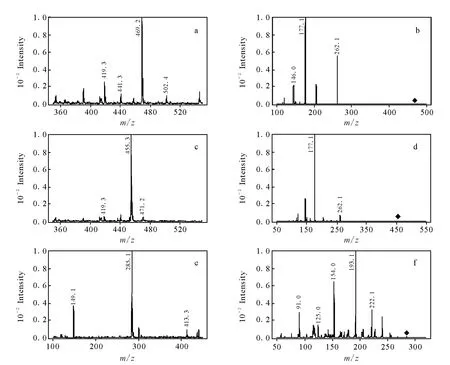
图1 伊伐布雷定、去甲伊伐布雷定及内标地西泮质谱图Fig.1 Mass spectrum of ivabradine,N-desmethylivabradine and Diazepam(IS)
精密称取4.63mg盐酸去甲伊伐布雷定标准品 (内含4.25mg去甲伊伐布雷定),置于10 mL容量瓶中,加入甲醇稀释至10mL,溶解摇匀,即得0.425g/L伊伐布雷定的储备液,然后用空白血浆依次稀释配制成浓度为0.085、0.255、0.85、2.55、8.5、17、25.5μg/L 的标准含药血浆。按照1.4.1方法进行处理并测定。同样步骤再次配制浓度为0.17、2.55、12.75μg/L的质控样品。
1.4.3 稳定性考察 在不同的试验条件下对质控样品进行稳定性试验(n=3):1)质控样品在-80℃冰箱中完全冷冻后取出,在室温环境下解冻,然后再次放入冰箱,如此反复3次后制备并测定;2)质控样品在室温下放置4h后制备并测定;3)质控样品在-80℃下避光保存,1个月后制备并测定;4)质控样品在进样器放置4h后制备并测定。
2 方法与结果
2.1 特异性考察
分别取6个不同受试者的1mL空白血浆,除不加入内标溶液外,其余按血浆样品分析方法处理,进样5μL,获得空白样品的色谱图,示于图2a;将一定浓度的伊伐布雷定标准溶液、去甲伊伐布雷定标准溶液和内标地西泮溶液加入空白血浆中,用相同的方法进行样品处理,获得相应的色谱图,示于图2b;受试者服药5mg伊伐布雷定片0.5h后的色谱图示于图2c。结果表明,空白血浆中的内源性杂质并未干扰伊伐布雷定、去甲伊伐布雷定和内标的测定。
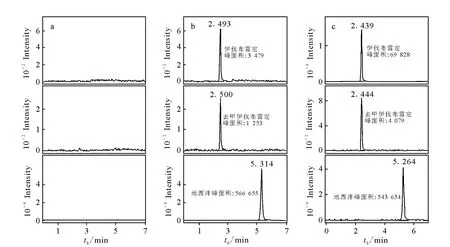
图2 血浆中伊伐布雷定、去甲伊伐布雷定、地西泮的典型多反应监色谱图Fig.2 Representative chromatograms for ivabradine,N-desmethylivabradine,and IS.
2.2 基质效应考察
分别用甲醇配制相当于血浆浓度0.202 6、5.065、75.975μg/L的伊伐布雷定样品各1 mL,相当于血浆浓度0.17、2.55、12.75μg/L的去甲伊伐布雷定样品各1mL,加入50μL内标,每种浓度各做10份,以氮气吹干。其中5份样品以200μL流动相复溶,另外5份以空白血浆提取液复溶,以16 000r/min离心8min,移取上清液至自动进样瓶,进样分析,流动相复溶峰面积比值平均值记为fR,空白血浆提取液复溶样品峰面积记为fs,按下式计算基质效应(RE),RE=(fs/fR)×100%。结果显示:伊伐布雷定高、中、低3个浓度的基质效应分别为2.8%、2.1%、3.7%,去甲伊伐布雷定高、中、低3个浓度的基质效应分别为2.5%、1.7%、6.3%,RSD均小于15%,可认为没有基质效应干扰。
2.3 标准曲线和线性范围
以待测化合物和内标峰面积为纵坐标,浓度为横坐标,权重系数1/x,进行线性回归计算,得到伊伐布雷定标准曲线:f=0.003 848+0.057 28C,线性相关系数r为0.998;去甲伊伐布雷定标准曲线:f=0.001 061+0.019 807C,线性相关系数r为0.999,而且各点标示浓度和计算浓度的偏差都在±15μg/L以内(最低定量限为±20μg/L)。伊伐布雷定的最低定量(LLOQ)浓度为0.101 3μg/L,其日内精密度RSD为10.8%,日间精密度RSD为5.4%;去甲伊伐布雷定的最低定量浓度为0.085μg/L,其日内精密度RSD为8.4%,日间精密度RSD为4.7%,符合要求。
2.4 精密度和准确度
方法学考核伊伐布雷定浓度为0.202 6、5.065、75.975μg/L的质控样品(n=6),去甲伊伐布雷定浓度为0.17、2.55、12.75μg/L的质控样品(n=6),考核批次为3次,结果列于表1。结果表明,此方法的精密度和准确度偏差均在±15%以内。
2.5 稳定性
分别在-80℃反复冻融3次、血浆室温放置4h、-80℃下冻存3个月、进样器放置4h(n=3),4种条件下考察方法的稳定性,结果列于表2。结果表明,伊伐布雷定及去甲伊伐布雷定在这4种条件下的稳定性良好。
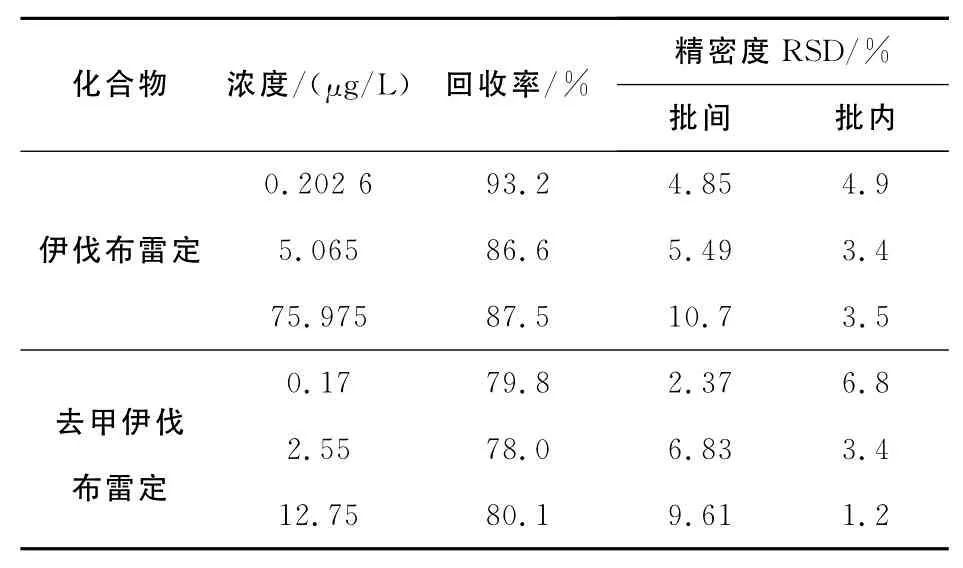
表1 伊伐布雷定和去甲伊伐布雷定的回收率和精密度Table 1 Precision and recovery of ivabradine and N-desmethylivabradine
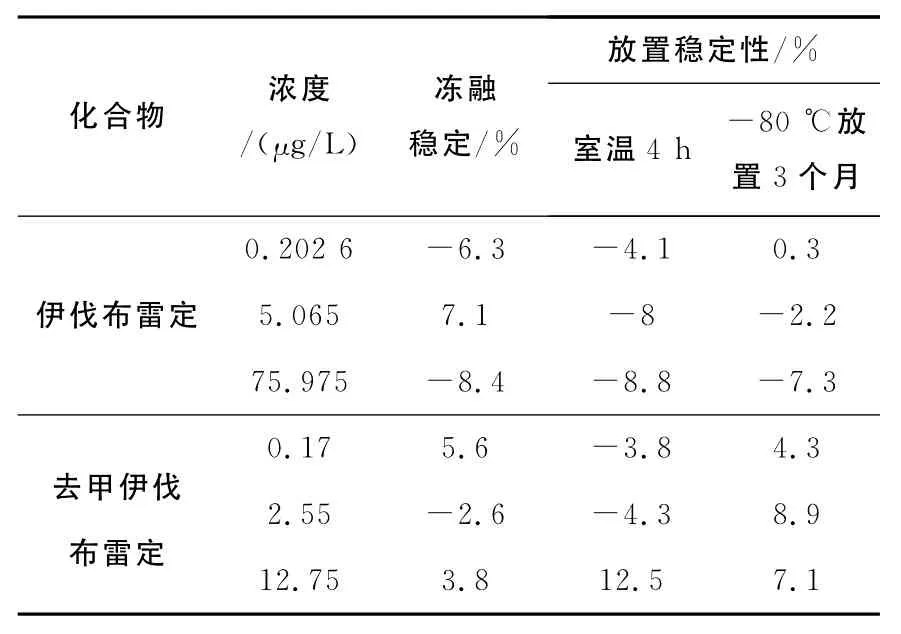
表2 伊伐布雷定和去甲伊伐布雷定的稳定性Table 2 Stability of ivabradine and N-desmethylivabradine
2.6 提取回收率试验
取10mL玻璃离心管数支,分别加入不同量的伊伐布雷定和去甲伊伐布雷定标准溶液,以氮气流吹干,加入2.5mL空白血浆提取液,配制成含0.202 6、5.065、75.975μg/L伊伐布雷定血浆样品及含0.17、2.55、12.75μg/L去甲伊伐布雷定血浆样品,涡漩混匀后,按1.4.1处理,记录色谱图,计算峰面积比值fi(fi=As/Ai)。并计算每种浓度的平均值。
取10mL玻璃离心管数支,配成含0.202 6、5.065、75.975μg/L的含伊伐布雷定血浆标准样品及含0.17、2.55、12.75μg/L的去甲伊伐布雷定血浆标准样品,每种浓度各做5份,除不加内标外,按1.4操作,取上清液2.5mL,加入50μL内标标准液,涡漩后,于35℃水浴中以氮气流吹干,用200μL流动相复溶,以16 000 r/min离心3min,移取上清液至自动进样器,5 μL进样分析,记录色谱图,计算峰面积比值fs(fs=As/Ai)。将上述fs和的比值代入下式,即可求得伊伐布雷定的绝对回收率(R%),R%结果列于表3。
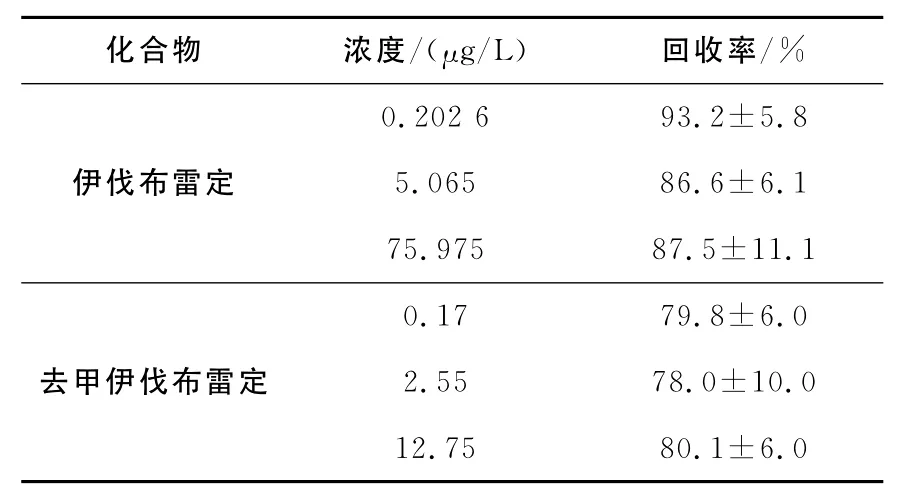
表3 伊伐布雷定、去甲伊伐布雷定的提取回收率Table 3 Recovery of ivabradine andN-desmethylivabradine
2.7 方法应用
应用本方法测定10名中国成年健康志愿者单剂量口服5mg盐酸伊伐布雷定后,不同时间血浆中伊伐布雷定和去甲伊伐布雷定的浓度,并计算药代动力学参数,其平均血药浓度-时间曲线示于图3。药代动力学参数结果为:伊伐布雷定t1/2:(5.18±1.20)h,AUC(0-48):(169.56±33.15)(μg·h)/L,Cmax:(35.88±8.88)μg/L,tmax:(1.08±0.53)h;代谢产物去甲伊伐布雷定t1/2:(9.91±1.24)h,AUC(0-48)(23.87±9.43)(μg·h)/L,Cmax为(3.11±1.62)μg/L,tmax:(1.30±0.26)h。

图3 健康志愿者口服5mg伊伐布雷定片后的平均血药浓度-时间曲线Fig.3 Mean plasma concentration-time profiles of ivabradine and N-desmethylivabradine after single oral dose of 5mg ivabradine hydrochloride tablets
3 讨论
目前国际上有3篇关于伊伐布雷定及去甲伊伐布雷定检测方法研究报道,其中1篇为荧光检 测 法[6],2 篇 为 质 谱 联 用 法[7-8]。 但 鉴 于 伊 伐布雷定及去甲伊伐布雷定的检测下限较低,采用质谱联用法较为妥当,但上述2篇研究报道均采用固相萃取处理方法,成本较高,不适用于大批样品的预处理。针对上述情况,本试验建立了液液萃取的样品预处理方法,成本低廉、重现性高、易于操作,且血浆中的杂质不干扰样品的测定。伊伐布雷定的标准曲线线性范围为0.101 3~101.3μg/L,去甲伊伐布雷定的标准曲线线性范围为0.085~25.5μg/L,线性关系良好;伊伐布雷定、去甲伊伐布雷定的高、中、低3个浓度的批内和批间精密度均小于15%;相对回收率在98.7~108.2%之间;伊伐布雷定、去甲伊伐布雷定血浆样品室温放置4h,-80℃下反复冻融3次,-80℃下冻存3个月及检测样品进样器放置4h条件下的稳定性良好,符合生物样品分析要求。此外,目前国际上有2篇关于伊伐布雷定与其他药物相互作用的文章[9-10],报道了肝药酶诱导剂卡马西平可提高伊伐布雷定的生物利用度高近80%,但主经肝药酶CYP3A4和CYP2C19代谢的奥美拉唑并不影响伊伐布雷定代谢,两者之间不存在任何相互作用,上述研究均提示在临床应用过程中需注意伊伐布雷定的应用,避免因药物相互作用而出现不良反应。
[1]FERRARI R,CARGNONI A,CECONI C.Antiischaemic effect of ivabradine[J].Pharmacology research,2006,53:435-439.
[2]BORER J S,FOX K,JAILLON P,et al.Ivabradine Investigators Group.Antianginal and antiischemic effects of ivabradine,an I(f)inhibitor,in stable angina:A randomized,double-blind,multicentered,placebo-controlled trial[J].Circulation,2003,107(6):817-823.
[3]LÓPEZ-BESCÓS L,FILIPOVA S,MARTOS R.Long-term safety and efficacy of ivabradine in patients with chronic stable angina[J].Cardiology,2007,108(4):387-396.
[4]RUZYLLO W,TENDERA M,FORD I,et al.Antianginal efficacy and safety of ivabradine compared with amlodipine in patients with stable effort angina pectoris: A 3-month randomised,double-blind,multicentre,noninferiority trial[J].Drugs,2007,67(3):393-405.
[5]SEBASTIAN N,HENNING E,ROBERT S H,et al.Reducing elevated heart rate in patients with multiple organ dysfunction syndrome by the If(funny channel current)inhibitor ivabradine MODIFY Trial[J].Clinical Research in Cardiology,2011,100(10):915-923.
[6]KLIPPERT P,JEANNIOT P,POLVE S,et al.Determination of ivabradine and its N-demethylated metabolite in human plasma and urine,and in rat and dog plasma by a validated high-performance liquid chromatographic method with fluorescence detection[J].Journal of Chromatography B,1998,719:125-133.
[7]FRANCOIS-BOUCHARD M,SIMONIN G,BOURSIER-NEYRET C.Simultaneous determination of ivabradine and its metabolites in human plasma by liquid chromatography-tandem mass spectrometry[J].Journal of Chromatography B,2000,745:261-269.
[8]RIESEN S C,NI W,CARNES C A,et al.Pharmacokinetics of oral ivabradine in healthy cats[J].J Vet Pharmacol Ther,2011,34(5):469-475.
[9]VLASE L,NEAG M,POPA A,et al.Pharmacokinetic interaction between ivabradine and carbamazepine in healthy volunteers[J].J Clin Pharm and Ther,2010,36(2):225-229.
[10]PORTOLéS A,CALVO A,TERLEIRA A,et al.Lack of pharmacokinetic interaction between omeprazole or lansoprazole and ivabradine in healthy volunteers:an open-label,randomized,crossover,pharmacokinetic interaction clinical trial[J].J Clin Pharmacol,2006,46(10):1 195-1 203.
Quantitative Determination of Ivabradine and N-Desmethylivabradine in Human Plasma by HPLC-MS/MS
JIA Yan-yan,LU Cheng-tao,SONG Ying,DING Li-kun,YANG Jing,CHEN Min-chun,LI Xue-qin,SONG Wei,ZHOU Lun,FENG Zhi-jun,WEN Ai-dong
(Department of Pharmacy,the First Affiliated Hospital of Fourth Military Medical University of PLA,Xi’an710032,China)
Ivabradine and N-desmethylivabradine in human plasma was determined by high performance liquid chromatography coupled with tandem mass spectrometry (HPLC-MS/MS).Diazepam was used as internal standard.Ivabradine and N-desmethylivabradine was separated on a Diamosil C18column(150mm×4.6mm×5μm).Electrospray ionization(ESI)source was applied,and multiple reaction monitoring(MRM)mode was operated in the positive mode with the monitor ions at m/z469.2→177.1for ivabradine,m/z455.2→177.1for N-desmethylivabradine and m/z285.1→193.1for the interna1standard,respectively.The linear calibration curve are obtained over the concentration range of 0.101 3—101.3μg/L for ivabradine and 0.085—25.5μg/L for N-desmethylivabradine.The limit of quantitation are 0.101 3μg/L and 0.085μg/L for ivabradine and N-desmethylivabradine,respectively.The inter-day and intra-day precision(RSD)is less than 15%.The average recoveries are above 75%.
ivabradine;N-desmethylivabradine;high performance liquid chromatography coupled with tandem mass spectrometry(HPLC-MS/MS);plasma concentration
O 657.63
A
1004-2997(2012)03-0081-06
2011-10-05;
2011-12-14
贾艳艳(1981~),女(汉),河北遵化人,主管药师,从事临床药理学研究。E-mail:jiayanyan-2004@hotmail.com。
文爱东(1965~),男(汉),陕西西安人,主任药师,从事临床药理学研究。E-mail:adwen-2004@hotmail.com
