血清中葡萄糖的测量比对—ID-LC-MS/MS法*
2012-01-08董晓杰徐蓓
董晓杰,徐蓓
(中国计量科学研究院化学所, 北京, 100013)
血清中葡萄糖的测量比对—ID-LC-MS/MS法*
董晓杰,徐蓓
(中国计量科学研究院化学所, 北京, 100013)
利用同位素稀释-液相色谱-质谱法(ID-LC-MS/MS)准确测定血清中葡萄糖含量。以[13C6]葡萄糖为内标,用重量法准确地与血清混合,离心沉淀蛋白后在碱性条件下与1-苯基-3-甲基-5-吡唑酮反应,以ZORBAX RX-SIL色谱柱分离,以乙腈-水(体积比25∶75)为流动相,使用电喷雾三重四极杆串联质谱多重反应监测模式(MRM)测定,同位素稀释的括号法进行定量。采用美国NIST的血清标准物质SRM 965b进行了确证,并用该方法参加JCTLM关于血清中葡萄糖含量的国际比对,测量值与均值的相对偏差分别为1.1%(A样),1.8%(B样),结果在等效范围内。
同位素稀释质谱法;JCTLM国际比对;血清;葡萄糖
血清葡萄糖对高糖、低糖血症的诊断、治疗、愈后监测具有重要意义,因此其含量测定是临床实验室频率最高的实验之一[1]。临床工作中常发现不同的实验室、同一实验室不同时间检测结果常因检测仪器、试剂、校准物、方法多样性等原因缺乏可比性。通过建立准确可溯源的血清葡萄糖测定参考方法,并用参考方法进行比对测量,进而考察已有参考方法的可比性,以保证量值传递结果的准确性和可靠性,使检验结果在准确、科学的基础上实现统一、互认[2]。
国际检验医学溯源性联合委员会(JCTLM)是在2002年由国际计量局(BIPM)、国际临床化学和检验医学联合会(IFCC)、国际实验室认可委员会(ILAC)共同倡导成立的,旨在建立一个世界性的溯源系统平台,推动和指导国际认可和接受的检验医学测量等效性的建立并溯源至适当的测量标准。它的工作成果表现在已经发布的国际计量局JCTLM数据库和IFCC 检验医学参考实验室外部质量评价计划(RELA )的比对结果[3]。目前已经有17家中国实验室通过该平台考查自己的能力。本次比对是中国计量科学研究院第二次参加该计划,通过比对证明了在血清葡萄糖测量方面的检测能力。
1 实验部分
1.1 主要仪器与试剂
液相色谱-串联质谱仪:6410B型,美国Agilent公司;
涡旋振荡器、离心机;
葡萄糖标准物质SRM 917b:纯度为(99.7±0.2)%,美国国家标准与技术研究院;
[13C6]葡萄糖:美国Cambridge Isotope Laboratories公司,标示同位素丰度99%;
衍生试剂:1-苯基-3-甲基-5-吡唑酮(PMP):纯度99%,美国Sigma公司;
无水乙醇、乙腈、氯仿:HPLC级,德国Merck公司;
血清样品:SRM 965b血清;
由JCTLM/IFCC提供A、B两个浓度水平的人血清冻干粉比对样品(2010年)。
1.2 样品前处理条件
样品前处理方法参照了张天娇等[4]建立的IDLC-MS/MS法测定血清葡萄糖的方法:以[13C6]葡萄糖为内标,用重量法准确地与血清混合,用无水乙醇除去蛋白后与衍生试剂1-苯基-3-甲基-5-吡唑酮(调pH值至9)反应,反应后静置冷却至室温,用乙酸溶液中和反应系统。加入超纯水和氯仿,旋涡振荡萃取两次,水相用0.22 μm的滤膜过滤后进行液相色谱-质谱的测定。
1.3 仪器条件
(1)色谱条件
色谱柱:Agilent ZORBAX RX-SIL(150 mm×2.1 mm,5μm);流动相:乙腈-水(含乙酸,pH=3.5)(体积比为25∶75),流速为0.3 mL/min;进样量:1 μL;色谱柱温度:30℃。
(2)质谱条件
ESI源,三重四极杆串联质谱测定,正离子多重反应监测扫描(MRM)模式。Fragmentor:165 V;CE:45 V;Delta EMV:600;雾化气压力:0.28 MPa;干燥气温度:350℃;干燥气流速:9 L/min;毛细管电压:4 000 V;扫描时间:407 ms;括号法定量;MRM监测的母离子、子离子分别为葡萄糖m/z511.3~175.2,[13C6]葡萄糖m/z517.3~175.2。
1.4 分析过程
每个样品与其对应的标准样品同一批测定。分析时以低标、样品、高标的次序进样,每个样品或标准重复进样测定3次,计算时以所得结果的均值作为一个有效数据。
1.5 结果计算
样品中葡萄糖的浓度比和峰面积比在两个校正标准之间符合线性关系,血清中葡萄糖的质量浓度可由以下公式计算:

式中:
c——血清中葡萄糖的浓度,mmol/L;
IS——血清样品中葡萄糖与标记葡萄糖的峰面积比;
WH——高标样品中葡萄糖与标记葡萄糖的质量比;
WL——低标样品中葡萄糖与标记葡萄糖的质量比;
IL——低标样品中葡萄糖与标记葡萄糖的峰面积比;
IH——高标样品中葡萄糖与标记葡萄糖的峰面积比;
MIS——加入血清样品中标记葡萄糖的质量,mg;
MSer——待测血清样品的质量,g;
Ds——血清的密度,g/mL。
1.6 方法验证
在测量比对样品前用本法测定了美国NIST标准物质SRM 965b水平3,平行测定3份。实测值与证书参考值6.575 mmol/L之间的相对偏差为0.4%,在标准值不确定度范围内,证明方法的准确性良好。
2 结果与讨论
2.1 比对样品测量结果
通过测定高标校准混合液、血清样品以及低标校准混合液中葡萄糖与标记葡萄糖峰面积比,以及相应样品对应的质量比,利用括弧法即可计算血清样品葡萄糖的准确含量。每个样品均插在高、低标校准样品中测量,至少保证从低到高、从高到低两轮校准测量。测量结果见表1、表2。

表1 血清样品A中葡萄糖含量测量结果 mmol/L
2.2 测量结果不确定度
测量涉及冻干血清样品复溶,样品及校准溶液、内标溶液的称量,血清密度的测量等过程,各不确定分量评定结果见表3。
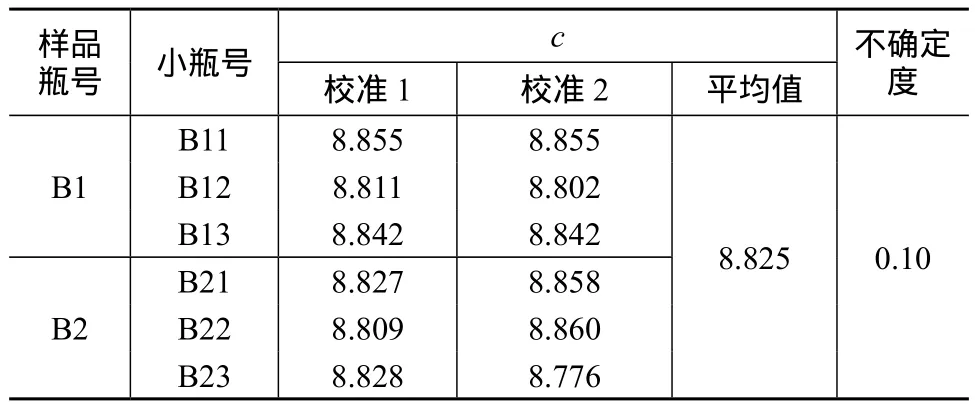
表2 血清样品B中葡萄糖含量测量结果 mmol/L

表3 不确定度分量及合成不确定度 %
2.3 参加测量比对实验室测量结果
本次比对样品中葡萄糖含量有两个浓度,记为A样、B样。共有16个实验室参加此次比对,所有实验室的测量结果见图1。由图1可知,中国计量科学研究院测定结果在等效范围内。
表4给出了使用同位素稀释质谱法的各实验室的测量结果。中国计量科学研究院为92号,是唯一采用ID-LC-MS/MS的实验室。按质谱方法统计,测量值与均值的差分别为1.1%(A样),1.8%(B样)[5],在等效范围内。

图1 血清中葡萄糖浓度的比对结果图

表4 血清中葡萄糖浓度的比对结果(同位素稀释质谱法)
[1]戴新华,齐韬,杨梦瑞,等.血清中葡萄糖含量的测定方法及其研究进展[J].化学分析计量,2008,17(3): 78-80.
[2]陈文祥,申子瑜,杨振华,等.临床生化检验参考方法的主要作用[J].中华检验医学杂志,2008,31(3): 245-249.
[3]徐蓓, 陈文祥. 临床检验溯源系统的建立// 2007中国计量论坛论文集 , 2007: 22-25.
[4]张天娇,张传宝,张江涛,等.同位素稀释液相色谱串联质谱法测定血清葡萄糖[J].中华检验医学杂志,2010,33(1): 75-80.
[5]http://www.dgkl-rfb.de:81/4Daction/g_search_RELA?sel ectAnalyte=Glucose&submitplot=show+result+plot&ses sion_id=00000000000000000000&cur_year=2010&LabCode=000
International Comparison on the Determination of Serum Glucose by ID-LC-MS/MS
Dong Xiaojie, Xu Bei
(National Institute of Metrology,National Research Center for CRMs, Beijing 100013,China)
The determination of glucose in human serum by liquid chromatography-isotope dilution-mass spectrometry was described.[13C6]glucose as internal standard was added to serum samples and equilibrated with endogenous glucose. Serum proteins were removed by a precipitation with anhydrous ethanol. Serum glucose and the internal standard were then reacted with l-phenyl-3-methyl-5-pyrazolone,separated by ZORBAX RX-SIL column using isocratic mobile phase of acetonitrile-water(volum ratio was 25∶75). A tandem mass spectrometer equipped with an electrospray ionization source operated in multiple reaction monitoring (MRM) mode,and the results of determination were calculated from peak area ratios by the bracketing method based on the theory of isotope dilution analysis. The method was validated by analyzing NIST serum reference material SRM 965b. International comparision of JCTLM for glucose content in serum was carried out by the method. The relative deviation between measured value and the mean were 1.1% (A sample),1.8% (B sample).
isotope dilution; mass spectrometry; international comparison of JCTLM; serum; glucose
O624
A
1008-6145(2012)04-0081-03
10.3969/j.issn.1008-6145.2012.04.025
*国家科技支撑项目(2011BAI02B05)
联系人:徐蓓;E-mail: xubei@nim.ac.cn
2012-04-21
