一个新的二维氰基桥连的混价铜Cu(I)/Cu(II)配位聚合物的合成、结构和性质研究
2011-10-13白丽霞天津渤海职业技术学院天津300221
白丽霞(天津渤海职业技术学院天津300221)
刘欣(南开大学天津300072)
一个新的二维氰基桥连的混价铜Cu(I)/Cu(II)配位聚合物的合成、结构和性质研究
白丽霞(天津渤海职业技术学院天津300221)
刘欣(南开大学天津300072)
设计合成了一个CN-连接的稳定的Cu(I)/Cu(II)的混价配位聚合物,测定了它的晶体结构,发现它拥有非常奇特的空间结构,并对它进行了光谱性质、电化学性质和磁学性质的研究。
混价铜配位聚合物晶体结构光谱电化学磁学性质
水溶液中的Cu(II)在有氰根CN-存在的情况下,很容易被还原成Cu(I),虽然C-Cu(II)键联的Cu(II)的化合物在室温下不稳定,但是研究表明,[1]选择具有很好的σ电子给予特性的配体,比如氨、吡啶,就可能稳定Cu(II)-CN配位键。最近几年,含有Cu(II)-CN配位键的配合物陆续被报道,[2]给金属有机配合物的发展注入了新的活力。含有CN-桥连的Cu(I)/Cu(II)混合价配合物的文献报道[3]非常多,这种混价铜Cu(I)/Cu(II)配合物往往拥有非常奇特的结构,引起了化学工作者极大的兴趣。在合成此类配合物的过程中,无论是通过Cu(I)的氧化还是通过Cu(II)的还原,选择合适的端基配体对于形成配合物新奇的结构以及配合物能否稳定存在有一定影响。目前,以CN-桥连稳定的Cu(II)/Cu(I)混价配位聚合物的报道并不多见,本文设计合成了一种CN-连接的稳定的Cu(I)/Cu(II)的混价配位聚合物,测定了它的晶体结构,并进行了光谱性质、电化学性质和磁学性质的研究。混价金属铜配位聚合物对于合成新型功能性材料方面有非常重要的理论指导意义,这些配合物在很多领域,比如沸石材料、分子的选择性反应、离子交换、导电性材料、催化剂、新型磁性材料等方面都有很大的应用潜力。[4-6]
1 实验部分
1.1 配位聚合物的合成
[Cu(I)Cu(II)(CN)3(py)3]2n:将Cu(ClO4)2·6H2O(74.1 mg,0.2mmol)的10.0mL水溶液和5.0m L的吡啶(py)分别滴入含有间苯基二乙腈(31.2mg,0.2mmol)的10.0m L的甲醇溶液中,室温下搅拌4 h,得到深蓝色溶液,过滤,滤液静置,在常温下缓慢挥发溶剂,一个月后得到适合X射线衍射分析的深蓝色块状单晶。产物产率约为26%,元素分析结果(%):(实验值)C,48.78;H,3.39;N,18.88;(理论值)C,48.82;H,3.42;N,18.99。
1.2 配位聚合物的结构
配位聚合物[Cu(I)Cu(II)(CN)3(py)3]2n的X射线衍射分析和晶体学数据列于表1,主要键长键角数据列于表2。

表1 配位聚合物[Cu(I)Cu(II)(CN)3(py)3]2n的X射线衍射晶表1体学数据

表2 配位聚合物[Cu(I)Cu(II)(CN)3(py)3]2n的主要键长键角数据
配位聚合物[Cu(I)Cu(II)(CN)(3py)3]2n的分子结构图见图1。它的空间结构是由24元环和12元环相互交替构成的,但是这些环并不是处于一个平面上(见图2)。每个24元环包含4个Cu(I)中心和4个Cu(II)中心,而每个12元环包含2个Cu(I)中心和2个Cu(II)中心。Cu(I)中心和Cu(II)中心之间均通过CN-连接起来,形成Cu(II)-NC-Cu(I)单元相互交替的环状结构。图2中,对应于Cu(II)的原子为Cu(2)的所有原子,对应于Cu(I)的原子为Cu(1)的所有原子。Cu(I)-Cu(II)之间的距离介于5.050~5.197之间。Cu(II)-NC-Cu(I)单元也不是线形结构,Cu(II)-N-C和Cu(I)-C-N的键角分别为170.6°和178.3°。Cu(I)中心的配位环境CuC3N为四面体的配位几何构型,在Cu(I)的4个配位原子中,来自于吡啶配体的1个N原子占据四面体中的顶点位置,而3个C原子占据四面体中三角底平面的3个顶点位置。Cu(II)中心的配位环境CuN5却是扭曲的三角双锥的结构。对于Cu(II)中心的5个配位原子中,来自于吡啶配体的2个N原子占据三角双锥的两个顶点,而另外的3个C原子均来自于CN-,它们占据三角双锥的三角平面的3个顶点。在分子结构中,12元环中的4个Cu原子处于1个平面上,而24元环中的4个Cu(II)原子和4个Cu(I)原子分别各自处于1个平面上,2个平面的二面角为14°。围绕Cu(II)中心的3个桥连CN-,两两与Cu(II)形成的键角即∠N-Cu(II)-N)分别为99.5°、106.3°、154.1°,同样围绕Cu(I)中心的3个桥连CN-,两两与Cu(I)形成的键角即∠C-Cu(I)-C分别为113.0°、113.2°、120.8°。由环构成的面与面之间的距离是7.734见图3)。
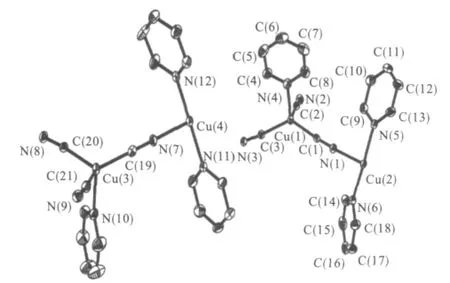
图1 配位聚合物[Cu(I)Cu(II)(CN)3(py)3]2n的分子结构(氢图1原子略掉)
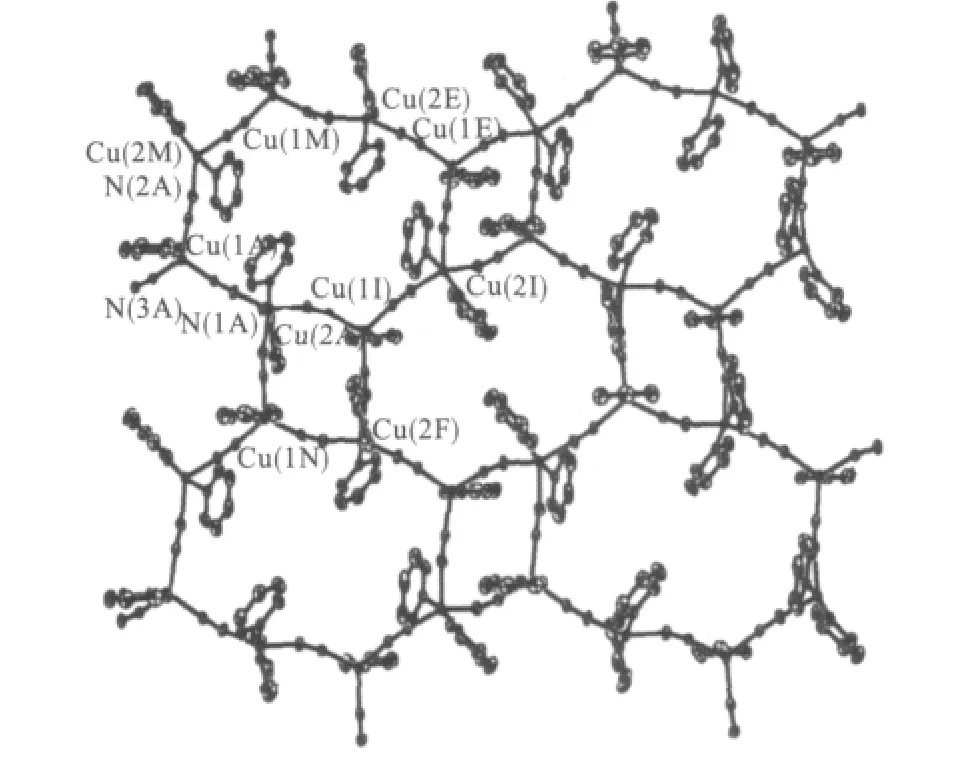
图2 配位聚合物[Cu(I)Cu(II)(CN)3(py)3]2n的空间无限二维非平面结构

图3 配位聚合物[Cu(I)Cu(II)(CN)3(py)3]2n的二维层状结构
2 结果与讨论
2.1 IR(红外)光谱
配位聚合物[Cu(I)Cu(II)(CN)3(py)3]2n的IR光谱图中,在2 150 cm-1处出现的尖锐的强峰被指派为CN-的伸缩振动υ(C≡N),符合CN-桥连的配位化合物的红外吸收峰的位置。1 600 cm-1、1 450 cm-1处的吸收峰被指派为吡啶环上的C=C和C=N伸缩振动。710 cm-1处的吸收峰被指派为吡啶环上的δ(C-H)弯曲振动。
2.2 UV-vis(紫外-可见)光谱
测定了室温下配位聚合物[Cu(I)Cu(II)(CN)3(py)3]2n在DMF(N,N-二甲基甲酰胺)溶液中的室温UV-vis谱。在414 nm(ε=2.2×102M-1cm-1)处的吸收峰被指派为配合物的d-d(2E′←2A′1)跃迁,此吸收峰的位置对应于Cu(II)N5的三角双锥结构,符合文献[7]所报道的铜三角双锥构型配合物的电子光谱特征。在271 nm(ε=5.1×103M-1cm-1)处的强吸收峰被指派为配体π→π的跃迁。
2.3 循环伏安性质
为了研究配合物的电化学行为,以经无水无氧处理过的DMSO(二甲基亚砜)作溶剂,0.1 M(n-Bu)4NBF4(自制)为支持电解质,被测活性物质的浓度为10-3~10-4M,扫描速率为200mV/s,采用三电极系统,工作电极为铂电极(Φ=200μ),参比电极为饱和甘汞电极,对电极为铂丝电极,测量温度为室温,在这样的条件下测定了配位聚合物[Cu(I)Cu(II)(CN)3(py)3]2n的循环伏安曲线(整个实验过程中均通高纯Ar气除O2,并用Al2O3打磨工作电极)。操作时以蒸馏水、无水乙醇、丙酮作清洗剂。[8-9]由循环伏安曲线(见图4)可知,所测配合物在-2 000~500mV范围内有一个氧化还原过程,Epc=-245mV,Epa=-150mV,E1/2=-197.5mV,ΔEp=95 mV,ΔEp<100mv表示这一个氧化还原过程为可逆过程(-1 000mV附近的氧化还原峰为支持电解质的峰)。这一氧化还原过程与下面的反应有关:

图4 配位聚合物[Cu(I)Cu(II)(CN)3(py)3]2n的循环伏安曲线
2.4 ESR谱
在室温与110 K下,测定了配位聚合物[Cu(I)Cu(II)(CN)3(py)3]2nX波段的ESR固体谱,图5(a)和(b)分别为配合物在低温110 K的ESR谱图和对它的拟合谱图。室温和低温的谱图形状相似,均没有出现超精细结构,只出现双重峰。对低温的实验谱进行拟合,拟合的结果为gx=2.16,gy=2.12,gz=2.07(110 K);拟合结果中gx、gy>gz,表明未成对电子位于dz2轨道上。这与晶体结构中Cu(II)原子的扭曲三角双锥构型一致。

图5 (a)配位聚合物[Cu(I)Cu(II)(CN)3(py)3]2n在低温110 K图5(a)下的ESR谱

图5 (b)配位聚合物[Cu(I)Cu(II)(CN)3(py)3]2n在低温110K图5(b)下的ESR拟合谱
2.5 磁性
在2~300 K的温度范围内测定了配位聚合物[Cu(I)Cu(II)(CN)3(py)3]2n的变温磁化率,χm-T和1/χm-T曲线图见图6。从数据中可以计算得知,室温下(298 K)配合物的有效磁矩μeff为1.72 B.M.(波尔磁子),略低于单核Cu(II)的仅自旋值(1.73 B.M.)。随着温度的降低μeff也随着降低为1.64 B.M.(73.49 K),这表明在两个Cu(II)之间存在着反铁磁相互作用。低温区μeff值的升高,可能是由于磁不纯引起的。根据Heisenberg自旋哈密顿算符,采用Cu(II)等间隔链的磁化率经验公式:
χM其中y=J/KT,N为阿佛加得罗常数,K为波尔兹曼常数,β为波尔磁子,g为g因子,T为绝对温度,J为双核单元的磁交换作用参数。使用最小二乘法技术使实验值与理论值达到最佳拟合,得到相应磁参数和拟合因子拟合结果:g=2.00,J=-0.067 cm-1,R=3.6×10-3。J<0表明双核金属之间存在着弱的反铁磁相互作用。这是由于在配合物中,Cu(II)被CN-Cu(I)-CN桥连单元隔开,使Cu(I)离子含有抗磁,而且两个磁性核Cu(II)之间的距离比较长,为8.481,造成了如此弱的反铁磁相互作用。■

图6 配位聚合物[Cu(I)Cu(II)(CN)3(py)3]2n的变温磁化率图6χM-T(○)和1/χM-T(□)曲线图
[1]Ian G.Dance,Philip A.W.Dean,etal.Gas-phase metal cyanide chemistry:formation,reactions and proposed linear structures of copper(I)and silver(I)cyanide clusters[J].Inorg.Chem.,1994(33):61-62.
[2]Yingjun Zhao,Maochun Hong,Weiping Su,etal.Synthesis and characterization of two copper cyanide complexes with hexagomal Cu6 unis[J].J.Chem.Soc.,Dalton Trans.,2000(16):85.
[3]Enrique Colacio,Raikko Kivekas,Francesc Lioret.Architecture dependence on the steric constrains of the ligand in cyano-bridged copper(I)-copper(II)mixed-valence polymer compounds containing diamines:crystal structuresand spectroscopic and magnetic properties[J].Inorg.Chem.,2002(41):41-51.
[4]S.F.Huang,H.H.Wei,Yu Wang.A new cyano-bridged one-dimensional polymeric mixed-valence Cu(II)/Cu(I)complex formed f rom reduction of a binuclear Cu(II)complex with sodium cyanide[J].Polyhedron,1997(10):17-47.
[5]Agnus,Y.,Gisselbrecht,J.P.,etal.Mixed-valence Cu(I)Cu(II)macrocyclic complex:a result of a Cu(II)-promoted oxidation of aziridines into cyanide[J].J.Am.Chem.Soc.,1989(111):14-94.
[6]Kappestein,C.,Schubert,U.X-ray crystal structure of two new mixed-valence copper cyanide complexes:unusual bi-co-ordinated copper(I)atoms in polymeric networks[J].J.Chem.Soc.,Chem.Commun.,1980(5):11-16.
[7]Z.L.Lu,C.Y.Duan,Y.P.Tian,etal.Synthesis characterization and crystal structure of tris(2-aminoethyl)amine copper complex with 4-dimethylaminopyridine ligand[J].Polyhedron,1996(11):17-69.
[8]周伟舫.电化学测量[M].上海:上海科学技术出版社,1985.
[9]高小霞.电化学分析导论[M].北京:科学出版社,1986.
注:本文为国家自然科学基金资助项目论文(批准号:20071020)。
2011-01-09
