三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物的研究进展
2011-09-29卢艳梅乐学义
卢艳梅 乐学义*,,2
(1华南农业大学理学院应用化学系,广州 510642)(2华南农业大学生物材料研究所,广州 510642)
综 述
三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物的研究进展
卢艳梅1乐学义*,1,2
(1华南农业大学理学院应用化学系,广州 510642)(2华南农业大学生物材料研究所,广州 510642)
三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物可作为化学核酸酶、SOD模拟物及植物生长抗逆增产剂等而吸引了科学家们的广泛关注。本文综述了国内外对三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物的研究,着重介绍了配合物的结构及其应用等。
铜(Ⅱ)配合物;芳胺;L-α-氨基酸
铜是生物体内重要的微量元素,广泛存在于动物、植物和微生物体内,并且通常与生物配体(氨基酸、小肽、蛋白质、核苷酸和核酸等)形成稳定的混配配合物,在生命过程中(酶的催化、物质的储存和运送以及铜离子的转运等)起着极其重要的作用[1]。芳胺具有生物分子中咪唑、嘌呤碱和嘧啶碱等配位基团类似的配位性质,并且本身具有抗菌、抗癌等生物活性,常常被用来设计、合成作为金属酶及蛋白的模型化合物[2-5]。L-α-氨基酸是蛋白质及相关代谢产物的结构单元,是生命活动所不可缺少的营养物质[6-7],作为配体不仅有助于提高配合物的生物活性,而且能够提高配合物在水中的溶解性,从而有助于减小配合物作为药物时在体内毒副作用及细胞对药物吸收效果不好等不足之处。
基于上述原因,人们研究了系列该类配合物在水溶液中的热力学及动力学性质[8-20],并深入研究了这些配合物的结构、性质及其应用等。研究发现,这类配合物对DNA具有良好的插入断裂作用,有可能作为新型DNA结构探针、DNA足迹试剂和DNA断裂试剂;对超氧阴离子自由基(O2-·)具有催化歧化作用,可作为超氧化物歧化酶模拟物;有助于提高作物抗逆境(干旱、盐碱等)作用可作为植物生长抗逆增产剂等。因此,研究三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物不仅具有理论意义而且潜在着广阔的应用前景。本文结合本课题组多年来的研究工作就国内外对三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物研究的进展,尤其是配合物的结构及其应用等作一综述。
1 三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物的结构
自Kwik等[21]1980年合成出以bipy、phen为芳胺配体的三元芳胺-铜(Ⅱ)-L-α-氨基酸系列配合物以来,国内外学者利用溶剂挥发法、液相扩散法及重结晶等多种方法合成了系列三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物,并通过元素分析、红外光谱、紫外可见光谱、X-射线单晶衍射等方法对这些配合物进行了结构表征。已合成的三元芳胺-铜-(Ⅱ)-L-α-氨基酸配合物[22-82]如表1所示。
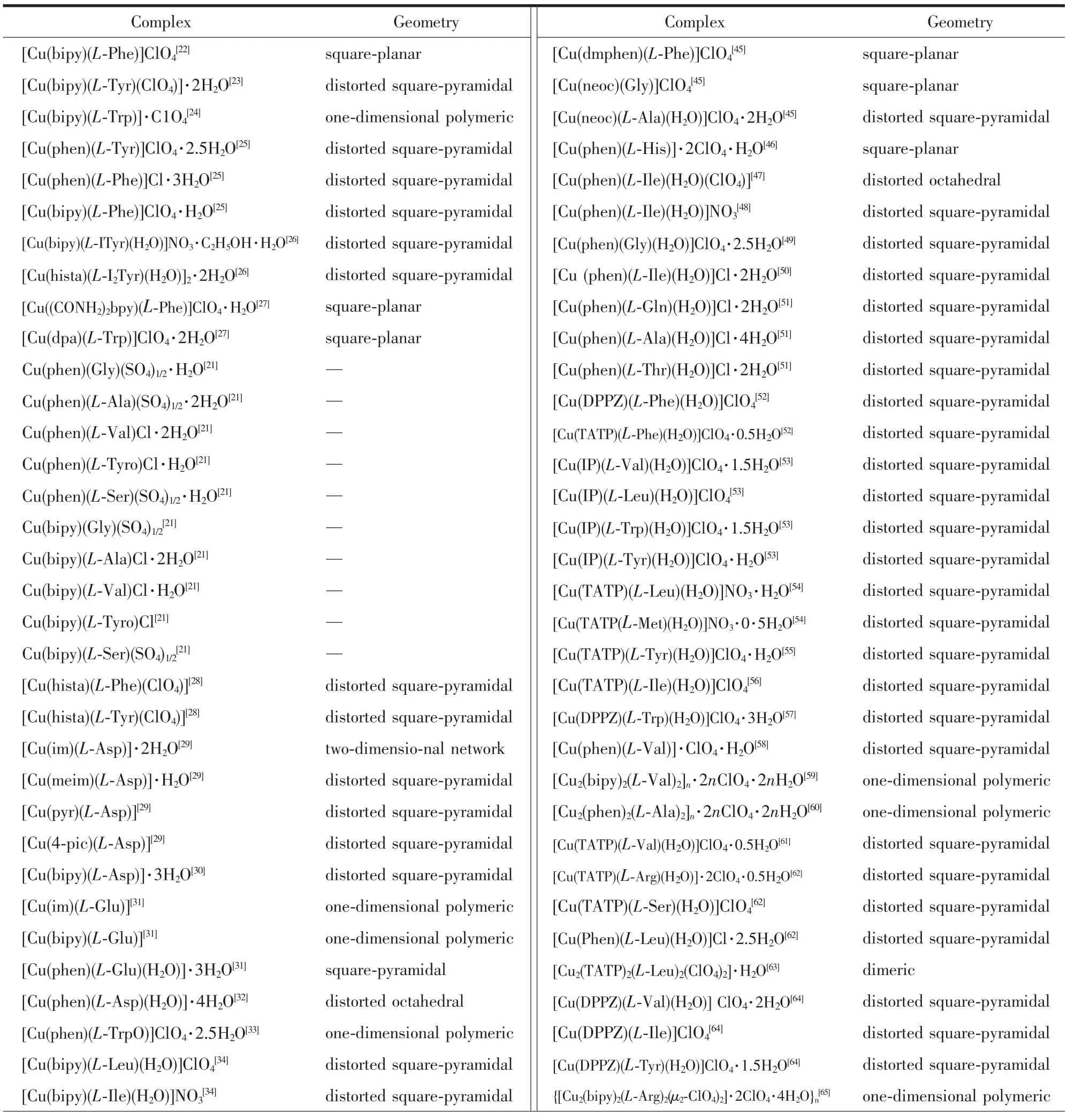
表1 已合成的三元 芳胺-铜(Ⅱ)-L-α-氨基酸 配合物及其结构Table1 Synthesised ternary copper(Ⅱ) complexes containing aromatic amine and L-α-amino acid and their molecular structures in the literatures[22-78]

续表1
表1中三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物分子中芳胺配体分子结构式如图1所示。
研究表明,三元芳胺-铜(Ⅱ)-L-α-氨基酸 配合物常见的分子结构类型有平面四边形、变形四方锥、变形八面体、二聚体、一维链状和二维网状结构等。
1.1 平面四边形结构
本课题组周晓华等[46]应用溶剂挥发法由phen、Cu(ClO4)2和L-His合成了配合物[Cu(phen)(L-His)]·2ClO4·H2O,X-射线单晶衍射测定结果表明该配合物分子具有平面四边形结构(图2)。中心Cu(Ⅱ)离子与配体phen的N1,N2及L-His的N3,O1形成四配位的变形平面四边形结构。配合物中L-His咪唑环上的N原子(N4,N5)未参与配位,而与邻近的平衡离子ClO-4通过结晶水分子(O1w)形成分子内氢键(图2中虚线所示):N5…O1w键长为 0.2757 nm,O9…O1w键长为0.2804 nm。
Yamauchi等合成的配合物[Cu(bipy)(L-IPhe)]Cl O4[22]和 [Cu((CONH2)2bpy)(L-Phe)]ClO4·H2O[27]、Su 等[45]合成的配合物[Cu(dmphen)(L-Phe)]ClO4及[Cu(neoc)(Gly)]ClO4,通过X-射线单晶衍射测定发现均具有上述类似的配位结构。
Yamauchi等[27]合成的另一个配合物[Cu(dpa)(LTrp)]ClO4·2H2O亦具有变形平面四边形结构(图3),不同之处在于dpa与中心Cu(Ⅱ)离子配位形成一个六元环,而其它配合物的芳胺配体与Cu(Ⅱ)离子配位形成五元环。
另外,Bhattacharya等[74]合成了系列[Cu(Ⅱ)(芳胺)(L-α-氨基酸)]BPh4型配合物,通过元素分析、红外光谱、紫外光谱及磁性测定等方法研究初步推测为变形平面四边形结构。
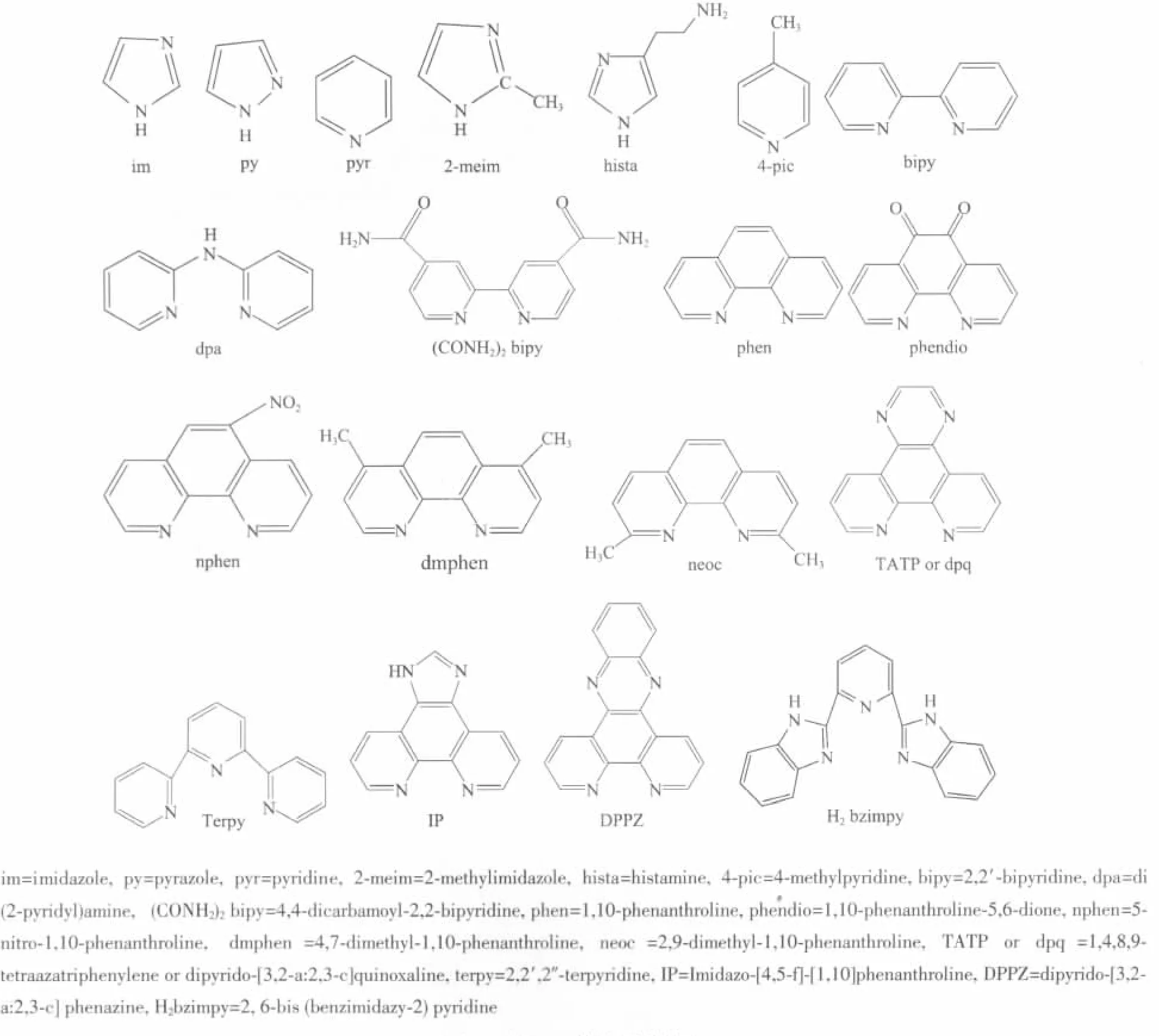
图1 芳胺配体分子结构式Fig.1 Molecular structures of aromatic amine ligands

图2 配合物[Cu(Phen)(L-His)]·2ClO4·H2O的分子结构Fig.2 Molecular structure for complex[Cu(Phen)(L-His)]·2ClO4·H2O
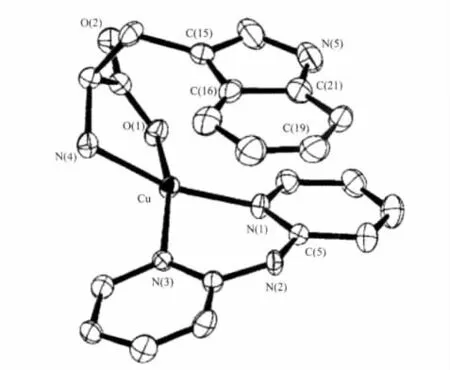
图3 配合物[Cu(dpa)(L-Trp)]ClO4·2H2O的分子结构Fig.3 Molecular structure for complex[Cu(dpa)(L-Trp)]ClO4·2H2O
1.2 变形四方锥结构
综合数十种三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物单晶测定解析结果,发现变形四方锥构型是该类配合物分子中铜(Ⅱ)离子最常见的配位结构。
Antolini 等[30]合 成 了 配 合 物[Cu(bipy)(L-Asp)]·3H2O,结构研究发现,该配合物具有变形四方锥配位结构(图4)。中心Cu(Ⅱ)离子与bipy的2个N原子、L-Asp离子其中1个α-甘氨酸部分的氨基N原子和羧基O原子配位形成四方锥的底面,水分子O原子位于四方锥的顶点。Antolini等[31]合成的另1个配合物[Cu(phen)(L-Glu)(H2O)]·3H2O也具有类似的变形四方锥结构(图5),不同之处在于该配合物晶胞中具有2个独立的配合物分子,这2个配合物分子中的键长及键角稍有不同。
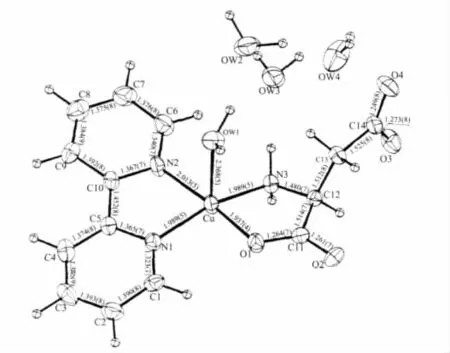
图4 配合物[Cu(bipy)(L-Asp)(H2O)]·3H2O的分子结构Fig.4 Molecular structure for complex[Cu(bipy)(L-Asp)(H2O)]·3H2O
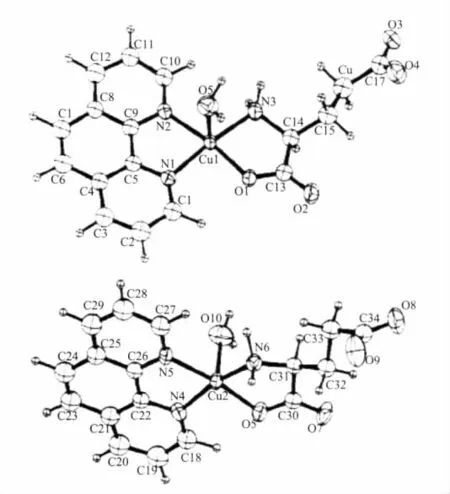
图5 配合物[Cu(phen)(L-Glu)(H2O)]·3H2O的分子结构Fig.5 Molecular structure for complex[Cu(phen)(L-Glu)(H2O)]·3H2O
近年来,本课题组合成并研究了系列具有此类结构的三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物[46-65]。在这些配合物中,芳胺中2个氮原子、L-α-氨基酸的氨基氮原子及其羧基上1个氧原子位于四方锥底面位置上,顶点一般为 H2O 分子或阴离子(NO-3、ClO-4、Cl-)。如乐学义等[55]用重结晶方法得到配合物[Cu(TATP)(L-Tyr)(H2O)]ClO4·H2O, 结 构 测 定 表 明 ,Cu(1)与TATP,L-Tyr及水分子配位形成五配位的变形四方锥结构(图 6)。TATP(N,N)与 L-Tyr(N,O)在四方锥底面上参与配位,而H2O的O原子在顶点上参与了配位。较为有趣的是,该配合物除了存在分子内芳环间堆积作用外,晶胞中α轴方向上邻位分子间L-Tyr侧链上苯环与TATP芳环间也存在着显著的分子间堆积作用,两芳环平面间二面角为1.15°,平面间质心距离为0.335 nm。这些芳环堆积及分子间键作用类似于稳定DNA双螺旋结构的碱基之间的作用。
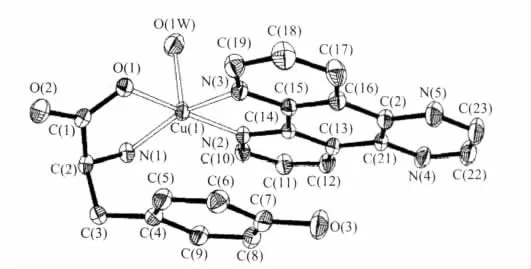
图6 配合物[Cu(TATP)(L-Tyr)(H2O)]ClO4·H2O的分子结构Fig.6 Molecular structure for complex[Cu(TATP)(L-Tyr)(H2O)]ClO4·H2O
Yamauchi[22,24-25,28]、Antolini[27-31]、Chakravarty[37-43]、Guo[69]和Chetana[34-36]等课题组分别合成的系列三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物以及周建良等[72]合成的配合物[Cu(DPPZ)(Gly)(H2O)]·NO3·H2O 均具有与本课题组所研究配合物类似的变形四方锥构型,并发现相关的键长和键角均相近。
Subramanian等[71]研究发现,配合物[Cu(bipy)(LHis)]ClO4·1.5H2O具有特殊的变形四方锥配位结构(图 7)。 在此配合物分子中,bipy(N,N)与 L-His(N,O)配位于四方锥底面上,而在顶点位置上参与配位的是L-His咪唑环上的N,使得该配合物分子中L-α-氨基酸以三齿配体形式与中心Cu(Ⅱ)离子配位。
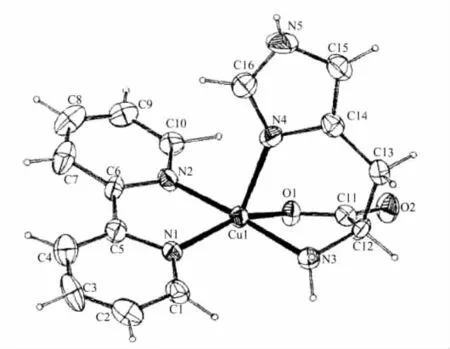
图7 配合物[Cu(bipy)(L-His)]ClO4·1.5H2O的分子结构Fig.7 Molecular structure for complex[Cu(bipy)(L-His)]ClO4·1.5H2O
此外,Su等[45]通过研究配合物[Cu(bipy)(Gly)(H2O)]ClO4·H2O、[Cu(neoc)(L-Ala)(H2O)]ClO4·2H2O 等在甲醇中的UV-Vis光谱并结合ESR光谱及在乙腈中的摩尔电导率,推测这些配合物分子具有变形四方锥配位结构。
1.3 变形八面体结构
1986年,Antolini等[32]合成了配合物[Cu(phen)(L-Asp)(H2O)]·4H2O(图8)。在该配合物分子结构中,Cu(Ⅱ)离子处于六配位的拉长八面体配位环境中,位于八面体赤道平面上4个配位原子为配体L-Asp中的氨基N原子和一个α-羧基O原子、及phen中2个N原子,八面体的2个轴向位置分别由H2O的O原子和作为三齿配体的L-Asp中的β-羧基O原子占据。

图8 配合物[Cu(phen)(L-Asp)(H2O)]·4H2O的分子结构图Fig.8 Molecular structure for for complex[Cu(phen)(L-Asp)(H2O)]·4H2O
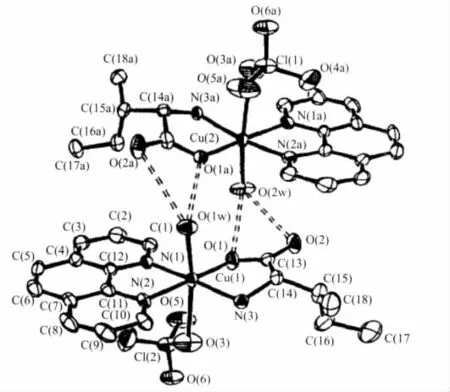
图9 配合物[Cu(phen)(L-Ile)(H2O)(ClO4)]的分子结构Fig.9 Molecular structure for complex[Cu(phen)(L-Ile)(H2O)(ClO4)]
本课题组刘小平等[47]在甲醇-水混合液中合成了配合物[Cu(phen)(L-Ile)(H2O)(ClO4)]。X-射线单晶衍射结果表明:该配合物分子中Cu(Ⅱ)离子也具有拉长八面体配位结构(图9),其中配体 L-Ile(N,O)与phen(N,N)处于八面体赤道平面上,而H2O(O)与ClO4-(O)分别位于八面体的2个顶点。配合物在乙腈中的摩尔电导率为 131.036 S·cm2·mol-1, 显示该配合物是1∶1型电解质,表明ClO4-的O配位原子配位较弱,这可以从Cu(1)与O(3)的键长为2.811 nm得到证实。另外,该配合物晶体中包含2个配位结构类似的配合物分子,相应的键长键角有一定差别,两分子间以镜面反对称方式交错重叠,双分子间由H2O配体与L-Ile羧基氧形成氢键缔合在一起(图9中虚线所示)。
1.4 二聚体
本课题组乐学义等[63]由 TATP、Cu(ClO4)2和LLeu合成了双核配合物[Cu2(TATP)2(L-Leu)2(ClO4)2]·H2O(图10)。晶体结构测定结果表明,每个晶胞中含有2个独立的双核配合物分子。配合物分子中的2个Cu(Ⅱ)离子的配位结构不一样,Cu2和Cu4具有变形四方锥的配位结构,TATP(N,N)与 L-Leu(N,O)位于赤道平面,ClO-4在轴向参与配位;Cu1和Cu3除与上述的原子配位外,还与邻近分子中L-Leu羧基上的一个O原子配位而形成具有变形八面体的配位结构。

图10 配合物[Cu2(TATP)2(L-Leu)2(ClO4)2]·H2O的分子结构Fig.10 Molecular structure for complex[Cu2(TATP)2(L-Leu)2(ClO4)2]·H2O
1.5 一维链状结构
在已合成的三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物中,一维链状亦是一类较为多见的结构。研究发现,在这些一维链状聚合物中,未参与配位的羧基O原子通过键合到邻近的Cu(Ⅱ)离子而起桥联作用。起桥联作用的羧基O原子所占据的位置因芳胺不同而存在差异,在单齿芳胺配合物中位于四方锥底部[31,78],而在二齿芳胺配合物中则位于顶点位置[23,33,59,60]。
1985年,Antolini等[31]合成了配合物[Cu(im)(LGlu)](图11)。X-射线单晶衍射测定显示该配合物具有一维链状结构,中心Cu(Ⅱ)离子由L-Glu离子桥联起来,其中L-Glu离子的α-甘氨酸部分(N1,O1)作为二齿配体与Cu(Ⅱ)离子配位,侧链羧酸(O3)键合到另一个Cu(Ⅱ)离子,Cu(Ⅱ)离子具有变形平面四边形的配位结构。这样的配位结构与铜(Ⅱ)和氨基酸或者小肽所形成的配位结构(通常情况下形成变形四方锥结构)存在极大差异。
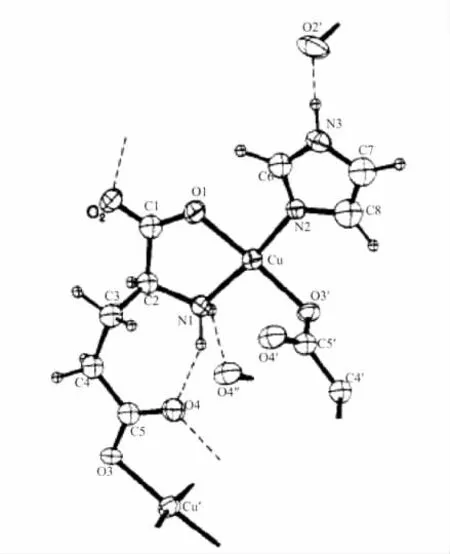
图11 配合物[Cu(im)(L-Glu)]的分子结构图Fig.11 Molecular structure for complex[Cu(im)(L-Glu)]
Estrader等[78]合成了配合物[Cu(im)(μ-Phe)(H2O)]n·(ClO4)n(图12)。中心Cu(Ⅱ)离子具有变形四方锥配位结构,单齿配体 im(N1)与 L-Phe(N3,O3)及相邻 LPhe(O2)位于四方锥的底部,H2O(O1)位于四方锥的顶点,中心Cu(Ⅱ)离子之间通过L-Phe(O2)桥联起来。
1987年,Aoki等[33]合成了配合物[Cu(phen)(LTrpO)]ClO4·2.5H2O(图 13)。结构研究发现,中心 Cu(Ⅱ)离子处在轻微扭曲的四方锥结构中,配体phen(N,N)与L-TrpO(N,O)位于四方锥底面上,与之相对称的相邻分子中L-TrpO的另一个羧酸氧位于顶点位置,将(Ⅱ)Cu(phen)(L-TrpO)(Ⅱ)n桥联在一起而形成一维链状结构。本课题组合成的配合物[Cu2(bipy)2(L-Val)2]n·2nClO4·2nH2O[59](图 14) 和 [Cu2(phen)2(L-Ala)2]n·2nClO4·2nH2O[60](图 15)及 Yamauchi等[24]合成的配合物[Cu(bipy)(L-Trp)]·ClO4也具有类似的一维链状结构。

图12 配合物[Cu(im)(μ-Phe)(H2O)]n·(ClO4)n的分子结构图Fig.12 Molecular structure for complex[Cu(im)(μ-Phe)(H2O)]n·(ClO4)n
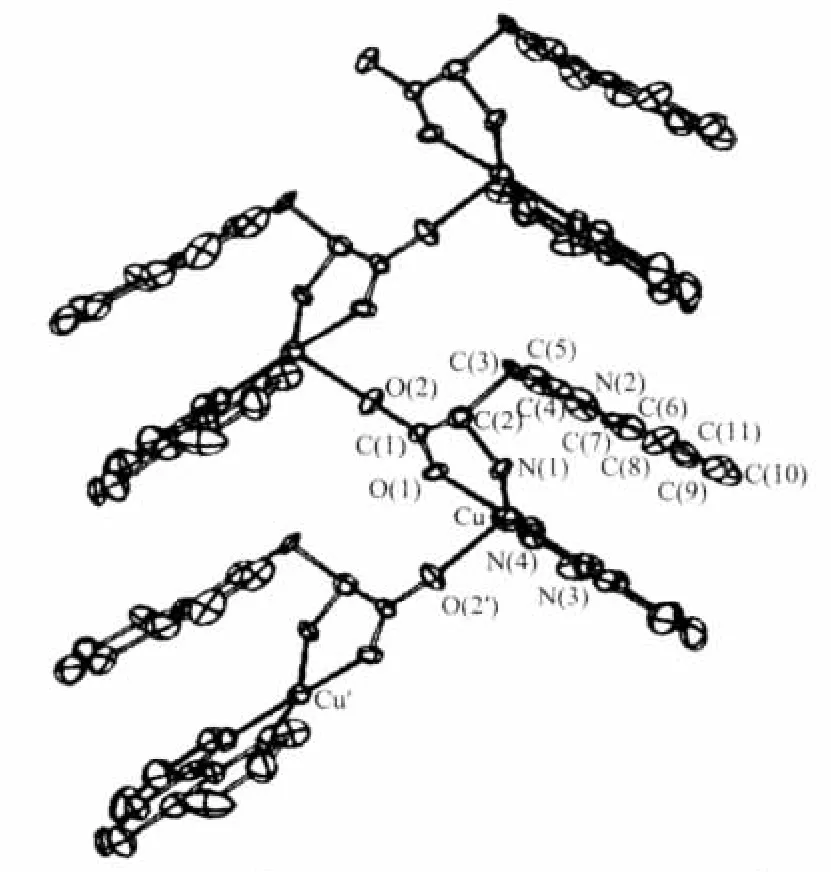
图13 配合物[Cu(Phen)(L-TrpO]ClO4·2.5H2O的分子结构图Fig.13 Molecular structure for complex[Cu(Phen)(L-TrpO]ClO4·2.5H2O
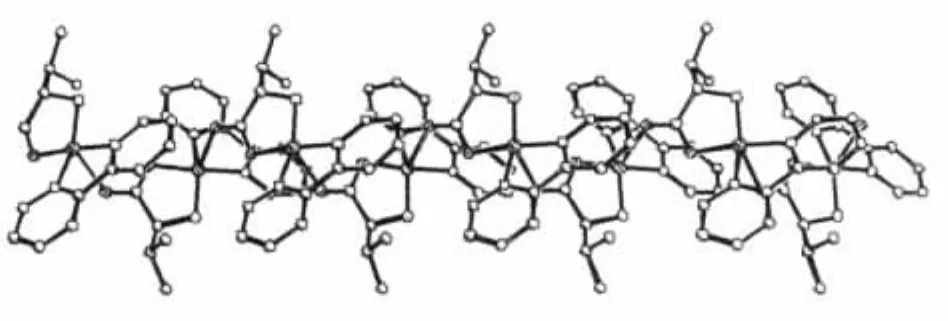
图14 配合物[Cu2(bipy)2(L-Val)2]n·2nClO4·2nH2O 的分子结构图Fig.14 Molecular structure for complex[Cu2(bipy)2(L-Val)2]n·2nClO4·2nH2O
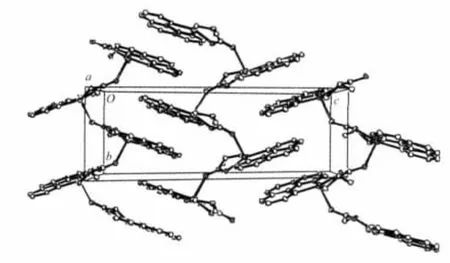
图15 配合物[Cu2(phen)2(L-Ala)2]n·2nClO4·2nH2O 的晶胞堆积图Fig.15 Packing view of the molecular structure for complex[Cu2(phen)2(L-Ala)2]n·2nClO4·2nH2O
此外,本课题组周晓华等[65]合成了一个结构新奇 的 一 维 链 状 物 {[Cu2(bipy)2(L-Arg)2-(μ2-ClO4)2]·2ClO4·4H2O}n(图16)。在该配合物长链阳离子{[Cu2(bipy)2(L-Arg)2(μ2-ClO4)2]2+}∞结构中,每个 Cu(Ⅱ)都具有相似的拉长八面体配位结构,bpy(N,N)与L-Arg(N,O)位于赤道平面上,2个ClO4-位于八面体的2个顶点并起着桥联作用。另外,在分子链中,2个近邻Cu(Ⅱ)配位结构中的键长与键角明显不同。
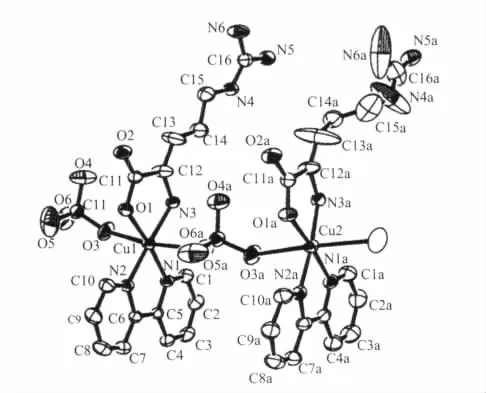
图16 配合物{[Cu2(bipy)2(L-Arg)2(μ2-ClO4)2]·2ClO4·4H2O}n的分子结构图Fig.16 Molecular structure for complex{[Cu2(bipy)2(L-Arg)2(μ2-ClO4)2]·2ClO4·4H2O}n
1.6 二维网状结构
1982年,Antolini等[29]合成了配合物[Cu(im)(LAsp)]·2H2O(图17)。该配合物具有二维网状结构,分子中中心Cu(Ⅱ)离子处于五配位的变形四方锥配位环境中。其中一个L-Asp同时桥联3个Cu(Ⅱ)离子,β-羧基(O3)、咪唑(N3)、另一个作为二齿配体的 L-Asp的α-羧基(O2)和氨基(N1)组成四方锥的底面,第三个L-Asp的α-羧基 (O1)占据四方锥的轴向位置。Cu(Ⅱ)离子之间通过L-Asp离子桥联在一起。另外,H2O分子通过与网状结构间的氢键作用进一步提高了配合物结构的稳定性。
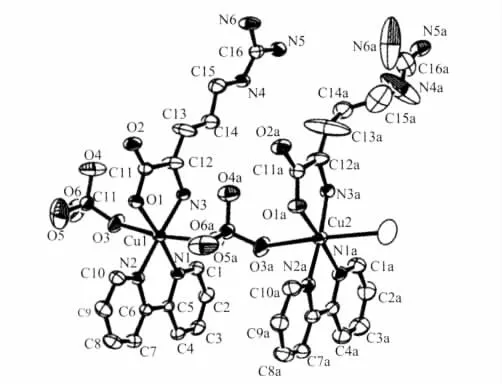
图17 配合物[Cu(im)(L-Asp)]·2H2O的分子结构图Fig.17 Molecular structure for complex[Cu(im)(L-Asp)]·2H2O
2008 年,Estrader等[78]合成了配合物[Cu(pz)(μ-Ala)(μ-ClO4)]n(图 18)。 X-射线单晶衍射结果显示该配合物中心Cu(Ⅱ)离子处于六配位的拉长八面体配位环境中,吡唑环(N1)、L-Ala(N3,O1)和另一 L-Ala(O2)位于八面体赤道平面,ClO4-(O3,O5)位于轴向位置。Cu(Ⅱ)离子之间通过 ClO4-(O3,O5)和 L-Ala(O2)桥联形成二维网状结构。
1.7 影响配合物分子结构的因素
综合以上结构分析结果,发现芳胺配体、铜盐阴离子及L-α-氨基酸配体对配合物的分子结构均有影响,其中芳胺配体的性质对配合物的结构起着重要作用。通常情况下芳胺的配位能力比L-α-氨基酸、水分子和阴离子要强,因此,在配合物的形成过程中,芳胺配体与Cu(Ⅱ)结合较紧密,配位后导致Cu(Ⅱ)中心电子云密度发生变化,而变化幅度与水分子及阴离子能否参与配位及配位的强弱密切相关,例如DPPZ、TATP及dpq所形成的配合物都是变形的四方锥结构,难以形成链状物,而im、pz、bipy及phen配合物的结构则较为多变。
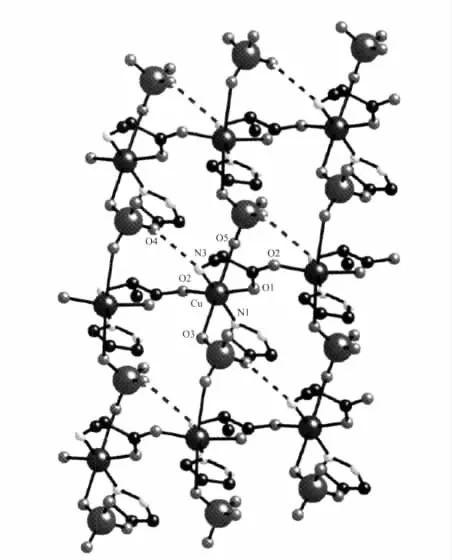
图18 配合物[Cu(pz)(μ-Ala)(μ-ClO4)]n的分子结构图Fig.18 Molecular structure for complex[Cu(pz)(μ-Ala)(μ-ClO4)]n
本课题组陈实等[48]合成的配合物[Cu(phen)(LIle)(H2O)]NO3为五配位的变形四方锥结构(图19),而本课题组刘小平[47]合成的配合物[Cu(phen)(L-Ile)(H2O)(ClO4)]为变形八面体结构,表明使用的铜盐不同,配合物的分子结构会有差异。NO3-一般不参与配位,因此以Cu(NO3)2制得的配合物,大多为变形四方锥结构。以Cu(ClO4)2制得的配合物,ClO4-有时能弱配位位于分子轴向的顶点,因此所形成的结构较为多变。以CuCl2制得的芳胺-铜(Ⅱ)-L-α-氨基酸配合物为变形四方锥结构,且Cl-有可能参与配位[41-42]。
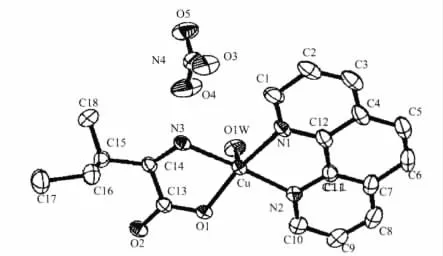
图19 配合物[Cu(phen)(L-Ile)(H2O)]NO3的分子结构Fig.19 Molecular structure for complex[Cu(phen)(L-Ile)(H2O)]NO3
另外,L-α-氨基酸结构对配合物的结构也有一定影响。 对于 L-Tyr、L-Phe、L-Trp、L-Pro 和 L-His等具有环侧链的L-α-氨基酸配体,由于侧链上的芳环具有较大的空间位阻,不利于在分子轴向的两个顶点同时有水或者阴离子参与配位而通常形成配位数为5的四方锥构型(图20,21),而侧链位阻较小的L-α-氨基酸配体有可能形成中心铜(Ⅱ)离子配位数为6的结构(图 9,10)或一维链状结构(图 14,15)。 对于含有2个羧基的L-Glu和L-Asp,由于具有相对较多的配位原子,有可能形成一维链状或二维网状结构(图11,17)。
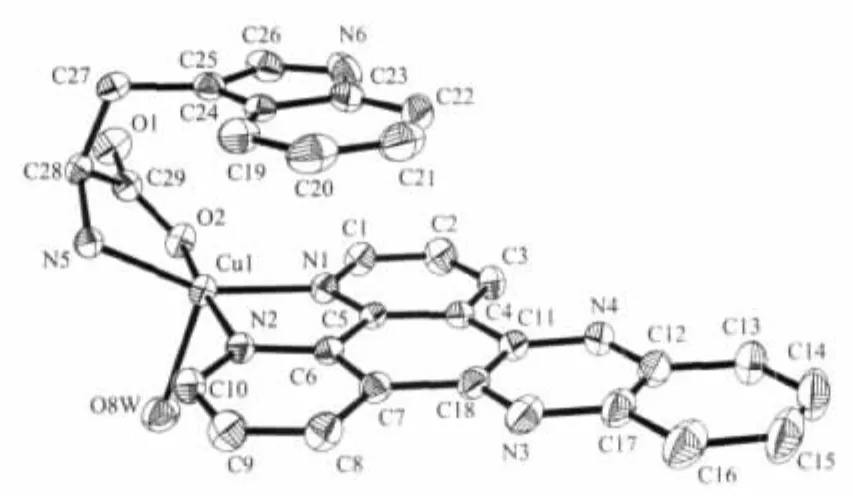
图20 配合物[Cu(DPPZ)(L-Trp)(H2O)]ClO4的分子结构Fig.20 Molecular structure for complex[Cu(DPPZ)(L-Trp)(H2O)]ClO4
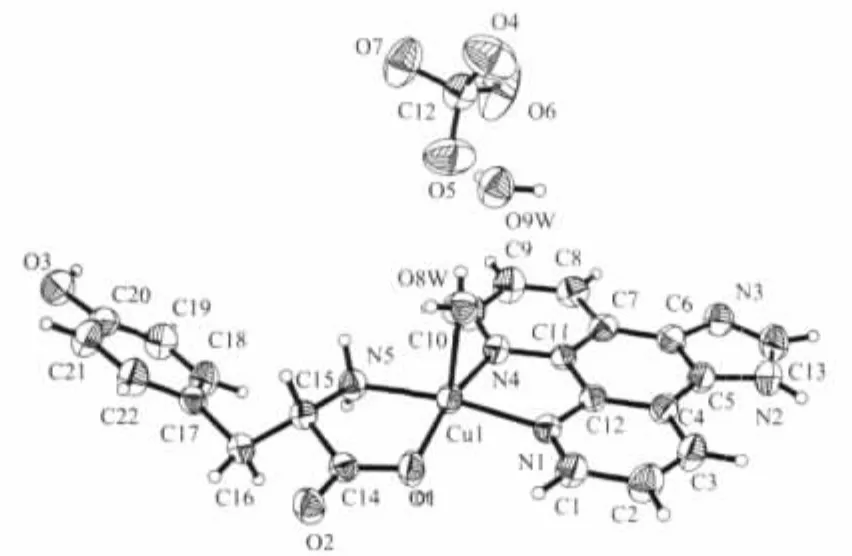
图21 配合物[Cu(IP)(L-Tyr)(H2O)]ClO4·H2O的分子结构Fig.21 Molecular structure for complex[Cu(IP)(L-Tyr)(H2O)]ClO4·H2O
2 芳胺-铜(Ⅱ)-L-α-氨基酸配合物的应用
研究三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物不仅具有理论意义,而且具有广泛的实际应用价值。这类配合物可作为化学核酸酶、SOD模拟物及植物生长抗逆增产剂等。
2.1 化学核酸酶
化学核酸酶可用于探测DNA结构及癌症治疗等,通过研究金属配合物与DNA的作用,对设计、合成新型化学核酸酶有重要意义。
2002年,Chikira等[83]通过ESR谱研究了系列三元邻菲咯啉-铜(Ⅱ)-L-α-氨基酸配合物与DNA的作用,并且揭示了这些配合物与DNA具有几种不同的作用模式。第一种是当配合物的g‖轴与DNA的双螺旋轴几乎平行时,表明配合物分子中邻菲咯啉芳环以插入的方式与DNA结合;并且由于联二吡啶相关铜配合物没有这种插入作用,表明邻菲咯啉分子芳环对于插入作用起关键作用。第二种是配合物与DNA以非插入模式结合,且其中又有两种情况,一种是以DNA分子上的某些基团 (碱基或磷酸盐)取代配合物分子中的配体L-α-氨基酸而相互结合,另一种是配合物分子中L-α-氨基酸并未被取代,仍然以三元配合物的形式与DNA作用,且与DNA结合的自由能变化相当或大于插入作用模式的自由能变化值,则配合物分子以邻菲咯啉芳环与DNA小沟结合。揭示了L-α-氨基酸侧链大小、形状及极性对这些作用模式有重要影响。另外,他们研究了在H2O2存在下这些配合物对DNA的切割作用,并提出作用机制与配合物Cu(phen)22+的类似。
2003年,本课题组与李红等[84-85]合作通过电化学实验方法研究了配合物[Cu(phen)(L-Met)(H2O)]NO3·H2O、[Cu(phen)(L-Leu)(H2O)]ClO4·2.5H2O 及[Cu(TATP)(L-phe)(H2O)]ClO4·0.5H2O与 DNA的相互作用。发现当把CT-DNA加入到配合物溶液中时,配合物的氧化还原电流明显降低,E⊖′发生轻微的正移,扩散系数会减小(图22),表明配合物与DNA发生了相互作用。通过UV-Vis、荧光光谱、粘度测定等方法进一步揭示了这些配合物可能通过插入方式与CT-DNA结合。而且发现在还原剂Vitamin C及H2O2存在的条件下,配合物[Cu(TATP)(L-Phe)(H2O)]ClO4·0.5H2O可以通过羟基自由基机理切割pBR322 DNA(图 23)。
2004年,郭子健课题组[69]通过UV-Vis、荧光光谱、CD光谱及凝胶电泳法等方法研究了配合物[Cu(phen)(L-Thr)(H2O)]ClO4与DNA的相互作用。CD光谱(图24)研究表明,随着配合物增加,275与245 nm处的峰强度都增强,推测这种现象可能与配合物对DNA插入作用有关,与UV-Vis及荧光光谱方法研究结果一致。

图22 [Cu(phen)(L-Leu)(H2O)]ClO4·2.5H2O 在不同 DNA浓度下的循环伏安图(a)和微分脉冲伏安图(b)Fig.22 Cyclic voltammograms(a)and differential pulse voltammograms(b)of[Cu(phen)(L-Leu)(H2O)]ClO4·2.5H2O as a function of DNA
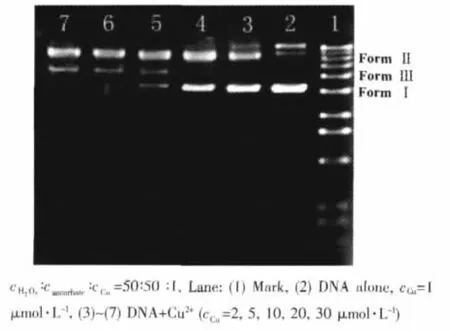
图23 在H2O2和抗坏血酸存在下,[Cu(TATP)(L-Phe)(H2O)]ClO4·0.5H2O 对 pBR322 DNA 的切割作用Fig.23 Electrophoretic separations of pBR322 DNAinduced by[Cu(TATP)(L-Phe)(H2O)]ClO4·0.5 H2O in the presence of H2O2and ascorbate
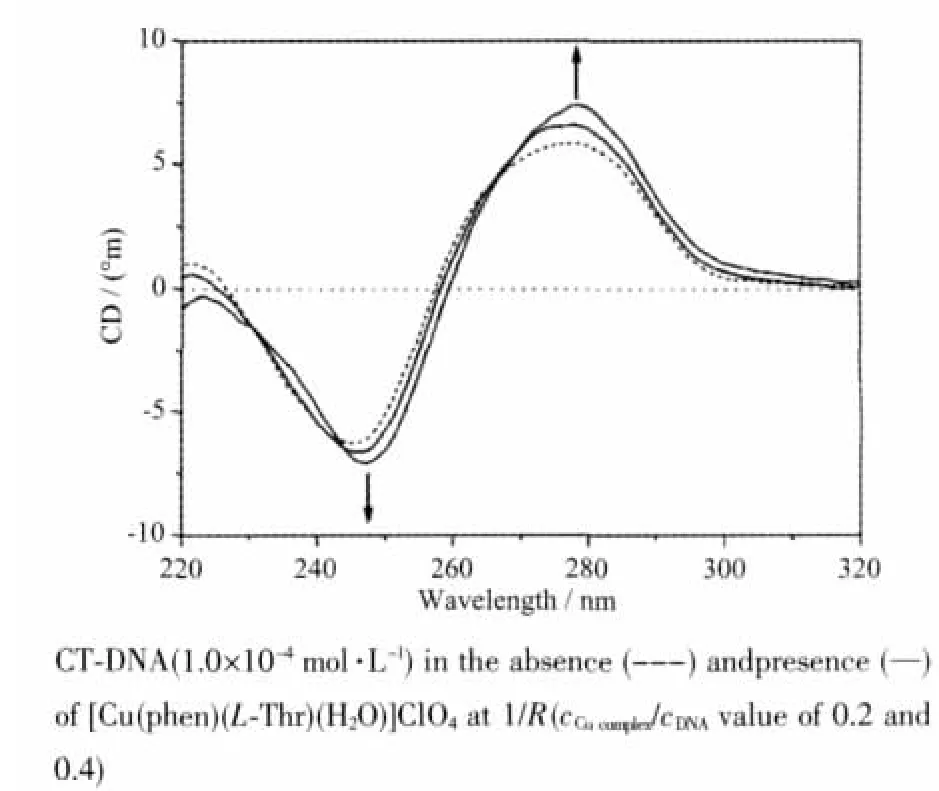
图24 [Cu(phen)(L-Thr)(H2O)]ClO4与DNA的相互作用的CD光谱Fig.24 CD spectra of the interaction between[Cu(phen)(L-Thr)(H2O)]ClO4and CT-DNA
近年来,本课题组[56-57,66,87-89]通过电子吸收光谱、荧光光谱、粘度测定及凝胶电泳等方法研究了系列三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物与DNA之间的相互作用。结果表明,作用强度随芳胺芳环增大而增强,随配合物空间位阻的增大而减小,由此推测这些配合物可能以插入或部分插入方式与DNA作用。此外,通过凝胶电泳实验,发现配合物在存在还原剂抗坏血酸而没有H2O2条件下也能够切割DNA,推测这种作用可能与配合物具有SOD活性[53],通过氧化还原反应生成羟基自由基(·OH)进而氧化切割DNA有关[63]。并且发现配合物与DNA的结合能力越强,其切割DNA的活性越大[88]。
Chakravarty等[37-43]应用DNA热变性实验研究了系列三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物与DNA的相互作用。发现配合物与DNA作用后,使DNA熔点升高了 1.6~5 ℃,且在 L-α-氨基酸相同的条件下,芳胺配体芳环面积越大配合物ΔTm升高越多,由此推测配合物可能以插入方式与DNA作用。此外,基于芳胺配体 dpq、DPPZ 及 L-α-氨基酸配体 L-Arg、LTrp、L-Lys都是光敏剂,该课题组用光诱导切割试验研究了配合物光诱导切割DNA的活性,发现在不需要还原剂存在的条件下,配合物通过氧化还原反应生成单线态氧(1O2)氧化切割DNA。同时发现,对于芳胺及L-α-氨基酸都是光敏剂所形成的双光敏剂配合物的光诱导切割活性比L-α-氨基酸是非光敏剂所形成的单光敏剂的配合物要强,具有较小芳环的bipy的配合物不具有光诱导切割活性。另外,研究发现配合物与DNA的相互作用愈强则其光诱导切割DNA的活性越强,表明光诱导切割DNA作用也可能与配合物对DNA的插入作用有关。
Chetana等[34-36]应用凝胶电泳实验研究了一系列三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物对DNA的切割作用。并且通过研究配合物 [Cu(dpq)(L-Ala)(H2O)]ClO4与DNA的相互作用探索了切割作用机理,提出这些配合物切割DNA螺旋结构除与羟基自由基有关外,还可能涉及到超氧阴离子自由基,与本课题组所得结果一致。
此外,周建良[72]、宋昭凤[79]、张志军[90]、张芳[91]等课题组分别通过电子吸收光谱、荧光光谱、粘度法和电化学等方法研究了系列三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物与DNA的相互作用,结果表明这些配合物通过非经典插入模式或部分插入模式与DNA作用。
2.2 模拟SOD
本课题组[50-51,53-54,58,61,64,66,92]在研究三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物的SOD活性方面做了大量工作。发现具有变形四方锥结构的系列配合物在 0.2~0.9 μmol·L-1浓度范围内对的抑制率达到 50%以上,配合物[Cu(TATP)(L-Val)(H2O)]ClO4·0.5H2O、[Cu(TATP)(L-Arg)(H2O)]·2ClO4·0.5H2O、[Cu(TATP)(LSer)(H2O)]ClO4、[Cu(TATP)(L-Tyr)(H2O)]ClO4·H2O 对应的 KQ值分别为 3.21×107mol-1·L·s-1、1.77×107mol-1·L·s-1、0.68×107mol-1·L·s-1和 0.57×107mol-1·L·s-1,表明这些配合物具有良好的超氧化歧化酶(SOD)活性。并且发现,这些具有变形四方锥结构配合物比文献[93-94]报道的变形四边形结构配合物SOD活性要高(文献中两个平面四边形配合物的IC50值分别为175和 5.86 μmol·L-1), 这归因于三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物分子的变形四方锥结构与天然SOD活性中心的变形四方锥构型相似,具有一个柔性的配位环境,Cu(Ⅱ)变形四方锥配位结构与Cu(Ⅱ)变形四面体配位结构间容易相互转化,氧还循环容易进行,从而能较快地催化歧化。另外,还发现侧链较小(空间位阻小)的L-α-氨基酸及具有带正电荷胍基的L-Arg侧链的配合物具有较高的SOD活性。这些研究结果对设计、合成新型SOD模拟物有重要意义。
2.3 植物生长抗逆增产剂
本课题组研究了部分三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物对水稻幼苗及玉米幼苗抗盐害胁迫性的影响[66,95,96]。研究结果表明[66,95],在中度盐害的情况下,用这些配合物水溶液对玉米浸种,八叶期后对幼苗的生理生化指标进行检测,发现生物量提高了31.95%~39.34%(鲜重)和 32.12%~48.76%(干重),叶绿素含量提高了3.25%~8.52%,生物体内SOD活性提高了37.78%~46.99%,表明这些配合物能有效抑制玉米幼苗所受的盐害胁迫作用;同时发现不同配合物作用的适宜浓度不同,如配合物[Cu(phen)(L-Leu)(H2O)]Cl·2.5H2O 较高浓度(0.5 μmol·L-1)处理效果较较低浓度下(0.1 μmol·L-1)效果要好,而配合物[Cu(phen)(L-Met)(H2O)]Cl·2H2O作用效果相反,表明这种生物活性与配合物分子结构有关。另外,本课题组[96]研究中等盐害胁迫条件下三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物对水稻幼苗生物量及SOD活性的影响也得到了类似的结果。目前,本课题组还正在进行有关这类配合物对作物抗干旱、抗水涝的作用及相关机理研究。
3 研究展望
长期以来,人们在三元芳胺-铜(Ⅱ)-L-α-氨基酸型配合物合成、结构表征、溶液中的稳定性及其与DNA相互作用和SOD活性研究等方面做了大量工作,并且近几年来对这类配合物的其它功能性方面,例如对作物抗逆和抗菌作用等方面的研究等也逐渐得到了人们的重视,然而还有许多工作有待于进一步研究。我们认为未来的研究将着重于:(1)进一步探索三元芳胺-铜(Ⅱ)-L-α-氨基酸型配合物与DNA的选择性识别作用机理及断裂机理,为设计、合成新型化学核酸酶提供科学依据;(2)研究三元芳胺-铜(Ⅱ)-L-α-氨基酸配合物的抗菌活性,并探索其作用机理;(3)在研究这类配合物SOD活性基础上,进一步研究配合物对作物抗逆(抗盐、抗旱等)性影响,并揭示其抗逆增产作用机制,为研制新型植物生长抗逆增长剂提供科学依据。
[1]LIAO Zhan-Ru(廖展如),ZHANG Yi-Sheng(张以胜),LEXue-Yi(乐学义).Studies of Trace Elements and Health(Weiliang Yuansu Yu Jiankang Yanjiu),1988,9(4):6-10
[2]Sugimori T,Masuda T,Ohata N,et al.Inorg.Chem.,1997,36(4):576-583
[3]Devereux M,McCann M,O′Shea D,et al.J.Inorg.Biochem.,2004,98(6):1023-1031
[4]Devereux M,O′Shea D,Kellett A,et al.J.Inorg.Biochem.,2007,101(6):881-892
[5]El-Sherif A A,Jeragh B J A.Spectrochim.Acta Part A,2007,68A(3):877-882
[6]Eichhorn G L.Inorganic Biochemistry.Amsterdam:Elsevier,1973.
[7]Sigel H.Metal Ions in Biological Systems.New York:Marcel Dekker,1973.
[8]Malik G S,Singh S P,Tandon J P.Monatshefte fuer Chemie,1979,110(1):149-155
[9]Fischer B E,Sigel H.J.Am.Chem.Soc.,1980,102(9):2998-3008
[10]CHEN Rong-Ti(陈荣悌),LIN Hua-Kuan(林华宽),GU Zong-Xin(古宗信).Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),1985,1:13-20
[11]CHEN Rong-Ti(陈荣悌),LIN Hua-Kuan(林华宽).Acta Chim.Sin.(Huaxue Xuebao),1986,44(5):449-454
[12]CHEN Rong-Ti(陈荣悌),LIN Hua-Kuan(林华宽),LIU Heng-Qian(刘恒潜).Acta Chim.Sin.(Huaxue Xuebao),1986,44(4):424-426
[13]Chen Y T,Lin H K,Zhu J Y.J.Chem.Soc.,Dalton Trans.:Inorg.Chem.,1990,11:3445-3447
[14]Shoukry A A.Trans.Metal Chem.,2005,30(7):814-827
[15]Prasad K,Mohan M S.J.Coord.Chem.,1987,16(1):1-7
[16]Prasad K,Rao A K,Mohan M S.J.Coord.Chem.,1987,16(3):251-262
[17]Shoukry M M,Khairy E M,El-Sherif A A.Trans.Metal Chem.,2002,27(6):656-664
[18]El-Sherif A A.J.Solution Chem.,2010,39(1):131-150
[19]El-Sherif A A,Shoukry M M.Spectrochim.Acta.Part A:Mol.Biomol.Spectr.,,2007,66(3):691-700
[20]Yamauchi O,Odani A.J.Am.Chem.Soc.,1985,107(21):5938-5945
[21]Kwik W L,Ang K P,Chen G.J.Inorg.Nucl.Chem.,1980,42(2):303-313
[22]Sugimori T,Masuda H,Yamauchi O.Bull.Chem.Soc.Jpn.,1994,67(1):131-137
[23]Masuda H,Sugimori T,Odani A,et al.Inorg.Chim.Acta,1991,180(1):73-79
[24]Yamauchi O,Odani A,Masuda H.Inorg.Chim.Acta,1992,198-200:749-761
[25]Sugimori T,Masuda H,Ohata N,et al.Inorg.Chem.,1997,36(4):576-583
[26]Zhang F,Yajima T,Masuda H,et al.Inorg.Chem.,1997,36(25):5777-5784
[27]Yajima T,Takamido R,Shimazaki Y,et al.Dalton Trans.,2007,3:299-307
[28]Yamauchi O,Odani A,Kohzuma T,et al.Inorg.Chem.,1989,28(22):4066-4068
[29]Antolini L,Marcotrigiano G,Menabue L,et al.Inorg.Chem.,1982,21(6):2263-2267
[30]Antolini L,Marcotrigiano G,Menabue L,et al.Inorg.Chem.,1983,22(1):141-145
[31]Antolini L,Marcotrigiano G,Menabue L,et al.Inorg.Chem.,1985,24(22):3621-3626
[32]Antolini L,Battaglia L P,Bonamartini Corradi A,et al.Inorg.Chem.,1986,25(16):2901-2904
[33]Aoki K,Yamazaki H.J.Chem.Soc.,Dalton Trans.,1987,8:2017-2021
[34]Rao R,Patra A K,Chetana P R.Polyhedron,2008,27(5):1343-1352
[35]Chetana P R,Rao R,Roy M,et al.Inorg.Chim.Acta,2009,362(13):4692-4698
[36]Rao R,Patra A,Chetana P R.Polyhedron,2007,26(18):5331-5338
[37]Patra A K,Dhar S,Nethaji M,et al.Chem.Commun.,2003,13:1562-1563
[38]Patra A K,Dhar S,Nethaji M,et al.Dalton Trans.,2005,5:896-902
[39]Patra A K,Bhowmick T,Ramakumar S,et al.Inorg.Chem.,2007,46(22):9030-9032
[40]Patra A K,Bhowmick T,Ramakumar S,et al.Dalton Trans.,2008,48:6966-6976
[41]Patra A K,Roy S,Chakravarty A R.Inorg.Chim.Acta,2009,362(5):1591-1599
[42]Patra A K,Bhowmick T,Roy S,et al.Inorg.Chem.,2009,48(7):2932-2943
[43]Patra A K,Nethaji M,Chakravarty A R.Dalton Trans.,2005,16:2798-2804
[44]Sgarabotto P,Bisceglie F,Pelosi G,et al.Polyhedron,1999,18(19):2505-2510
[45]Su C C,Tai T Y,Wu S P,et al.Polyhedron,1999,18(18):2361-2368
[46]ZHOU Xiao-Hua(周晓华),LE Xue-Yi(乐学义),LI Ming-Hua(李明华).Chem.J.Chinese Universities(Gaodeng Xuexiao Huaxue Xuebao),2000,21(5):681-682
[47]LIU Xiao-Ping(刘小平),YANG Chi(杨迟),LE Xue-Yi(乐学义),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2003,19(10):1085-1089
[48]CHEN Shi(陈实),LE Xue-Yi(乐学义),ZHOU Xiao-Hua(周晓华),et al.Chem.Bull.(Huaxue Tongbao),2004,67(6):461-464
[49]ZHOU Xiao-Hua(周晓华),LE Xue-Yi(乐学义),LI Ming-Hua(李明华).Chem.Bull.(Huaxue Tongbao),2001,64(1):48-49
[50]LIAO Sheng-Rong(廖升荣),LE Xue-Yi(乐学义),LU Qi-Ming(卢其明),et al.J.South China Agric.Univ.:Nat.Sci.Ed.(Huanan Nongye Daxue Xuebao:Ziran Kexue Ban),2006,27(3):122-124
[51]LIAO Sheng-Rong(廖升荣),LE Xue-Yi(乐学义),LIN Qing-Bin(林庆斌),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2006,22(2):203-206
[52]LE Xue-Yi(乐学义),CHEN Shi(陈 实).Chin.J.Synth.Chem.(Hecheng Huaxue),2001,9(6):531-533
[53]GU Qin(古琴),LE Xue-Yi(乐学义),LIN Qing-Bin(林庆斌),et al.Chinese J.Chem.(Zhongguo Huaxue),2007,25(6):791-796
[54]GU Qin(古琴),LIAO Sheng-Rong(廖升荣),LU Qi-Ming(卢其明),et al.Chem.Res.Appl.(Huaxue Yanjiu Yu Yingyong),2006,18(1):76-79
[55]LE Xue-Yi(乐学义),TONG Ming-Liang(童明良),FU Yin-Lian(付银莲),et al.Acta Chim.Sin.(Huaxue Xuebao),2002,60(2):367-371
[56]SONG Zhi-Jun(宋智君),LE Xue-Yi(乐学义),LI Hong(李红),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2005,21(4):527-530
[57]Le X Y,Gu Q,Song Z J,et al.J.Coord.Chem.,2007,60(13):1359-1371
[58]Le X Y,Liao S R,Liu X P,et al.J.Coord.Chem.,2006,59(9):985-995
[59]Zhou X Y,Le X Y,Chen S.J.Coord.Chem.,2005,58(12):993-1001
[60]LIN Qing-Bin(林庆斌),LE Xue-Yi(乐学义),XIONG Ya-Hong(熊亚红),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2006,22(11):2080-2084
[61]GU Qin(古琴),LIN Qing-Bin(林庆斌),LE Xue-Yi(乐学义).Chem.Bull.(Huaxue Tongbao),2007,70(6):450-455
[62]Le X Y,Zhou X Y,Song Z J,et al.J.Coord.Chem.,2003,56(10):861-867
[63]Gu Q,Lin Q B,Liu Y J,et al.Chem.Res.Chin.Univ.,2008,24(4):401-406
[64]LIN Qing-Bin(林庆斌),DING Yang(丁杨),GU Qin(古琴),et al.Chem.Res.(Huaxue Yanjiu),2007,18(1):5-8
[65]Zhou X H,Yang C,Le X Y,et al.J.Coord.Chem.,2004,57(5):401-409
[66]LIAO Sheng-Rong(廖升荣),REN Xiang-Xiang(任祥祥),MAO Xiao-Yun(毛小云),et al.Chinese Agric.Sci.Bull.(Zhongguo Nongxue Tongbao),2008,24(6):237-242
[67]Kwik W L,Ang K P.Trans.Met.Chem.,1985,10(2):50-54
[68]Abdel-RahmanLH,BattagliaLP,Mahmoud,MR.Polyhedron,1996,15(2):327-334
[69]Zhang S C,Zhu Y G,Tu C,et al.J.Inorg.Biochem.,2004,98(12):2099-2106
[70]Lu L P,Zhu M L,Yang P.Acta Cryst.Section C:Cryst.Struct.Commun.,2004,C60(1):m21-m23
[71]Subramanian P S,Suresh E,Dastidar P,et al.Inorg.Chem.,2001,40(17):4291-4301
[72]ZHOU Jian-Liang(周建良),CHUN Xiao-Gai(春晓改),ZHOU Lin-Jiao(周琳娇),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2010,26(4):645-650
[73]Xu G J,Kou Y Y,Feng L,et al.Appl.Organometal.Chem.,2006,20(5):351-356
[74]Emanuel N A,Bhattacharya P K.Polyhedron,1987,6(5):845-848
[75]Hu N H,Aoki K,Yamazaki H.Inorg.Chim.Acta,1989,163(1):105-113
[76]Martin-Polo J J,Driessen W L,Cervantes-Lee F,et al.J.Inorg.Biochem.,1995,59(1):53-62
[77]Solans X,Ruiz-Ramirez L,Martinez A,et al.Acta Cryst.Section C:Cryst.Struct.Commun.,1988,C44(4):628-31
[78]Estrader M,Diaz C,Ribas J,et al.Inorg.Chim.Acta,2008,361(14/15):3963-3969
[79]SONG Zhao-Feng(宋昭凤),XIAO Xiao-Ming(肖小明),ZHU Yan-Hua(朱艳华).Chin.J.Spectrosco.Lab.(Guangpu Shiyanshi),2005,24(4):722-724
[80]ZHOU Xiao-Hua(周晓华),CHEN Shi(陈实),HUANG He(黄鹤),et al.J.South China Agriculture Univ.:Nat.Sci.Ed.(Huanan Nongye Daxue Xuebao:Ziran Kexue Ban),2004,25(2):115-117
[81]ZHOU Xiao-Hua(周晓华),LI Ming-Hua(李明华),LE Xue-Yi(乐学义).Chin.J.Syn.Chem.(Hecheng Huaxue),1999,7(2):213-215
[82]ZHOU Xiao-Hua(周晓华),CHEN Shi(陈实),HUANG He(黄鹤),et al.Chin.J.Syn.Chem.(Hecheng Huaxue),2003,11(6):503-506
[83]Chikira M,Tomizawa Y,Fukita D,et al.J.Inorg.Biochem.,2002,89(3/4):163-173
[84]LI Hong(李红),LE Xue-Yi(乐学义),JI Liang-Nian(计亮年),et al.Chem.Bull.(Huaxue Tongbao),2003,66(12):847-850
[85]LI Hong(李红),LE Xue-Yi(乐学义),WU Jian-Zhong(吴建中),et al.Acta Chim.Sin.(Huaxue Xuebao),2003,61(2):245-250
[86]Li H,Le X Y,Pang D W,et al.J.Inorg.Biochem.,2005,99(11):2240-2247
[87]GU Qin(古琴),REN Xiang-Xiang(任祥祥),LE Xue-Yi(乐学义).Acta Phys.-Chim.Sin.(Wuli Huaxue Xuebao),2008,24(6):1068-1072
[88]GU Qin(古琴),REN Xiang-Xiang(任祥祥),LE Xue-Yi(乐学义).Chem.Bull.(Huaxue Tongbao),2009,72(9):809-814
[89]GU Qin(古琴),LE Xue-Yi(乐学义),XIE Yun(谢韵),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2006,22(4):757-760
[90]ZHANG Zhi-Jun(张志军),LI Xi(李曦),HAO Li(郝莉),et al.J Huazhong Normal Univ.:Nat.Sci.Ed.(Huazhong Shifan Daxue Xuebao:Ziran Kexue Ban),2008,42(3):409-414
[91]ZHANG Fang(张芳),ZHANG Qian-Qian(张前前),ZHU Chen-Jian(祝陈坚),et al.Spectrosco.Spectr.Anal.(Guangpu Yu Guangpu Fenxi),2005,25(9):1439-1442
[92]REN Xiang-Xiang(任祥祥),DING Yang(丁杨),LIN Qing-Bin(林庆斌),et al.Chem.Res.&Appl.(Huaxue Yanjiu Yu Yingyong),2008,20(11):4540-4541
[93]Casanova J,Alzuet G,Ferrer S,et al.Inorg.Chim.Acta,2000,304(2):170-177
[94]Patel R N.Spectrochim.Acta.Part A:Mol.Biomol.Spectr.,2004,60(10):2201-2208
[95]LIAOSheng-Rong(廖升荣),MAOXiao-Yun(毛小云),ZHANG Zhao-Qi(张昭其),et al.Chin.J.Soil Sci.(Turang Tongbao),2007,38(5):962-965
[96]LIN Qing-Bin(林 庆 斌),DING Yang(丁 杨),WANG Hai-Bo(王海波),et al.Chin.J.Soil Sci.(Turang Tongbao),2009,40(5):1163-1166
Recent Research Progress in Ternary Copper(Ⅱ)Complexes Containing Aromatic Amine and L-α-Amino Acid
LU Yan-Mei1LE Xue-Yi*,1,2
(1Department of Applied Chemistry,South China Agricultural University,Guangzhou 510642,China)(2Institue of Biomaterial,South China Agricultural University,Guangzhou 510642,China)
Ternary copper(Ⅱ) complexes containing aromatic amine and L-α-amino acid attract abroad attention since the complexes can be used as chemical nucleases,SOD mimics and the regulators of plants growth against the environmental menaces.This paper summarizes the recent research advancement of ternary copper(Ⅱ)complexes containing aromatic amine and L-α-amino acid,which focuses chiefly on the structure and application of this kind of complexes.
copper(Ⅱ) complexes;aromatic amine;L-α-amino acid
O614.121
:A
:1001-4861(2011)02-0199-15
2010-07-20。收修改稿日期:2010-08-31。
广东省科技计划项目(2009B020312010)及华南农业大学211工程项目(2009B010100001)资助。
*通讯联系人。 E-mail:lexyfu@163.com,Tel:08620-85287010;会员登记号:S060000184M。
