猪圆环病毒2型感染的诊断与防治
2011-05-31杨冬玲
杨冬玲
(青海省海晏县金滩乡畜牧兽医站,青海海晏812200)
1911年,在加拿大北部地区的猪群中暴发了一种以断乳仔猪呼吸急促或困难、腹泻、贫血明显的淋巴组织病变和进行性消瘦为主要特征的疾病,严重影响猪的生长发育,造成了巨大的经济损失。目前,本病已经遍及世界各养猪国家,已成为养猪生产中突出的问题之一。近期研究表明,PCV2与猪皮炎与肾病综合征(PMWS)、猪的流产和系列障碍、猪增生性坏死性肺炎(PNP)和猪先天性脑震颤(CT)等的发生密切相关。PCV2常与猪呼吸与繁殖综合征病毒(PPRSV)或猪细小病毒(PPV)并发感染或继发细菌感染,使患病猪病情加重,死亡率升高。
一、病原
猪圆环病毒2型(PCV2)属圆环病毒科(Circovirdae)圆环病毒属(Circovirdae)。PCV2是一种小而无囊膜、二十面体、共价闭合、环状的单股DNA病毒。病毒粒子直径平均为17 nm,分子量为0.58×106Da。PCV2在氯化铯中浮密度为1.37 g/cm3,蔗糖梯度离心的沉降系数为52S,对PH3的酸性环境、氯仿作用或高温环境(70℃)有较强的抵抗力。不凝集牛、羊、猪、鸡等多种动物和人的红细胞。
PCV2完整的基因组大小多数为1768 bp,少数为1767 bp。各分离株之间核苷酸序列的同源性大于96%,而与PCV1分离株之间的核苷酸序列的同源性小于80%。PCV1和PCV2的ORF1的核苷酸和推导氯基酸序列的同源性分别为80%和86%,而ORF2的仅为67%和65%。PCV2可在PK15细胞上良好生长,但不产生细胞病变,也可在其他猪源细胞上生长,同样不产生细胞病变。用300mM的D氨基葡萄糖处理接种PCV后的细胞培养物30 min,能够促进病毒的增殖,病毒在原价胎猪肾细胞,恒河猴肾细胞、BHK-21细胞上不能生长。
二、流行病学
猪是PCV2的天然宿主,各种年龄、不同性别的猪都可感染,但并不能表现出临诊症状。病猪和带毒猪是主要的传染源。经口腔和鼻内实验感染新生仔猪能复制出典型的PMWS,易感猪与发病猪病触后引发PMWS,证实PCV2可在猪群中水平传播,已有证据表明PCV2可通过胎盘垂直传播。
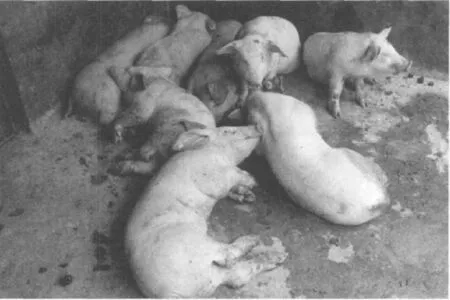
由PCV2感染所致的猪断奶后多系统衰竭综合征(PMWS)主要发生在哺乳期和保育期的仔猪,尤其是5~12周龄的仔猪,一般于断奶后2~3 d或1周开始发病,急性发病猪群中,病死率可达10%,在PMWS发病猪群,常常由于并发或继发其他细菌(如副猪嗜血杆菌)或病毒感染而使死亡率大大增加,有时可高达50%以上,在疾病流行感染过的猪群中,发病率和死亡率都有所降低。
猪皮炎与肾病综合征(PDNS)主要发生于保育和生长育肥猪,一般呈散发,死亡率低,由PCV2感染引起的繁殖障碍主要危害初产的后备母猪和新建的种猪群。
三、发病机理
PCV2感染的确切致病机理仍不清楚,这也是目前研究的热点。越来越多的研究表明,PCV2感染可造成猪体的免疫功能抑制。PMWS自然病例的外周血白细胞亚群的研究发现,发病猪血液中单核细胞和未成熟粒细胞增加,而CD4+T细胞和B细胞数量减少,急性PMWS发病猪的T细胞和B细胞的免疫功能受到影响,从而缺乏有效的免病应答。现在有研究表明,一些病原体如猪细小病毒(PPV)、猪繁殖与呼吸综合征病毒(PRRSV)、猪多杀性巴氏杆菌、猪肺炎支原体等在PCV2的致病作用中起着协同致病作用。免疫刺激(如佐剂和疫苗)、环境因素(如氨气、内毒素),以及其他应激因素(如运输和猪的混群)也是促进PCV2感染发生PMWS的因素。
PRRSV的存在可使单核/巨噬细胞活化,从而增强了PCV2的复制功能,佐剂或疫苗的刺激作用于猪的单核/巨噬细胞。对病毒的定量分析发现,发病猪体内病毒感染的细胞数量似乎总是高于带毒猪相对细胞的感染数量,或许猪体内的病毒含量达到一定数目后才表现出临诊症状。这些试验结果表明,引发PMWS的直接原因虽然是PCV2,但疾病的发生还需要其他致病因子的协同作用,这可以很好地解释为什么PCV3血清抗体检测阳性的猪群不一定发生PMWS。
免疫系统的刺激对激发PMWS是一个重要的因素,另一方面,严重感染的猪,淋巴组织病变如淋巴细胞缺如和淋巴细胞亚群的变化是该病的主要特征,因此,认为PMWS感染猪不能产生对其他免疫原的有效免疫应答,这是此病的致病机理之一。
PCV2感染引起的PDNS认为是由免疫反应介导的损害皮肤和肾肌的血管疾病。此外,一些病原体如多杀性巴氏杆菌和PRRSV的混合感染可以诱导PDNS。
四、临诊症状
(一)猪断奶后多系统衰竭综合征 PMWS的临诊症状有6个方面的基本表现,最常见的临诊症状是消瘦或生长迟缓,这也是诊断PMWS所必需的。此外,还可见呼吸困难,淋巴结肿大,腹泻,贫血和黄疸。在一只猪可能见不到上述所有的基本临诊症状,但在发病猪群可以见到所有的症状。其他比较少见的临诊症状有咳嗽、发热、胃溃疡、中枢神经系统障碍和突然死亡。一些临诊症状可能与继发感染有关,或者完全是由继发感染所引起的。PMWS急性发病猪群,病死率可达10%。但常常由于并发或继发细菌或病毒感染而使死亡率大大增加。各种环境因素如拥挤、空气污浊、各种年龄的猪混养及其他各种应激因素也可能加重病情。
(二)猪皮炎与肾病综合征 (PDNS)
最常见的临诊症状是猪皮上形成圆形或形状不规则、呈红色到紫色的病变,腹部也可扩散至喉、体侧或耳。感染轻的猪可自行康复,感染严重的猪可表现出跛行、发热、厌食、体重下降。
(三)繁殖障碍 PCV2感染母猪可出现繁殖障碍,临诊表现包括流产,产死胎、木乃伊胎和产弱仔,仔猪断奶前死亡率升高。
(四)肺炎 已有一些研究和临诊资料表明,PCV2与猪呼吸道疾病综合征(PRDC)有关,PCV2感染可以引起肺炎,并且PCV2在PRDC中起着十分重要的作用。
(五)肠炎 已有越来越多的临诊观察和诊断表明,PCV2感染可以引起肉芽肿性肠炎,猪只表现为腹泻、消瘦。
(六)先天性震颤 临诊上早已观察到猪的先天性震颤,近年来证实先天性震颤的初生仔猪的大脑和脊髓中含有PCV2核酸和抗原。
五、病理变化
肉眼可见的病理损伤变化很大,常见的变化包括肺脏肿胀,间质增宽,质度坚硬或似橡皮,其上散在有大小不等的褐色病变区,实变区可在肺脏的前下缘融合成片。全身淋巴结,特别是腹沟、纵隔、肺脏和肠系膜淋巴结显著肿大,切面为灰黄色,或有出血。肾脏灰白,皮质部散在或弥漫性分布白色坏死灶,大小由正常到显著扩大和肿胀。脾脏轻度肿胀。肝脏可能有中等程度的黄疸和/或肝萎缩伴有肝小叶融合。胃肠道有时呈现不同程度的损伤,骨的食管黏膜苍白、水肿和非出血性溃疡,肠道尤是回肠和结肠段肠壁变薄,肠管内液体充盈。继发细菌感染的病例可出现相应疾病的病理变化,如胸膜炎、心包炎、腹膜炎、关节炎等。
PDNS病例在猪的后肢和会阴部,乃至全身出现明显的坏死性皮炎;肾脏苍白、极度肿胀,皮质部有出血或淤血斑点。
PMWS在疾病早期阶段,组织病理学变化表观为肺呈现局灶或弥散性间质性肺炎,慢性感染猪出现肉芽肿性间质肺炎灶,灶中可见许多巨细胞和多核合胞体细胞。淋巴细胞和组织细胞漫润到所有肺小叶。淋巴结、脾脏和扁桃体可见B细胞滤泡消失,T细胞区域可被组织细胞和多核细胞所扩张;B细胞依赖区域单核细胞内多见的嗜碱性细胞浆内包涵体可见于疾病早期,淋巴结可出现多灶性凝固性坏死,坏死细胞内出现嗜酸性核内包涵体,肾脏、肝脏和胰腺出现不同程度的淋巴细胞浸润、实质细胞变性等。
六、诊断
由PCV2感染引起的断奶后多系统衰竭综合征,依据流行特点和临诊症状、剖检病变,可以作出初步诊断,确切诊断需依靠实验室相关技术,而与PCV2感染有关的繁殖障碍、肺炎、肠炎等,仅靠临诊症状是没有诊断价值的。
(一)临诊诊断要点
1.PMWS主要发生在5~12周龄的仔猪,仔猪断奶前生长发育良好。
2.在一定时期内,猪场中同窝或不同窝的断奶仔猪既有呼吸道症状,又有腹泻等表现,抗生素治疗无效或疗效不佳,病程长的猪生长发育迟缓、体重下降,有时出现皮肤苍白或黄疸。
3.死亡猪只剖检具有PMWS的病理变化,尤其是淋巴结肿胀,切面出血或呈灰黄色,脾脏轻度肿胀,肺脏肿胀,间质增宽,表面散在有大小不等的褐色实变区。其他脏器也可能有不同程度的病变和损伤。
(二)实验室诊断
1.病毒的分离与鉴定。无PCV污染的PK15细胞最常用于PCV2的分离,可取死亡猪的肺脏、淋巴结、肾脏、血清等作为病原的分离材料。由于PCV2在细胞培养中不产生细胞病变,因此,病料盲传1~6.3代后应进行PCV2抗原或核酸的检测加以鉴定。
2.病毒的检测。可彩用PCR、原位核酸杂交、间接免疫荧光试验,间接免疫过氧化物酶试验等直接检测病料的PCV2核酸或抗原。
3.抗体检测。可采用酶联免疫吸附试验(ELISA)、免疫荧光抗体技术、免疫过氧化物酶试验等,检测猪血清中的PCV2抗体,但由于PCV1和PCV2之间存在抗原交叉反应,因此已有的方法不能完全区分PCV1和PCV2感染。制备PCV2特异性的单克隆抗体,或者特异性的重组抗原能够满足建立特异性血清学方法的的需要。国内已建立了利用基因工程表达的PCV2重组蛋白作为抗原的ELISA抗体检测方法。需要注意的是目前在临诊上多种病原的合并感染十分普遍,因此在检测PCV2的同时,应同时检测其他病原体(如PRRSV、PRV、PPV、副猪嗜血杆菌等)。
七、防制
迄今为止还没有控制和消灭PMWS及PCV2感染所致其他疾病的有效措施,也没有切实有效的商品化疫苗和药物用来防御PCV2感染,而且PCV2对常规消毒剂抵抗力很强,给猪场的净化工作带来了困难。目前,控制PMWS应采取综合性的控制措施。
1.改变和完善饲养方式,做到养猪生产各阶段的全进全出,避免将不同日龄的猪混群饲养,从而降低猪群之间PCV2的接触感染机会。
2.建立猪场完善的生物安全体系,将消毒卫生工作贯穿于养猪生产的各个环节,最大限度地降低猪场内污染的病原微生物,减少或杜绝猪群继发感染的几率。由于PCV2对一般的消毒剂抵抗力强。因此,在消毒剂的选择上应考虑使用广谱的消毒药。
3.加强猪群的饲养管理,降低猪群的应激因素。很多应激因素都可诱发、促进PMWS的发生和加重发病猪群的病情,导致死亡率上升。因此,应尽可能地减少猪群的应激因素,避免饲喂发霉变质或含有菌毒素的饲料,做好猪舍的通风换气,改善猪舍的空气质量,降低氨气浓度,保持猪舍干燥,降低猪群的饲养密度。
4.提高猪群的营养水平,由于PCV2感染可以导致猪群的免疫功能下降,因此,营养是影响PMWS的一个重要因素。通过提高猪群的蛋白质、氨基酸、维生素和微量元素的饮水,可以在一定程度上降低PMWS的发生率和造成的损失。
(1)仔猪用药:哺乳仔猪在3、7、21日龄注射长效土霉素(200 mg/ml)每次0.5 ml,或者在1、7日龄和断奶时各注射头胞噻呋(500 mg/ml)0.2 ml,;断奶前1周至断奶后1个月,用泰妙菌素(50 g/t)+金霉素或土霉素或强力霉素(150 g/t)+阿莫西林(500 g)。拌料饲喂,或者添加2%氟苯尼考(1000~1500 g/t)+泰 妙 菌 素(200~ 250 g/t)。继发感染严重的猪场,可在28、35、42日龄各注射头胞噻呋(500 mg/ml)0.2 ml。
(2)母猪用药:母猪在产前1周和产后1周,饲料中添加支原净(100 g/t)+金霉素或土霉素(300 g/t)。
5.做好猪场猪瘟,伪狂犬病、猪细小病毒感染、气喘病等疫苗的免疫接种,规模化猪场应提倡使用猪气喘病灭活疫苗免疫接种,有利于提高猪群呼吸道和肺脏的免疫力,可减少呼吸道病原体的继发感染。
略)