2种盐酸特比萘芬乳膏体外透皮扩散试验研究Δ
2011-05-22林华庆张肖玲李欣蔚广东药学院药物研究所广东省药物新剂型重点实验室广州市510006
邓 红,张 蜀,林华庆,张肖玲,卜 水,李欣蔚(广东药学院药物研究所/广东省药物新剂型重点实验室,广州市 510006)
盐酸特比萘芬(Terbinafine hydrochloride)是一种新型的丙烯胺类抗真菌药,是真菌角鲨烯环氧化酶特异性抑制剂,用于治疗浅表皮肤真菌病,可经皮肤给药以达局部治疗目的。本试验采用小型猪离体皮肤及改良Franz扩散池,考察供试药盐酸特比萘芬乳膏的皮肤透过率以及皮肤局部贮药量,并与上市产品盐酸特比萘芬乳膏(商品名:兰美抒®)进行比较,旨在阐明制剂的起效途径,预测供试药与已上市产品的一致性。
1 仪器与材料
TK-12B型透皮扩散试验仪(上海锴凯科技贸易有限公司);U3000高效液相色谱(HPLC)仪、二极管阵列检测器(美国Dionex公司);KQ-100TDB超声波清洗器(昆山市超声仪器有限公司);LXJ-IIB型多管离心机(上海安亭科学仪器厂)。
供试药盐酸特比萘芬乳膏(批号:090501,规格:0.1 g∶10 g)、空白基质(批号:100501)均由桂林华信制药有限公司提供;对照药1%盐酸特比萘芬乳膏(商品名兰美抒®,中美天津史克制药有限公司,批号:09110223);盐酸特比萘芬原料药(济南明鑫制药有限公司,批号:081108122,含量:99.7%);盐酸特比萘芬标准品(中国药品生物制品检定所,批号:100563-200301,供含量测定用);甲醇、乙腈均为色谱纯,其余试剂为分析纯。
西藏小型猪,♀♂各1只,体重35~40 kg,南方医科大学实验动物中心,实验动物许可证号:SCXK(粤)2006-0015。
2 方法与结果
2.1 透皮扩散试验方法的建立
2.1.1 透皮扩散试验一般条件。采用立式改良Franz扩散池(18 mL)及猪腹部离体皮肤。离体皮肤固定于样品池与接受池之间,角质层面向样品池,均匀涂抹乳膏,皮肤背面与接受液紧密接触(不得有气泡)。有效扩散面积约3.3 cm2,接受系统置于(37±0.5)℃的恒温水浴中,电磁搅拌,转速为180 r·min-1。分别于1、3、6、12、24 h取接受液2 mL,并补充相同体积的接受液,24 h后终止试验。
2.1.2 猪离体皮肤的处理。取猪放血处死,经观察皮肤无红肿、充血、破损现象。用电动剃须刀除去腹部毛,取下已去毛的腹部猪皮,小心除去皮下脂肪,洗净,切割成小块皮肤,立即进行透皮试验,其余离体皮肤浸泡于生理盐水中,置于-4℃冰箱中备用。
2.1.3 接受液的选择。接受液应具有接受透皮药物的能力,并尽可能符合类似体内的漏槽条件,常用的接受液有生理盐水和等渗的磷酸盐缓冲液等[1]。盐酸特比萘芬易溶于无水乙醇或甲醇,微溶或极微溶于水[2],根据药物的性质和接受液尽可能接近体内环境的原则,制备了系列溶液进行溶解度试验,结果盐酸特比萘芬原料药在各溶液中的溶解度由大到小依次为:3%甲醇溶液>水≈含0.2%聚山梨酯-80的生理盐水>生理盐水(0.9%氯化钠溶液)>pH7.4磷酸盐缓冲液(取磷酸二氢钾1.36 g,加0.1 mol·L-1氢氧化钠溶液79 mL,用水稀释至200 mL,即得)。参考文献[3,4],在皮肤扩散面积为3.3 cm2时,体外透皮试验用乳膏量通常为0.2~1 g,当乳膏用量为1 g时,若药物的皮肤透过率分别为100%、50%和10%,则接受液中的药物浓度分别为0.56、0.28 、0.056 mg·mL-1,据此考察盐酸特比萘芬原料药在3%甲醇溶液、水与生理盐水中能否达到漏槽条件,结果见表1。

表1 漏槽条件试验结果Tab 1 Results of sink condition test
可见,药物在上述3种溶剂中能否达到漏槽条件要视乳膏中药物的皮肤透过率而定。因此,结合药物的性质及人体体液的实际情况,初步选定3%甲醇溶液、水与生理盐水为接受液。
2.1.4 透皮扩散试验的条件确定。分别取0.2、0.5、1.0 g供试药,均匀涂抹于猪离体皮肤上,分别以上述3种溶液为接受液,每种乳膏用量用每种接受液各做1份,按“2.1.1”项下方法试验,过滤,滤液注入液相色谱仪测定,结果3种不同用量供试品在3种接受液中均未检出盐酸特比萘芬。因此,在样品池能承载的前提下,选定试验用乳膏量为1.0 g;由于预试验结果乳膏中药物几乎不透过皮肤(即皮肤透过率<10%),生理盐水完全可达到漏槽条件,因此,接受液选定生理盐水。
2.2 含量测定方法的建立
2.2.1 色谱条件。色谱柱:Gemini C18(250 mm×4.6 mm,5 μm);流动相:乙腈-甲醇-pH7.5缓冲液(50∶40∶10)(其中缓冲液的制备方法为:取2.0 mL三乙胺,加水至1000 mL,稀醋酸调节pH至7.5);流速:1 mL·min-1;检测波长:224 nm;柱温:室温;进样量:20µL。在此条件下,盐酸特比萘芬的保留时间约为10 min,理论板数不低于10000。
2.2.2 溶液的制备。精密称取盐酸特比萘芬标准品0.01146 g,置于200 mL容量瓶中,加甲醇溶解并稀释至刻度,作为标准品贮备液。精密量取上述溶液1 mL置于10 mL容量瓶中,加生理盐水稀释至刻度,作为标准品溶液(5.73 μg·mL-1,约相当于乳膏透过1%的浓度)。
由于透皮扩散预试验中,各种条件在接受液中均未检出盐酸特比萘芬,因此,取上述标准品贮备液1 mL置于10 mL容量瓶中,加空白基质透过皮肤所得的生理盐水空白渗透液稀释至刻度,滤过,作为供试品溶液a;另取做完扩散试验的整块皮肤,刮去表面残留药膏,用生理盐水冲洗,稍晾干,剪去多余皮肤,将与软膏接触的面积约为3.3 cm2的皮肤剪碎研磨至乳糜状,移至具塞锥形瓶中,加入20 mL无水乙醇,超声提取40 min,5000 r·min-1离心,倾取上清液,滤过,挥干,用甲醇溶解,移至5 mL容量瓶并稀释至刻度,即得供试品溶液b。
取空白基质1 g,按“2.1.1”项下方法试验,24 h后取出空白基质透过皮肤所得的全部接受液,作为阴性对照溶液a;取下皮肤,按上述供试品溶液b的制备方法制备,得皮肤贮留的阴性对照溶液b。
2.2.3 专属性试验。分别取上述标准品溶液、供试品溶液和阴性对照溶液注入液相色谱仪,记录色谱。结果,在同一色谱条件下,接受液的阴性对照溶液a和皮肤贮留的阴性对照溶液b均对测定无干扰,详见图1。
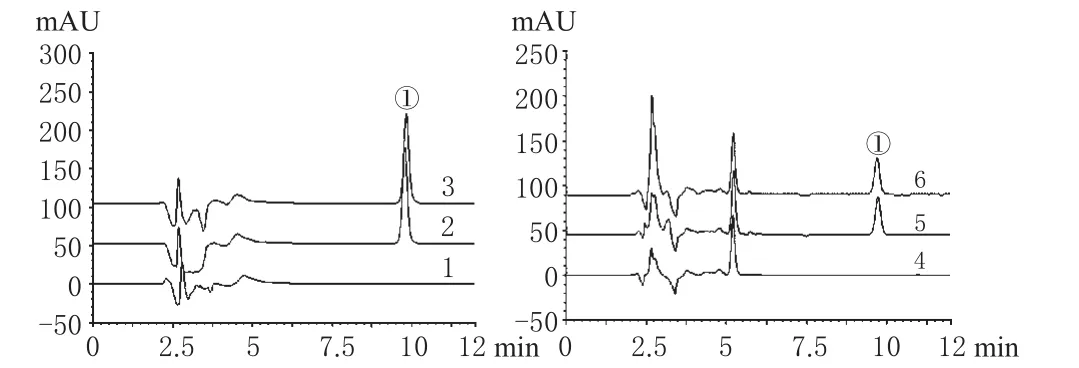
图1 高效液相色谱图1.阴性对照溶液a;2.标准品;3.供试品溶液a;4.阴性对照溶液b;5.标准品;6.供试品溶液b;①.盐酸特比萘芬Fig 1 HPLC chromatograms1.negative control a;2.standard substance;3.test sample a;4.negative control b;5.standard substance;6.test sample b;①.terbinafine hydrochloride
2.2.4 线性及范围。分别精密吸取标准品溶液1、5、10、20、30、40、50µL进样,按上述色谱条件测定,将所得峰面积(A)与实际进样量(X,μg)进行线性回归,得线性方程为A=222.19X+0.2442(r=0.9999),表明盐酸特比萘芬进样量线性范围为0.00573~0.2865 μg。
2.2.5 回收率试验。(1)皮肤透过量的回收率试验:经透皮扩散预试验,接受液中未检出盐酸特比萘芬,因此回收率试验选择了相当于透过0.3%、0.7%、1%3种较低的浓度进行。取空白基质各1 g共6份,均匀涂抹于离体皮肤上,以生理盐水为接受液,按“2.1.1”项下方法试验,24 h后取出全部接受液,作为空白渗透溶液;取下试验后的皮肤,刮去表面残留空白基质,用生理盐水洗净,备用。精密量取“2.2.2”项下标准品贮备液0.3、0.7、1 mL各3份,分别置于10 mL容量瓶内,加空白渗透溶液稀释至刻度;滤过,取滤液,依法测定,记录色谱,代入线性方程,计算得平均回收率为93.43%,RSD为6.92%。(2)皮肤贮留量的回收率试验:取上述空白试验后的皮肤(6块),剪去多余皮肤,将与空白基质接触的面积约为3.3 cm2的皮肤剪碎并研磨至乳糜状,平均分成6份,分别置于具塞锥形瓶中,分别精密加入“2.2.2”项下标准品贮备液1 mL,再加无水乙醇20 mL,超声提取40 min,5000 r·min-1离心,倾取上清液,滤过,挥干,用甲醇溶解,移至5 mL容量瓶并稀释至刻度,滤过;取滤液,依法测定,记录色谱,计算得平均回收率为91.68%,RSD为5.76%。
2.2.6 最低定量限及最低检测限。精密量取供试品溶液a 1 mL(2份),分别置于50、20 mL容量瓶中,加生理盐水稀释至刻度,制成浓度分别为0.1146、0.2865 μg·mL-1的溶液,进样,以信噪比为3时作为最低检测限,信噪比为10时作为最低定量限,结果得盐酸特比萘芬的最低检测限为0.078 μg·mL-1(相当于皮肤透过率0.01%),最低定量限为0.29 μg·mL-1(相当于皮肤透过率0.05%)。
2.2.7 仪器精密度试验。取回收率试验中皮肤透过量供试品溶液和皮肤贮留量供试品溶液,分别连续进样6次,记录峰面积,计算RSD值分别为1.2%、1.7%,表明精密度良好。2.2.8 稳定性试验。取回收率试验中皮肤透过量供试品溶液和皮肤贮留量供试品溶液,分别在于0、1、4、9、12、24 h各测定1次,记录峰面积,计算其RSD值。结果溶液在9 h内较稳定(RSD分别为2.6%、2.2%),在24 h时峰面积均略呈下降趋势,因此,取样后应尽快测定。
2.3 透皮扩散试验结果
取供试药和对照药依法进行透皮扩散试验,分别于1、3、6、12、24 h取接受液2 mL(并即时补充同温度同体积的生理盐水),过滤,滤液注入液相色谱仪,测定药物的皮肤透过率(累积透过率(%)=()(/W样×标示量×106)×100%。其中,cn为第n个取样点的药物浓度(μg·mL-1);ci为第(ii≤n-1)个取样点的药物浓度(μg·mL-1);W样为取样量(g);标示量为10 g∶0.1 g。24 h终止试验后,立即取出皮肤,按“2.2.2”项下供试品溶液b的制备方法制备供试品溶液,依法测定药物皮肤的贮留量,结果见表2。

表2 透皮扩散试验结果(n=6)Tab 2 Results of transdermal diffusion test(n=6)
可见,2种样品中盐酸特比萘芬几乎不透过皮肤,皮肤局部贮药量相近。
3 讨论
由于人皮肤很难获得,根据文献[5]小型猪的皮肤与人的皮肤较为接近,因此选用小型猪腹部皮肤作为体外透皮吸收对比试验的离体皮肤。
[2,6]比较了不同的色谱条件,最终确定了本试验所采用的色谱条件;盐酸特比萘芬在大约224、280 nm波长处有最大吸收,其中224 nm波长处的响应值较大,而本品的皮肤透过率和皮肤贮药量低,为提高检测灵敏度,选定224 nm为测定波长;检测方法中的回收率值结果偏低、RSD值偏大,分析原因可能是检测的浓度较低及皮肤细胞的某些脂质成分可能对药液略有干扰所致。
盐酸特比萘芬乳膏是经皮肤给药以达局部治疗目的,不主张透过皮肤起全身治疗作用。本试验采用小型猪离体皮肤及改良Franz扩散池,考察药物的皮肤透过率,以及皮肤局部的载药情况,结果2种样品中盐酸特比萘芬几乎不透过皮肤,皮肤局部贮药量相近,说明盐酸特比萘芬乳膏发挥的是局部治疗作用,预测2种制剂的药效和安全性基本一致。
参考文献
[1]梁 颖,杨新建.4种透皮吸收促进剂对盐酸苯海拉明透皮性能的影响[J].中国药房,2008,19(31):2414.
[2]British Pharmacopoeia Commission.Terbinafine hydrochloride[DB/OL].www.drugfuture.com/Pharmacopoeia/BP 2009/download.aspx?filename=Terbinafine-Hydrochloride-5893.2010-08-03.
[3]李冬梅,路绪文,苏 芳,等.阿西美辛脂质体凝胶剂的体外透皮扩散研究[J].中国医院药学杂志,2003,23(6):330.
[4]陈 鹰,汤 韧,刘 辉,等.阿昔洛韦棕榈酸酯脂质体凝胶剂的局部透皮试验[J].中国医院药学杂志,2000,20(6):324.
[5]谢松梅,杨志敏,吕 东,等.新法规下皮肤外用药物临床试验要求的相关考虑[EB/OL].www.cde.org.cn/dzkw.do?method=largePage&id=311532.2009-12-02.2010-06-23.
[6]余仕汝,高邵阳,朱红玲,等.盐酸特比萘芬乳膏含量测定方法的改进研究[J].药物分析杂志,2008,28(4):656.
