IEC 60601-1-2医用电气设备电磁兼容标准研究
2011-01-26牛帅蒋岁
【作 者】牛帅,蒋岁
上海市医疗器械检测所,上海市,200070
医用电气设备的电磁兼容(EMC,Electromagnetic Compatibility)涉及公众的健康和安全。近年来,随着公众安全意识的提高,医用电气设备的电磁兼容得到了极大关注。国家食品药品监督管理局于2005年发布了强制性行业标准YY 0505-2005《医用电气设备 第1-2部分:安全通用要求 并列标准:电磁兼容 要求和试验》[1],等同采用国际标准IEC 60601-1-2:2001。YY 0505-2005作为我国第一部涉及医疗器械行业的电磁兼容标准,对整个行业的电磁兼容性研究和发展起到了指导作用[2]。近年来,国内医疗器械相关单位经过积极学习和探索,电磁兼容设计和检测水平明显提高。
研究国际医用电气设备电磁兼容标准,是提高我国医疗器械行业管理水平,加强医疗器械的安全性和质量控制,推动医疗器械行业发展的重要途径。国际标准发展迅速,IEC 60601-1-2新版标准已经发布。本文将通过介绍国际标准的发展,对国内外标准的差异进行初步分析和研究。
1 IEC 60601-1-2的发展过程
IEC 60601-1-2是IEC 60601-1的并列标准,各版本发布时间见图1。
国际电工委员会于1993年发布了IEC 60601-1-2第1版。随后在2001年发布了IEC 60601-1-2第2版,是目前国际广泛流行的医用电气设备的电磁兼容标准。
第2版与第1版的差异主要在以下几方面:
* 包含了有意射频发射器、大型设备的内容;
* 增加了IEC 61000-3-2、IEC 61000-3-3、IEC 61000-4-6、IEC 61000-4-8和 IEC 61000-4-11标准的试验要求;
* 抗扰度试验要求基于“基本性能”、“基本安全”;
* 给出了更加详细的试验方法和要求;
* 包括了可能影响“医用电气设备和系统基本性能”的非医用电气设备。
在此基础上,国际电工委员会于2004年发布了IEC 60601-1-2 Edition2.1[3](以下称IEC 60601-1-2 第2.1版),包括了IEC 60601-1-2:2001和修改件Amend.1。此版本内容变化较多,是本文探讨的重点。IEC 60601-1-2第3版发布于2007年,与IEC 60601-1-2第2.1版相比,最显著的变化为重新制定了条款编号,本文不做讨论。
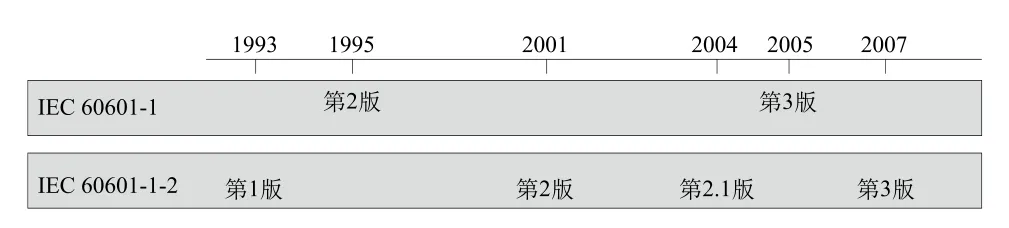
图1 IEC 60601-1、IEC 60601-1-2各版本发布时间Fig.1 – The release time of IEC 60601-1 and IEC 60601-1-2
2 国内外标准的差异
2.1 基本性能
基本性能是医用电气设备一个重要概念。任何设备或系统都有其相应的功能,但并非所有功能都可视为基本性能。YY 0505-2005对“基本性能”有明确定义:保持残留风险在可接受限值内的必需的性能特征。标准规定:设备和系统的基本性能应由风险分析来鉴别。如果没有进行风险分析,设备或系统的所有功能都应考虑作为基本性能进行抗扰度试验。因此,YY 0505-2005标准在实施中应该注意:对设备或系统进行符合性判定的时候,需要检查风险分析文件;如果没有进行风险分析,则通过检查能证实设备或系统的所有功能已按36.202规定进行试验的文件来检验是否符合要求。
IEC 60601-1-2第2.1版删去了“基本性能”的定义。因为IEC 60601-1第二版标准不涉及基本性能。直到IEC 60601-1第3版才提出了“基本安全和基本性能”的概念。为了与IEC 60601-1第2版保持一致,避免与IEC 60601-1第三版的概念冲突,IEC 60601-1-2第2.1版删去了“基本性能”的定义。对于基本性能,第2.1版标准规定:除非判定出设备或系统的基本性能(基本性能判定指南参见附录GGG),否则设备或系统的所有功能都应考虑作为基本性能进行抗扰度试验。基本性能应在随机文件中说明。通过检查随机文件来检验是否符合要求,如果没有进行判定,则通过检查能证实设备或系统所有功能的性能已按36.202规定进行试验的文件来检验是否符合要求。
基本性能是与安全相关的关键准则,缺失和降级都会导致不可接受的风险。IEC 60601-1-2 第2.1版在实施中应该注意:附录GGG并没有给出基本性能的具体判定方法,只有简单一句话“基本性能的定义和判定正在考虑中,在此期间,基本性能概念的进一步资料见IEC 60601-1第3版草案”。因此对于医用电气设备和系统的基本性能,在IEC 60601-1-2 第2.1版中仅仅规定了要求,并没有提供判定方法。这就把设备和系统基本性能如何来确定交给了生产商,要求生产商在随机文件中包含基本性能,通过验证基本性能以便于决定医用电气设备是否合理通过了电磁兼容抗扰度试验。
2.2 非医用电气设备或系统
根据YY 0505-2005标准:“如果满足可适用的国际电磁兼容标准,并能合理地预见其发射和抗扰度不影响系统的基本性能或不增加设备的发射,就可免予本标准要求的电磁兼容试验。不影响系统的基本性能的合理预见的判断应基于风险分析。”作为系统的一部分提供的非医用电气设备,不一定都得根据标准进行电磁兼容试验,可以节约时间和成本。执行本项要求的关键在于,相关人员对非医用电气设备的发射和抗扰度,需要基于风险分析进行一个合理性预判。因此,风险分析文件内容是否准确,决定了这个“合理性预见”的难度。
IEC 60601-1-2 第2.1版的3.201条,对非医用电气设备免于试验有了进一步说明。作为系统的一部分提供的非医用电气设备,可免于本标准要求的电磁兼容试验,如果能证明满足以下所有条件:
(1) 非医用电气设备符合适用的国际电磁兼容标准;
(2) 证实非医用电气设备的发射和抗扰度不会对系统的基本性能或安全产生不利的影响;
(3) 证实非医用电气设备不会导致系统的发射超过适用的限值。
通过检查证实文件和其他适合的文件或证书来检验是否符合要求,如果没有进行证实,则通过检查能证实非医用电气设备已根据本标准规定进行试验的文件来检验是否符合要求。
同时IEC 60601-1-2 第2.1版以流程图的形式给出了系统内的非医用电气设备免于电磁兼容试验要求的判定指南。
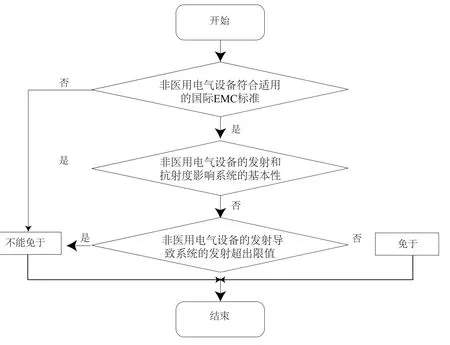
图2 系统内的非医用电气设备是否免于本标准电磁兼容试验要求的判定流程Figure 2 – Procedure for determining if non-medical electrical equipment used in a system is exempt from the EMC testing requirements of this standard
显而易见,IEC 60601-1-2 第2.1版比YY 0505-2005标准要求更加明确,操作性更强。非医用电气设备免于电磁兼容试验需要同时满足上述a)、b)、c)三个条件。IEC 60601-1-2 第2.1版标准实施的关键在于:制造商必须提供能证实非医用电气满足三个条件的证实性文件或其他适合的证书,这些证实性的文件或证书不一定是风险分析文件。如果没有证实文件,那么非医用电气需要进行标准规定的EMC试验。
2.3 风险分析
用于预防、诊断和治疗人体疾病的医疗器械,普遍存在着可能造成不同程度的人体伤害的风险。风险管理是使产品的风险—获益平衡达到最优化的过程[5]。我国在2000年等同转化ISO 14971-1:1998,发布了YY/T 0316 -2000[6]《医疗器械—风险管理:第一部分—风险分析对医疗器械的应用》。根据YY 0316中的定义,风险管理主要包括风险分析、风险评价、风险控制和生产后信息评估四个过程。YY 0505-2005标准引入了风险分析。纵观 YY0505-2005,风险分析主要出现在两部分。其中一部分是伴随基本性能出现的,强调使用风险分析来判定设备抗扰度试验必须检验的基本性能;另一部分是伴随非医用电气设备出现的,强调使用风险分析来判定非医用电气设备是否需要按标准进行试验。
IEC 60601-1-2第2.1版直接要求医用电气设备的基本性能包含在随机文件中,不用通过风险分析来确定基本性能。非医用电气设备免于电磁兼容试验的方法是检查证实文件和其他适合的文件或证书,并不一定是风险分析文件。因此,第2.1版相应的删去了风险分析的内容。
在我国,虽然YY/T 0316标准是推荐性的,但并不意味着风险管理活动在医疗器械中是可以不实施的。在《医疗器械注册管理办法》中,对“境内第二、三类产品首次注册申请”和“未获得境外上市许可的第二、三类境外产品首次注册申请”,均要求必须提交“安全风险分析报告”。IEC 60601-1:2005《医用电气设备 第1部分:基本安全性和基本性能的通用要求》开始引入了风险管理。第4.2条款声明:必须履行符合ISO 14971 规范的风险管理流程。换句话说,要满足第3版的规定,就必须符合ISO 14971。因此,我国医疗器械生产企业必须具备ISO 14971规定的风险管理手段。
2.4 A型专用设备和系统
“A型专用设备和系统”作为IEC 60601-1-2 第2.1版新增的定义,相应增加了试验和随机文件等一系列要求。
在我国,设备或系统对无线电业务的保护,按照GB 4824根据制造商规定的预期用途分成1组或2组和A类或B类。A类和B类是由设备或系统的预期使用环境决定的。A类设备用于与公共电网隔离的工业或轻工环境(比如医院),B类设备用于连接到公共电网中(比如家庭或居民区等其他环境)。B类限值更严酷,对允许的发射有更低的限值要求。
IEC 60601-1-2 第2.1版中,“A型专用设备和系统”定义是:“设备或系统符合CISPR 11的2组B类(除基频的第三次谐波),而第三次谐波符合2组A类电磁辐射骚扰限值的专用设备或系统。”准确把握A型专业设备和系统的实施重点,需理解三个方面:
(1) 使用者
A型专用设备和系统的使用者是有明确的规定,需要由专业医护人员使用。设备和系统“由专业医护人员使用”与“在医疗监督下”是两个不同的概念。“由专业医护人员使用”比“在医疗监督下”范围窄。第2.1版标准中“专用设备和系统”限制了在36.201.1 a)6)中规定由专业医护人员直接操作的设备和系统许可的适用性。相反,“在医疗监督下”包括由专业医护人员通过处方指定使用设备和系统,甚至当专业医护人员不在场时由患者或其他护理提供者操作的设备和系统。
(2) 使用环境
A型专用设备和系统预期在家用设施中使用或连接到公共电网。
用于预防、诊断和治疗人体疾病的某些设备和系统,由于其基频的第三次谐波可能不满足CISPR 11的2组B类电磁辐射骚扰限值,这些设备和系统将不能在家用设施中使用或连接到公共电网上使用。那么这些设备和系统只能限定在与公共电网隔离的场所使用(如医院),而不能在居民区内的诊所或医疗保健提供者的办公室内使用。然而,一些提供理疗服务的诊所通常设在居民区内,没有独立变压器与公共电网隔离。如果没有第2.1版标准的这项许可,这些设备将只能建议用在屏蔽室或医院,其结果是许多患者无法接受治疗,或不得不等待更长的时间来接受治疗。虽然此类设备和系统在家用设施中使用将是合理的,但这种使用可能导致无线电干扰。因此,对这种可能性,有必要向使用者提出警告,并给出降低干扰的建议。
(3) 发射要求
除了基频的第三次谐波之外,A型专业设备和系统应符合CISPR 11的 2组B类,并且第三次谐波符合2组A类电磁辐射骚扰限值。例如,用于理疗的射频治疗设备工作在短波或超高频工科医频率,连续模式下产生400 W,脉冲模式下产生1000 W 的能量来治疗疾病或者缩短康复治疗时间。这些射频能量通过开放的容性或感性“天线”施加给患者。即使目前设备符合在工科医频段对有意射频发生器的要求,如对寄生辐射信号有40dB~60dB的抑制要求,但是设备基频的第三次谐波无法满足CISPR 11的2组B类电磁辐射骚扰限值,然而这些设备和系统有连接到公共电网的使用需求。对于此类设备和系统,根据第2.1版标准36.201.1 a)6)条,允许在家庭设施中使用或连接到公共电网使用,但随机文件应包括设备或系统基频的第三次谐波不满足CISPR 11的2组B类电磁辐射骚扰限值的理由。理由应该基于重要物理方面、技术方面或生理方面的限制。
3 总结
讨论和研究IEC 60601-1-2 国际标准的发展,对YY 0505-2005的制修订具有重要的启发作用。发展和完善YY 0505-2005,必将有助于保障我国医疗器械的安全、有效,保持良好的医疗环境,进一步提高我国医疗器械的市场竞争能力。IEC 60601-1-2标准的内容非常丰富,本文只是对标准的初步理解,希望引起大家的关注和研究,有助于我国医疗器械行业转化国际标准的合理性和准确性。
[1] YY 0505—2005. 医用电气设备 第1-2 部分: 安全通用要求并列标准: 电磁兼容 要求和试验 [S].
[2] 刘京林. 解读医疗EMC法规——YY0505[J]. 现代医学仪器与应用. 2007, 19(2): 34-37.
[3] IEC 60601-1-2 edition2.1.Medical electrical equipment –Part 1-2: General requirements for safety –Collateral standard:Electromagnetic compatibility –Requirements and tests [S].
[4] IEC 60601-1: 2005. Medical electrical equipment – Part 1: General requirements for basic safety and essential performance [S].
[5] 王兰明. 谈我国医疗器械风险管理的法规要求[J]. 中国医疗器械杂志. 2007, 33(1): 46-50.
[6] YY/T 0316—2008. 医疗器械 风险管理对医疗器械的应用[S].
