非晶态磷酸锡去除高盐介质中Pb (II)研究
2011-01-12祝春水王丽萍贡梅玲曹文秀
祝春水, 王丽萍 , 贡梅玲, 曹文秀
(1. 淮海工学院 化学工程学院, 江苏 连云港 222005; 2. 中国矿业大学 环境与测绘工程学院, 江苏 徐州221008)
非晶态磷酸锡去除高盐介质中Pb (II)研究
祝春水1,2, 王丽萍2, 贡梅玲1, 曹文秀1
(1. 淮海工学院 化学工程学院, 江苏 连云港 222005; 2. 中国矿业大学 环境与测绘工程学院, 江苏 徐州221008)
利用合成的非晶态磷酸锡作为吸附剂, 研究了多种因素(pH、吸附时间、初始浓度、温度、离子强度)对吸附剂吸附水溶液中Pb2+的影响。结果表明, 非晶态磷酸锡对Pb2+的吸附量随着pH(3~6)以及吸附时间的增大而增加。用Freundlich、Langmuir模型对等温吸附数据进行处理, Langmuir方程拟合效果最好, 20℃时饱和吸附量达到377.36 mg/g。Dubinin-Radushkevich (D-R)模型研究表明, 吸附机理属于化学离子交换。反应机理为非晶态磷酸锡中的H+与溶液中的Pb2+发生了离子交换反应。吸附过程的热力学研究表明, 非晶态磷酸锡对Pb2+的吸附是一个自发的, 吸热的过程, 升温有利于吸附。离子强度实验结果表明, 高盐强度对非晶态磷酸锡吸附 Pb2+有一定的不利影响, 但幅度不大, 可以用于去除养殖海水中的Pb2+。所吸附的Pb2+可以用HCl解吸, 说明非晶态磷酸锡具有重复利用的潜能。
非晶态磷酸锡; 高盐介质; 铅; 离子交换
随着经济发展的加快, 沿海城市的港口建设、临海工业、近海养殖等海洋开发活动获得了前所未有的发展, 也给近岸海域的环境带来了不利的影响。反过来, 海水污染又损害了水产养殖产品的品质。其中重金属是影响水产品品质的重要污染物。
重金属离子具有分布范围广, 持续时间长, 不易在物质循环和能量交换中分解的特点, 可以在生物体内富集并沿食物链传递, 最终危害到人类[1]。徐颖[2]在全国第2次海洋污染基线调查工作基础上, 研究了连云港附近海域水环境质量, 结果表明, 连云港附近海域已受到重金属和有机物的污染, 其中 Pb和Hg的污染较重。陈秀开等[3]研究了海州湾近海海水、沉积物及贝类体内重金属的含量和分布特征, 发现所检7种生物样品共36个, 均检出Hg、As、Cu、Pb、Cd、Zn等6种重金属, 并都有不同程度的超标。王晓宇等[4]发现, 四角蛤蜊对 Cd2+和 Hg2+有较强的耐受特性, 容易产生富集, 而不易表现出受胁迫症状。Kumaqai和 Sacki[5]测定日本缀锦蛤体内的重金属元素发现, Hg、Cd、Pb、As含量随体长的增长而增加。
作为一种新兴的重金属去除技术, 吸附法具有投资少、操作简单、适用性强等优点, 目前研究十分活跃。然而, 大多数吸附剂的吸附性能都随着离子强度的增加而快速递减[6-10], 在高盐强度的海水环境中无法应用。
磷酸锡具有不溶于水和有机溶剂, 能耐强的酸度和一定碱度, 耐辐射, 热稳定性和机械强度很强, 化学稳定性较高, 比表面积大, 表面电荷密度较大等优点。本研究通过化学合成得到非晶态磷酸锡, 用于去除高盐废水中的铅离子。可以为养殖海水中重金属离子的去除提供有益的参考和指导。
1 材料与方法
1.1 仪器与试剂
电子天平(BS224S, 北京赛多利斯天平有限公司); 精密 pH计(PHSJ-5, 上海雷磁公司); 智能全温空气振荡器(HZQ-QX, 哈尔滨市东联电子技术开发有限公司); 电位滴定仪(ZDJ-4A, 上海精密科学仪器有限公司); 原子吸收分光光度计(TAS-990, 北京普析通用仪器有限公司); X射线衍射仪(X’TRA, 瑞士ARL公司)。
实验中所用试剂均为分析纯。
1.2 材料制备
按照文献方法制备非晶态磷酸锡[11]。室温下将0.3 mol/L的SnCl4逐滴滴加到0.6 mol/L的H3PO4溶液中, 并且不断搅拌, 反应完毕后, 过夜陈化。然后用蒸馏水洗涤产物, 直至洗涤液中未检出 Cl-。真空干燥(45℃)、研磨、过160目筛, 保存于干燥器中备用。
所得样品的XRD图见图1, 其中在2θ为21°、26°等位置附近有微弱的磷酸锡的衍射峰, 表明产品为非晶态磷酸锡(图1)。

图1 非晶态磷酸锡XRD图Fig. 1 XRD spectrum of amorphous tin (IV) hydrogenphosphate
1.3 实验方法
1.3.1 吸附平衡实验
称取一定质量的样品于250 mL锥形瓶中, 加入一定体积的Pb2+贮备液, 加蒸馏水至50 mL, 得到所需浓度的溶液, 用0.5 mol/L NaOH或HCl调节溶液pH, 置于恒温振荡器中于一定温度下振荡(120 r/min)。到达反应时间后取出样品, 用滤纸过滤, 弃去初始 30 mL滤液, 用火焰原子吸收法测定余下的滤液中Pb2+的含量。
按下式计算吸附量q(mg/g):

式中:C0为 Pb2+的初始质量浓度, mg/L;Ce为 Pb2+的平衡浓度, mg/L;V为Pb2+溶液体积, L;m为样品质量,g。
1.3.2 Pb2+分析方法
Pb2+的浓度用原子吸收光度法(GB/T 7475-1987)分析。
2 结果与讨论
2.1 pH因素的影响
准确移取50 mL 50 mg/L的Pb2+溶液6份于250 mL锥形瓶中, 分别调节pH至3.0, 4.0, 4.5, 5.0, 5.5,6.0, 加入0.100 0 g样品, 在25℃下振荡24 h后过滤,测定浓度。实验结果见图2。

图2 pH对非晶态磷酸锡吸附Pb2+的影响Fig. 2 Effect of pH on the sorption of Pb (II) with amorphous SnP
pH对吸附剂的表面电荷和电离程度会产生影响[12], 因而在吸附过程中是一个重要的影响因素。从图2中可以看出, 非晶态磷酸锡对 Pb2+的吸附量在3~4.5范围内随着pH的升高而快速增加, 当pH>4.5时, 吸附量没有明显的变化。这可能是因为, 当 pH较低时, 溶液中的 H+较多, 环绕在吸附剂周围, 对正电荷金属离子产生斥力, 影响吸附剂对 Pb2+的吸附[13]。当pH升至4.5以上时, 吸附量q值接近非晶态磷酸锡对 Pb2+的吸附能力, 基本达到一个动态平衡, 因而吸附量的变化减小。后续吸附实验确定pH5。
2.2 时间对吸附过程的影响
准确移入50 mL50 mg/L的铅标准使用液于一系列锥形瓶中, 调节pH至5.00±0.02, 分别加入0.100 0 g样品, 于温度20、25、30℃下, 分别振荡10、30、60、120、180、300、360、480 min 后过滤, 测定滤液中Pb2+浓度, 结果见图3。
由图3可知, 相同温度下, 非晶态磷酸锡对Pb2+的吸附量随时间呈现上升趋势, 在相同的吸附时间内, 吸附量随着温度的升高而增大。在60 min前, 由于吸附剂表面有足够的吸附位点, 吸附量迅速增加,随着 Pb2+的覆盖范围越来越大, 吸附位点越来越少[14], 60 min以后q增加速度减慢, 360 min以后吸附量基本达到平衡, 由此可以取吸附最佳时间为 360 min。

图3 不同温度下非晶态磷酸锡吸附Pb2+的动力学曲线Fig. 3 Effect of time on the removal of lead at different temperatures
Li等[15]在 10、20、30、40℃4 个温度下, 用废弃的小麦粒吸附水溶液中的Pb2+, 均在30 min后吸附达到平衡, 吸附量在3.4 mg/g左右。与本实验相比,吸附速率比本实验快, 但本实验的吸附效果较好,吸附量为24.5~25 mg/g。
2.3 等温吸附研究
准确移取初始浓度为 29、48、96、195、486、778、973 mg/L的铅标准溶液各50 mL, pH均调至5.0±0.02, 分别投加 0.100 0 g样品, 于 20℃下振荡360 min后过滤, 测定滤液Pb2+浓度。在25、30℃下重复上述实验。结果见图4。

图4 非晶态磷酸锡吸附Pb2+的吸附等温线Fig. 4 Sorption isotherm of Pb2+ on amorphous SnP at different temperatures
评价吸附剂吸附能力最好的方法是将整个吸附过程用吸附等温线来描述。本论文利用Langmuir模型、Freundlich模型和Dubinin-Radushkevich模型进行拟合。
(1)Langmuir模型

式中:qm为平衡时铅离子的最大吸附量, mg/g;Ce为溶液平衡浓度, mg/L;b为与吸附亲和力有关的常数,L/mg。
(2) Freundlich模型
式中:qe是平衡状态下的吸附量, mg/g;Ce是平衡状态下溶液中金属的浓度, mg/L;Kf和n是两个经验常数, 对于指定的吸附系统, 它们是温度的函数, 分别代表吸附能力和吸附优惠性强度[16]。
(3) Dubinin-Radushkevich(D-R)等温方程

ε值可由下式计算得到:

式中:β——与吸附能有关的常数, mol2/kJ2;
ε——波兰尼吸附势, kJ/mol;
Ce——溶液的平衡浓度, mol/L;
q,qm——平衡吸附量和最大吸附量, mol/g;
Es——吸附能, kJ/mol。
Langmuir和Freundlich模型拟合参数见表1。
由表1可见, Langmuir和Freundlich模型均可较好地拟合该等温吸附过程, 但 Langmuir拟合效果更佳, 相关系数r达到0.99以上。最大吸附量qm随着温度的升高而增大, 说明升温有利于吸附的进行。b是与吸附强度有关的常数, 该参数越大, 说明趋近最大吸附量所对应的平衡质量浓度越低, 吸附剂的低质量浓度吸附性能越好[17], 且吸附呈单分子层形式。
平衡参数RL(Separation factor or Equilibrium parameter)定义为:

式中:b为 Langmuir常数;C0为溶液的初始浓度(mg/L)。
以RL对C0作图, 见图5。

表1 Langmuir和Freundlich模型拟合参数Tab. 1 Parameters of Langmuir and Freundlich isotherm

图5 三个温度下不同浓度的平衡常数RLFig. 5 Curves of RL vs. C0 at different temperatures and concentrations
当 0<RL<1 时, 表明有利于吸附,RL>1 时表明不利于吸附[18], 通过计算, 本实验中的平衡参数RL均在0至1之间。由此看出, 选用非晶态磷酸锡作为吸附剂去除水溶液中的Pb2+是可行的, 且温度越高,RL值越小, 越有利于吸附。
上述Langmuir和Freundlich 模型还不足以解释吸附过程的物理和化学吸附特性, 而 D-R模型可用于判断吸附过程的性质[15]。D-R模型的拟合参数见表2。

表2 D-R方程拟合参数Tab. 2 Parameters of D-R equation
D-R方程中Es值反映了在吸附剂表面每 1mol离子发生离子交换需要的能量,Es值介于 8~16 kJ/mol之间时, 表明该吸附过程是化学离子交换;当Es值小于8 kJ/mol时, 表明该吸附过程是物理吸附过程[19]。由表2可知, 在三个温度下Es的值均在8~16 kJ/mol之间, 因此本实验的吸附机理属于化学离子交换。
2.4 解吸实验
准确移取50 mL 1 000 mg/L铅标准溶液, 将pH调至5, 投加0.200 0g非晶态磷酸锡, 振荡6 h后过滤、稀释, 测定滤液中Pb2+浓度。收集滤纸上的非晶态磷酸锡, 用少量蒸馏水洗涤, 干燥。分别用0.5、3、5 mol/L HCl和3 mol/LHNO3溶液浸泡收集的样品,振荡6 h后过滤, 稀释, 测定解吸液中Pb2+浓度。解吸实验结果见表3。
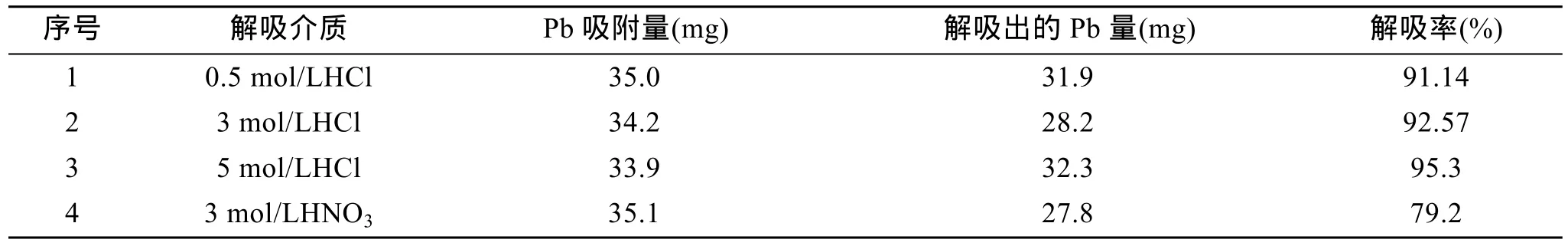
表3 非晶态磷酸锡所吸附Pb(II)的解吸率Tab. 3 Desorption ratios of Pb (II)
从上表中可以看出, 随着HCl浓度增加, Pb2+的解吸率随之提高, 用5 mol/L HCl解吸时, 解吸率达到95.3%, 解吸效果良好, 说明非晶态磷酸锡具有重复利用的潜能。表3还表明, HCl比HNO3更适合作为解吸介质。
2.5 离子强度实验
通过离子强度实验, 可以判断制备的材料在高盐强度(海水介质)下应用的可行性。
实验中, 分别配制 50 mL铅浓度为 50 mg/L、NaCl浓度为 0、0.15、0.3、0.6 mol/L的混合溶液, 其他条件同2.3进行吸附实验。结果见图6。

图6 NaCl浓度对非晶态磷酸锡吸附Pb2+的影响Fig. 6 Effect of NaCl concentration on the sorption of Pb2+with amorphous SnP
徐洁等[20]研究了离子强度对东北草甸棕壤吸附Pb2+的影响, 在加入 1mol/L NaNO3后, 吸附量由 9 mg/g降低至2 mg/g, 说明体系离子强度增大不利于东北草吸附 Pb2+。林友文等[21]用羧甲基壳聚糖吸附Pb2+, 随着 KNO3浓度增大, 吸附速度逐渐减慢, 吸附量逐渐减小。李英敏等[22]用小球藻吸附Pb2+, 以高氯酸钠调节离子强度, 当浓度由0.005 mol/L提高到0.5 mol/L时, 去除率由73.2%降低到63.8%。
本研究中, 随着溶液中的 NaCl浓度的增加, 吸附量有少量减小。溶液中的NaCl浓度达到0.6 mol/L时, 非晶态磷酸锡对 Pb2+的吸附量仍然达到 21.684 mg/g, 是不含NaCl时吸附量的87.34 %, 说明体系离子强度对非晶态磷酸锡吸附 Pb2+存在不利影响, 但影响幅度不大。
已知海水中的含盐量约为3 %(约合NaCl 浓度0.5 mol/L), 而本研究中 NaCl设定浓度为 0~0.6 mol/L, 因此, 用非晶态磷酸锡去除养殖海水中的Pb2+是完全可行的。
2.6 热力学研究
Gibbs自由能ΔG0是衡量反应自发进行的标准,如果ΔG0为负值, 说明在一定温度下反应是自发进行的。在吸附反应中, 自由能变ΔG0与平衡常数k有关, 存在以下关系式[23]:

式中:ΔG0是反应自由能变, kJ/mol;R是气体反应常数, 为 8.314 J/(mol·K);T是绝对温度,K。k=b×207.2×1000,b为Langmuir常数。

式中:ΔH0为反应焓, kJ/mol; ΔS0为反应熵,kJ/(mol·K)。
以ΔG0对 T作图, 其截距即为ΔH0, 其斜率即为ΔS0。不同温度下的热力学参数见表4。

表4 非晶态磷酸锡吸附Pb2+的热力学参数Tab. 4 Thermodynamic parameters of Pb2+ sorption with amorphous SnP
由表4可见, 各温度下吉布斯自由能ΔG0为负值,说明非晶态磷酸锡对铅离子的吸附是自发的。随着温度的升高, ΔG0减小, 表明温度越高自发程度越大。反应焓变ΔH0反映了吸附系统热的变化情况, 在本实验中ΔH0为正值, 说明非晶态磷酸锡吸附铅为吸热过程, 升温有利于吸附。
根据熵增原理, ΔS0>0意味着反应时吸附界面上的混乱度增加。这可能是因为 Pb2+在溶液中不仅以简单的离子形式存在, 还会发生水解生成 Pb(OH)+及与水结合形成水合离子, 当它们被吸附时, OH-及结合水离解出来, 从而增加系统的熵值, 导致ΔS0>0。
2.7 反应机理分析
2.7.1 pH变化与吸附量的关系
吸附反应前, 溶液的 pH值均调节为 5, 吸附反应后, 溶液中的pH值都不同程度的降低。在20℃的等温吸附实验后, 分别测定不同初始浓度的剩余溶液的pH值, 以样品吸附的Pb2+量为横坐标, 吸附前后的H+变化量为纵坐标作图, 见图7。
由图7可见, Pb2+吸附量越大, pH值下降程度越大, H+量增加越多。说明样品的吸附过程为非晶态磷酸锡中的H+与其表面吸附的Pb2+发生了离子交换反应。直线的斜率为 2.07, 接近 Pb2+与 H+的理论反应摩尔比 2.0, 表明吸附过程可能的反应机理如下:Sn(HPO4)2·2H2O+ Pb2+→SnPb(PO4)2·2H2O + 2H+。
2.7.2 电位滴定实验
(1) 空白实验:在溶液杯中加入 50 mL 0.1 mol/L的NaCl溶液, 用0.01mol/L的NaOH溶液调节pH, 用电位滴定仪滴定至pH为9时, 停止滴定。

图7 Pb2+的吸附量与吸附后溶液中H+增加量关系Fig. 7 Relation between pH and sorption capacity
(2) 在NaCl溶液中分别加入0.100 0 g非晶态磷酸锡, 25 mL100mg/L铅标准溶液, 及同时加入上述两种物质, 用电位滴定仪滴定。
以加入的NaOH溶液体积为横坐标, 以pH为纵坐标作图, 得图8、9:

图8 NaCl介质中的空白滴定Fig. 8 pH-titration in the media of NaCl (blank titration)

图9 NaCl介质中样品滴定Fig. 9 pH titration curves in the media of NaCl
将加入样品后的曲线与空白实验做比较可以看出, 加入样品后, 溶液的 pH值明显下降了, 进一步验证了吸附剂对 Pb2+的吸附机理是样品吸附的 Pb2+与样品中的H+发生了离子交换反应。
3 结论
(1) 在20、25、30℃3个温度下, 吸附过程均很好的符合 Langmuir等温式, 饱和吸附量分别为377.36、378.79和 408.16 mg/g。
(2) 非晶态磷酸锡吸附铅的过程是一个化学离子交换过程。吸附机理是非晶态磷酸锡中的H+与溶液中的Pb2+发生了离子交换反应。
(3) 在较高浓度的HCl介质中, 非晶态磷酸锡吸附的铅可以解吸回收, 说明非晶态磷酸锡具有重复利用的潜能。
(4) 离子强度实验结果表明, 用非晶态磷酸锡去除高盐度介质(如养殖海水)中的 Pb2+是完全可行的。
[1]王晓宇, 杨红生, 王清. 重金属污染胁迫对双壳贝类生态毒理效应研究进展[J]. 海洋科学, 2009, 33(10):112-118.
[2]徐颖. 连云港附近海域水环境质量评价[J]. 海洋环境科学, 2001, 20(4):54-60.
[3]陈秀开, 田慧娟, 刘吉堂, 等. 海州湾近海海水、沉积物及贝类体内重金属的含量和分布特征[J]. 检验检疫学刊, 2009, 19(5):6-11.
[4]王晓宇, 王清, 杨红生. 镉和汞两种重金属离子对四角蛤蜊的急性毒性[J]. 海洋科学, 2009, 33(12):24-29.
[5]Kumaqai H, Sacki K. Variation pattern of heavy metal content of short neck clamTapes japonicawith its growth [J]. Bulletin of the Japanese Society of Fisheries Oceanography, 1998, 47(11):1511-1513.
[6]黄鑫, 高乃云, 张巧丽. 改性活性炭对镉的吸附研究[J].同济大学学报(自然科学版), 2008, 36(4):508-517.
[7]刘峙嵘, 韦鹏, 曾凯. pH和离子强度对泥煤吸附镍的影响[J]. 煤炭学报, 2007, 32(8):854-861.
[8]彭华荣, 李晓湘. 钠基累托石对水溶液中镍(Ⅱ)离子的吸附性能[J]. 材料保护, 2009, 42(2):79-81.
[9]张波涛, 董德明, 杨帆, 等. 溶液离子强度对自然水体生物膜吸附 Pb2+和 Cd2+的影响[J]. 吉林大学学报(地球科学版), 2004, 34(4):566-570.
[10]张晋京, 王帅, 窦森, 等. 土壤粗胡敏素对铜离子的吸附作用及其影响因素[J]. 环境科学学报, 2008,28(12):2527-2533.
[11]Varshney K G, Rafiquee M Z A, Amita somya. Effect of surfactants on the adsorption behavior of tin(IV) phosphate, cation exchanger for alkaline earths and heavy metal ions [J]. Colloids and Surfaces A:Physicochem Eng Aspects, 2007, 224-228.
[12]Mustafa Imamoglu, Oktay Tekir. Removal of copper (II)and lead (II) ions from aqueous solutions by adsorption on activated carbon from a new precursor hazelnut husks [J]. Desalination ,2008, 228:108-113.
[13]Ismail Kiran, Tamer Akar, Sibel Tunali. Biosorption of Pb(II) and Cu(II) from aqueous solutions by pretreated biomass of Neurospora crassa[J]. Process Biochemistry,2005, 40:3550-3558.
[14]Zhang Shuqin, Hou Wanguo. Adsorption behavior of Pb(II) on montmorillonite [J]. Colloids and Surfaces A:Physicochem Eng Aspects, 2008, 320:92–97.
[15]Zhu Liqing, Chai Liyuan, Yang Zhihui, et al. Kinetics and thermodynamics of Pb(II) adsorption onto modified spent grain from aqueous solutions[J]. Applied Surface Science, 2009, 255:4298-4303.
[16]Jung M W, Ahn K H, Lee Y H. Evaluation on the adsorption capabilities of new chemically modified polymeric adsorbents with protoporphyrin IX [J]. J Chromatogr A, 2001, 917(1):87-93.
[17]刘丽莉, 景有海, 欧阳通. 水合氧化铈吸附水中磷酸根特性的研究[J]. 安全与环境学报, 2007, 7(2):64-67.
[18]Koble R A, Corrigan T E. Adsorption isotherms for pure hydrocarbons [J]. Ind Eng Chem, 2004, 279:307-313.
[19]Ahmet Sar, Mustafa Tuzen, Ozgur Dogan Uluozlu, et al.Biosorption of Pb(II) and Ni(II) from aqueous solution by lichen (Cladonia furcata) biomass[J]. Biochemical Engineering Journal, 2007, 37:151-158.
[20]徐洁, 侯万国, 周维芝, 等. 东北草甸棕壤对重金属铅的吸附行为研究[J]. 山东大学学报. 2007, 42(5):50-54.
[21]林友文, 陈伟, 罗红斌. 羧甲基壳聚糖对铅离子的吸附性能研究[J]. 离子交换与吸附, 2001, 17(4):333-338.
[22]李英敏, 杨海波, 吕福荣, 等. 小球藻对 Pb2+的吸附及生物吸附机理探讨[J]. 农业环境科学学报, 2004,23(4):696-699.
[23]邱宇平, 陈金龙, 李爱民, 等. 超高交联树脂吸附酚类的热力学研究与机理探讨[J]. 水处理技术, 2004,30(2):82-87.
Removal of lead(II) from hypersaline media with amorphous tin(IV) phosphate
ZHU Chun-shui1,2, WANG Li-ping2, GONG Meiling1, CAO Wen-xiu1
(1. School of Chemical Engineering, Huai-hai Institute of Technology, Lianyungang 222005, China; 2. School of Environment Science and Spatial Informatics, China university of Mining and technology, Xuzhou, 221008, China)
Aug., 31, 2010
amorphous tin(IV) phosphate; hypersaline media; lead; ion exchange
Amorphous tin (IV) phosphate was used as an adsorbent to remove Pb (II) from aqueous solution. The extent of adsorption was investigated as a function of pH, contact time, adsorbate concentration, reaction temperature, and ionic strength. Experimental results showed that the amount of adsorbed lead ions increased with the increases of solution pH in the examined range (3~6) and reaction time. The equilibrium data were analyzed using the Freundlich or Langmuir isotherm model depending on temperature. The results showed that the sorption process followed the Langmuir model well. The maximum sorption capacity amounted to 377.36 mg/g at 20℃.The free energyEs(kJ/mol) obtained from the D-R isotherm also indicated the sorption process was mediated by an ion-exchange mechanism between Pb2+and H+. The negative ΔG0values and the positive ΔH0and ΔS0at various temperatures confirmed the adsorption processes were spontaneous and endothermic. Ionic strength experiments showed that it was feasible for amorphous tin(IV) phosphate in removing Pb2+from hyper-saline media, such as marine culture wastewater. Desorption experiment in the media of HCl solution indicated the adsorbent could be reused, which enhanced its feasibility in practical application.
X55 文献标识码:A 文章编号:1000-3096(2011)11-0090-07
2010-08-31;
2010-11-28
江苏省海洋资源开发研究院科技开放基金项目(JSIMR09D03); 江苏省研究生培养创新工程项目, 淮海工学院自然科学基金项目(Z2009017)
祝春水(1979-), 男, 浙江江山人, 讲师, 博士研究生,研究方向:环境污染治理,电话 :0518-85895410, E-mail:silk588@126.com
康亦兼)
