西他列汀外消旋体的合成及拆分*
2010-11-26高仁孝丁志新
叶 飞, 高仁孝,, 沈 宁, 丁志新
(1. 西安建筑科技大学 理学院 化学系,陕西 西安 710055; 2. 西安瑞联近代电子材料有限责任公司,陕西 西安 710077)
西他列汀{8,化学名7-[(3R)-3-氨基-1-氧-4-(2,4,5-三氟苯基)丁基]-3-三氟甲基-5,6,7,8-四氢[1,2,4]三唑并[4,3-a]哌嗪磷酸水合物}是默克公司研发并于2006年经美国食品药品管理局批准,用于治疗Ⅱ型糖尿病的首个DDP-Ⅳ抑制剂,其商品名为Januvia。8主要通过保护胰高血糖素样肽-1(GLP-1)和肠抑胃肽(GIP)以达到治疗糖尿病的目的[1]。Scott等[2]的研究显示,8具有良好的耐药性和安全性。
8的合成方法较多,工业上主要采用默克公司[3~6]的最新方法:以[(COD)RhCl]2和Josiphos SL-J002-1为手性催化剂不对称氢化烯胺(氢化转化率82%~89%,ee值89%~95%);再与磷酸生成8的磷酸盐。该路线需昂贵的催化剂,且反应条件苛刻。
本文改用廉价的NaBH4代替昂贵的手性催化剂,并以(-)-二对甲苯酰-L-酒石酸为拆分剂制得8。



Scheme1
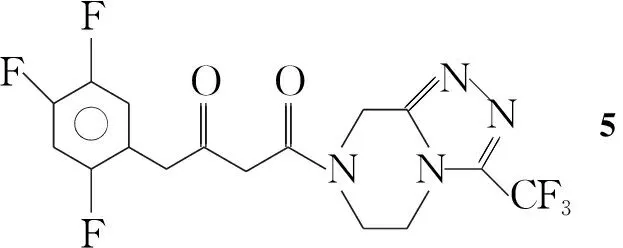
以2-氯吡嗪为原料制备3-(三氟甲基)-5,6,7,8-四氢-3-三氟甲基-1,2,4-三唑并[4,3-a]吡嗪盐酸盐(3)[7~9]。N,N-羰基二咪唑活化2,4,5-三氟苯乙酸与丙二酸亚异丙酯反应得5-[1-羟基-2-(2,4,5-三氟苯基)亚乙基]-2,2-二甲基-1,3-二氧六环-4,6-二酮(4);4与3缩合制得4-氧代-4-[3-(三氟甲基)-5,6-二氢[1,2,4]三唑并[4,3-a]哌嗪-7(8H)-基]-1-(2,4,5-三氟苯基)丁烷-2-酮(5);5在甲醇中完成氨化制得6;6经NaBH4还原制得西他列汀外消旋体(7);7经(-)-二对甲苯酰-L-酒石酸拆分,再与磷酸反应合成了ee>93%的8(Scheme 1),其结构经1H NMR, IR和MS表征。
1 实验部分
1.1 仪器与试剂
Bruker Avanceav 500型核磁共振仪(D2O为溶剂, TMS为内标);Bruker TENSOR 27型傅立叶变换红外光谱仪(KBr压片);Shimadzu LCMS-2010EV型质谱仪;Shimadzu LC-10ATVP型液相色谱仪(HPLC); Shimadzu DSC-60型示差扫描量热分析仪。
2-氯吡嗪,河北省邯郸市赵都精细化工厂;2,4,5-三氟苯乙酸,上海瀚威化学发展有限公司;丙二酸亚异丙酯,常州莱茵达医药原料有限公司;N,N-羰基二咪唑,盐城市药物化工厂;(-)-二对甲苯酰-L-酒石酸,上海翰鸿化工科技有限责任公司;其余所用试剂均为工业品。
1.2 合成
(1) 2-肼基吡嗪(1)的合成
氮气保护。在三口瓶中加入80%水合肼62.6 g(1.0 mol),搅拌下于60 ℃滴加2-氯吡嗪23 g(0.2 mol),滴毕,于65 ℃反应5 h(TLC跟踪)。冰浴降温至2 ℃(析出浅黄色晶体),过滤,滤饼干燥得浅黄色固体120.9 g,收率95.0%,纯度97.4%(HPLC,下同);ESI-MSm/z: 111(M++H)。
(2) 3-(三氟甲基)-1,2,4-三唑并[4,3-a]吡嗪(2)的合成
氮气保护。在三口瓶中加入111.0 g(0.1 mol),冷却至-5 ℃,搅拌下缓慢滴加三氟乙酸酐42 mL(0.3 mol)(控制在0 ℃以下),滴毕,于室温反应2 h;加入多聚磷酸(未稀释)50 mL(反应液变为橘红色),回流反应2 h。滴加水100 mL(控制在40 ℃以下),滴毕,用NaOH溶液调至pH 7~8(反应液由橘红色变为黄色,并有大量浅黄色固体析出)。过滤,滤液用乙酸乙酯(3×100 mL)萃取,合并有机层,用饱和食盐水洗涤,无水硫酸镁干燥,蒸干溶剂,残余物用正己烷重结晶得淡黄色固体27.7 g,收率70.1%,纯度99.8%, m.p.104.7 ℃; ESI-MSm/z: 189(M++H)。
(3)3的合成
在三口瓶中加入23.5 g(19 mmol),乙醇100 mL和10%Pd/C 0.8 g,于30 ℃常压加氢反应4.5 h(TLC跟踪)。滤除钯碳,滤液浓缩至原体积的1/2,于室温通入HCl气体至不再有白色固体析出。过滤,滤饼干燥得白色晶体32.5 g,收率59.8%,纯度97.7%; ESI-MSm/z: 193(M++H)。
(4)4的合成
在三口瓶中加入2,4,5-三氟苯乙酸5.0 g(26 mmol)的THF(80 mL)溶液,N,N-羰基二咪唑5.0 g(31 mmol)活化,搅拌下于50 ℃加入丙二酸亚异丙酯4.2 g(29 mmol),反应5 h(TLC跟踪);缓慢降温至30 ℃。加入50%乙酸异丙酯水溶液60 mL(反应液颜色变为橘红色),反应30 min。用浓盐酸调至pH 2~3,静置分层,有机层蒸干溶剂后得浅黄色固体,用混合溶剂[V(正庚烷) ∶V(乙酸异丙酯)=2 ∶1]60 mL于2 ℃搅拌1 h后过滤,滤饼干燥得白色针状晶体46.1 g,收率87.2%,纯度99.2%, m.p.121.9 ℃; ESI-MSm/z: 317(M++H)。
(5)5的合成
在三口瓶中加入乙酸异丙酯50 mL,45.0 g(16 mmol)和33.6 g(16 mmol),搅拌下滴加N,N-二异丙基乙胺3 mL,滴毕,于80 ℃反应5 h。缓慢降温至30 ℃,加水50 mL,分液,有机层用水(3×50 mL)洗涤,浓缩至10 mL,滴加正庚烷60 mL,滴毕,搅拌2 h,过滤,滤饼干燥得浅黄色固体54.3 g,收率66.7%,纯度90.1%。
(6)6的合成
在三口瓶中加入510.0 g(25 mmol)的甲醇(100 mL)溶液,醋酸铵9.5 g(125 mmol),氨水10 mL,搅拌下于58 ℃反应30 min后有白色固体析出,继续反应2 h。降至室温后过滤,滤饼干燥得白色固体69.2 g,收率92.2%,纯度99.3%, m.p.197.3 ℃; ESI-MSm/z: 406(M++H)。
(7)7的合成
在三口瓶中加入THF 50 mL,于-10 ℃加入NaBH41.0 g,搅拌下滴加甲基磺酸2.0 g(保持-5 ℃左右),滴毕,加入61.0 g(2 mmol)的异丙醇(10 mL)溶液,于-15 ℃反应4.5 h。加水30 mL,用乙酸乙酯(2×60 mL)萃取,合并有机相,用无水硫酸镁干燥,旋干溶剂得无色油状液体70.6 g,收率59.7%。
(8)8的合成
在三口瓶中加入(-)-二对甲苯酰-L-酒石酸0.5 g的异丙醇(15 mL)溶液,于65 ℃加入70.5 g(1 mmol)的甲醇(15 mL)溶液,搅拌30 min后有白色固体析出。过滤,滤饼用50%甲醇重结晶;将其加入水中,用氨水调至pH 10,用甲基叔丁基醚萃取,萃取液减压脱溶后加入异丙醇30 mL,搅拌下滴加85%H3PO4,过滤,滤饼干燥得白色固体80.2 g,收率31.1%,纯度99.5%,ee>93%, m.p.209.2 ℃;1H NMRδ: 7.06(m, 1H), 6.92(m, 1 H), 4.76(s, 2H), 4.75(d,J=17.6 Hz, 1H), 4.70(d,J=17.6 Hz, 1H), 4.11(m, 2H), 4.08(m, 1H), 4.03(m, 1H), 3.89~3.78(m, 2H), 3.79(m, 2H), 2.92(m, 2H), 2.86~2.79(m, 1H), 2.79(dd,J=17.1 Hz, 1H), 2.68(m, 1H); IRν: 3 196, 3 027, 2 926, 2 861, 1 649, 1 521, 1 453, 1 425, 1 339, 1 278, 1 230, 1 167, 1 093, 1 021, 960, 850, 552 cm-1; ESI-MSm/z: 408(M++H)。
2 结果与讨论
2.1 合成
在1的合成过程中,采用冷却、过滤的方法,简化了操作步骤,收率从文献的81.0%[7]提高到95.0%。
合成4时,对比了N,N-羰基二咪唑与特戊酰氯两种助剂对2,4,5-三氟苯乙酸的活化性能。结果发现,在不加催化剂二甲氨基吡啶(DMAP)的情况下,特戊酰氯对2,4,5-三氟苯乙酸没有活化作用,而N,N-羰基二咪唑的活化作用明显。

表 1 添加剂对6转化率的影响*Table 1 Effect of additives on conversion of 6
*反应条件同1.2(7)
合成7时,其它条件同1.2(7),尝试了不同添加剂对6转化率的影响,结果见表1。从表1可以看出,不加添加剂时,反应无法进行,这说明添加剂对反应起到了催化作用。三氟化硼乙醚络合物与甲基磺酸对该反应的活化能力最强,考虑到三氟化硼的剧毒性,因此甲基磺酸是最合适的添加剂。
2.2 拆分
拆分剂尝试了(-)-L-酒石酸与(-)-二对甲苯酰-L-酒石酸,结果发现,用(-)-L-酒石酸拆分,8的ee值只有4%左右;用(-)-二对甲苯酰-L-酒石酸拆分,8的ee值在93%以上。
[1] Herman G A, Bergman A, Stevens C,etal. Effect of single oral doses of sitagliptin,a dipeptidyl peptidase-4 inhibitor,on incretin and plasma glucose levels after an oral glucose tolerance test in patients with type 2 diabetes[J].J Clin Endocrinol metab,2006,91(11):4612-4619.
[2] Cottr, Wu M, Scanchezm. Efficacy and tolerability of the dipeptidyl-4 inhibitor sitagliptin as monotherapy over 12 weeks in patients with type 2 diabetes[J].Int J Clin Pract,2007,61(1):171-180.
[3] Hasegawa P A. Combination of a dipeptidyl peptidase-4 inhibitor and antihypertensive agent for the treatment of diabetes and hypertension[P].WO 2 007 050 485,2007.
[4] Xiao Y, Armstrong J D, Krska S W,etal. Process for the preparation of chiraoβ-amino acid derivatives by asymmetric hydrogenation[P].WO 2 004 085 378,2004.
[5] Hsiao Y, Rivera N R, Rosner T,etal. Higly efficient synthesis ofβ-amino acid derivatives via asymmetric hydrogenation of unprotected enamines[J].J Am Chem Soc,2004,126(32): 9918-9919.
[6] Karl B Hansen, Yi Hsiao, Feng Xu,etal. Highly efficient asymmetric synthesis of sitagliptin[J].J Am Chem Soc,2009,131(25):8798-8804.
[7] Hansen K B, Balsells J, Dreher S,etal. First generation process for the preparation of the DPP-Ⅳ inhibitor sitagliptin[J].Org Process Res Dev,2005,9(5):634-639.
[8] Edmondson S D, Fisher M H, Kim D. Beta-amino heterocyclic dipeptidyl peptidase inhibitors for the treatment or prevention of diabetes[P].US 6 699 871,2004.
[9] Kim D, Wang L P, Beconi M. (2R)-4-oxo-4-{3[(trifluoromethyl)-5,6-dihydro[1,2,4]triazolo[4,3-a]pyrazin-7(8H)-yl}-1-(2,4,5-trifluorophenyl)butan-2-amine:A potent,orally active dipeptidyl peptidase Ⅳ inhibitor for treatment of typi 2 diabetes[J].J Med Chem,2005,48(11):141-151.
