对羟基苯甲醛的异戊烯烷基化反应*
2010-11-26赵艳敏杨金会
赵艳敏, 杨金会
(1. 宁夏大学 能源化工重点实验室,宁夏 银川 750021; 2. 银川大学 石油化工学院,宁夏 银川 750105)
异戊烯基结构单元在天然产物中普遍存在,尤其在天然黄酮类和香豆素类化合物中最为普遍,异戊烯基侧链的存在大大加强了这类天然产物的生理及药理活性[1~4]。研究在芳环上引入异戊烯基的方法,对合成这类化合物具有重要的应用和学术价值。
本文在KOH/H2O[5], K2CO3/丙酮[6], NaH/甲苯[7]和n-BuLi/THF[8]碱性条件下,研究了对羟基苯甲醛(1)与4-溴异戊烯(2)的烷基化反应(Scheme 1)。由Scheme 1可见,反应的主要产物为C-烷基化产物——m-异戊烯基对羟基苯甲醛(3)和p-异戊烯基苯酚(4);O-烷基化产物——p-异戊烯氧基苯甲醛(5)以及C-烷基化-O-烷基化产物——m-异戊烯基-p-异戊烯氧基苯甲醛(6)。3~6的结构经1H NMR, IR和MS表征。
1 实验部分
1.1 仪器与试剂
AM-400型核磁共振仪(CDCl3为溶剂,TMS为内标);FT-IR-8430S型红外光谱仪(KBr压片);HP-5988型质谱仪(El源,70 eV)。
200目~300目及GF254硅胶,青岛海洋化工厂;所用溶剂作常规无水处理。


Scheme1
1.2 不同碱性条件下1的异戊烯烷基化反应
(1) KOH/H2O
在圆底烧瓶中加入KOH 480 mg(10 mmol)的水(10 mL)溶液,搅拌下于0 ℃加入1 610 mg(5 mmol),待其完全溶解后缓慢滴加21.2 mL(10 mmol),滴毕,反应1 h;于室温避光反应8 h(TLC跟踪,下同)。用3 mol·L-1盐酸调至pH<3,乙酸乙酯 (3×30 mL) 萃取。合并有机相,依次用蒸馏水、饱和食盐水洗涤,无水硫酸镁干燥,减压蒸去溶剂,残余物经硅胶柱层析[洗脱剂:A=V(石油醚) ∶V(乙酸乙酯)=8 ∶1]分离得无色油状液体3和5 。
(2) K2CO3/丙酮
在圆底烧瓶中加入1 1.22 g(10 mmol),丙酮30 mL和少量n-Bu4NBr(相转移催化剂),剧烈搅拌下加入K2CO31.83 g(15 mmol),回流反应15 min;缓慢滴加22.35 mL(20 mmol),滴毕,回流反应45 min。减压蒸出溶剂,残余物用水溶解,乙酸乙酯(3×20 mL)萃取。其余后处理方式同1.2(1),制得无色油状液体5(洗脱剂:A=10 ∶1)。
(3) NaH/甲苯
在圆底烧瓶中加入1 1.22 g(10 mmol)的甲苯(35mL)溶液,剧烈搅拌下加入60%NaH 400 mg(10 mmol),回流反应1 h;自然冷却至室温,用注射器逐滴加入22.35 mL(20mmol),于室温反应30 min;回流反应3 h。冷却至室温,加水5 mL,用乙酸乙酯(3×20 mL)萃取。其余后处理方式同1.2(2),制得无色油状液体5和6。
(4)n-BuLi/THF
在圆底烧瓶中加入1 1.22 g(10 mmol),氮气保护下加入THF 25 mL,搅拌下于-78 ℃(丙酮-液氮)逐滴加入22.35 mL(20 mmol),反应10 min;缓慢滴加1.6 mol·L-1n-BuLi的THF溶液2.1 mL(3.34 mmol),自然恢复到室温,反应7 h。逐滴缓慢加入1 mol·L-1盐酸4.7 mL(pH 7~8),用乙酸乙酯(3×20 mL)萃取。其余后处理方式同1.2(2),制得无色油状液体4和6。
3:1H NMRδ: 9.84(s, 1H, CHO), 8.32(br s, 1H, OH), 7.67(d,J=7.6 Hz, 1H, ArH), 6.94(d,J=7.6 Hz, 1H, ArH), 6.56(s, 1H, ArH), 5.33(t,J=7.2 Hz, 1H, =CH), 3.42(d,J=7.2 Hz, 2H, CH2), 1.78, 1.79(s, 6H, CH3); IRν: 3 340, 2 924, 1 375, 1 363 cm-1; MSm/z(%): 190(M+, 2), 147(100), 135(32), 107(42), 91(64), 43(66)。
4:1H NMRδ: 8.36(br s, 1H, OH),7.64(d,J=7.6 Hz, 1H, ArH), 6.90(d, 1H,J=7.6 Hz, ArH), 6.87(d,J=8.4 Hz, 1H, ArH), 6.52(s, 1H, ArH), 5.25(t,J=7.2 Hz, 1H, =CH), 3.32(d,J=7.2 Hz, 2H, CH2), 1.74, 1.76(s, 6H, CH3); IRν: 3 545, 2 954, 1 175, 1 063 cm-1; MSm/z(%): 162(M+, 12), 145(100), 79(54)。
5:1H NMRδ: 9.89(s, 1H, CHO), 7.61(d,J=1.6 Hz, 1H, ArH), 6.88(d,J=6.4 Hz, 1H, ArH), 6.50(s, 1H, ArH), 6.44(d,J=1.6 Hz, 1H, ArH), 5.33(t,J=7.2 Hz, 1H, =CH), 4.49(d,J=5.6 Hz, 2H, OCH2), 1.71, 1.76(s, 6H, CH3); IRν: 3 289, 2 450, 1 230, 1 233 cm-1; MSm/z(%): 190(M+, 3), 161(100), 144(62), 75(42), 59(76)。
6:1H NMRδ: 9.90(s, 1H, CHO), 7.64(d,J=2.4 Hz, 1H, ArH), 6.84(d,J=2.4 Hz, 1H, ArH), 6.51(s, 1H, ArH), 5.33(t,J=7.2 Hz, 1H, =CH), 5.28(t,J=7.2 Hz, 1H, =CH), 5.20(t,J=7.2 Hz, 1H, =CH) 4.52(d,J=5.6 Hz, 2H, OCH2), 3.42(d,J=7.2 Hz, 2H, CH2), 1.78, 1.79(s, 6H, CH3), 1.71, 1.74(s, 6H, CH3); IRν: 3 562, 3 212, 1 674, 1 395, 1 364 cm-1; MSm/z(%): 258(M+, 4), 189(100), 120(22), 104(42), 78(66)。
2 结果与讨论
在不同碱性条件下1的异戊烯烷基化反应结果见表1。由表1可见,在弱酸K2CO3催化下加入相转移催化剂n-Bu4NBr主要得到O-烷基化产物5;在n-BuLi催化下,可以在对羟基苯甲醛上引入两个异戊烯基,即得到C-烷基化-O-烷基化产物6;在KOH催化下可以同时得到C-烷基化产物3和O-烷基化产物5。另外我们还试图用Ag2O作催化剂,还尝试了用K2CO3作催化剂不加相转移催化剂以及用KOH作催化剂在CH3OH溶液中反应,TLC跟踪发现生成物较多,极性相近,产率较低,不易分离。
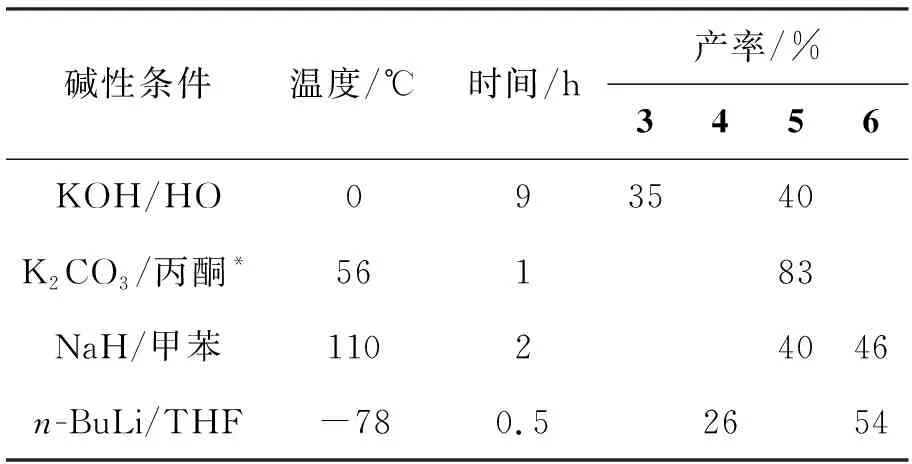
表 1 1的异戊烯基化反应结果Table 1 Resluts of isopentene alkylation of 1
*少量n-Bu4NBr
[1] J B Daskiewicz, F Depeint, L Viornery,etal. Effects of flavonoids on cell proliferation and caspase activation in a human colonic cell Line HT29:An SAR study[J].J Medicine Chemical,2005,48(8):2790-2804.
[2] G Comte, J B Daskiewicz, C Bayet,etal. Rearrangement of 5-O-prenyl flavones:A regioselective access to 6-C-(1,1-dimethylallyl)- and 8-C-(3,3-dimethylallyl)-flavones[J].J Medicine Chemical,2001,44:763-768.
[3] M Na, J Jang, D Njamen,etal. Prenylated flavonoids with PTP1B inhibitory activity from the root bark of erythrina mildbraedii[J].J Nature Product,2006,69:1572-1576.
[4] J B Harborne, C A Williams. Anthocyanins and other flavonoids[J].Nature Product Report,2001,18:310-333.
[5] 谭问飞. 几种天然吡喃型黄酮类化合物的全合成[D].兰州:兰州大学,1998.
[6] 赵艳敏,杨金会,肖冬彩,等. (±)-Abyssinone I 的全合成[J].合成化学,2010,18(1):10-12.
[7] XIE Z X, HU Y, LI Y. First asymmetric synthesis of methyl 2,2-dimethyl-3-hydroxychromanyl-6-formate[J].Chinese Pharmaceutical Science,2004,13:115-118.
[8] T L Shih, M J Wyvartatt. Total synthesis of (&)-5-O-methyllicoricidin[J].J Org Chem,1987,52:2029-2033.
