FePO4包覆尖晶石Li1.1Mn1.9O4的高温循环性能
2010-07-05程海山曾照强
程海山,曾照强
(清华大学材料科学与工程系,新型陶瓷与精细工艺国家重点实验室,北京 100084)
尖晶石LiMn2O4在高温下的循环性能较差,限制了它的进一步应用和发展[1]。尖晶石LiM n2O4在循环过程中容量损失的主要原因是:①Jahn-Teller效应[2];②电解液的分解[3];③正极材料的溶解[4]。人们主要采用掺杂[5]、包覆[6]及合成富锂型化合物Li1+xMn2-xO4[7]等方法,来解决尖晶石LiMn2O4高温循环性能的问题。
合成富锂型化合物通过提高Mn4+的含量,进而抑制Jahn-Teller效应,但效果不太理想;而包覆能防止电解液和正极材料接触造成的Mn溶解,进而抑制Jahn-Teller效应,对改善高温循环性能的作用较为明显,但会降低正极材料的比容量。结合上述两种方法来对LiMn2O4改性的报道较少。
FePO4在电解液中的稳定性良好,有一定的离子和电子电导率,用于包覆改性其他正极材料,效果较好[8]。本文作者用化学沉积法,在尖晶石Li1.1Mn1.9O4表面包覆FePO4,分析了包覆量对产物高温循环性能的影响。
1 实验
1.1 样品的制备
将MnO2(北京产,AR)和Li2CO3(福州产,AR)以物质的量比 1.90∶0.55混合,在800℃下烧结两次,分别保温20 h,制得 Li1.1Mn1.9O4。
分别配制 0.08 mol/L Fe(NO3)3(北京产,≥98.5%)和0.07 mol/L(NH4)2HPO4(北京产,≥99.0%)溶液。根据包覆量的不同,依次取两种溶液各40 ml(包覆量为1%)、120 ml(包覆量为 3%)和 200 ml(包覆量为 5%),在 KQ-250DE型数控超声波容器清洗器(昆山产)中,将(NH4)2HPO4溶液缓慢滴入不断搅拌的Fe(NO3)3溶液中,生成FePO4纳米颗粒,再加入去离子水,使混合液的体积达到500 ml。反应完毕后,将制得的Li1.1Mn1.9O4缓慢加到所得混合液中,加入的 Li1.1Mn1.9O4的质量分别为49.5 g(包覆量为1%)、48.5 g(包覆量为 3%)和47.5 g(包覆量为5%),边搅拌边加热(70℃)。待混合液中的水分完全蒸发后,将得到的固体置于烘箱中,在90℃下保温10 h,研磨、过200目筛后,再置于马弗炉中,在500℃下保温10 h,得到FePO4包覆尖晶石Li1.1M n1.9O4的样品。
1.2 实验电池的组装
将正极活性物质、乙炔黑(北京产,电池级)和聚偏氟乙烯(北京产,电池级)按质量比20∶1∶1在N-甲基吡咯烷酮(天津产,AR)中混合,搅拌均匀后,以120 r/min的转速球磨(球料比 1∶1)1 h。将球磨后的浆料涂覆在 20 μ m厚的铝箔(河南产,≥99.9%)上,在120℃下烘干2 h后,剪切成1 cm×1 cm的极片,刮角后,以20 MPa的压力压制10 s。每片极片含有17.5~21.5 mg活性物质。
把极片点焊在电池壳(广东产)内,以金属锂片(北京产,电池级)为对电极,1 mol/L LiPF6/EC+DMC(体积比1∶1,北京产,电池级)为电解液,Celgard 2340膜(美国产)为隔膜,在充满氮气的手套箱中组装2032型扣式实验电池。
1.3 性能测试与分析
在D/Max-2500型X射线粉末衍射仪(日本产)上进行XRD分析,Cu靶,λ=0.154 178 nm。
在配有电子能谱仪的SSX-550扫描电子显微镜(日本产)上观察粉末的颗粒形貌和元素面分布。
在电池测试系统(深圳产)上进行充放电实验,电压为3.0~4.3 V,电流为1 mA。
2 结果与讨论
2.1 结构与形貌分析
图1为未包覆和FePO4包覆的 Li1.1Mn1.9O4的XRD图。
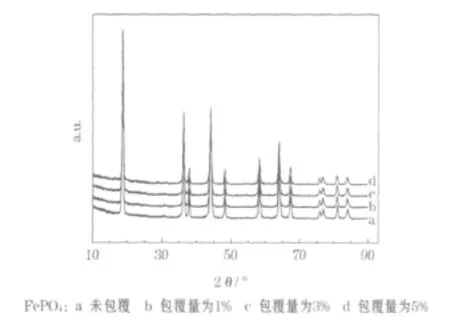
图1 未包覆和FePO4包覆的Li1.1Mn1.9O4的XRD图Fig.1 XRD patterns of Li1.1Mn1.9O4uncoated and coated with FePO4
从图1可知,FePO4包覆的Li1.1Mn1.9O4保持着完好的尖晶石结构,未发现其他衍射峰;包覆前后的 Li1.1Mn1.9O4衍射峰的2θ值没有明显的变化。
计算发现,包覆前后Li1.1Mn1.9O4的晶胞参数发生了规律性变化,结果见表1。
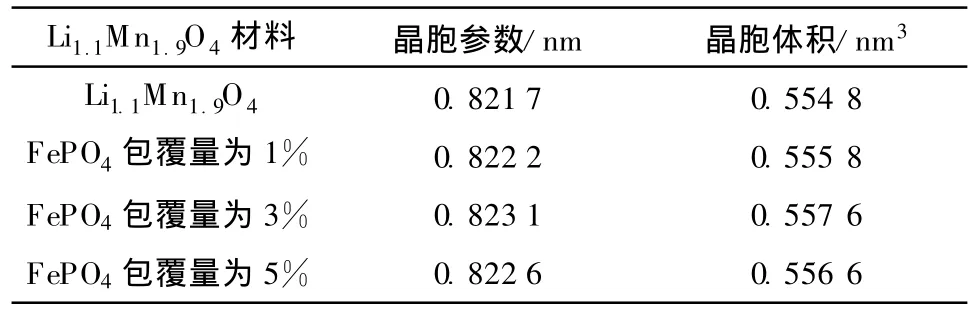
表1 FePO4包覆前后Li1.1Mn1.9O4的晶胞参数和晶胞体积Table 1 Lattice parameters and cell volumes of Li1.1Mn1.9O4 before and after coating with FePO4
从表1可知,晶胞参数随着包覆量的增加先增加,后减小。这可能是因为 Fe3+取代了Mn3+位置上的 Li+,使晶胞参数变大;当包覆量为5%时,随着反应的进行,Mn3+的空位趋向饱和,晶胞参数变小。由于Fe3+的半径(0.64 nm)与Mn3+的半径(0.66 nm)接近,Fe3+取代了晶格中Mn3+的位置,导致空位变小,生成了Li1.1FeyMn1.9-yO4化合物。这与W.Cho等[9]研究的结果类似。
图2为未包覆和FePO4包覆的Li1.1Mn1.9O4(包覆量为5%)的SEM图。

图2 未包覆和FePO4包覆的 Li1.1Mn1.9O4的SEM图Fig.2 SEM photographs of Li1.1Mn1.9O4uncoated and coated with FePO4
从图2可知,包覆前后Li1.1Mn1.9O4的形貌没有明显的变化,但包覆后的 Li1.1Mn1.9O4表面有一层包覆物。
FePO4包覆的Li1.1Mn1.9O4(包覆量为5%)中Fe、P的面分布图见图3。

图3 FePO4包覆 Li1.1Mn1.9O4的能量分散谱(EDS)Fig.3 Energy dispersive spectrometer(EDS)photographs of Li1.1Mn1.9O4coated with FePO4
从图3可知,Li1.1Mn1.9O4的表面均匀地覆盖了一层Fe-PO4。能量分散谱(EDS)对重元素敏感,因此Fe在图中显得分布较多。
2.2 电化学性能测试
未包覆和FePO4包覆的Li1.1Mn1.9O4在室温下的循环性能见图4。
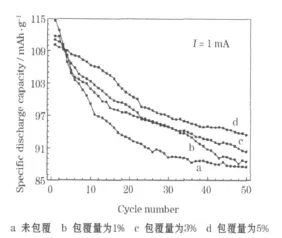
图4 未包覆和FePO4包覆的Li1.1Mn1.9O4在室温下的循环性能Fig.4 Cycle performance of Li1.1Mn1.9O4uncoated and coated with FePO4under room temperature
从图4可知,在1 mA的电流下,Li1.1Mn1.9O4的首次放电比容量为114.7 mAh/g,FePO4包覆量为1%、3%和5%的Li1.1Mn1.9O4分别为 111.1 mAh/g、111.7 mAh/g和 110.1 mAh/g,未包覆的Li1.1Mn1.9O4首次放电比容量更高。第50次循环时,未包覆的Li1.1Mn1.9O4的容量保持率为76.93%,FePO4包覆量为 1%、3%和5%的 Li1.1Mn1.9O4分别为79.65%、80.81%和84.80%。
未包覆和FePO4包覆的Li1.1Mn1.9O4在高温(55℃)下30次循环的循环性能见图5。
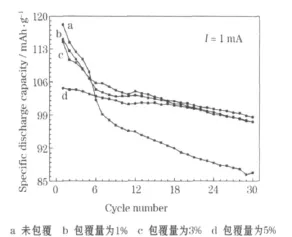
图5 未包覆和FePO4包覆的Li1.1Mn1.9O4在高温(55℃)下的循环性能Fig.5 Cycle performance of Li1.1Mn1.9O4uncoated and coated with FePO4under high temperature(55℃)
从图5可知,在1 mA的电流下,Li1.1Mn1.9O4在55℃下的首次放电比容量为118.16 mAh/g,FePO4包覆量为1%、3%和 5%的Li1.1Mn1.9O4分别为 115.08 mAh/g、114.53 mAh/g和104.69 mAh/g。在55℃下的首次放电比容量总体上高于室温下的首次放电比容量,可能是因为高温下电池的内阻变小,Li+的迁移速率增大。未包覆的 Li1.1Mn1.9O4的首次放电比容量略高于FePO4包覆量为1%和3%时,比FePO4包覆量为5%时高出较多,有一个原因是FePO4不参与充放电。第30次循环时,未包覆的Li1.1Mn1.9O4的容量保持率为73.48%,FePO4包覆量为1%、3%和5%的Li1.1Mn1.9O4分别为84.88%、86.08%和93.25%。Li1.1Mn1.9O4的容量保持率随着包覆量的增加而提高,说明包覆量为1%和3%时,包覆不完整或包覆层太薄,不能完全有效地隔离电解液和正极材料。
实验结果说明:在Li1.1Mn1.9O4表面包覆一层FePO4,可抑制Li1.1Mn1.9O4与电解液的直接接触,从而抑制Mn3+的溶解和电解液的分解,保证Li1.1Mn1.9O4的尖晶石结构在高温下的稳定。
3 结论
用化学沉积的方法,在尖晶石Li1.1Mn1.9O4的表面包覆了FePO4。
XRD和SEM分析表明:Li1.1Mn1.9O4的结构和形貌没有变化,且没有引入杂质。
在室温和高温(55℃)下的循环性能测试结果表明:FePO4包覆层能在55℃下隔离电解液和正极材料,因此提高了Li1.1Mn1.9O4的高温循环性能。
[1]T hackeray M M,Johnson P J,Picciotto D,et al.Electrochemical extraction of lithium from LiM n2O4[J].Mater Res Bull,1984,19(2):179-187.
[2]Aurbach D.Review of selected electrode-solution interactions which determine the performance of Li and Li ion batteries[J].J Power Sources,2000,89(2):206-218.
[3]Arora P,White R E,Doyle M.Capacity fade mechanisms and side reactions in lithium-ion batteries[J].J Electrochem Soc,1998,145(10):3 647-3 667.
[4]Xia Y Y,Zhou Y H,Yoshio M.Capacity fading on cycling of 4 V Li/LiMn2O4cells[J].J Electrochem Soc,1997,144(8):2 593-2 600.
[5]Thackeray M M.Manganese oxides for lithium batteries[J].Prog Solid State Chem,1997,25(1-2):1-71.
[6]FENG Chuan-qi(冯传启),LI Hua(李华),WANG Shi-yin(王世银),et al.TiO2包覆的尖晶石LiMn2O4的电化学性能[J].Battery Bimonthly(电池),2009,39(5):257-259.
[7]Lu W,Belharouak I,Park S H,et al.Isothermal calorimetry investigation of Li1+xMn2-yAlzO4spinel[J].Electrochim Acta,2007,52(19):5 837-5 842.
[8]CHEN Meng(陈猛),PI Qing-li(皮庆立),WANG Wen-gang(王文刚),et al.FePO4包覆LiNi0.3Co0.7O2正极材料的改性研究[J].Dianchi Gongye(电池工业),2009,14(3):161-165.
[9]Cho W,Ra W,Shirakawa J,et al.Synthesis and electrochemical properties of nonstoichiometric LiAlxMn2-xO4-delta as cathode materials for rechargeable lithium ion battery[J].J Solid State Chem,2006,197(11):3 534-3 540.
