SFP-AQ法预处理麦秸秆酶解五碳糖得率的变化规律
2010-02-23王艳丽曹云峰
王艳丽, 曹云峰, 杨 洋
(南京林业大学江苏省制浆造纸重点实验室, 江苏 南京 210037)
0 前言
当前经济过分依赖于石油、煤炭等化石燃料,其不可再生性正导致资源逐渐枯竭,同时燃烧产生的二氧化碳已造成气候环境日益恶化,寻找可再生的清洁能源成为各国科研人员关注的焦点[1,2].在众多可替代的生物能源中,燃料乙醇是源于可再生生物质的重要能源之一.可再生的木质纤维作为农林废弃物低成本原料[3],因其潜在的生物燃料和附加值产品功能,已经被公认为首选的生物能资源之一[4].我国是农业大国,年农作物秸秆约7亿吨,其中玉米秸秆占35%,小麦秸秆占21%,稻草占19%[5],麦秸秆是最充裕的农作物废弃物之一[6].木质纤维素炼制燃料乙醇过程通常包括预处理、水解、发酵、蒸馏等单元操作,其中纤维素水解为可发酵糖是纤维素乙醇炼制过程中至关重要的环节.如能研究利用农作物秸秆作为廉价的糖源,实现其有效的转化燃料酒精[7],则对于保护森林资源、提高农作物秸秆的利用价值、防止环境污染等具有重要的现实意义[8].本文以麦秸秆为原料,经SFP-AQ法预处理后再进行酶解,对酶解五碳糖得率分析比较,从中找出了较适宜的预处理和酶解条件.
1 材料与方法
1.1 实验原料和试剂
原料:小麦秸秆,取自南京市郊,为了原料的均匀性,将麦秸秆去根去穗去叶,剪成3~5 cm的小段,平衡水分备用.
蒸煮试剂:Na2SO3、甲醛溶液和蒽醌,均为分析纯.
酶解液:纤维素酶(CCN03110,酶活118 IU/mL)、木聚糖酶(CFN00244,酶活1 196 IU/mL)、β-纤维二糖酶(DCN00207,酶活480 IU/mL),由Novozymes(中国)投资有限公司提供,酶活按照文献[9]提供的方法测定.将此3种酶按上述顺序以酶活比为1 FPU∶1.2 FXU∶1 CBU混合,混合酶液的酶活以纤维素酶滤纸酶活计为20 FPU/mL,加入过量的β-纤维二糖酶以防止酶解过程中纤维二糖的积累[10].3 g/L叠氮钠防腐的醋酸-醋酸钠缓冲液(pH值为4.8),冷藏备用.
1.2 实验仪器
10×1 L油浴锅、粉碎机、烘箱、马弗炉、灭菌锅、紫外光栅分光光度计、恒温振荡器(SHA-C)、Dionex ICS-3000离子色谱仪、真空干燥器.
1.3 实验方法
1.3.1 原料预处理
每罐各取绝干草片80 g,固液比为1∶6,在10×1 L油浴锅中于150 ℃、160 ℃下分别蒸煮1 h、2 h, Na2SO3用量分别为0、4%、8%、12%、16%,Na2SO3与甲醛摩尔比为1∶1,蒽醌用量为0.1%.蒸煮后将浆料洗净、风干、粉碎,备用.
注:为表述方便,将蒸煮温度150 ℃,保温时间1 h、2 h和蒸煮温度160 ℃,保温时间1 h、2 h分别记为150-1、150-2、160-1和160-2.
1.3.2 酶解
各称取1 g(精确到0.000 1 g)预处理后的绝干浆料,转移到50 mL离心管中进行酶解处理,酶用量分别取5 FPU/g、10 FPU/g、20 FPU/g、40 FPU/g,浆浓为5%,加3 g/L叠氮钠防腐的醋酸-醋酸钠缓冲液.先加一定量的醋酸-醋酸钠缓冲液于25℃环境下润胀麦草粉6 h,再加入复合酶置于恒温振荡器上50℃反应48 h,酶解结束后在5 000 r/min下离心15 min,分离酶解液,然后于Dionex ICS-3000离子色谱仪上进行还原糖的测定.
1.3.3 原料中五碳糖含量的测定
称取0.333 3 g绝干原料加入具塞锥形瓶中,加入5 mL冷却至12~15 ℃的(72±0.1)%硫酸,将其置于18~20℃水浴中2.5 h,并不时摇荡锥形瓶.达到上述时间后将锥形瓶内容物在蒸馏水的漂洗下全部转移到耐高温玻璃瓶中,加蒸馏水稀释至总体积为196 mL.将耐高温玻璃瓶置于高温灭菌锅中煮沸1.5 h,冷却后用G2砂芯漏斗过滤,取上层清液在离子色谱中测定五碳糖的含量.
1.3.4 五碳糖含量的测定
将酶解液置于沸水浴中5 min使酶蛋白沉淀,离心后分离清液,加入L-岩藻糖作为内标,稀释1 000倍后用Dionex ICS-3000离子色谱仪分析单糖含量,检测器为HPAEC-PAD脉冲安培检测器.样品经孔径为0.22 μm的尼龙滤器过滤,进样量为5 μL.以超纯水配置的18 mM NaOH溶液和200 mM NaOH溶液分别作为流动相和洗脱液,在流速为0.25 mL/min下分析阿拉伯糖和木糖的含量,两种糖含量之和即为五碳糖的含量.

图1 蒸煮浆得率与Na2SO3用量的关系
2 实验结果与讨论
2.1 蒸煮得率分析
SFP-AQ法在不同温度、不同时间蒸煮条件下,蒸煮浆得率和Na2SO3用量之间的关系如图1所示.
由图1可知,随着蒸煮温度的升高、保温时间的延长以及Na2SO3用量的增大,浆的得率逐渐下降.当蒸煮温度从150 ℃升至160 ℃,浆的得率下降3%~8%,并且随着保温时间的延长,浆的得率下降更多:4%~10%;Na2SO3用量从0增大到16%,浆的得率下降20%~25%左右.这是因为温度升高、蒸煮时间延长、Na2SO3用量增大时,碳水化合物降解程度增加,同时使得木素溶出.另外,从浆的得率下降的幅度得知,增加Na2SO3的用量所导致浆的得率下降的幅度,比升高温度和延长保温时间导致浆的得率下降的幅度大得多,因此本次试验中蒸煮浆的得率的决定性因素是Na2SO3的用量.
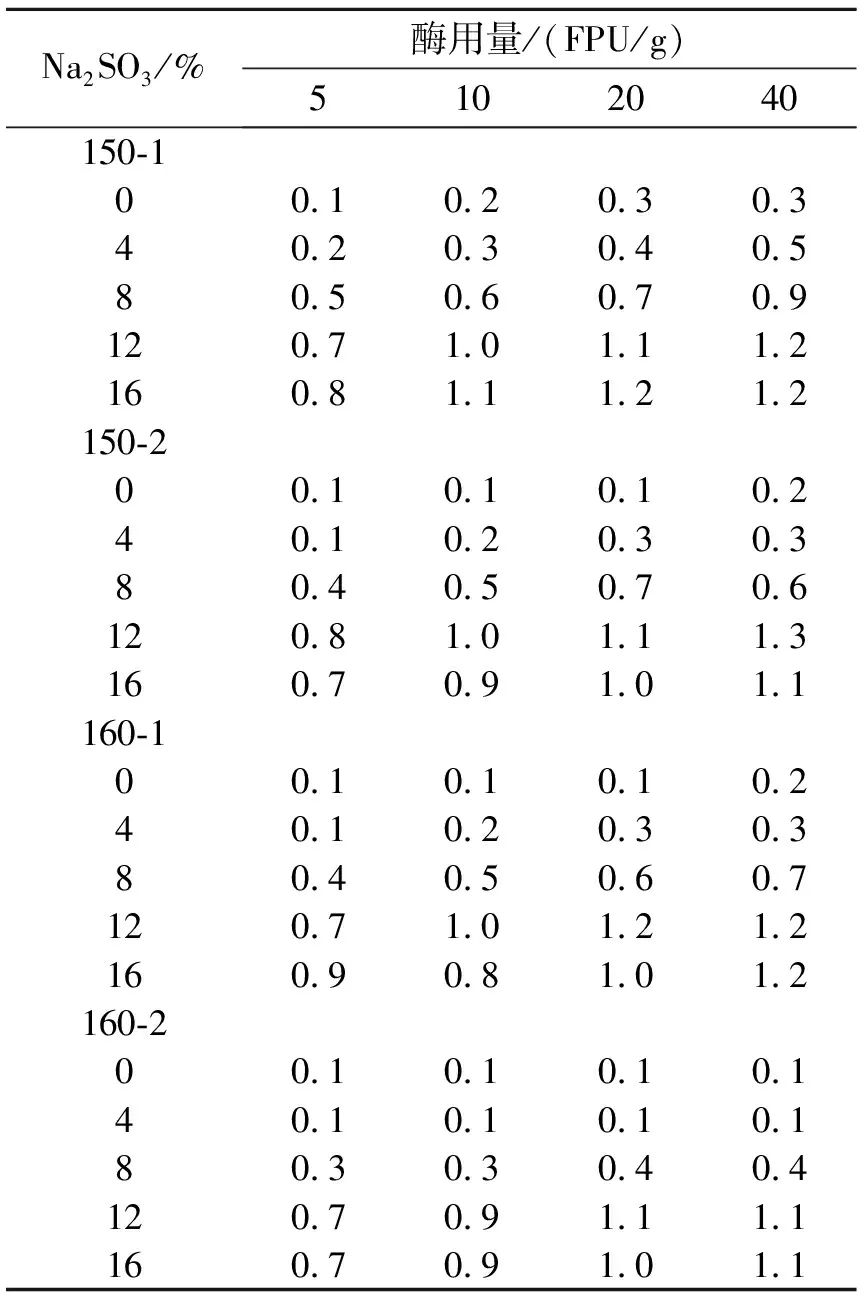
表1 酶解阿拉伯糖得率与Na2SO3用量和酶用量的关系
2.2 五碳糖的酶解
酶解所得的五碳糖来自于秸秆中的半纤维素,半纤维素中五碳糖主要由木糖、少量阿拉伯糖等组成.下面对阿拉伯糖和木糖的酶解得率进行分析.
2.2.1 酶解阿拉伯糖的得率
分别经不同温度和不同保温时间预处理的SFP-AQ法浆料在进行酶解后,酶解液中的阿拉伯糖含量(相对于原料)得率如表1所示.
从表1可以看出,阿拉伯糖的得率比较低,介于0.1%~1.3%之间.由于原料麦秸秆中阿拉伯糖含量为2%,含量较低,数据波动较大不宜进行分析,所以下面着重对木糖酶解得率进行分析.
2.2.2 酶解木糖的得率
分别经不同温度和不同保温时间预处理的SFP-AQ法浆料在进行酶解后,酶解液中的木糖含量(相对于麦秸秆原料)得率如图2~图5所示(图例0.4%、8%、12%、16%表示蒸煮时Na2SO3的用量).
从Na2SO3的用量来看,图2~图5中Na2SO3的用量与酶解木糖得率间的关系为:Y12%>Y16%>Y8%>Y0,Y4%(注:Y表示得率).随着Na2SO3用量的增加,秸秆中的木素被大量脱除,使得半纤维素被较大程度的暴露出来,更易与酶接触从而提高酶解木糖的得率.但是,从图1中可以看出,随着Na2SO3的用量从12%增加到16%,蒸煮浆料的得率急剧降低,原料中半纤维素在预处理过程中被大量降解,由于木糖的得率是相对于原料而言的,这样就出现了Na2SO3用量为12%时的酶解木糖得率反而比16% 时高的情况.在Na2SO3用量为4%和0时,木糖得率都很低,这是因为4%的Na2SO3用量较少,对于木素的脱除效果较差,同时对纤维素和半纤维素仍有一定程度的降解作用,在这一正一反的作用下,其结果与不加Na2SO3的自水解处理浆料的酶解效果相近.综上可得最佳的Na2SO3的用量为12%.

图2 150-1酶解木糖得率与酶用量的关系(对原料)
从酶用量来看,图2~图5中木糖得率随着酶用量的增加而增加,当酶用量从5 FPU/g增加到20 FPU/g时,木糖的得率增加0.1~0.8倍不等,效果较为明显,而当酶用量继续增加时,木糖得率增加缓慢,从0.1~0.3倍不等.这是由于随着酶用量的增加,使得酶解作用增强,反应更加彻底,当酶与浆料已经充分接触后,继续加入过量的酶,对提高酶解木糖的得率没有明显效果,不仅造成了酶液的浪费,而且导致成本增加,由此选定20 FPU/g为最佳酶用量.
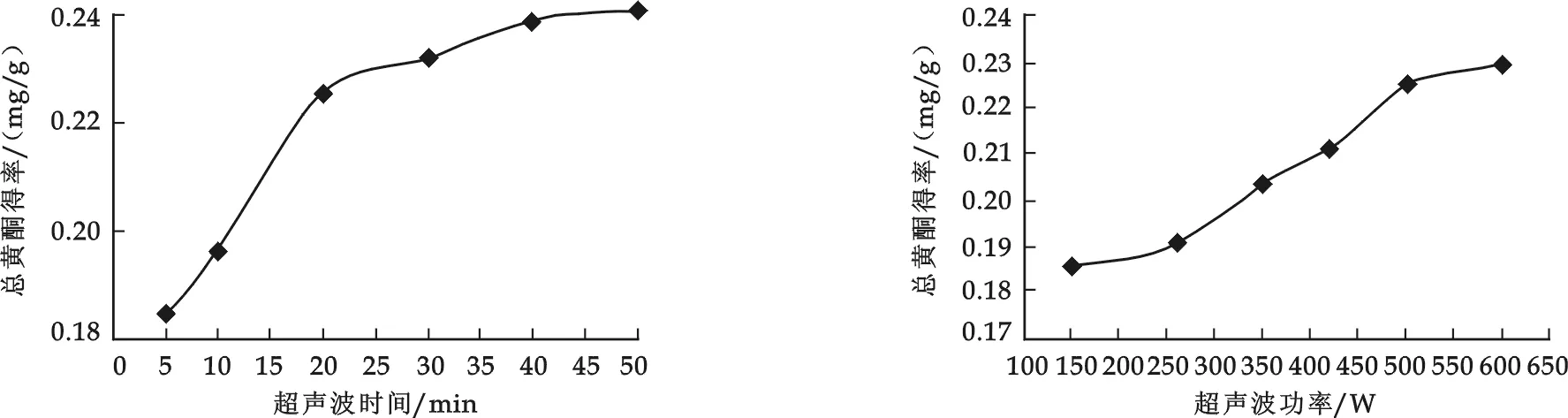
图4 160-1酶解木糖得率与酶用量的关系(对原料)
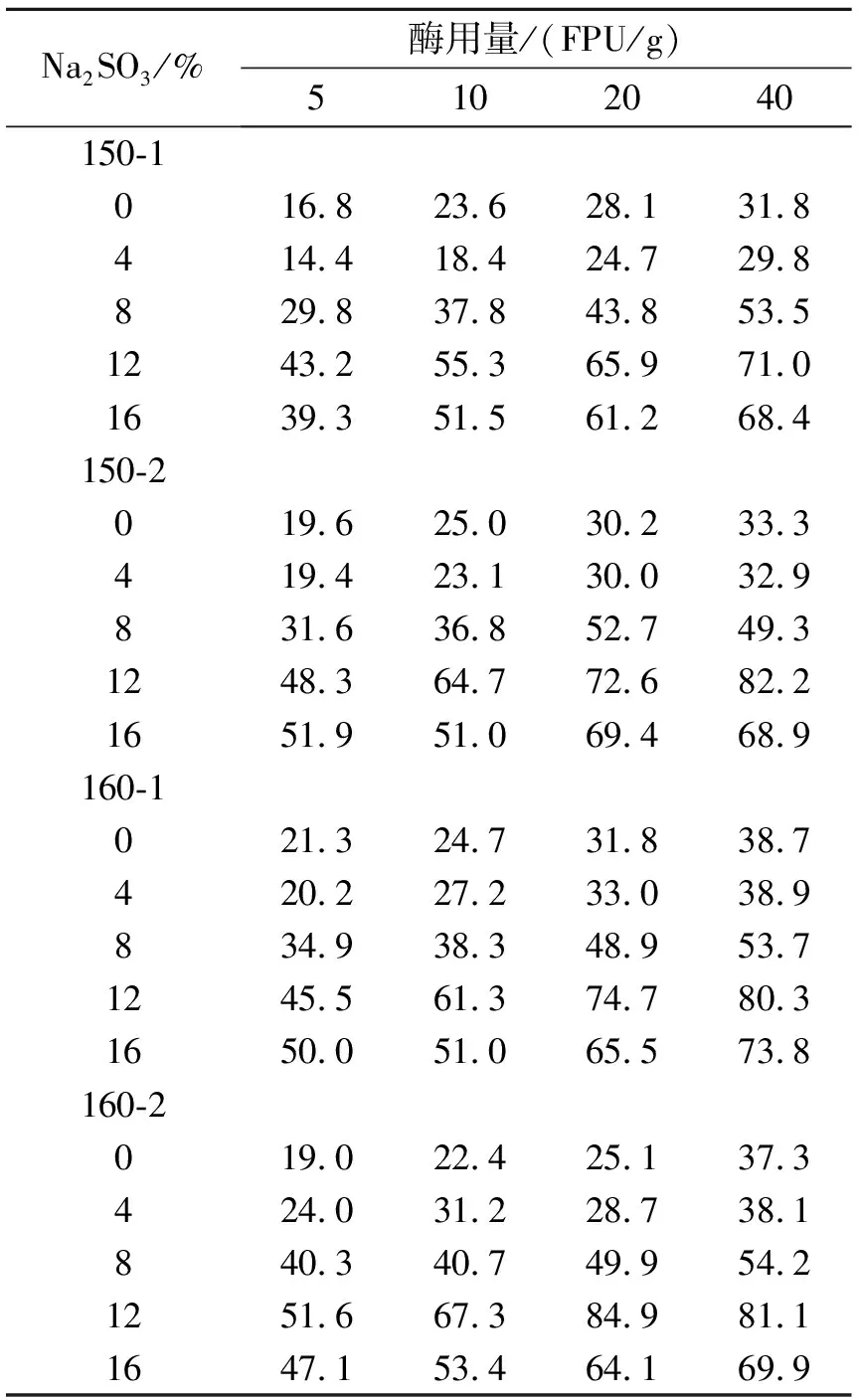
表2 酶解木糖对麦秸秆原料中木糖的转化率
从蒸煮最高温度和保温时间来看,选定酶用量20 FPU/g、Na2SO3用量12%,分别对150-1、150-2、160-1和160-2时的酶解木糖得率进行比较,结果如下:Y160-2(17.5%)>Y160-1(15.4%)>Y150-2(14.3%)>Y150-1(13.6%).可见随着最高蒸煮温度的升高和保温时间的延长,酶解木糖的得率也在随之增加.因为随着蒸煮最高温度的升高和保温时间的延长,预处理浆料中木素被更多的脱除,从而暴露出更多的半纤维素,使其容易与酶接触,反应更加彻底,因此酶解木糖的得率提高.
2.3 酶解液中木糖占原料中木糖的转化率
从表2中容易得到,在Na2SO3用量12%,酶解酶用量分别为20 FPU/g、40 FPU/g的条件下,酶解木糖对原料中木糖的转化率都很高.在160-2,Na2SO3用量12%,酶解酶用量20 FPU/g时,酶解木糖转化率达到最高值84.9%.综合考虑酶价格、产率等因素可以得到:160-2,Na2SO3用量12%,酶用量20 FPU/g为最佳的处理条件.
3 结论
SFP-AQ法预处理麦秸秆酶解木糖得率的变化规律:木糖得率随着预处理中Na2SO3用量的增加先升高后降低,在12%时木糖得率最高;木糖得率随着酶用量的增加而迅速升高,当酶用量超过20 FPU/g时,提高缓慢;木糖得率随蒸煮最高温度的升高和保温时间的延长而增加.较适宜的预处理和酶解条件分别为:蒸煮最高温度160 ℃,保温时间2 h,Na2SO3用量为12%,纤维素酶、木聚糖酶、β-纤维二糖酶3种复合酶用量为20 FPU/g.此时,木糖得率可达到17.5%,酶解木糖对原料中木糖的转化率为84.9%.
[1] Lynd L R, Weimer P J, Van Zyl W H,etal. Microbial cellulose utilization: fundamentals and biotechnology[J]. Microbiology and Molecular Biology Reviews, 2002, 66(3): 506-577.
[2] Herrera S. Bonkers about biofuels [J]. Nature Biotechnology, 2006, 24(7): 755-760.
[3] M.G.Adsul, J.E.Ghule. Enzymatic hydrolysis of delignified bagasse polysaccharides[J]. Carbohydrate Polymers,2005,(62):6-10.
[4] Raj Kumar,Sompal Singh,Om V. Singh. Bioconversion of lignocellulosic biomass: biochemical and molecular perspectives[J]. J Ind Microbiol Biotechnol, 2008,(35): 377-391.
[5] 王乃菊,宋 萍. 农作物秸秆制取燃料酒精的研究[J]. 酿酒,2007, 11(34): 51.
[6] M.G. Tabka, I. Herpo¨el-Gimbert. Enzymatic saccharification of wheat straw for bioethanol production by a combined cellulase xylanase and feruloyl esterase treatment[J]. Enzyme and Microbial Technology,2006,(39):897-902.
[7] 张继泉,郭利美,王瑞明. 玉米秸秆发酵生产燃料酒精工艺探讨[J]. 广州食品工业科技, 2003,(2): 24-25.
[8] 连海兰,周定国,尤纪雪. 麦秸秆成分剖析及其胶合性能的研究[J]. 林产化工与工业, 2005, 3(25): 69-70.
[9] Ghose, T.K. Measurement of cellulase activities[J]. Pure & Appl. Chem., 1987, 59:257-268.
[10] Emmel, A.; Mathias, A.L.; Wypych F.etal. Fractionation of eucalyptus grandis chips by dilute acid-catalysed steam explosion [J]. Bioresour. Technology., 2003, 86 (2), 105-115.
