国内外牛肉中兽药残留限量对比及国内相应检测标准研究进展
2023-07-17刘忠莹王小平朱敏敏谭亚男何叶馨王鑫
刘忠莹 王小平 朱敏敏 谭亚男 何叶馨 王鑫

摘 要:近年来我国牛肉需求量较大,进口牛肉已占据较大的市场份额。作为牛肉消费大国,国内牛肉特别是进口牛肉的质量安全问题受到我国食品安全监管机构和消费者等的广泛关注,兽药残留则是牛肉中重要的质量安全问题之一。建立适宜、全面的牛肉兽药残留限量标准是监控牛肉质量安全的重要举措。本文对我国与主要牛肉进口国、某些发达国家或组织关于牛肉中兽药残留标准进行比较及分析,我国关于牛肉中兽药残留限量标准已较为完善,但部分兽药残留限量与某些发达国家或组织的相关食品安全标准仍存在一定差异,且部分兽药缺乏对应的检测标准。未来我国仍需结合兽药实际使用情况和监测结果进一步完善牛肉中兽药残留限量及检测的相关标准,规范国内牛养殖环节的兽药使用行为,提升进口牛肉的质量安全,保障消费者的食品健康安全。
关键词:兽药残留;牛肉;最大残留限量;对比分析;检测标准
Comparison of Veterinary Drug Residue Limits in Beef in China and Abroad and A Review of Chinese Testing Standards
LIU Zhongying, WANG Xiaoping, ZHU Minmin, TAN Yanan, HE Yexin, WANG Xin*
(Key Laboratory of Baijiu Supervising Technology for State Market Regulation, Sichuan Institute of Food Inspection,
Chengdu 610097, China)
Abstract: In recent years, the demand for beef in China has been relatively high, and imported beef has occupied a large market share. China is a major consumer of beef, and the quality and safety of beef in China, especially imported beef, have received widespread attention from food safety regulatory agencies and consumers in the country. Residues of veterinary drugs in beef are one of the important quality and safety issues. Establishing appropriate and comprehensive standards for veterinary drug residue limits in beef is an important measure for monitoring the quality and safety of beef. This article compares Chinas, major beef exporting countries and some developed countries or organizations standards for veterinary drug residue limits in beef. The results show that Chinas standards for veterinary drug residue limits in beef are relatively perfect. However, the Chinese maximum residue limits for some veterinary drugs are not consistent with the food safety standards of some developed countries or organizations and the country has not set testing standards for some veterinary drugs. In the future, this country still needs to further improve the standards for veterinary drug residue limits in beef and the testing standards by synthesizing the practical use and monitored data of veterinary drugs in order to standardize the use of veterinary drugs on cattle farms, upgrade the quality and safety of imported beef and, more broadly, ensure the safety and health of consumers.
Keywords: veterinary drug residues; beef; maximum residue limit; comparative analysis; testing standard
DOI:10.7506/rlyj1001-8123-20230410-026
中圖分类号:TS207.2 文献标志码:A 文章编号:1001-8123(2023)06-0065-09
引文格式:
刘忠莹, 王小平, 朱敏敏, 等. 国内外牛肉中兽药残留限量对比及国内相应检测标准研究进展[J]. 肉类研究, 2023, 37(6): 65-73. DOI:10.7506/rlyj1001-8123-20230410-026. http://www.rlyj.net.cn
LIU Zhongying, WANG Xiaoping, ZHU Minmin, et al. Comparison of veterinary drug residue limits in beef in China and abroad and a review of Chinese testing standards[J]. Meat Research, 2023, 37(6): 65-73. (in Chinese with English abstract) DOI:10.7506/rlyj1001-8123-20230410-026. http://www.rlyj.net.cn
现阶段,我国农业对外开放面临诸多问题,真正的挑战在于农业竞争力和食物自给率持续下降[1]。其中,近年来我国牛肉产量远远落后于需求量,国内牛肉市场存在严重的供需不足问题。在此情况下,我国开始增加对国外牛肉的进口,来补足牛肉的供需缺口[2-3]。根据国家统计局数据,2022年我国牛肉产量718 万t,环比2021年增加21 万t,增长3.0%[4];根据中国海关总署发布的数据,2022年1—12月,我国总计进口牛肉约269 万t,环比2021年1—12月(233 万t),上涨15.3%;进口额约为1 187 亿人民币,环比2021年1—12月(807 亿人民币),上涨47.1%[5-6]。牛肉进口量一直居高不下,且主要进口国相对集中在巴西、阿根廷、美国、新西兰、澳大利亚等国家,巴西一直居于首位[7-10]。由于发展程度、饮食习惯等不同,各国食品安全监管体系、针对食品的技术法规标准要求存在很大差异。这种标准上的差异往往成为进口食品安全风险[11]。在进口牛肉的同时,也需关注其质量安全。作为重要消费产品,牛肉中的兽药残留问题是影响牛肉质量安全的最重要因素之一,一直备受养殖场、市场监管机构和消费者的关注[12-15]。陈泽宇等[16-17]收集、编译、综述2015年以来部分国内外牛肉相关法规标准修订更新情况,从牛肉产品标准规范、质量等级、限量、检验、标签、进出口六方面出发进行梳理、研究,还对国内外牛肉的农药残留限量标准作了对比研究,但未对牛肉相关兽药残留限量及其检测标准做深入剖析。
卢阳等[18]也将我国与国外牛肉的兽药残留限量标准进行了对比研究,但仅限于和美国、日本、国际食品法典委员会(Codex Alimentarius Commission,CAC)比较。孙彩霞等[19]概述我国与澳大利亚、CAC牛肉的兽药残留、农药残留、重金属限量标准,但年限较为久远,不适用于最新标准对比。刘鑫等[20]仅将我国的新兽药残留标准作了详细解析。此外还有大量国内外兽药残留限量标准的对比研究报道,但集中于除牛肉外的其他品种,如乳及乳制品[21-22]、水产品[23-24]、畜禽产品[15,24-25]等。鉴于我国牛肉主要依赖进口,本文分别比较分析我国与上述主要牛肉进口国(巴西、阿根廷、美国、新西兰、澳大利亚)、以及日本和CAC等组织或国家的牛肉中兽药残留限量标准的差异,保证进口牛肉的质量安全同时也能保证我国牛肉出口时减少遭遇技术性贸易壁垒,减少在进出口贸易中的经济损失,预防牛肉中的兽药残留问题引发世界范围的公共卫生危害,同时为完善我国牛肉相关的兽药残留限量标准和检测标准提供参考。
1 我国牛肉中兽药残留标准的概况
作为国内兽药残留最全标准GB 31650—2019《食品安全国家标准 食品中兽药最大残留限量》[26]于2020年4月1日正式实施,标准中规定的267 种(类)兽药在动物性食品中的2 191 项残留限量,全面采用CAC、欧盟和美国等发达国家或地区的最严标准,实现与国际接轨,基本覆盖了我国常用兽药品种和主要食品动物及组织,标志着我国兽药残留标准体系建设进入新阶段[27]。此外2022年9月,农业农村部、国家卫生健康委员会及国家市场监督管理总局联合发布GB 31650.1—2022《食品安全国家标准 食品中41 种兽药最大残留限量》[28],并于2023年
2月1日起实施。牛肉中兽药残留限量在GB 31650—2019及GB 31650.1—2022中共涉及已批准用于动物性食品中最大残留限量规定的兽药74 种;新批准兽药清单中11 种;允许用于食品动物,但不需要制定残留限量的兽药137 种;允许作治疗用,但不得在动物性食品中检出的兽药7 种;食品动物中禁止使用的药品及其他化合物的名单中21 项。目前,有最大残留限量规定的共有91 种,涉及抗菌药类45 种、抗菌增效剂1 种、解热镇痛抗炎药5 种、抗梨形虫药1 种、抗球虫药6 种、抗吸虫药4 种、抗线虫药11 种、抗锥虫药2 种、驱虫药2 种、杀虫药10 種、抗蠕虫药1 种、糖皮质激素类药4 种。其中抗菌药类最多,接近最大残留限量规定的兽药总数的一半,类别又可细分为11 类,包括:头孢菌素类、多肽类、四环素类、酰胺醇类、林可胺类、大环内酯类、氨基糖苷类、β-内酰胺类、β-内酰胺酶抑制剂、磺胺类、喹诺酮类及其他抗菌药。
2 我国牛肉中兽药残留限量与其他国家或组织对比
2.1 与主要进口国(巴西、阿根廷、美国、新西兰、澳大利亚)对比
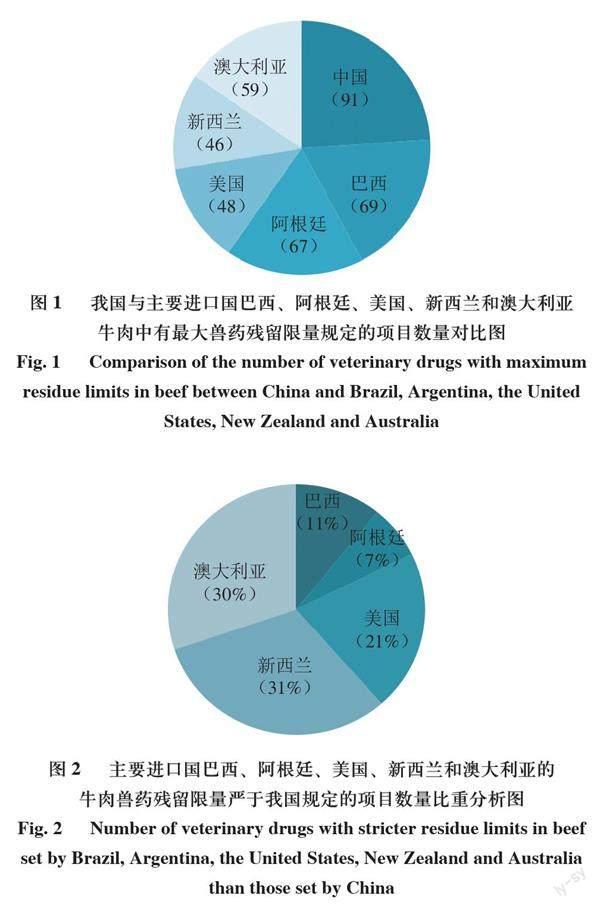
巴西的《动物源食品内兽药最大残留限量规定》[29]由巴西卫生监督局2019年6月24日公布,规定了动物源食品内兽药的最大残留限量。涉及牛肉中有最大残留限量的兽药共计69 项,其中头孢匹林、安普霉素、泰妙菌素、托芬那酸、拉沙洛西、氟雷拉纳、氯舒隆、沙奎那韦、溴氰菊酯9 项严于我国,除溴氰菊酯外其余8 项我国均无限量。
阿根廷国家动物健康服务部2011年8月18日发布559/2011号决议[30],制订了动物源性食品中主要兽药成分的最大残留限量。决议中包含了上百种有机酸、麻醉剂、镇定剂、抗球虫药、抗真菌剂、防腐剂、抗炎药、抗组胺、抗微生物剂、外用和内用抗寄生虫药、激素、矿物质和维生素补充剂、草本和植物萃取物、营养素,以及循环、呼吸、消化和泌尿系统用药物。该决议和我国限值相比,相同的有56 项之多,此外还包括二氟沙星(200 μg/kg,我国400 μg/kg)、溴氰菊酯(10 μg/kg,我国30 μg/kg)、卡洛芬、氯舒隆、甲基泼尼松龙、奈韦拉平6 项严于我国,后4 种我国未见规定。
美国兽药残留限量标准由美国食品药品管理局负责制定,目前最新版本为2019年7月11日实施。兽药限量可在《美国联邦法規汇编》第21篇“食品和药品”第556部分“食品中新型兽药的残留容许量”[31]查询。该法规由A、B两部分组成,A部分为一般条款,B部分为各种兽药的具体残留限量要求。经过查询目前在该法规中牛肉中有最大残留限量的兽药共涉及47 种,包括抗生素类、驱虫类等。将我国与美国的牛肉中兽药残留限量值对比发现,美国严于我国的兽药包括头孢匹林、红霉素等共计15 项,其中属于β-内酰胺类抗生素的阿莫西林、氨苄西林、氯唑西林限量值仅为10 μg/kg,为我国的1/5,而氯唑西林限值10 μg/kg,仅为我国的1/30,海他西林我国还未设定限值。可见美国对β-内酰胺类抗生素的控制更加严格。作为我国最常用的5 类抗生素之一,β-内酰胺类抗生素生产量和销售份额在众多抗生素中名列前茅[32]。可见针对此类抗生素,应考虑更加严格的控制。此外我国严于美国的共计70 项,其中美国有66 项都未设定限值。可见我国除了极个别抗生素和美国有一定差距外,整体情况都优于美国。
《新西兰农用化合物(包括农药和兽药)最大残留限量标准》[33]由新西兰食品安全局根据“食品法”制定。该标准由注意事项、农用化合物最大残留限量表、植物用化合物最大残留限量豁免表、动物用化合物最大残留限量豁免表4 部分组成。需要注意的是,对具体限量标准未涉及的农用化合物残留,新西兰设定了
0.1 mg/kg的默认标准。其最新版本牛肉中的兽药残留有规定限量的项目数量在该法规中共涉及46 种。新西兰牛肉中兽药残留最大限量严于我国的有23 项,有相当部分都是我国未设置最大残留限量的项目,包括头孢匹林、阿维菌素、喷沙西林、托拉菌素、卡洛芬和地克珠利,其中氯唑西林限值(新西兰50 μg/kg)仅为我国的1/6,马拉硫磷(新西兰500 μg/kg)仅为我国的1/8。其他,如吡利霉素、替米考星、链霉素、双氢链霉素、三氯苯达唑、乙酰氨基阿维菌素、非班太尔、芬苯达唑、奥芬达唑、伊维菌素、阿苯达唑、三氟氯氰菊酯等限值低于我国2~3 倍。
澳大利亚农药兽药管理局(Australian Pesticides and Veterinary Medicines Authority,APVMA)负责制定农产品,特别是进入食物链的农产品中的化学农药和兽药最大残留限量标准[34],2022年5月14日为最新修订。澳大利亚的农兽药残留限量标准由2 部分组成,第1部分是其术语解释,第2部分由5 个表格构成,分别为:食品中化学农药、兽药和相关物质的最大残留限量;最大残留限量标准适用的产品部位(取样分析部分);残留定义;动物饲料中农药的最大残留限量;不需要设定最大残留限量的农兽药及相应的使用方法。需要指出的是,根据相关规定,如果某种农兽药或者某种农兽药在某种农产品中的残留未在限量表中列出,澳大利亚一律要求不得检出。在其最新版本,牛肉中的兽药残留有规定限量的项目数量在该法规中共涉及59 种。有21 项严于我国,阿莫西林限量(10 μg/kg)仅为我国1/5,克拉维酸限量(10 μg/kg)仅为我国1/10。有22 项虽然均宽于我国限量,且有部分兽药限值虽然远高于我国,但考虑到其溶解性能是脂溶性的,所以该国特地注明该限量是应用于脂肪中,包括伊维菌素、噻苯达唑、氟佐隆和氟氯苯氰菊酯。
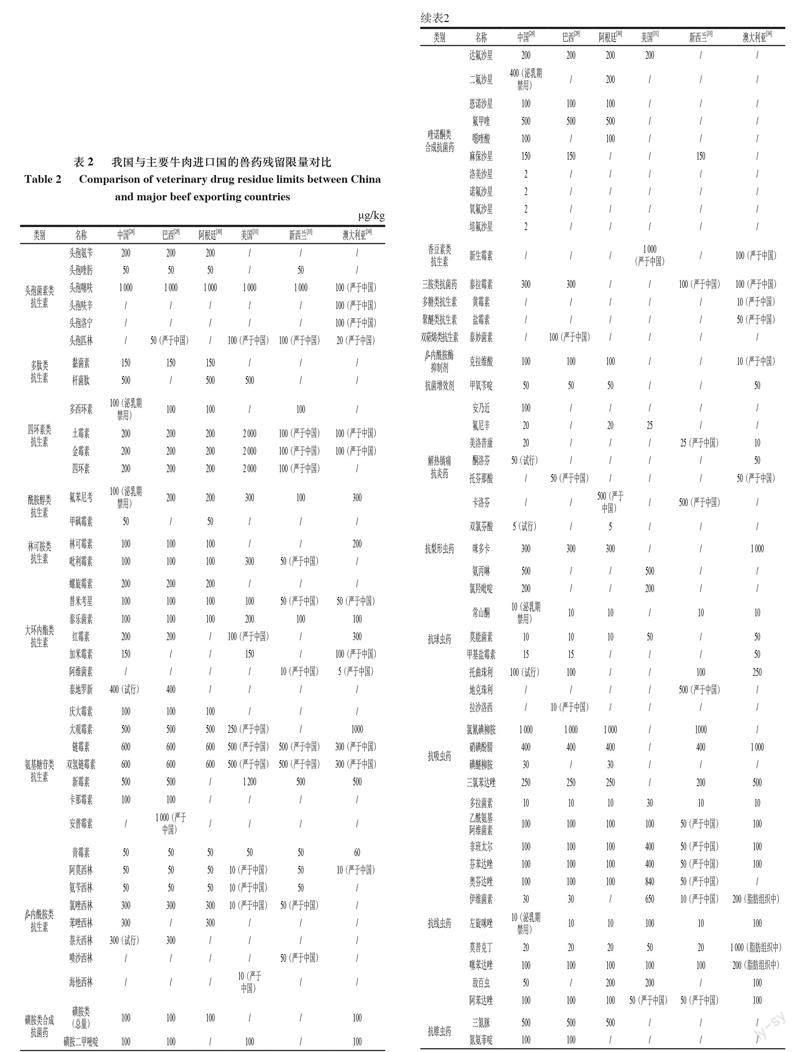
由图1~2可知,牛肉中有最大兽药残留限量规定的项目数量,我国占91 项,是规定最多的国家,而美国、新西兰分别仅占48、46 项,仅为我国的55%左右。可见在项目数量上,我国已在几个主要进口国遥遥领先。此外,几个进口国依然有不同程度严于我国限量的情况,新西兰和澳大利亚严于我国限量的项目数量比重较高,达30%及以上。我国在个别兽药残留种类把控上略显宽松。比如头孢菌素类抗生素,澳大利亚是控制最严的国家,尤其是头孢噻呋(100 μg/kg),仅为我国的1/10,且头孢呋辛、头孢洛宁、头孢匹林都是我国未规定限量的。又如四环素类抗生素土四金,新西兰和澳大利亚均是控制较严的国家,单项限量(100 μg/kg)均为我国的一半。美国(500 μg/kg)、新西兰(500 μg/kg)、澳大利亚(300 μg/kg)的链霉素和双氢链霉素限量均严于我国(600 μg/kg)。美国对β-内酰胺类抗生素的限量也相当严格,阿莫西林、氨苄西林、氯唑西林均只有我国(50 μg/kg)的1/5,且海他西林还是我国未规定限量的。澳大利亚的香豆素类抗生素新生霉素、三胺类抗菌药泰拉霉素、多糖类抗生素黄霉素、聚醚类抗生素盐霉素均严于我国,其中除泰拉霉素有试行限量外,其余3 种都未规定限量。双萜烯类抗生素泰妙菌素目前仅阿根廷有限量规定,为100 μg/kg。新西兰对抗线虫药中的乙酰氨基阿维菌素、非班太尔、芬苯达唑、奥芬达唑、伊维菌素、阿苯达唑的限量规定均比我国较严。抗血吸虫药氯舒隆,巴西、阿根廷、美国、澳大利亚均有限值,而我国未规定。以及抗病毒药沙奎那韦和奈韦拉平我国均未设限。可见一方面我国在牛肉中对个别种类兽药残留,如抗生素类、抗线虫药类、抗血吸虫药以及抗病毒药类需要继续考察接轨,尤其是抗生素类兽药残留,需要加强监管,因为抗生素的滥用可能会导致微生物群的改变,引起疾病,并可能产生耐药菌株,导致抗生素治疗失败[35-38]。另一方面也提示我国在进口牛肉时多关注这些限量严于我国的兽药残留项目,防止他国以次充好,将满足我国却不满足他国限量标准的牛肉出口到我国。
2.2 与CAC对比
CAC兽药残留限量标准[39]规定了β-肾上腺素受体阻断剂、抗寄生虫药、抗菌剂、抗真菌剂、驱虫剂、抗微生物剂、抗原生动物剂、抗真菌剂、抗原生生物剂、驱虫剂、杀虫剂、杀锥虫剂、肾上腺素受体激动剂、生产助剂、生长促进剂、糖皮质甾类及镇定剂等药物的最大残留限量。其中牛肉中的兽药残留有规定限量的项目数量在该标准中共涉及47 种。CAC是世界贸易组织(World Trade Organization,WTO)认可的唯一向世界各国政府推荐国际食品法典标准的组织,其标准也是WTO在国际食品贸易领域的仲裁标准。作为最低门槛,CAC牛肉中47 项有最大残留限量的兽药与我国相同的有44 项,宽于我国的有3 项。即CAC牛肉中有兽药残留限量规定的,我国已达到全部与CAC相同或更严。
2.3 与日本对比
日本因其“肯定列表制度”[40]是作为农兽药残留规定最为严苛的国家,本文对两国牛肉中兽药残留限量进行详细对比。日本兽药残留限量标准由日本厚生劳动省制定,都收录在2006年颁布的肯定列表中。“肯定列表制度”是日本为加强食品(包括可食用农产品)中农业化学品(包括农药、兽药和饲料添加剂)残留管理而制定的一项新制度。该制度要求:食品中农业化学品含量不得超过最大残留限量标准;对于未制订最大残留限量标准的农业化学品,其在食品中的含量不得超过“一律标准”,即0.01 mg/kg。日本的“肯定列表制度”中,牛肉中的兽药残留有最大限量规定的共涉及86 种。根据我国与日本的牛肉中兽药残留限量值对比发现,我国91 项有最大残留限量规定的兽药其中有64 项兽药残留限值和日本相同或更严,其中有14 项限值严于日本。即牛肉中我国有限值规定的近70%(60/86)兽药,其残留限量达到甚至严于日本规定,但存在有28 项兽药残留严于我国的情况(表1)。需要关注的有限值高于甚至远高于日本的,比如氯唑西林(日本40 μg/kg,我国为其7.5 倍)、咪多卡(日本30 μg/kg,我国为其10 倍)、阿苯达唑(日本20 μg/kg,我国为其5 倍)等。此外,同美国一样,日本也对β-内酰胺类抗生素控制较为严格,该类抗生素设定了限值的包括青霉素、阿莫西林、氨苄西林、氯唑西林、萘夫西林、美西林、双氯西林,而我国未对后2 种规定限值。萘夫西林的限值也是在GB 31650—2019公布之后,出自农业农村部公告第385号,日本对萘夫西林的控制相当严格,仅5 μg/kg,我国为其60 倍。日本还对我国牛肉中未控制聚醚类抗生素盐霉素规定了限值。解热镇痛抗炎药也是日本控制相当严格的兽药种类,除未对安乃近规定限值外,其他几种解热镇痛抗炎药,如氟尼克辛、酮洛芬、托芬那酸、卡洛芬均设定了限值,而我国仅对氟尼克辛、酮洛芬设定了限值。日本还对抗病毒类药物沙奎那韦设定了限值,而我国未设定相关此类药物的限值。
3 我国牛肉中兽药残留检测标准分析
结合表2统计情况,对我国牛肉中的每项兽药的检测标准进行查询,发现存在以下4 种情况:1)国内牛肉中有限量但暂时无牛肉基质检测标准的兽药;2)国内牛肉中有试行限量、规定试行检测方法的兽药;3)国外牛肉有限量、国内牛肉中尚无限量但有牛肉基质检测标准规定的兽药;4)国内牛肉中尚无限量规定且无牛肉检测标准的兽药。根据表3中我国牛肉中限量与检测方法需要及时跟进或补充的兽药统计情况,对4 种情况进行梳理并给出建议。
3.1 国内有限量但暂时无牛肉基质国家检测标准的兽药
我國牛肉的兽药残留中有限量规定但还无国家检测标准的包括头孢喹肟、多西环素、卡那霉素、苯唑西林、咪多卡、氯羟吡啶、莫能菌素、甲基盐霉素、硝碘酚腈、三氯苯达唑、噻苯达唑、倍他米松、美洛昔康、莫奈太尔共计14 种。其中GB/T 22960—2008《河豚鱼和鳗鱼中头孢唑啉、头孢匹林、头孢氨苄、头孢洛宁、头孢喹肟残留量的测定 液相色谱-串联质谱法》、GB 31657.3—2022《食品安全国家标准 蜂产品中头孢类药物残留量的测定 液相色谱-串联质谱法》、GB 31659.3—2022《食品安全国家标准 奶和奶粉中头孢类药物残留量的测定液相色谱-串联质谱法》可检测头孢喹肟的标准均无牛肉基质;即将实施的GB 31659.2—2022《食品安全国家标准 禽蛋、奶和奶粉中多西环素残留量的测定液相色谱-串联质谱法》可检测多西环素但也不适用于牛肉基质;现行的GB/T 22969—2008《奶粉和牛奶中链霉素、双氢链霉素和卡那霉素残留量的测定 液相色谱-串联质谱法》、GB/T 22995—2008《蜂蜜中链霉素、双氢链霉素和卡那霉素残留量的测定 液相色谱-串联质谱法》、GB/T 22945—2008《蜂王浆中链霉素、双氢链霉素和卡那霉素残留量的测定 液相色谱-串联质谱法》、GB/T 22954—2008《河豚鱼和鳗鱼中链霉素、双氢链霉素和卡那霉素残留量的测定 液相色谱-串联质谱法》也均不适用于牛肉中卡那霉素的检测;现行的有关苯唑西林的检测标准GB/T 22975—2008《牛奶和奶粉中阿莫西林、氨苄西林、哌拉西林、青霉素G、青霉素V、苯唑西林、氯唑西林、萘夫西林和双氯西林残留量的测定 液相色谱-串联质谱法》、现行有效的有关氯羟吡啶的检测标准GB 29699—2013《食品安全国家标准 鸡肌肉组织中氯羟吡啶残留量的测定 气相色谱-质谱法》等也无牛肉基质;现行有效的有关阿维菌素的检测标准GB 31659.4—2022《食品安全国家标准 奶及奶粉中阿维菌素类药物残留量的测定 液相色谱-串联质谱法》、有关噻苯达唑的检测标准GB/T 22972—2008《牛奶和奶粉中噻苯达唑、阿苯达唑、芬苯达唑、奥芬达唑、苯硫氨酯残留量的测定 液相色谱-串联质谱法》适用基质均为牛乳和乳粉;咪多卡和莫能菌素可分别参考《中华人民共和国农业农村部公告 第608号、第283号》相关试行检测方法;甲基盐霉素、硝碘酚腈、三氯苯唑和倍他米松均无任何参考标准;莫奈太尔在《中华人民共和国农业农村部公告 第355号》中有试行检测方法,但其适用范围为绵羊可食性组织。
3.2 国内有试行限量规定、需要及时考察整合限量及发布正式检测方法的兽药
GB 31650—2019及GB 31650.1—2022《食品安全国家标准 食品中41 种兽药最大残留限量》发布之后,中华人民共和国农业农村部又陆续规定了一系列在牛肉中的兽药残留限量,这些兽药均分散在各个公告,因此需要及时整合,以维持兽药残留标准的完整性。同时这类药物的检测方法也只在相应公告的附件中出行了试行检测方法,也需要及时考察后发布正式检测方法。如泰拉霉素是一种治疗和预防对泰拉霉素敏感的溶血巴氏杆菌、多杀巴氏杆菌、睡眠嗜血杆菌和支原体引起的牛呼吸道疾病的兽药,《中华人民共和国农业农村部公告 第165号》规定该药物在牛肉中的限量为300 μg/kg,并同时发布了试行的检测方法。在《中华人民共和国农业农村部公告 第273号》中规定托(妥)曲珠利在牛肉中的限量为100 μg/kg,并同时发布了试行的检测方法。此外虽有妥曲珠利的检测方法,如农业部2349号公告-1—2015、SN/T 2318—2009《动物源食品中地克珠利、妥曲珠利、妥曲珠利亚砜和妥曲珠利砜残留量的检测 高效液相色谱-质谱/质谱法》等,但前者仅适用于饲料中,后者也无牛肉基质适用范围。加米霉素对临床分离的多杀性巴氏杆菌、溶血性曼氏杆菌、牛支原体和链球菌均有良好的体外抗菌活性,已有临床上可用加米霉素制剂防治牛呼吸道疾病的文献报道[41-42],由于牛支原体菌株易耐药,传统用于牛支原体肺炎治疗的药物大多有耐药性,已广泛使用的替米考星、泰乐菌素等大环内酯类抗生素在很多地区都出现了不同程度的耐药性,大大降低了药物的使用效果,在此情况下加米霉素的使用具有非常广阔的前景,对加米霉素的监管也应随之加强,《中华人民共和国农业农村部公告 第15号》规定我国牛肉中加米霉素的限量为150 μg/kg,并同时发布了试行的检测方法。泰地罗新是一种新型十六元环动物专用的大环内酯类半合成抗生素,对牛、猪的呼吸道疾病具有十分明显的治疗效果,具有良好的开发应用价值[43]。酮洛芬用于治疗奶牛临床型乳房炎引起的炎症、发热与肌肉疼痛等,参照日本有关标准制定了酮洛芬的试行限量为20 μg/kg,并同时发布了试行的检测方法。羟氯扎胺用于治疗牛肝片吸虫病,参照欧盟有关标准制定了牛肉中羟氯扎胺的试行限量为20 μg/kg,二者可见于《中华人民共和国农业农村部公告 第327号》。双氯芬酸用于辅助治疗奶牛临床型乳房炎引起的发热,《中华人民共和国农业农村部公告 第186号》发布其试行限量为5 μg/kg,并同时发布了试行的检测方法。《中华人民共和国农业农村部公告 第355号》发布泼尼松龙试行限量为4 μg/kg(参照欧盟有关标准),并同时发布了试行的检测方法。
上述9 种兽药的残留限量均为申报单位申报兽药时参考已有国家或组织标准制定的限量,仅为试行。是否有必要将其纳入正式限量规定标准中还需要结合实际情况进行考察。如其中氟尼辛、萘夫西林、酮洛芬、双氯芬酸等兽药虽在牛肉中制定了试行限量,但是根据其适用对象和适应症可发现,此类兽药多用于奶牛的乳房炎治疗[44-46],在肉牛中是否有使用的可能成为是否需要制定其在牛肉中限量规定的依据。
3.3 国外有限量但国内尚无限量规定的兽药
通过对比发现国内牛肉中尚无限量规定的兽药包括头孢洛宁、头孢匹林、雙氯西林、阿维菌素、氯舒隆、地克珠利、泰妙菌素、利巴韦林、头孢呋辛、安普霉素、巴龙霉素、美西林、喷沙西林、海他西林、奥比沙星、新生霉素、黄霉素、盐霉素、托芬那酸、卡洛芬、拉沙洛西、哈洛克酮、氟雷拉纳、曲吡那敏、甲基泼尼松龙、奈韦拉平、诺司孕甾酮共计27 种。其中,前8 种为国内牛肉中尚无限量规定但有标准检测方法的兽药,后19 种为国内牛肉中尚无限量规定且无标准检测方法的兽药。其中,双氯西林、奥比沙星相关检测标准
GB/T 22975—2008、GB/T 22985—2008《牛奶和奶粉中恩诺沙星、达氟沙星、环丙沙星、沙拉沙星、奥比沙星、二氟沙星和麻保沙星残留量的测定 液相色谱-串联质谱法》规定适用于牛乳和乳粉中;新生霉素SN 0674—1997《出口肉及肉制品中新生霉素残留量检验方法滤纸片法》已经废止;黄霉素、盐霉素、拉沙洛西仅有饲料中的检测方法;其余皆无相应检测标准。
虽然有部分兽药我国未在牛肉中规定,但考虑到我国实际生产养殖过程中,兽药的限量并不是越严越先进,设置兽残的种类也并非越多越高标准。这些兽药在牛肉中限量制定是否必要需要结合我国实际情况进一步考察。如巴龙霉素,虽然目前仅欧盟的牛肉中规定了限值,但因其药物本身的局限性,其抗菌谱与新霉素和卡那霉素基本相同,而耳、肾毒性大,鲜有用于牛的养殖过程中的报道。因此,此类药物可根据实际生产过程暂时无须严格要求。又如新生霉素等在国外广泛用于牛乳房炎药物[42],但多用于奶牛而不是肉牛中,因此对牛肉中规定此药物的限量也并不适合。
但是国外有限量但国内牛肉中尚无限量规定的兽药仍然是需要关注的兽药。《食品安全法》第九十二条规定,进口的食品、食品添加剂、食品相关产品应当符合我国食品安全国家标准。同时《中华人民共和国进出口食品安全管理办法(海关总署第249号令)第九条》也规定,进口食品应当符合中国法律法规和食品安全国家标准,中国缔结或者参加的国际条约、协定有特殊要求的,还应当符合国际条约、协定的要求。对于上述牛肉中既没有限量规定,又无相应检测方法的兽药则亟需重点关注。这类牛肉进口或有可能符合我国食品安全国家标准,但不符合出口方(出口国)的相关要求。《食品安全法》第九十三条规定,进口尚无食品安全国家标准的食品,由境外出口商、境外生产企业或者其委托的进口商向国务院卫生行政部门提交所执行的相关国家(地区)标准或者国际标准。国务院卫生行政部门对相关标准进行审查,认为符合食品安全要求的,决定暂予适用,并及时制定相应的食品安全国家标准。因此,对于上述牛肉中我国既没有限量规定,又无相应检测方法的兽药则亟需有关部门及时关注制定检测标准,防止出口方将符合我国却不符合他国的次品牛肉出口到我国。
4 国际新型兽药残留动态
氟雷拉纳曾广泛用于猫、犬的防蚤类药物[47],而近段时间已有巴西、澳大利亚将其实行了牛肉中的限量规定。2019年8月13日,APVMA发布2019年第16号公报,修订《澳新食品标准法典》表20最大残留限量标准,制定氟雷拉纳在牛肉中的暂定最大残留限量5 μg/kg,巴西国家卫生监督局2021年4月14日在政府公报上发布了规范性指令,规定氟雷拉纳在牛肉中限量为75 μg/kg。氟雷拉纳不仅与现有杀虫剂无显著的交互抗性,甚至对部分抗性害虫也具有较好的杀虫活性。经查,GB 31650—2019《食品安全国家标准 食品中兽药最大残留限量》以及其他现行有效涉及兽药残留限量的中华人民共和国农业农村部公告第250号、中华人民共和国农业部公告第2292号、中华人民共和国农业部公告第2428号、中华人民共和国农业部公告第2583号、中华人民共和国农业部公告第2638号等公告,未规定氟雷拉纳的限量。况且我国也没有像日本一样在残留限量上采用“一律标准”(既非“豁免物质”也未制定“最大残留限量标准”的农业化学品在食品中的残留制定的统一標准)。因此,鉴于新型兽残氟雷拉纳有广阔的应用前景,相关限量和检测标准应紧随其上。此外我国近几年还研制了一系列新型兽药,如新型兽药沙咪珠利,其具有高效的抗球虫活性,成为继喹烯酮之后我国在兽用化学药物领域又一个可在食品动物中使用的新型兽药,研究表明,沙咪珠利低毒、安全、广谱,具有广阔的研究前景[48]。但其在牛的养殖中是否可用,是否需要制定限量也需要及时跟进观察。此外,在现代畜禽养殖业中,一些不法分子长期大量使用各种蛋白同化制剂和人工合成激素类药物,因此动物源性食品中的药物残留成为了食源性兴奋剂的来源。超高效液相色谱-四极杆/飞行时间质谱快速筛查和确证猪肉和牛肉中30 种兴奋剂残留,为食源性兴奋剂的风险监测提供了一种有力的技术手段[49]。提示在进行常规兽药监管的同时也要注意新型兽药、未规定限量兽药检测技术的进展。
5 结 语
根据以上分析,对牛肉的兽药残留限量提出以下建议:1)结合兽药实际使用情况和监测结果进一步完善牛肉中兽药残留限量及检测的相关标准;2)规范国内牛养殖环节的兽药使用行为,提升进口牛肉的质量安全,保障消费者的食品健康安全;3)对于牛肉中我国既没有限量规定,又无相应检测方法的兽药则亟需有关部门及时关注制定检测标准,防止出口方将符合我国却不符合他国的次品牛肉出口到我国;4)及时关注新型兽药残留的动态,充分利用非靶向筛查技术提升监督检测手段,发现标准规定之外的兽药残留,以全面监管牛肉的兽药残留情况,最大程度规范兽药在肉牛中的使用。
经本文对比分析后发现,与几个主要牛肉进口国巴西、阿根廷、美国、新西兰、澳大利亚相比,我国牛肉中有最大兽药残留项目数量规定的种类相当但数量最多,表明我国在进口他国牛肉的时候,兽药残留质量管控相对更严,但仍有个别类别的兽药整体限量严于我国,在进口时需要充分关注,如抗生素类(头孢菌素类、β-内酰胺类、香豆素类、三胺类、多糖类、聚醚类等)、抗线虫药类、抗血吸虫药以及抗病毒药类。与农药、兽药残留规定最严的日本相比,我国GB 31650—2019仍然存在一定差异,缺乏包括头孢呋辛、阿维菌素等在内的12 项兽药残留规定。此外本文还统计了我国兽药残留检测标准缺乏的情况,在91 项有规定的兽药残留中,还存在包括头孢喹肟等14 项无牛肉基质检测标准的情况,另外还有包括加米霉素等9 项有农业农村部公布的试行限量和试行检测标准,此外还有19 项我国牛肉中既无限量规定也无检测标准的兽药,其中需要特别关注新型兽药弗雷拉纳。
未来我国仍需结合兽药实际使用情况以及其他贸易国家限量要求及检测方法、进一步完善牛肉中兽药残留限量及检测的相关标准,对我国兽药限量标准低于国外标准的兽药进行分析,加强监管和关注,进行风险分析,严格控制产品质量安全,使其向国际先进水平进一步靠拢,一方面进一步约束国内不规范的兽药使用行为,另一方面保障进口牛肉食品的安全。
参考文献:
[1] 中国国际经济交流中心课题组. 新时期我国农业对外开放与高质量发展问题研究[J]. 全球化, 2022(1): 5-26; 134. DOI:10.16845/j.cnki.ccieeqqh.2022.01.001.
[2] 董思淼. 中国牛肉进口影响因素研究[D]. 石家庄: 河北经贸大学, 2021: 1-2. DOI:10.27106/d.cnki.ghbju.2021.000590.
[3] 罗菲. 消费者牛肉偏好的原产地效应及影响因素研究[D]. 南昌: 江西财经大学, 2021: 1-2. DOI:10.27175/d.cnki.gjxcu.2021.000711.
[4] 王贵荣: 粮食生产再获丰收 畜牧业稳定发展[EB/OL]. (2023-01-18) [2023-06-10]. http://www.stats.gov.cn/sj/sjjd/202302/t20230202_1896736.html.
[5] 中华人民共和国海关总署统计分析司. (14) 2022年12月进口主要商品量值表(人民币值)[EB/OL]. (2023-01-18) [2023-06-10]. http://www.customs.gov.cn/tjs/sjgb/4926700/4807029/index.html.
[6] 中华人民共和国海关总署. (14) 2021年12月进口主要商品量值表(人民币值)[EB/OL]. (2022-01-18) [2023-06-10]. http://www.customs.gov.cn//customs/302249/zfxxgk/2799825/302274/302277/302276/4127968/index.html.
[7] 禄粞麟, 起建凌, 王安奎, 等. 中新牛肉贸易发展对策研究[J]. 安徽农学通报, 2021, 27(14): 131-134. DOI:10.16377/j.cnki.issn1007-7731.2021.14.048.
[8] 梁雪婷. 中国牛肉进口研究[D]. 上海: 上海财经大学, 2021: 7-8. DOI:10.27296/d.cnki.gshcu.2021.000004.
[9] 伊禹澄. 中澳牛肉贸易现状与发展前景[J]. 农业经济, 2020(6): 127-129.
[10] 刘鹏. 巴西: 近五成出口牛肉进入中国[J]. 中国食品, 2018(9): 91.
[11] 陈孟裕, 赵明刚, 焦阳 等. 进口食品安全口岸监管相关问题研究[J]. 中国标准化, 2022(23): 58-62.
[12] 高鹏飞, 龚威, 汤亚云, 等. 牛、羊肉和牛、羊奶中兽药残留现状分析及检测技术研究进展[J]. 中国兽药杂志, 2022, 56(1): 77-85.
[13] 周迎春, 刘少博, 华向美. 我国动物源性食品中兽药残留的危害及现状[J]. 粮食与油脂, 2021, 34(6): 18-20.
[14] 贝君, 王珂雯, 程雅晴, 等. 我国肉制品安全风险及监管建议[J]. 食品安全质量检测学报, 2020, 11(16): 5540-5546. DOI:10.19812/j.cnki.jfsq11-5956/ts.2020.16.035.
[15] 汤晓艳, 郑锌, 王敏, 等. 畜禽产品兽药残留限量标准现状与发展方向[J]. 食品科学技术学报, 2017, 35(4): 8-12.
[16] 陈泽宇, 张云, 张信仁. 国内外牛肉相关法规标准研究进展[J]. 食品工业科技, 2022, 43(15): 436-443. DOI:10.13386/j.issn1002-0306.2021080115.
[17] 陈泽宇, 卢立洋, 黄享云, 等. 我国与国外牛肉产品中农残限量标准比对研究[J]. 天津农业科学, 2022, 28(3): 65-69; 74.
[18] 卢阳, 陈晋元, 贺兆源, 等. 中国与国外牛、羊肉及其产品兽药残留限量标准的对比研究[J]. 中国兽药杂志, 2020, 54(11): 57-64.
[19] 孙彩霞, 杨明升, 崔野韩, 等. 主要贸易国牛肉质量安全标准研究[J]. 江苏农业科学, 2011, 39(4): 366-368. DOI:10.15889/j.issn.1002-1302.2011.04.185.
[20] 刘鑫, 高家瑞, 王建军, 等. 奶牛养殖场兽药残留限量新标准解析[J]. 当代畜牧, 2020(1): 31-32.
[21] 孙颖宜, 成姗, 林琳, 等. 国内外乳及乳制品中兽药残留限量标准比较分析[J]. 食品安全质量检测学报, 2016(1): 378-382. DOI:10.19812/j.cnki.jfsq11-5956/ts.2016.01.071.
[22] 孙星雅, 刘睿, 张素霞, 等. 中国与欧盟和美国牛乳中兽药残留限量标准的对比研究[J]. 食品安全质量检测学报, 2021, 12(24): 9317-9325. DOI:10.19812/j.cnki.jfsq11-5956/ts.2021.24.001.
[23] 吴海燕, 张志华, 朱文嘉, 等. 水产品中兽药残留限量标准的对比
分析[J]. 食品安全质量检测学报, 2018, 9(18): 4877-4884.
[24] 杨杰, 黄文锋, 陈创钦, 等. 国内外禽蛋类产品兽药残留限量标准比对分析[J]. 中国家禽, 2018, 40(23): 1-4. DOI:10.16372/j.issn.1004-6364.2018.23.001.
[25] 毛智琼, 金永才, 刘璇, 等. 我国与欧盟、美国、国际食品法典委员会的禽蛋抗生素类兽药残留限量标准对比分析[J]. 食品安全质量检测学报, 2020, 11(12): 4034-4040. DOI:10.19812/j.cnki.jfsq11-5956/ts.2020.12.052.
[26] 中华人民共和国农业农村部, 中华人民共和国国家卫生健康委员会, 国家市场监督管理总局. 食品安全国家标准 食品中兽药最大残留限量: GB 31650—2019[S]. 北京: 中国标准出版社, 2019.
[27] 陈岩, 刘雯雯, 耿安静, 等. 基于兽药残留限量的GB 31650与CAC标准异同分析[J]. 现代食品科技, 2022, 38(5): 270-277; 164. DOI:10.13982/j.mfst.1673-9078.2022.5.0885.
[28] 中華人民共和国农业农村部, 中华人民共和国国家卫生健康委员会, 国家市场监督管理总局. 食品安全国家标准 食品中41 种兽药最大残留限量: GB 31650.1—2022[S]. 北京: 中国标准出版社, 2022.
[29] Agência Nacional de Vigil?ncia Sanitária. Limites máximos de resíduos de medicamentos veterinários em alimentos de origem animal[EB/OL]. (2018) [2023-06-10]. http://antigo.anvisa.gov.br/documents/219201/219401/Med+Vet_Documento+base+discussa~o+18.10/69d161b5-785c-4907-862c-2294b48a79c5.
[30] National Animal Health Service. Apruébanse los límites de residuos en alimentos de origen animal[EB/OL]. [2023-06-10]. http://servicios.infoleg.gob.ar/infolegInternet/anexos/185000-189999/185988/norma.htm.
[31] U.S. Food and Drug Administration. Part 556 Tolerances for residues of new animal drugs in food[EB/OL]. [2023-06-07]. https://www.ecfr.gov/current/title-21/chapter-I/subchapter-E/part-556.
[32] 張昱, 冯皓迪, 唐妹, 等. β-内酰胺类抗生素的环境行为与制药行业源头控制技术研究进展[J]. 环境工程学报, 2020, 14(8): 1993-2010.
[33] New Zealand Food Safety Authority. New Zealand (maximum residue levels for agricultural compounds) food standards [EB/OL]. [2023-06-10]. https://www.mpi.govt.nz/dmsdocument/19550-Maximum-Residue-Levels-for-Agricultural-Compounds.
[34] Australian Pesticides and Veterinary Medicines Authority. Agricultural and veterinary chemicals code (MRL standard) instrument 2019[EB/OL].
[2023-06-10]. https://www.legislation.gov.au/Browse/Results/ByTitle/LegislativeInstruments/InForce/A/0/MRL/principal.
[35] ZEMA B, BLN A, SSAT A, et al. Antibiotic residues in food animals: public health concern[J]. Acta Ecologica Sinica, 2019, 39(5): 411-415. DOI:10.1016/j.chnaes.2018.10.004.
[36] WANG Hexing, REN Lingshuang, YU Xin, et al. Antibiotic residues in meat, milk and aquatic products in Shanghai and human exposure assessment[J]. Food Control, 2017, 80: 217-225. DOI:10.1016/j.foodcont.2017.04.034.
[37] 张义楠, 袁文焕, 兰力伟, 等. 抗生素耐药与肠道菌群的研究进展[J].
饲料研究, 2021, 44(1): 139-142. DOI:10.13557/j.cnki.issn1002-2813.2021.01.038.
[38] VIKRAM A, ROVIRA P, AGGA G E, et al. Impact of “raised without antibiotics” beef cattle production practices on occurrences of antimicrobial resistance[J]. Applied and Environmental Microbiology, 2017, 83(22): e01682-17. DOI:10.1128/aem.01682-17.
[39] Joint FAO/WHO Committee Food Additives. Codex committee veterinary drugs food. Maximum residue limits (MRLs)[EB/OL]. [2023-06-10]. https://www.fao.org/fao-who-codexalimentarius/codex-texts/maximum-residue-limits/en/.
[40] Ministry of Health, Labour and Welfare. Maximum residue limits (MRLs) list of agricultural chemicals in foods[EB/OL]. [2023-06-10]. https://db.ffcr.or.jp/front/food_group_detail?id=14100.
[41] 周德刚, 卢基忠, 李朋朋, 等. 加米霉素对牛呼吸道疾病相关病原菌临床分离株的体外药敏试验[J]. 安徽农业科学, 2020, 48(2): 113-116.
[42] 冯言言, 魏秀丽, 郑莉, 等. 加米霉素注射液治疗多杀性巴氏杆菌引起牛呼吸道疾病的临床疗效观察[J]. 中国兽医杂志, 2019, 55(9): 97-100.
[43] 刘天钰, 一种泰地罗新的制备方法: 中国, CN106749457A[P]. 2017-05-31.
[44] 刘桂兰, 邓旭明, 刘爱玲, 等. 牛乳房炎用药国内外制剂审批情况[J]. 中国兽医杂志, 2017, 53(10): 117-120.
[45] 王方雨, 李宁, 曹帅, 等. 采用科学方法准确检测牛的肌肉和肝脏中双氯芬酸残留[J]. 中国食品, 2020(20): 100-103.
[46] 赵婷婷, 孙德孝, 席库, 等. 三种干奶药对奶牛乳房炎在干奶期的治疗、预防效果比较[J]. 中国奶牛, 2022(6): 20-24. DOI:10.19305/j.cnki.11-3009/s.2022.06.005.
[47] 刘春双, 韩明月, 王宏磊, 等. 新型异噁唑啉类化合物氟雷拉纳研究应用现状[J]. 中国兽药杂志, 2022, 56(4): 76-86.
[48] 张志浩. 新型抗球虫药物沙咪珠利(Ethanamizuril)的药代动力学研究[D]. 重庆: 重庆师范大学, 2019: 7-8.
[49] 马俊美, 范素芳, 李强, 等. 超高效液相色谱-四极杆/飞行时间质谱检测猪肉和牛肉中30 种食源性兴奋剂类药物残留[J]. 食品科学, 2021, 42(14): 276-285. DOI:10.7506/spkx1002-6630-20200624-329.
收稿日期:2023-04-10
基金项目:四川省市场监督管理局科技计划项目(SCSJ2021027)
第一作者简介:刘忠莹(1988—)(ORCID: 0000-0003-3979-4891),女,工程师,硕士,研究方向为食品检验。
E-mail: lzyqiao@126.com
*通信作者简介:王鑫(1983—)(ORCID: 0000-0003-4929-1438),女,高级工程师,硕士,研究方向为食品营养与安全。
E-mail: 271600249@qq.com
