“化学实验技术”大赛中铁含量测定方法影响因素分析
2023-02-02易承学
易承学,徐 茜
(镇江高等专科学校 医药技术学院,江苏 镇江 212028)
化学实验技术作为职业院校技能大赛赛项之一,2022年竞赛项目由“样品中金属组分(钴或镍)含量的测定”“样品中铁含量的测定”“乙酸乙酯的合成及质量评价”3个模块组成。涉及物质的定性分析、定量分析、产品制备和质量控制,主要考核选手的化学理论功底、实验操作基本技能、规范操作意识及安全意识等职业素养。其中,“样品中铁含量的测定”模块需要选手根据赛场提供的已知条件,选择磺基水杨酸分光光度法或1,10-菲啰啉分光光度法,自行设计实验方案,在规定时间内完成试样测定,得到准确的测定结果。该模块对方法的精密度和准确度要求较高,然而实验过程中的影响因素也较多,如玻璃器皿清洁、标准储备液稀释、待测溶液配制、溶液显色时间等都会对最终结果产生较大影响。笔者围绕以上影响因素进行分析,提出改进措施,以期提高测定结果的准确性,帮助选手在技能大赛中创造佳绩。
1 实验部分
1.1 实验材料
1.1.1 仪器与玻璃器皿
UV-1800PC-DS2型紫外—可见分光光度计(上海美谱达仪器有限公司),GL2004B型电子天平(上海佑科仪器仪表有限公司)。容量瓶、吸量管、量筒(杯)、烧杯,实验室其他常见玻璃器皿。
1.1.2 试剂
乙酸、三水乙酸钠、抗坏血酸、硫酸、氨水、氯化铵、磺基水杨酸、1,10-菲啰啉、十二水合硫酸铁铵均为分析纯(国药集团化学试剂有限公司),实验用水为去离子水。
1.1.3 溶液配制
1) 乙酸-乙酸钠缓冲液:称取三水乙酸钠272 g,加水500 mL溶解,加入乙酸240 mL,最后加水稀释到1 000 mL,即得。
2) 氨-氯化铵缓冲液:称取氯化铵54 g,加少量水溶解后,加氨水350 mL,再加水稀释至1 000 mL,即得。
3) 抗坏血酸溶液(20 g·L-1):称取20 g抗坏血酸,加水溶解稀释到1 000 mL,即得。
4) 磺基水杨酸溶液(100 g·L-1):称取100 g磺基水杨酸,加水溶解稀释到1000 mL,即得。
5) 1,10-菲啰啉溶液(2 g·L-1):称取2 g 1,10-菲啰啉,加水溶解稀释到1 000 mL,即得。
6) 铁离子标准储备液(2.000 g·L-1):准确称取17.270 g十二水合硫酸铁铵,用400 mL水溶解,加入1∶1硫酸溶液100 mL,加水定容至1 000 mL,摇匀即得。
7) 铁离子标准中间液A(80.000 mg·L-1)与中间液B(40.000 mg·L-1):分别精密移取铁离子标准储备液10.00 mL,5.00 mL于不同的250 mL容量瓶中,加水稀释并定容至刻度,摇匀即得。
1.2 标准曲线绘制
1.2.1 磺基水杨酸分光光度法
1) 系列标准溶液配制。分别精密吸取0.00 mL,1.00 mL,2.00 mL,4.00 mL,6.00 mL,8.00 mL,10.00 mL铁离子标准中间液A(80.000 mg·L-1)于7个100 mL容量瓶中,分别依次加入5 mL磺基水杨酸溶液和20 mL氨-氯化铵缓冲液,用水稀释至刻度,摇匀,即得浓度范围为0.000~8.000 mg·L-1的系列标准溶液(按浓度从小到大记为1~7 号溶液)。
2) 标准曲线绘制。以1号溶液为空白溶液,在最大吸收波长420 nm处测定上述1~7 号溶液的吸光度,以浓度(C)为横坐标,以相应的吸光度(A)为纵坐标绘制标准曲线。得到的标准曲线为:A=0.101 84C+0.00133(r=0.999 990)。测定结果见表1。

表1 2种分光光度法测定的吸光度
1.2.2 1,10-菲啰啉分光光度法
1) 系列标准溶液配制。分别精密吸取0.00 mL,1.00 mL,2.00 mL,4.00 mL,6.00 mL,8.00 mL,10.00 mL铁离子标准中间液B(40.000 mg·L-1)于7个100 mL容量瓶中,分别加入2 mL抗坏血酸溶液,摇匀后再依次加入20 mL乙酸-乙酸钠缓冲液和10 mL 1,10-菲啰啉溶液,用水稀释至刻度,摇匀,即得浓度范围为0.000~4.000 mg·L-1的系列标准溶液(按浓度从小到大记为1′~7′号溶液)。
2) 标准曲线绘制。以1′号溶液为空白溶液,在最大吸收波长510 nm处测定上述1′~7′号溶液的吸光度,以浓度(C)为横坐标,以相应的吸光度(A)为纵坐标绘制标准曲线。得到的标准曲线为:A= 0.20762C- 0.00049(r= 0.999 994)。测定结果见表1。
1.3 试样分析
1.3.1 铁试样制备
准确称取17.270 g十二水合硫酸铁铵,以400 mL水溶解,加入1∶1硫酸溶液100 mL,加水定容至1 000 mL,即得铁试样,铁离子质量浓度为2.000 g·L-1。
1.3.2 待测溶液制备与测定
1) 磺基水杨酸分光光度法。精密吸取上述铁试样8.00 mL于100 mL容量瓶中,加水稀释至刻度,摇匀,精密吸取该稀释液3.00 mL于100 mL容量瓶中,依次加入5 mL磺基水杨酸溶液和20 mL氨-氯化铵缓冲液,用水稀释至刻度,摇匀,静置10 min即得待测溶液。平行制备3份。
2) 1,10-菲啰啉分光光度法。精密吸取上述铁试样4.00 mL于100 mL容量瓶中,加水稀释至刻度,摇匀,精密吸取该稀释液3.00 mL于100 mL容量瓶中,先加入2 mL抗坏血酸溶液,摇匀后再依次加入20 mL乙酸-乙酸钠缓冲液和10 mL 1,10-菲啰啉溶液,用水稀释至刻度,摇匀,静置10 min 即得待测溶液。平行制备3份。
3) 待测溶液测定。以1号溶液、1′号溶液为空白溶液,分别测定磺基水杨酸、1,10-菲啰啉分光光度法的3份待测溶液的吸光度。根据测得的吸光度,从标准曲线查得待测溶液中铁的质量浓度(ρx)。测定结果见表2。
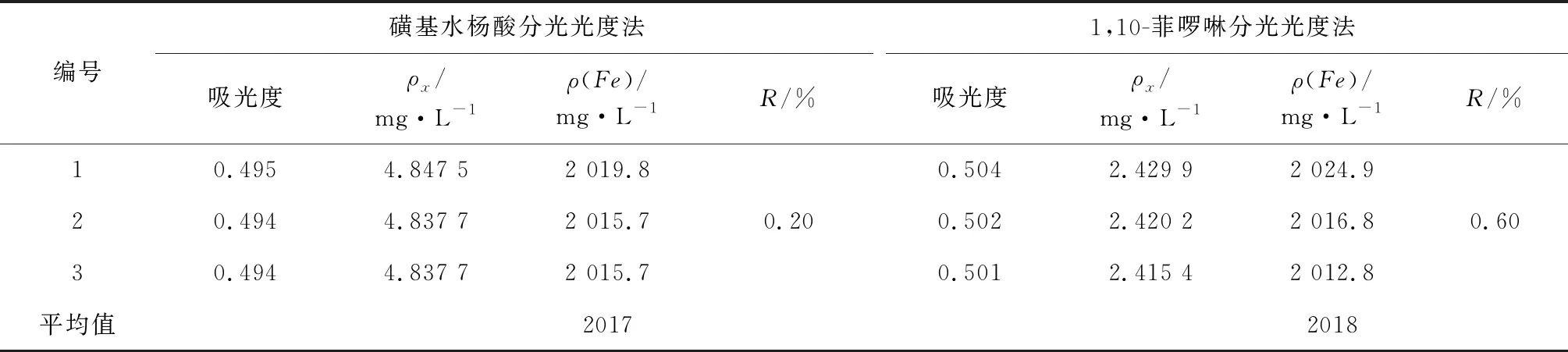
表2 试样中铁含量测定结果
1.3.3 结果计算
1) 试样中铁含量计算。按式(1)计算出试样中铁含量,以ρ(Fe)表示,取3次测定结果的算术平均值作为最终结果,结果保留4位有效数字。计算结果见表2。
ρ(Fe)=ρx×n。
(1)
式(1)中,ρ(Fe)表示试样中铁的质量浓度,mg·L-1;ρx表示从标准曲线查得的待测溶液中铁的质量浓度,mg·L-1;n表示试样溶液的稀释倍数,倍。
2) 误差分析。按式(2)计算出试样中铁含量测定结果的精密度,以相对极差R表示,结果精确至小数点后2位。计算结果见表2。
(2)

2 影响因素分析
2.1 玻璃器皿清洁
比赛需要使用多种规格的容量瓶、吸量管、量筒(杯)和烧杯等玻璃器皿,其洁净与否会直接影响实验结果的准确性。王婷婷[1]在水质监测中,经常出现总氮测定值小于氨氮测定值的问题,而玻璃器皿干净程度是影响因素之一。通过将玻璃器皿应用体积分数1+9盐酸溶液或1+35硫酸溶液浸泡24 h后,再分别用自来水和无氨水冲洗数次,洗净后立即使用可以提高总氮的准确率。吴瑞业[2]在用原子荧光法测汞时,因该元素容易吸附在玻璃器皿表面而造成污染,致使标准空白过高,对实验结果产生较大影响。必须先用酸性洗液长时间浸泡玻璃器皿以去除表面吸附的汞,降低污染。由此可见,洁净的玻璃器皿是实验取得成功的先决条件,务必在开展实验之前将玻璃器皿清洗干净,以满足实验要求。经洗涤后,如玻璃器皿内外壁既无水滴聚集,也无成股流下的现象,完全被水均匀润湿,表明已被清洗干净。
2.1.1 新购玻璃器皿洗涤方法
新购置的玻璃器皿表面附有游离碱,可先用毛刷蘸去污粉刷洗器壁,用自来水冲洗,去除灰尘等杂物,之后浸泡于2%盐酸溶液中24 h,再用自来水彻底冲洗干净,最后用少量去离子水荡洗2~3次,干燥备用。
2.1.2 常用玻璃器皿洗涤方法
1) 一般性实验玻璃器皿洗涤。此类器皿一般不附着难去除的残留物,容易洗净。先倒去容器内残液用自来水冲洗,再用毛刷蘸取肥皂粉或洗衣粉,仔细刷洗内外壁,然后用自来水反复冲洗。容量瓶、吸量管、量筒等不宜刷洗的计量器皿先用洗涤剂液浸泡后用水冲洗,最后用少量去离子水荡洗2~3次。
2) 油脂污物玻璃器皿洗涤。容量瓶、吸量管、量筒等计量器皿的内壁若有油污,势必产生水珠挂壁现象,将严重影响体积的准确测量。应选用碱性洗液、碱性酒精洗液、碱性高锰酸钾洗液、铬酸洗液浸泡1~3 d,除去内壁的油污,后用自来水反复冲洗,最后用去离子水冲洗2~3次。各种洗涤液配制方法详见文献[3-4]。
3) 金属离子残留玻璃器皿洗涤。一般用稀盐酸、稀硝酸浸泡清洗,对于污垢较重容器再用体积分数1+1盐酸或1+1硝酸溶液浸泡8 h以上,然后用自来水冲净酸液,最后用少量去离子水荡洗2~3次。
2.2 标准储备液稀释
由赛场提供的铁离子标准储备液已标明浓度(2022年江苏省职业院校技能大赛该储备液的浓度为2.000 g·L-1),选手需根据赛场给定的玻璃器皿品种和数量(250 mL容量瓶1个,100 mL容量瓶7个,10 mL吸量管1支,5 mL,10 mL,25 mL,100 mL量筒各1个,100 mL烧杯3个),精密移取一定体积的储备液到250 mL容量瓶,加水定容至刻度进行稀释,制成铁离子标准中间液,继续精密移取不同体积的该中间液至7个100 mL容量瓶中(分别移取0.00 mL,1.00 mL,2.00 mL,4.00 mL,6.00 mL,8.00 mL,10.00 mL于100 mL容量瓶中,加入缓冲液和显色剂后定容至刻度),制成铁离子系列标准溶液。注意事项:1) 在稀释过程中,铁离子质量浓度和体积的倍数要易于理解和计算,并且尽可能便于操作;2) 至少有3个浓度点的吸光度在0.2~0.8,方能保证标准曲线是合理的,不会被扣除分值[5-6];3) 铁离子标准中间液浓度应≤80.000 mg·L-1(磺基水杨酸法)或≤45.000 mg·L-1(1,10-菲啰啉法),否则标准曲线上最高浓度点的吸光度将远超最适工作范围(0.2~0.8),使分析误差增大,不会得到满意的结果。
经过十余年的发展,职业技能大赛已是职业院校教育教学活动的一种重要形式和有效延伸,成为检验和展示各大院校办学成果的一项盛事。与此同时,比赛还受到了各级政府、行业协会和用人单位的广泛关注[7-8]。为了争取难得的荣誉,选手之间的比拼越发激烈。因此,在备赛期间模拟设计铁离子标准储备液的稀释方案,反复训练并熟练掌握显得至关重要,这样有助于提升临场应变能力,保持良好的心态。笔者的铁离子标准储备液稀释训练方案如表3所示。

表3 不同浓度铁离子标准储备液稀释方案
2.3 待测溶液配制
比赛测定的未知铁试样已标明浓度范围(2022年江苏省职业院校技能大赛铁试样的浓度范围为1 600~2 000 mg·L-1),要求选手根据已知浓度的铁离子标准储备液,依托赛场给定的紫外设备和玻璃器皿条件(100 mL容量瓶7个,10 mL吸量管1支,5 mL,10 mL,25 mL,100 mL量筒各1个,100 mL烧杯3个),测定出铁试样的准确浓度。依照朗伯—比尔(Lambert-Beer)定律,当样品的吸光度等于0.434时,测量误差最小,此时的样品浓度可视为最佳点[9]。因此,选手应根据赛场给定的未知铁试样的浓度范围,结合现场提供的容量瓶、吸量管的具体规格和数量,设计出合理且便于操作的未知铁试样的配制方案,同时使待测溶液的浓度尽量接近最佳点。
由于未知铁试样和待测溶液之间的浓度相差悬殊,宜使用二步稀释法进行稀释。笔者以2022年江苏省职业院校技能大赛铁试样为例,详述其配制方案。该铁试样的浓度范围为1 600~2 000 mg·L-1,取中间值1 800 mg·L-1为估算浓度。在实际操作中,标准曲线上编号5的浓度点(在笔者实验部分中为4.800 mg·L-1或2.400 mg·L-1),可作为待测溶液铁离子的参考浓度。二步稀释过程见表4。

表4 未知铁试样待测溶液配制方案
2.4 溶液显色时间
文献报道磺基水杨酸分光光度法的显色时间有10 min[10],20 min[11],1,10-菲啰啉分光光度法的显色时间有10 min[12],20 min[13],60 min[14],显色反应的充分和产物的稳定是影响测定准确度的主要因素[5],因此有必要对这2种分光光度法的显色时间进行考察。方法如下:1) 磺基水杨酸分光光度法。移取6 mL铁离子标准中间液A于100 mL容量瓶中,依次加入5 mL磺基水杨酸溶液和20 mL氨-氯化铵缓冲液,用水稀释至刻度;2) 1,10-菲啰啉分光光度法。移取6 mL铁离子标准中间液B于100 mL容量瓶中,加入2 mL抗坏血酸溶液,摇匀后再依次加入20 mL乙酸-乙酸钠缓冲液和10 mL 1,10-菲啰啉溶液,用水稀释至刻度。配制完毕的2种溶液依次放置5 min,10 min,15 min,20 min,25 min,30 min,40 min,50 min,60 min,然后分别在波长420 nm和510 nm处,以空白溶液为参比溶液,测定其吸光度。如图1所示,吸光度随显色时间的延长而增大,当显色时间到达10 min后,吸光度已达稳定状态,不再变化,表明显色反应已经快速完成,且至少在60 min内保持不变。

图1 显色时间对吸光度的影响
3 结束语
在化学实验技术大赛中,还有很多其他因素会对紫外—可见分光光度法的测定结果带来影响,例如人员的操作,仪器设备、试剂纯度、环境条件等。所以我们要注重应用各种有效措施,减少各类因素造成的影响,提高测定结果的准确性,进而在比赛中获胜。
