铜锌沉淀洗涤对甲醇合成催化剂性能的影响
2023-01-09叶晓东邱祥海
叶晓东,于 杨,邱祥海,刘 明
(中国石化 南京化学工业有限公司,江苏 南京 210048)
甲醇是重要的碳一化工原料和能源载体,截 至2021年底,我国甲醇产能已达到96.90 Mt/a。甲醇作为能源载体,是氢碳比最高的低温液态船用燃料,随着我国氢能技术的发展,甲醇市场的需求必将持续扩大[1]。甲醇装置大型化要求甲醇合成技术不断迭代升级,催化剂是合成技术的关键[2]。目前,工业上甲醇合成采用的催化剂是铜基催化剂,它具有较高的甲醇合成活性、成熟的合成工艺以及廉价的原材料。对甲醇合成铜基催化剂的研究主要围绕组成的调变,包括助剂[3-5]和载体[6-8],以及合成方法的探索[8-10]和催化机理的研究[11-12]。研究者对传统工业甲醇合成催化剂Cu/ZnO/Al2O3的合成工艺进行了深入的研究[13-14],该催化剂的合成主要采用共沉淀法,一般以碳酸钠为沉淀剂。合成过程中铜锌二元沉淀的原位老化是关键步骤,老化过程伴随着溶液颜色的变化。铜锌二元沉淀中锌孔雀石相的形成和富集有利于增强催化剂中Cu和ZnO的相互作用,能够提高催化剂的甲醇合成性能[10]。老化过程中pH和沉淀粒径分布均发生变化,温度越高老化变色点的pH越低,在80℃下老化变色点的pH约为7.5[15]。工业铜基甲醇合成催化剂的合成工艺还包括对前体的洗涤,目的是尽可能降低前体中钠的含量,抑制催化剂的烧结失活[16-17],用于洗涤催化剂前体的去离子水的pH一般低于7.0,这主要是由于去离子水与空气接触后溶解了酸性气体CO2。洗涤过程对催化剂前体组成、催化剂结构和催化性能的影响鲜有文献报道。
本工作采用分步沉淀法合成了Cu/ZnO/Al2O3催化剂,以易热解的碳酸铵溶液作为洗涤铜锌沉淀的去离子水的pH调节剂,考察了去离子水pH、洗涤次数、碱性调节剂对铜锌沉淀的影响,进一步研究了铜锌沉淀的洗涤对Cu/ZnO/Al2O3催化剂性能的影响,并分析了催化剂的构效关系。
1 实验部分
1.1 试剂与仪器
Cu(NO3)2·3H2O、Zn(NO3)2·6H2O、Al(NO3)3·9H2O、Na2CO3、25%(w)氨水、碳酸铵:分析纯,国药集团化学试剂有限公司;高纯去离子水:自制。
90 Plus型超声波粒度分析仪:Brook Haven公司;BSWHGHY-5型水处理设备:无锡市蓝天水处理设备有限公司,管径50 mm,工作压力不高于1.0 MPa;LE438型pH计:Mettler Toledo公司;IRIS Advantage(HR)型电感耦合等离子体原子发射光谱仪:Thermo公司。
1.2 催化剂的合成
采用分步沉淀法合成催化剂。配制2 L含铜离子60 g/L、锌离子15 g/L的铜锌混合硝酸盐溶液,用1 mol/L的Na2CO3溶液作为沉淀剂,在65℃下将混合硝酸盐溶液以200 mL/min的流速和沉淀剂并流加入到含500 mL去离子水的中和桶中,在剧烈搅拌下进行中和反应,控制中和过程的pH为7.0~7.2,终点pH为7.2。中和反应结束后原位搅拌老化1 h,溶液的颜色逐渐由蓝色转变为翠绿色,然后过滤得到二元样滤饼。将滤饼平均分成4份,在65 ℃下分别用pH=6.5,7.0,7.2,7.5的4种去离子水(其中,pH=6.5的去离子水是原去离子水,其他3种是向原去离子水中滴加0.2 mol/L的碳酸铵溶液调节而成)洗涤滤饼,每次洗涤用水量为1.5 L,搅拌5 min,然后离心分离,每个试样洗涤7次,洗涤后得到的4种滤饼分别命名为P1,P2,P3,P4。
在常温下将10%(w)的氨水滴加到1 L质量浓度为10 g/L的Al(NO3)3溶液中,并剧烈搅拌直到pH=7.0,然后过滤得到载体滤饼,用pH=7.0的去离子水洗涤除去载体滤饼中残留的NH4+。将载体滤饼平均分成4份,分别与P1~P4滤饼分散在800 mL、65 ℃、pH=7.0的去离子水中,剧烈搅拌10 min后过滤,4种滤饼于100 ℃下干燥4 h,350℃下空气气氛中焙烧2 h,然后添加2%(w)的石墨作为成型助剂,压片成型后破碎至20~40目制得催化剂,依次命名为PC1,PC2,PC3,PC4。
1.3 催化剂的表征
采用Bruker公司AXS D8 Focus型粉末X射线衍射仪进行XRD表征,CuKα射线源(λ=0.154 06 nm),管电压和管电流分别为40 kV和40 mA,扫描速率为 6 (°)/min,扫描范围 10°<2θ<80°。采用Scherrer公式计算试样的平均晶粒。
采用N2O化学吸附法[18]测定Cu的比表面积,在天津市鹏翔科技有限公司PX200型催化剂化学吸附仪上进行。称取200 mg 20~40目催化剂加入到石英管微型反应器中,在50 mL/min的He气中于350 ℃下吹扫1 h,降至室温;将气体切换成50 mL/min的5%(φ)H2/He,吹扫稳定后,以10℃/min的速率升温至350 ℃并维持1 h,然后在50 mL/min的He气流中降温至60 ℃并达到稳定,待基线走平后,将事先校正好流量(1.5 mL/min)的2%(φ)N2O/He气阀打开,并使用质谱仪记录N2和N2O的信号值。假设Cu原子的密度为1.46×1019m-2,每个Cu原子的截面积则为1/(1.46×1019)=6.85×10-20m2, 根 据 2Cu+N2O=Cu2O+N2计 算 Cu的比表面积。
采用 Quantachrome公司NOVA 4200e型比表面积及孔径分析仪进行N2吸附-脱附表征。采用BET方法计算比表面积,BJH法(脱附支)计算孔径分布。
采用Thermo Scientific公司ESCALAB 250型X射线光电子能谱仪进行XPS表征,以单色AlKα(1 486.6 eV)为激发光源,试样压片后经抽真空处理(真空度高于5×10-8Pa),室温下采集谱图,以表面污染碳C 1s284.6 eV为内标校正试样表面的电荷效应。
1.4 催化性能评价
催化剂性能评价在不锈钢固定床反应器(长540 mm,内径11 mm)上进行。称取2 mL 20~40目催化剂装于反应器中,用5(φ)H2/N2混合气对催化剂进行原位常压还原,还原终温为230 ℃,然后切换为组成为V(CO)∶V(CO2)∶V(H2)∶V(N2)=20∶5∶60∶15的原料气,气时空速为10 000 h-1;升压至5 MPa,反应稳定2 h后,放空收集器中的液体并开始计时,每2 h取样一次,进行称重和色谱分析,以3次的平均值作为甲醇时空收率,计为耐热前的甲醇时空收率。继续升温至400 ℃并维持5 h,再恢复至230 ℃,稳定2 h后放空液体收集器并开始计时,重复上述取样分析、计算步骤,所得结果为耐热后的甲醇时空收率。收集液体,采用Agilent公司GC7890A型气相色谱仪进行离线分析,分析条件:SE-54型毛细管柱(25 m×0.32 mm×1 μm);FID检测,检测器温度220 ℃;进样器温度220 ℃;程序升温,100 ℃维持1 min后,以5 ℃/min的速率升至120 ℃。采用归一化法定量。
2 结果与讨论
2.1 铜锌沉淀粒径的变化
考察了用不同pH的去离子水洗涤铜锌沉淀的过程中,铜锌沉淀粒径的变化,结果见图1。从图1可看出,当去离子水pH≥7.0时,铜锌沉淀的平均粒径随洗涤次数的增加稍有波动,但总体变化不大;但采用pH=6.5的去离子水洗涤沉淀时,随着洗涤次数的增加,铜锌沉淀平均粒径逐渐减小,减小过程大致可以分为缓慢、快速和缓慢三个阶段。这可以解释为,由于铜锌沉淀的终点pH=7.2,碱性沉淀剂过量,洗涤初期,滤饼中夹杂或吸附的沉淀剂逐渐释放出来,尽管去离子水pH显酸性,但洗涤液pH仍偏碱性。随着洗涤的进行,沉淀剂逐渐被洗脱,洗涤液pH与去离子水pH逐渐接近,在酸性环境下,铜锌沉淀粒径由于酸解而迅速减小。当洗涤液pH等于去离子水pH时,洗涤过程中酸解与沉淀逐渐达到平衡,整体表现为粒径减小趋势变缓。
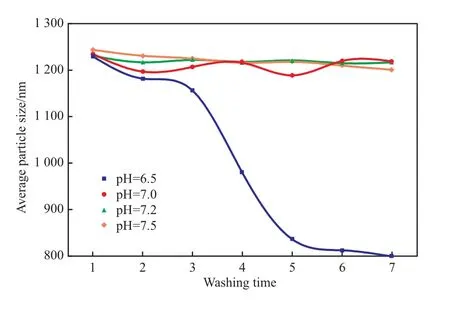
图1 铜锌沉淀粒径随洗涤次数的变化Fig.1 Change of particle size of Cu-Zn precipitate with washing times.
2.2 滤液中离子浓度的变化
为了考察洗脱效果,测定了洗涤后滤液中的离子浓度,结果见表1。由表1可见,初始洗涤滤液中Na+含量非常高,约为3 000 mg/L;随着洗涤的进行,Na+含量迅速下降,洗涤5次后,Na+含量保持在10 mg/L以内。同时,滤液中还有微量的Cu2+和Zn2+。当采用pH=6.5的去离子水洗涤时,随着洗涤的进行,滤液中Cu2+和Zn2+含量逐渐升高,这主要归因于酸解引起的催化剂有效组分流失,与图1结果一致。当采用pH=7.0或7.2的去离子水洗涤时,滤液中Cu2+和Zn2+含量分别在1.26~1.33 mg/L和1.16~1.22 mg/L范围内波动,没有呈现上升趋势。然而,采用pH=7.5的去离子水洗涤时,Cu2+和Zn2+含量也呈逐渐升高的趋势,这主要与调节去离子水pH时加入的碳酸铵溶液有关,由于碳酸铵的双水解,随着碳酸铵溶液加入量的提高,溶液中NH3浓度逐渐增大,导致少量的Cu2+和Zn2+形成了氨络合离子而溶解在滤液中。
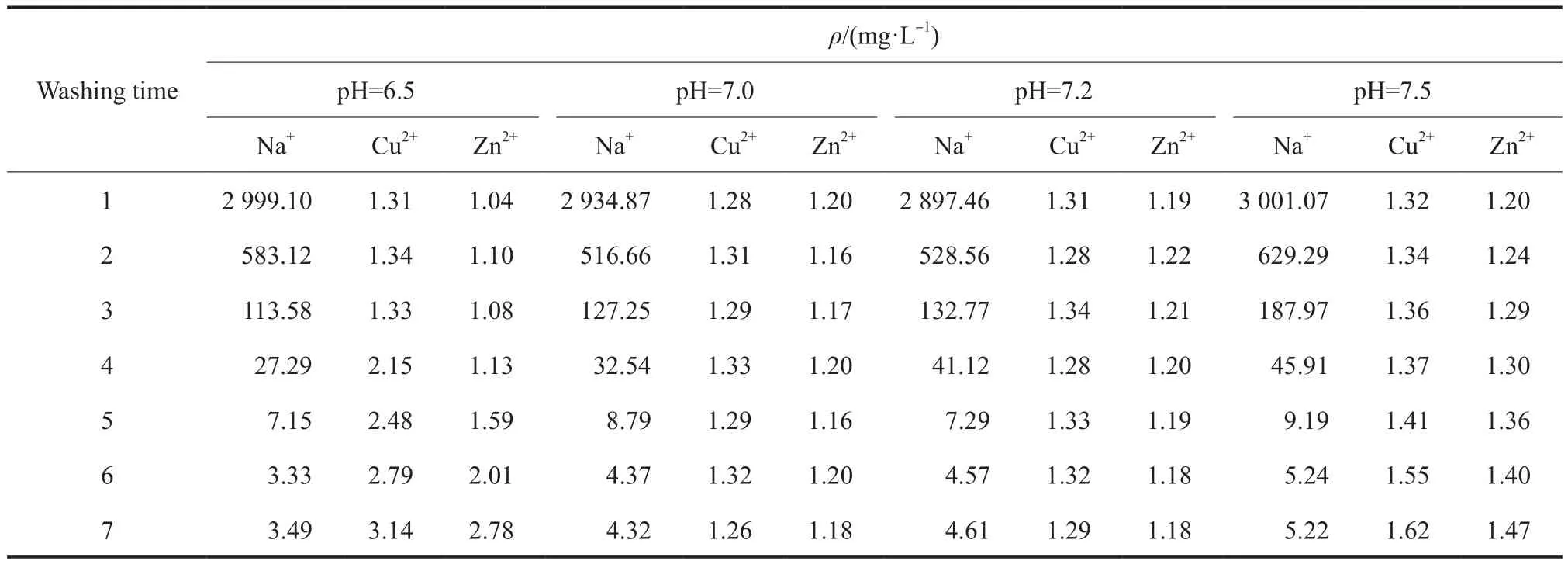
表1 铜锌沉淀洗涤滤液中离子含量随洗涤次数的变化Table 1 Change of ion content in the filtrate of washing Cu-Zn precipitate with washing times
2.3 XRD表征结果
对用不同pH去离子水洗涤得到的铜锌沉淀以及焙烧后的催化剂进行XRD表征,结果见图2和3。图2中的P1-1表示用pH=6.5的去离子水洗涤1次后的铜锌沉淀,P1-2表示用pH=6.5的去离子水洗涤2次后的沉淀,以此类推。根据1.2节可知, P1为洗涤7次后的铜锌沉淀。

图2 铜锌沉淀的XRD谱图Fig.2 XRD patterns of the Cu-Zn precipitates.
由图2可知,铜锌沉淀主要由锌孔雀石相、孔雀石相和绿铜锌矿组成,其中,锌孔雀石相占比较大[11]。研究结果表明,锌孔雀石相热解后能够形成活性前体Cu-Zn-O固溶体[19-21]。基于铜锌沉淀中锌孔雀石相对甲醇合成催化剂的重要性,针对锌孔雀石相在2θ=14.8°,17.5°,24.2°处的三个主要衍射峰,采用Scherrer公式计算晶粒尺寸,取三个结果的算数平均值作为锌孔雀石相的晶粒尺寸,结果见表2。从表2可看出,当洗涤用去离子水的pH≥7.0时,洗涤7次后,锌孔雀石相晶粒尺寸在18.4~18.8 nm范围内。当采用pH=6.5的去离子水洗涤时,随着洗涤的进行,锌孔雀石相晶粒尺寸逐渐减小,这主要归因于酸性去离子水洗涤引起的锌孔雀石相酸解,这也是导致滤液中Cu2+和Zn2+含量增大的原因。
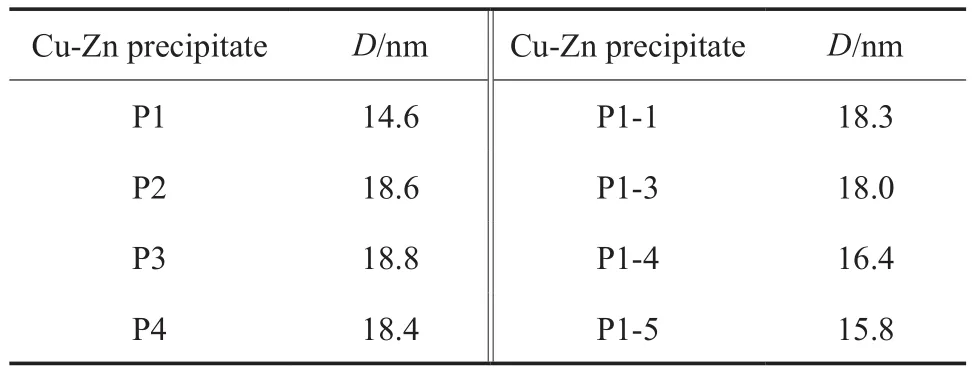
表2 不同铜锌沉淀中锌孔雀石相的晶粒尺寸Table 2 Crystallite sizes of Rosasite phase(D) in the different Cu-Zn precipitates
由图3可见,4种催化剂的XRD谱图上都出现了CuO、ZnO和成型助剂石墨的特征衍射峰,通过Scherrer公式计算得到4种催化剂中CuO的晶粒尺寸介于7.7~7.9 nm之间。在所有XRD谱图中均未发现Al2O3的特征衍射峰,表明Al2O3以无定形或高度分散状态存在[11]。XRD表征结果显示,不同pH去离子水洗涤的铜锌沉淀对催化剂的晶相组成和活性相晶粒尺寸影响不大。
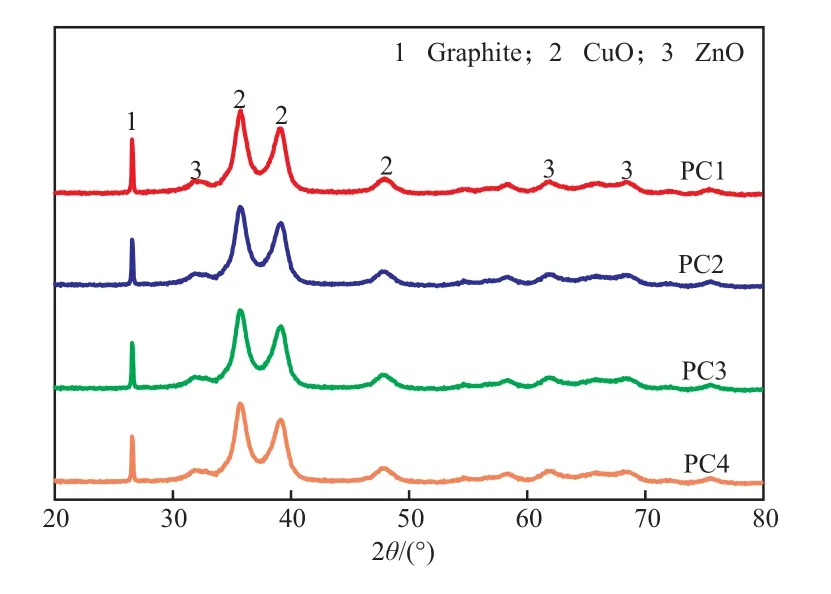
图3 焙烧后催化剂的XRD谱图Fig.3 XRD patterns of the calcined catalysts.
2.4 XPS表征结果
焙烧后和还原后催化剂的XPS谱图见图4和图5。从图4可看出,933.0 eV附近的峰对应Cu 2p3/2,954.0 eV附近的峰对应Cu 2p1/2,二者均为Cu2+的特征峰[22-23],942.5 eV附近的峰是Cu2+的卫星峰,说明焙烧后的4种催化剂中Cu均以Cu2+形式存在。与焙烧后的催化剂相比,经过还原后,4种催化剂表面Cu 2p3/2的电子结合能均不同程度地降低,且卫星峰消失。这表明还原后,催化剂中Cu以还原态Cu0或Cu+的形式存在。为了进一步揭示还原态催化剂中Cu的存在形式,对还原后的PC1催化剂进行了俄歇动能表征,结果如图6所示。经测定,还原后的PC1催化剂的Cu LMM动能为918.6 eV,而Cu0和Cu+的Cu LMM动能分别为918.6 eV和917.4 eV[24-25]。因此,确定还原态PC1催化剂表面的Cu主要以Cu0形式存在。
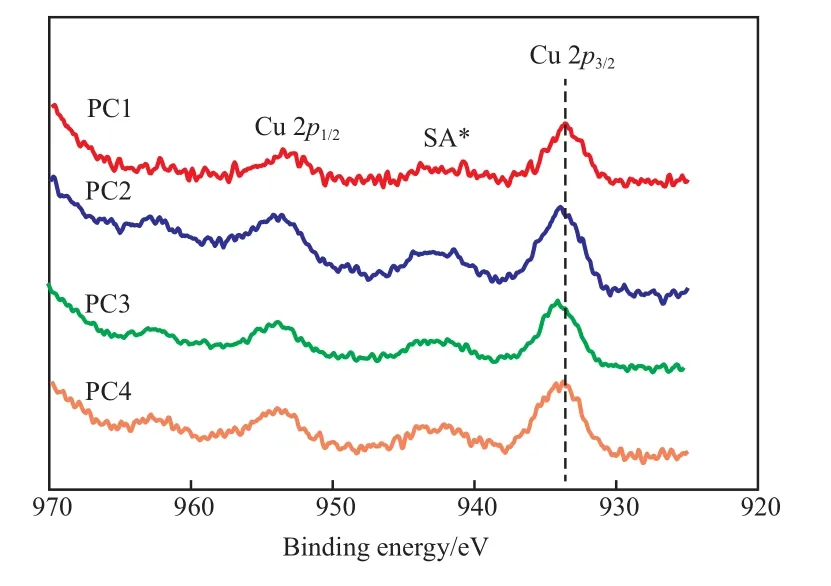
图4 焙烧后催化剂的XPS谱图Fig.4 Cu 2p XPS spectra of the calcined catalysts.SA*:satellite peak.

图5 还原后催化剂的XPS谱图Fig.5 Cu 2p XPS spectra of the reduced catalysts.
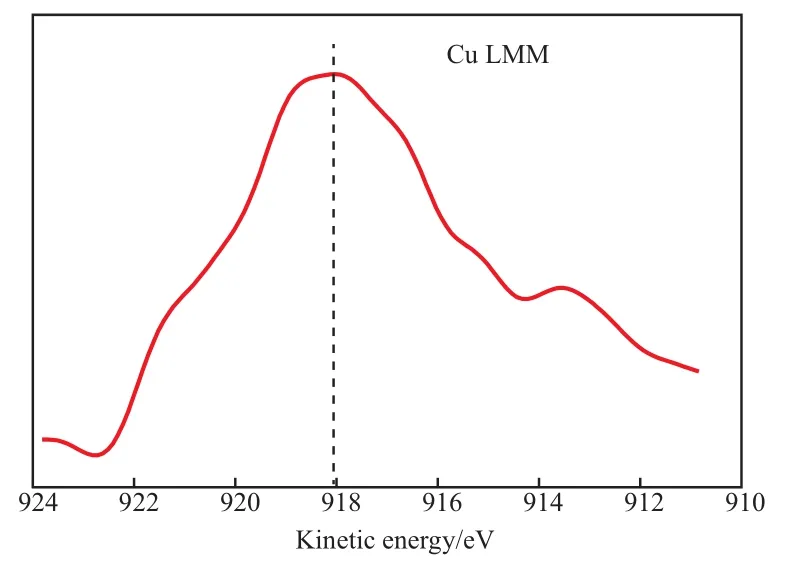
图6 还原后PC1催化剂的Cu LMM俄歇动能谱图Fig.6 Kinetic energy spectrum of Auger at Cu LMM of the reduced PC1 catalyst.
对焙烧后和还原后催化剂表面的Cu 2p3/2电子结合能进行了比较,结果见表3。由表3可见,用pH=6.5的去离子水洗涤铜锌沉淀制得的PC1催化剂,焙烧后和还原后催化剂表面的Cu 2p3/2电子结合能都最低,随着洗涤用去离子pH的升高,焙烧后和还原后催化剂的Cu 2p3/2电子结合能总体呈现升高的趋势,但当pH从7.2升至7.5时,电子结合能反而降低。PC1和PC4两种催化剂在焙烧后以及还原后呈现出较低的Cu 2p3/2电子结合能,可能与洗涤铜锌沉淀过程中Cu2+的酸解和氨络合离子的形成有关。
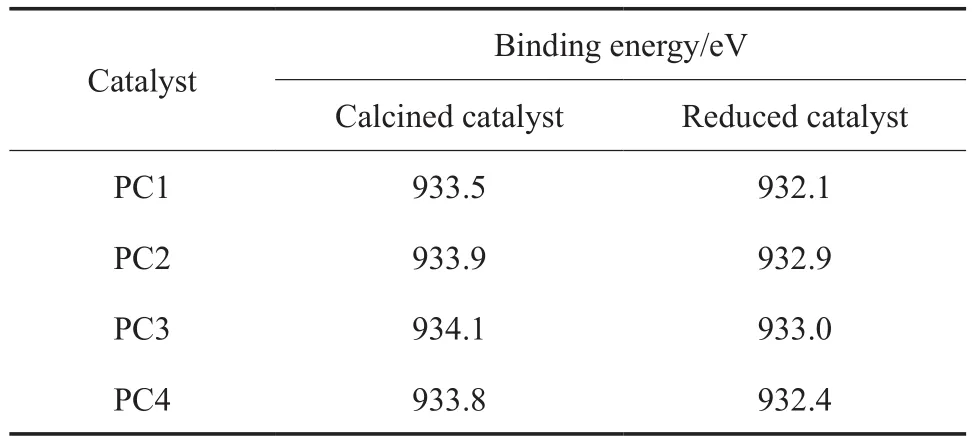
表3 不同催化剂表面Cu 2p3/2的电子结合能Table 3 Binding energy of Cu 2p3/2 on the surface of different catalysts
2.5 Na含量和比表面积分析
催化剂本体Na含量、比表面积和活性Cu比表面积见表4。由表4可见,4种催化剂的本体Na含量介于0.39~0.42 mg/g范围内,小于0.50 mg/g,Na含量符合甲醇合成催化剂对杂质的要求[16]。4种催化剂的比表面积相差不大,介于93.9~96.2 m2/g范围内。然而,4种催化剂还原后的活性Cu比表面积相差较大,从大到小依次为PC3>PC2>PC4>PC1。导致活性Cu比表面积差异的原因与洗涤过程发生的酸解及氨络合离子的形成有关。

表4 催化剂本体Na含量、比表面积和活性Cu比表面积Table 4 Na content,specific surface area and Cu specific surface area of the catalysts
2.6 甲醇合成催化性能分析
催化剂的甲醇合成催化性能见表5。从表5可看出,耐热前,PC3催化剂的总碳转化率和甲醇时空收率最大,分别为42.5%和1.48 g/(mL·h);PC1催化剂最小,分别为39.9%和1.38 g/(mL·h);催化剂活性从高到低依次是PC3>PC2>PC4>PC1;4种催化剂对甲醇的选择性相差不大,介于97.0%~97.6%。耐热后,4种催化剂的甲醇时空收率的大小顺序没变,但差距进一步扩大。当以耐热后甲醇时空收率与耐热前甲醇时空收率的百分比作为衡量催化剂热稳定性的指标时,4种催化剂中热稳定性最好的是PC3催化剂,比值为93.2%,稳定性最差的是PC1催化剂,比值为84.8%,热稳定性从高到低的顺序与催化剂活性顺序一致。
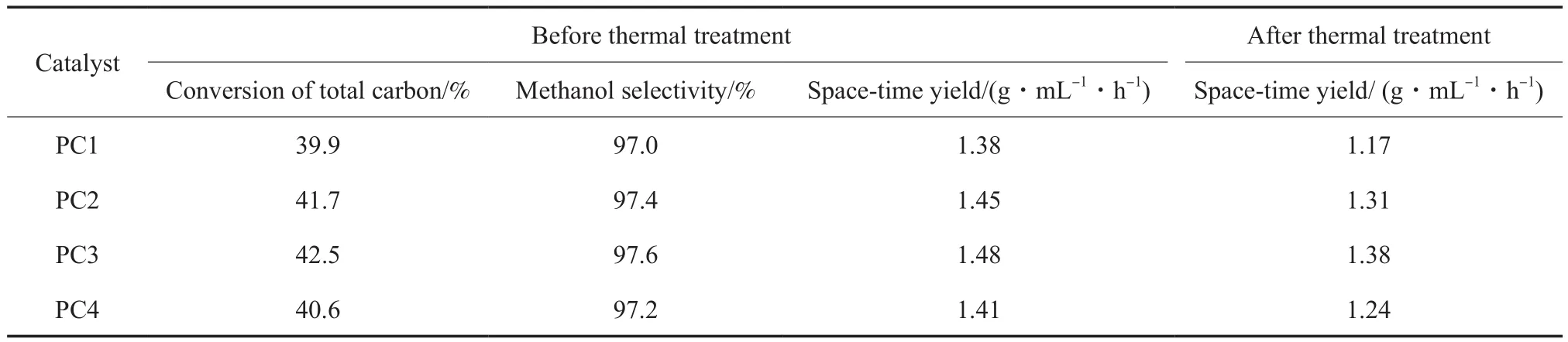
表5 催化剂的甲醇合成催化性能Table 5 Catalytic performance of methanol synthesis over catalysts
Farahani等[14]认为,Cu/ZnO甲醇合成催化剂上甲醇时空收率与还原态催化剂的活性Cu比表面积呈正相关。此外,郝爱香等[26]的研究结果表明,甲醇合成催化剂表面金属Cu的电子结合能越高,越有利于反应物CO的吸附与活化,对提高铜基甲醇合成催化剂的性能有利。结合催化剂的表征结果可知,当使用碳酸铵为pH调节剂时,洗涤铜锌沉淀的去离子水pH偏低或偏高都会导致铜锌沉淀粒径减小,分别发生酸溶或氨络合物碱溶,进而造成还原态催化剂金属Cu的比表面积和表面金属Cu的电子结合能降低,最终导致催化剂在甲醇合成反应中的活性和热稳定性下降。
3 结论
1)用pH=6.5的去离子水洗涤铜锌沉淀时,在洗脱Na+的同时会导致沉淀较快地溶解,引起活性组分流失,导致沉淀粒径逐渐减小,给固液分离带来一定的困难;同时,还会促使铜锌沉淀中的活性相锌孔雀石晶粒尺寸减小,进而引起催化剂表面Cu0的电子结合能降低,活性Cu比表面积减小。
2)当滴加碳酸铵溶液提高去离子水pH时,能够明显抑制洗涤过程中活性组分的流失、铜锌沉淀粒径的减小和锌孔雀石相晶粒尺寸的减小,从而保障催化剂表面Cu0具有较高的电子结合能和活性Cu比表面积。但当pH=7.5时,由于较高浓度的碳酸铵会引起双水解,生成的NH3易与Cu2+和Zn2+形成氨络合离子,引起铜锌沉淀溶解。
3)在甲醇合成反应中,PC3催化剂的活性和热稳定性较好,PC1催化剂最差,这主要归因于前者具有较高的表面Cu0电子结合能和活性Cu比表面积。
猜你喜欢
——非均布滤饼的局部比阻与平均比阻的测定与计算方法
