新疆紫草、黄花软紫草HPLC指纹图谱建立及化学模式识别分析
2022-12-04丁文欢张雪佳樊思恩徐海燕
丁文欢, 李 洁, 张雪佳, 樊思恩, 徐海燕*
(1.新疆医科大学中心实验室,新疆 乌鲁木齐 830054;2.新疆医科大学第一附属医院药学部,新疆 乌鲁木齐 830054;3.中国药科大学中药学院,江苏 南京 211198;4.新疆医科大学中医学院,新疆 乌鲁木齐 830054)
紫草被誉为“凉血之圣药”,活性成分为紫草素及其衍生物,有抗炎、抗菌、抗病毒等作用[1-7],为紫草科植物新疆紫草Arnebiaeuchroma(Royle)Johnst.、内蒙紫草ArnebiaguttataBunge的干燥根[8],其中后者即《中国植物志》记载的黄花软紫草[9]。紫草中萘醌类成分含量差异较大,导致药材品质参差不齐[10-12],有学者建立了新疆紫草指纹图谱[13-16],但其所用药材大多源于市售,会存在基源不清的可能,而且未与黄花软紫草进行比较。
课题组前期对野外采集的新疆紫草、黄花软紫草中萘醌类成分进行含量测定[17-19],发现存在较大差异,并且不同产地同一药材亦然。本实验建立新疆紫草、黄花软紫草HPLC指纹图谱,并进行化学模式识别分析,以期为两者质量综合评价标准提供科学依据。
1 材料
MS105DU型电子天平(十万分之一,瑞士梅特勒-托利多公司);KQ5200DE型数控超声波清洗器(昆山市超声仪器有限公司);Agilent 1260高效液相色谱仪(美国Agilent公司)。β,β′-二甲基丙烯酰紫草素(批号15102821)、左旋紫草素(批号15102721)、去氧紫草素(批号15062422)、乙酰紫草素对照品(批号15120431)均由上海同田生物技术有限公司提供;β-乙酰氧基异戊酰紫草素对照品(批号P05M7F14235)由上海源叶生物技术有限公司提供;异丁酰紫草素对照品(批号wkq16101302)由四川省维克奇生物科技有限公司提供;(2-甲基正丁酰基)紫草素对照品(批号AV51-LDQR)由日本化成工业株式会社提供。新疆紫草、黄花软紫草采自新疆,经新疆医科大学中药资源教研室徐海燕教授鉴定为正品,具体信息见表1。乙腈、甲酸为色谱纯;石油醚(60~90 ℃)为分析纯;水为超纯水(由艾科超纯水机制备)。
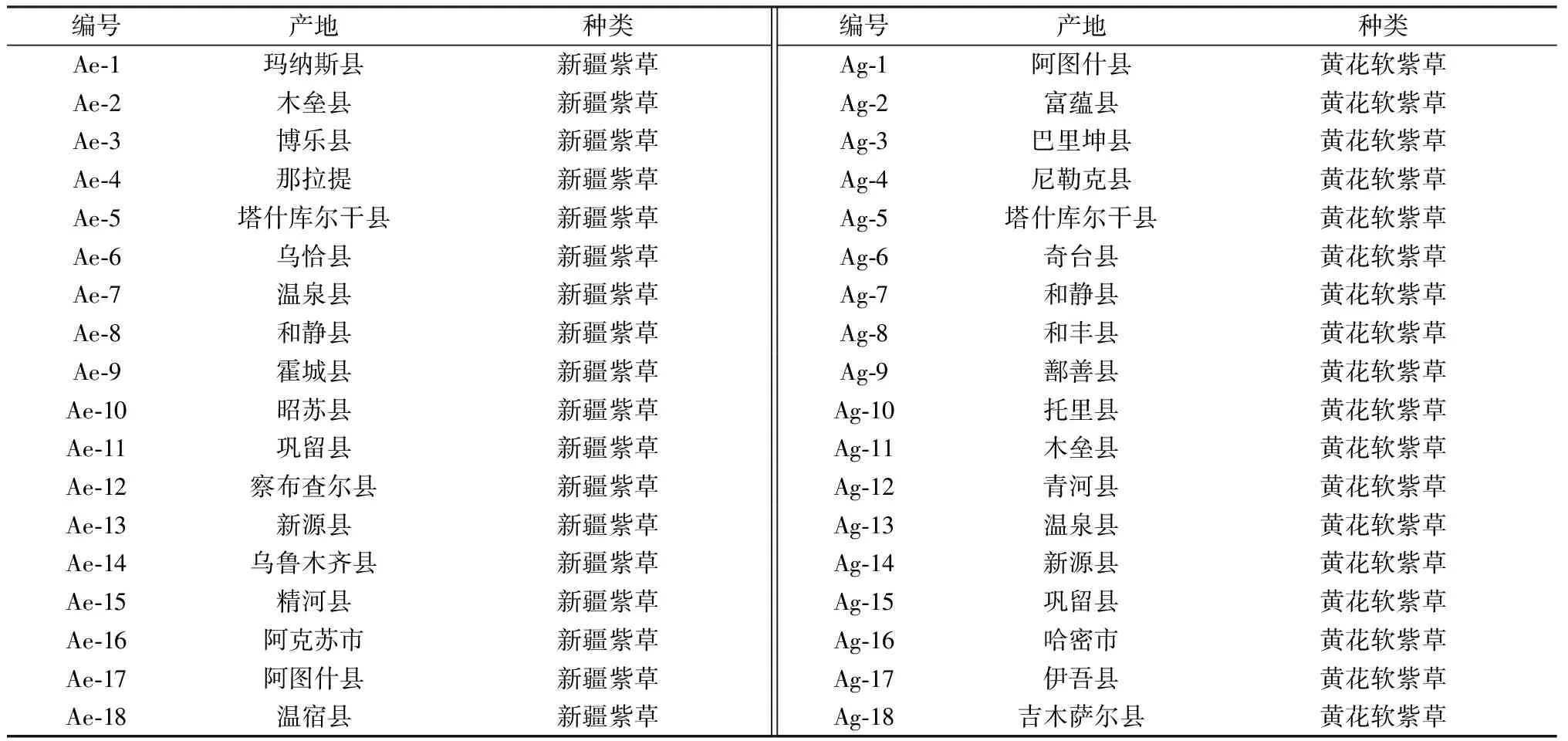
表1 样品信息
2 方法
2.1 对照品溶液制备 分别精密称取左旋紫草素、乙酰紫草素、β-乙酰氧基异戊酰阿卡宁、去氧紫草素、异丁酰紫草素、β,β′-二甲基丙烯酰阿卡宁、(2-甲基正丁酰基)紫草素对照品2、10、10、1、10、5、25 mg,置于25 mL量瓶中,乙腈定容至刻度,即得。取除(2-甲基正丁酰基)紫草素以外的6种对照品溶液适量,置于同一10 mL量瓶中混合;另取(2-甲基正丁酰基)紫草素对照品溶液3.5 mL,置于10 mL量瓶中。
2.2 供试品溶液制备 药材粉碎后过4号筛,取粉末约1.0 g,精密称定,置于锥形瓶中,加入石油醚(60~90 ℃)50 mL,超声处理30 min,冷却,石油醚(60~90 ℃)补足减失的质量,滤过,量取续滤液(新疆紫草10 mL、黄花软紫草30 mL),蒸干,残渣加乙腈溶解,转移至10 mL量瓶中,乙腈定容至刻度,摇匀,即得。
2.3 色谱条件 参考文献[17]报道,Agilent-C18色谱柱(250 mm×4.6 mm,5 μm);流动相乙腈-0.05%甲酸(70∶30);体积流量1 mL/min;柱温30 ℃;检测波长275 nm;进样量10 μL。
2.4 方法学考察
2.4.1 精密度试验 取新疆紫草供试品溶液适量,在“2.3”项色谱条件下进样测定6次,测得左旋紫草素、乙酰紫草素、β-乙酰氧基异戊酰阿卡宁、去氧紫草素、异丁酰紫草素、β,β′-二甲基丙烯酰阿卡宁、(2-甲基正丁酰基)紫草素峰面积RSD分别为0.35%、0.22%、0.53%、1.70%、0.28%、0.45%、0.24%,表明仪器精密度良好。
2.4.2 稳定性试验 取新疆紫草供试品溶液适量,于0、2、4、6、8、10、12、24 h 在“2.3”项色谱条件下进样测定,测得左旋紫草素、乙酰紫草素、β-乙酰氧基异戊酰阿卡宁、去氧紫草素、异丁酰紫草素、β,β′-二甲基丙烯酰阿卡宁、(2-甲基正丁酰基)紫草素峰面积RSD分别为1.52%、0.45%、1.27%、1.84%、0.70%、1.12%、0.48%,表明溶液在24 h内稳定性良好。
2.4.3 重复性试验 精密称取新疆紫草粉末6份,按“2.2”项下方法制备供试品溶液,在“2.3”项色谱条件下进样测定,测得左旋紫草素、乙酰紫草素、β-乙酰氧基异戊酰阿卡宁、去氧紫草素、异丁酰紫草素、β,β′-二甲基丙烯酰阿卡宁、(2-甲基正丁酰基)紫草素含量RSD分别为1.67%、1.99%、1.84%、1.02%、2.05%、1.92%、2.07%,表明该方法重复性良好。
2.5 HPLC指纹图谱建立
2.5.1 共有峰确认 36批样品按“2.2”项下方法制备供试品溶液,在“2.3”项色谱条件下进样测定,将所得色谱图导入“中药色谱指纹图谱相似度评价系统”(2012A版)进行峰匹配,见图1~2,共发现19个色谱峰,其中共有峰5个,即F-10、F-11、F-14、F-18、F-19;18批新疆紫草共有7个共有峰,即F-6、F-10、F-11、F-14、F-16、F-18、F-19;18批黄花软紫草有6个共有峰,即F-10、F-11、F-12、F-14、F-18、F-19,由于各批样品均含有2-甲基正丁酰基,而且含量高,分离效果好,故选择其作为参照,测得相对保留时间RSD为0~0.79%,相对峰面积RSD为0~96.41%。
2.5.2 相似度分析 采用《中药色谱指纹图谱相似度评价系统(2012A版)》进行相似度评价,结果见表2。由此可知,新疆紫草除Ae-5、Ae-6相似度低于0.7外,其余16批均高于0.9;黄花软紫草除Ag-9、Ag-13相似度低于0.8外,其余16批均高于0.8;黄花软紫草、新疆紫草之间的相似度降低。
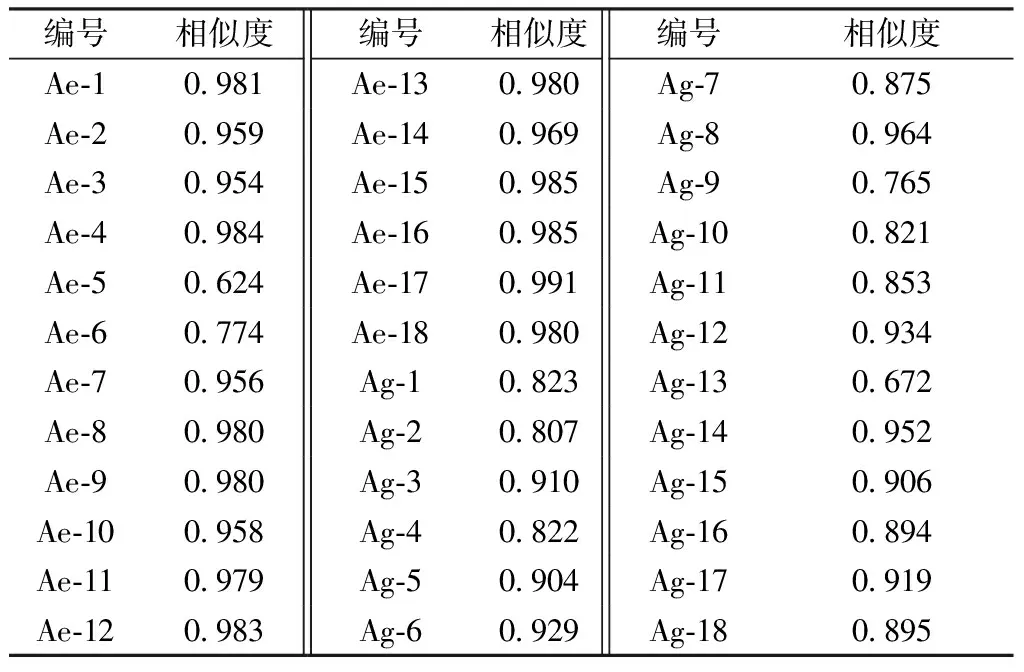
表2 36批样品相似度
2.6 聚类分析 将19个色谱峰峰面积导入Mataboanalyst进行聚类分析,结果见图3。由此可知,距离设定为15时,36批样品可聚为2类,2个品种之间有交叉现象,F-6、F-11、F-13、F-16、F-18、F-19在第1类样品中较低,而在第2类样品中较高;距离设定为10时,36批样品可分为4类,2个品种之间无交叉现象,其中第1类又可分为Ⅰ类(Ae-2、Ae-3、Ae-5、Ae-6、Ae-14、Ae-16、Ae-18)和Ⅱ类(Ag-2、Ag-3、Ag-4、Ag-6、Ag-7、Ag-8、Ag-10、Ag-11、Ag-12、Ag-13、Ag-14、Ag-15、Ag-16、Ag-17),F-6、F-11、F-13、F-16、F-18、F-19在Ⅰ类样品中峰面积较低,而在Ⅱ类样品中几乎未出现,并且Ⅱ类样品中F-12峰面积较大,但Ⅰ类样品中不含该色谱峰,而第2类又可分为Ⅲ类(剩余11批新疆紫草)、Ⅳ类(剩余4批黄花软紫草),其区别主要是所有色谱峰峰面积在Ⅳ类样品中均较高,而Ⅲ类样品中仅F-6、F-11、F-13、F-16、F-18、F-19峰面积较高,与相似度分析结果基本一致。
2.7 主成分分析(PCA) 图4显示,前2个主成分累积贡献率超过60%,故选择两者进行区分;36批样品分布比较集中,2个品种之间有重叠部分,表明其HPLC指纹图谱相似性较高,但大部分样品分布与种属一致,并且同一品种分布更集中。
2.8 正交偏最小二乘法判别分析(OPLS-DA) 图5显示,解释能力参数R2X为0.945,R2Y为0.791,预测能力参数Q2为0.662,表明数据拟合效果较好,可用于区分2个品种。再提取OPLS-DA模型中19个色谱峰峰面积的变量投影重要性(VIP)值,见图6,可知大于1者有7个,分别为F-16(异丁酰紫草素)、F-18(β,β′-二甲基丙烯酰阿卡宁)、F-6(左旋紫草素)、F-19(2-甲基正丁酰基紫草素)、F-12、F-11(乙酰紫草素)、F-1,可作为差异标志物。
3 讨论
结果显示,新疆紫草、黄花软紫草并非完全按照种属归类,而是均有重合部分,其原因为两者均为软紫草属植物,亲缘关系较近,并且均被2020年版《中国药典》收录,但新疆地域广阔,前者在大多生长于海拔2 000~4 200 m的山地向阳坡、砾石山坡、洪积扇、草地等处,而后者大多分布在前山荒漠、砾石质山坡、戈壁等处,生境差异较大,同一品种不同产地亦然。另外,药材中化学成分的积累除了受生境、种类的影响外,也与生长年限相关,但本实验中的新疆紫草、黄花软紫草均为野外采集,不能确定其生长年限。
野外调查发现,新疆紫草根发达,栓化较明显,色深,特异性气味明显;黄花软紫草主根明显,但不够发达,木栓层较薄,黄白色木部所占比例较大,特异性气味弱,两者性状存在明显差异,导致新疆药农并未采集收购黄花软紫草。因此,要想解决紫草野生资源短缺的问题,就应加大对其人工种植的研究,并制定政策,鼓励新疆紫草人工栽培。
