具有“核壳”结构的乳清分离蛋白-黄原胶复合颗粒的构建
2022-10-31李梦飞李博睿孙梦雅陈存社刘新旗庞志花
李梦飞,李博睿,孙梦雅,陈存社,李 赫,刘新旗,庞志花
(北京工商大学食品与健康学院,北京 100089)
随着生活水平的提高,人们对健康越来越重视,对低脂食品的需求也越来越大,食品行业一直非常关注低脂产品的开发。由于去除脂肪后的食品外观、风味、口感和质地的不良变化,消费者对低脂食品的接受度往往不高。而脂肪替代物是在保证食品的安全性和感官品质的基础上,部分或全部替代脂肪,降低食品的总热量,满足消费者对低脂低热量的健康需求的物质。
可用于替代脂肪的潜在添加剂是基于多糖或蛋白质的脂肪替代品,例如角叉菜胶、黄原胶(xanthan gum,XG)、瓜尔胶、魔芋、改性淀粉、膳食纤维、大豆分离蛋白和乳清分离蛋白(whey protein isolate,WPI)。多糖由于良好的亲水性可以改善食品中水相的结构,将水稳定为凝胶状的三维网状结构,并截留大量水分,被截留的水分具有很好的流动性,进而改善食品的体积、黏度和结构,产生类似脂肪的口感。蛋白质通过微粒化处理,形成纳米或微米级的球形蛋白颗粒,在液体和半固体食品基质中起到“滚珠轴承”的润滑性能,从而产生乳脂状的口感。但蛋白质在高温下结构具有不稳定性、易变性,导致颗粒的尺寸变大,影响其功能特性。而蛋白质与离子型多糖可以通过静电相互作用,复合形成具有“核(蛋白颗粒)-壳(多糖)”结构的高度结构化生物聚集物,这种复合物的形成可以有效控制蛋白质的热聚集。蛋白质/多糖复合物的研究目前备受关注,用于功能成分的递送、乳液的稳定、控制食品的结构、质地和稳定性特征等。高效构建具有良好“核壳”结构的特定尺寸的复合物颗粒是该领域研究的基础。
WPI是乳制品工业中的副产物,由牛乳除去酪蛋白后得到乳清蛋白,再经进一步加工处理得到的,纯度超过90%。WPI具有良好的凝胶特性、乳化性,被广泛应用于食品与药品中。谢彩凤等分析了不同电解质对变性WPI初级团聚体的团聚动力学的影响,发现胶粒稳定性与电解质离子类型和浓度密切相关;舒蒙等通过对WPI和阿拉伯胶(gum arabic,GA)进行热处理,使蛋白在聚集过程中与GA缠绕,形成稳定的WPI/GA复合物颗粒,也改善了WPI/GA分子内复合物的pH值敏感性。
黄原胶(xanthan gum,XG)是一种由黄单胞菌属经有氧发酵产生的细胞外杂多糖,是一种阴离子多糖,其带有负电荷的三糖侧链环绕主链,使分子结构相当牢固,对热、酸和碱都具有非常好的稳定性,并具有良好的水溶性、独特的流变学特性,可作为增稠剂、稳定剂、乳化剂等,在食品、医药领域得到了广泛使用。Be Rtrand等研究pH值、GA添加量和NaCl对WPI-GA凝胶形成的影响,发现在不同条件(pH值、离子强度等)下获得的混合凝胶类型将允许更优化地使用混合凝胶。
由于之前对WPI/GA复合物的研究并没有对结构进行过多阐述,并且在一定pH值范围内蛋白质带正电荷的结构域与带负电荷的GA相互作用形成弱复合物,这些复合物不会形成凝聚层,形成的颗粒稳定性差,而WPIXG复合物可以通过两种组分之间的静电分子缔合产生高度稳定的乳液,因此利用XG和WPI形成复合颗粒进一步研究其结构特性及稳定性。当蛋白质/多糖复合体系在接近pI的pH值条件下加热到蛋白质的变性温度以上时,就会形成复合物颗粒。多糖依附在蛋白质表面,形成具有“核壳”结构的复合颗粒并在很宽的pH值和离子强度范围内相对稳定,不会聚集离子强度或解离;因此pH值和离子强度在复合物及核壳结构的形成中起着关键作用。本实验选用乳清分离蛋白、阴离子多糖黄原胶作为基础原料制备复合颗粒,通过调节pH值、离子强度、热处理温度、混合方式和剪切条件,调控复合颗粒的粒径、电位和浊度,明确复合颗粒的形成规律、稳定性以及结构,以丰富构建蛋白质/多糖复合颗粒的理论。
1 材料与方法
1.1 材料与试剂
WPI 山东汇益生物科技有限公司;XG 阿泽雷斯国际贸易(上海)有限公司;氯化钠、盐酸、氢氧化钠(均为分析纯) 国药集团化学试剂有限公司。
1.2 仪器与设备
FE20 pH计 梅特勒-托利多仪器(上海)有限公司;Cary-60紫外-可见光分光度计 安捷伦科技(中国)有限公司;ZS90 Zeta电位仪 英国马尔文仪器有限公司;GHJ-6水浴磁力搅拌器 苏州市国飞实验仪器有限公司;FSH-2高速匀浆器 江苏省金坛市荣华仪器制造有限公司;X-30R离心机 贝克曼库尔特有限公司;8400全自动凯氏定氮仪 福斯华(北京)科贸有限公司。
1.3 方法
1.3.1 WPI-XG复合体系的制备
准确称取适量的WPI粉末溶于去离子水中配制成WPI-XG质量比为9∶1的WPI储备液,在25 ℃条件下用电子搅拌器在500 r/min搅拌30 min后,置于4 ℃冰箱水化一夜。准确称取适量XG溶于去离子水中配制成质量分数为0.1%储备液,在25 ℃条件下用电子搅拌器在500 r/min搅拌30 min后静置,除去气泡。
混合相应的储备溶液,制备WPI-XG质量比为9∶1的混合溶液,控制混合后总聚合物质量分数为0.5%,对于离子强度的影响,向WPI-XG质量比为9∶1的混合液中添加NaCl调节离子强度((NaCl)=0、20、50、100、200 mmol/L)。
1.3.2 浊度的测定
采用紫外-可见分光光度计对浊度进行测定,使用1 cm石英比色皿,测定波长为600 nm。分光光度计的透光率通过去离子水进行校准为100%,样品的浊度表示为(100-)%。滴定开始前,首先用0.1 mol/L NaOH将WPI-XG混合溶液、WPI溶液和XG溶液的pH值调节至7.0±0.2,同时固定溶液内总生物聚合物质量分数为0.1%。每当体系pH值变化0.1~0.2时,取样测定其浊度,同时记下对应的pH值。为保证整个体系混合均匀,滴定过程在磁力搅拌器上进行。
1.3.3 颗粒组成的测定
选用两种方法制备颗粒:
方法1:配制WPI-XG质量比为9∶1的混合溶液,控制总生物聚合物质量分数为0.5%,调节pH值,并分别在75、85、95 ℃热处理30 min,热处理采用恒温水浴磁力搅拌器,热处理后用冰水将溶液迅速冷却至室温,所获得的颗粒称为I型颗粒。
方法2:准备0.9%的WPI溶液,调节pH值,并分别在75、85、95 ℃热处理30 min,热处理后用冰水将溶液迅速冷却至室温,再加入0.1%的XG储备液使混合液中蛋白质与多糖的质量比(WPI-XG)为9∶1且生物大分子质量分数为0.5%,充分混合均匀,所获得的颗粒称为II型颗粒。
分别将两种方法制得的混合液在4 ℃、9 000×离心30 min,复合颗粒被离心至试管底部。分别采用凯氏定氮法和苯酚-硫酸法测定上清液中的蛋白质和多糖含量,结合总的蛋白质和多糖添加量即可算出沉淀中的蛋白质和多糖含量。
1.3.4 粒径和Zeta电位的测定
将热处理后的混合液用高速匀浆器在剪切速率为10 000 r/min剪切2 min,再稀释至总生物聚合物质量分数为0.1%,采用Zeta电位仪测定剪切后的粒径和Zeta电位,用于溶剂和复合颗粒的折射率分别为1.33和1.50。所有测量均在25 ℃并重复3 次。
1.3.5 激光共聚焦显微镜
采用激光共聚焦电子显微镜观察颗粒中的蛋白质和多糖分布。分别向WPI储备液和XG储备液中加入荧光染料尼罗蓝和5-氨基荧光素进行荧光标记,室温下搅拌1 h后。对于WPI组,将WPI储备液pH值调至4.32后经75 ℃热处理30 min,冰水冷却后,加入去离子水充分搅拌并调节pH值,使溶液pH 4.32且总生物聚合物质量分数为0.5%。随后将溶液在10 000 r/min高速剪切2 min。按照1.3.3节方法2制备在75 ℃和95 ℃热处理条件下的WPIXG混合溶液,加热前后分别将pH值调节为4.32,最后在10 000 r/min高速剪切2 min。取400 μL溶液滴于共聚焦小皿并盖上盖玻片。尼罗蓝和5-氨基荧光素的激发波长分别为633 nm和488 nm,采集荧光图像,观察颗粒的构成形态。
1.4 数据处理与分析
实验数据使用SPSS统计软件进行分析处理,采用单因素方差分析,在95%置信区间下分析评估结果的显著性。
2 结果与分析
2.1 WPI-XG复合凝聚的行为
2.1.1 pH值对WPI-XG复合凝聚的影响
pH值在蛋白质和多糖复合凝聚中起到了关键作用。对于蛋白质和阴离子多糖复合体系,当pH值小于pI时,蛋白质带正电荷,可与阴离子多糖结合形成复合物,并改变体系的透明度。因此,浊度测定是监测复合物形成的最常见且最直观的方法。图1显示了WPI与WPI-XG溶液的浊度在不含盐离子条件下随pH值的变化曲线。随着酸化的进行,pH值逐渐降低,当pH值达到5.54时,WPI-XG溶液的浊度开始增大,说明在静电力的作用下,WPI与XG部分结合。当pH值达到5.32时,溶液浊度迅速增大并观察到不溶物的生成。当pH值达到4.32时,溶液浊度最大,此时静电相互作用最强。然而随着pH值继续降低,溶液的浊度也开始降低。这一现象是由于XG的p在3附近,因此随着溶液pH值的降低,WPI与XG间的静电相互作用减弱,WPI-XG复合颗粒开始解离。此外,WPI在等电点附近显示出最高的浊度。从结果看,黄原胶的浊度不会随着pH值的变化而变化。因此,加入黄原胶之后浊度最高对应的pH值虽然接近,单纯黄原胶的浊度不随pH值变化,可以说明浊度受到复合颗粒生成的影响而产生变化。
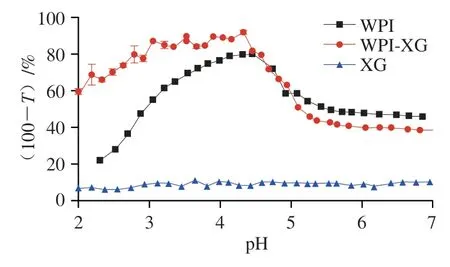
图1 WPI颗粒和WPI-XG溶液浊度随pH值变化的曲线Fig.1 Turbidity curves of WPI particles and WPI-XG solution as a function of pH
2.1.2 离子强度对WPI-XG复合凝聚的影响
盐离子主要通过屏蔽生物大分子的表面电荷影响蛋白质和多糖之间的复合凝聚过程。图2显示了不同离子强度下WPI-XG溶液的浊度随pH值变化的曲线,可以明显看出离子强度对溶液的浊度有着剧烈的影响。
由图2可以看出,从中性向酸性滴定时,在pH值相同的条件下,盐离子浓度为20 mmol/L的浊度高于空白组,盐离子浓度高于20 mmol/L的组别浊度低于空白组。但随着酸化的进行,空白组的溶液在pH值为4.32时率先达到浊度最高点且其浊度高于含有盐离子的其他组别。盐离子浓度越高,其浊度的最高值点越低且达到浊度最高值点时的pH值也越低。随着pH值进一步降低,各组的浊度逐渐降低,最终趋于近似。这表明在pH值较高时,少量盐离子可以改善生物聚合物的溶解性从而加强WPI与XG间的静电相互作用,聚集程度增加;大量盐离子对生物大分子表面电荷存在屏蔽作用,削弱了WPI与XG间的静电相互作用,聚集程度降低。随着pH值逐渐降低,由于盐离子对生物大分子的表面电荷有屏蔽作用,WPI与XG间的静电力减弱,因此生物大分子需要在更低的pH值下才能完成聚集,此时蛋白质能携更多的带正电荷,从而导致浊度的最高值减少且达到浊度最高值点时的pH值也降低,盐离子浓度越高,屏蔽作用越强,生物大分子形成聚集体所需的pH值越低。当pH值进一步降低时,由于氢离子的存在,盐离子对生物大分子表面电荷的屏蔽作用减弱,但由于此时pH值接近XG的p,静电相互作用减弱,WPIXG开始解离,因而各组浊度下降并趋近。

图2 不同离子强度下WPI-XG溶液浊度随pH值变化的曲线Fig.2 Turbidity curves of WPI-XG solution as a function of pH with various ionic strengths
2.2 WPI-XG复合颗粒的组成
表1展示了不同热处理温度和混合方式对WPI-XG复合颗粒组成成分的影响,发现混合方式对颗粒中WPI的含量没有显著影响,对XG含量有显著影响,I型比II型的XG含量高。这是由于I型是在热处理前,WPI和XG在静电力作用下结合,热处理时,WPI内部的疏水键展开,WPI分子间的疏水相互作用增强,可能形成二硫键共价结合,部分XG被WPI分子裹挟进入聚集体内部,同时,游离的XG在静电力作用下附着在WPI聚集体表面,形成WPI-XG复合颗粒;II型是WPI受热解折叠,在疏水相互作用下聚合成为“核”,XG在静电力作用下包裹在“核”的表面,形成“核壳”结构的WPI-XG复合颗粒。热处理温度对II型颗粒的蛋白质/多糖比例具有显著影响。这可能是由于热处理温度越高,蛋白质聚集程度越高,聚集体表面基团和电性变化使得多糖难以完全覆盖蛋白质表面,因此蛋白质/多糖比例增大。
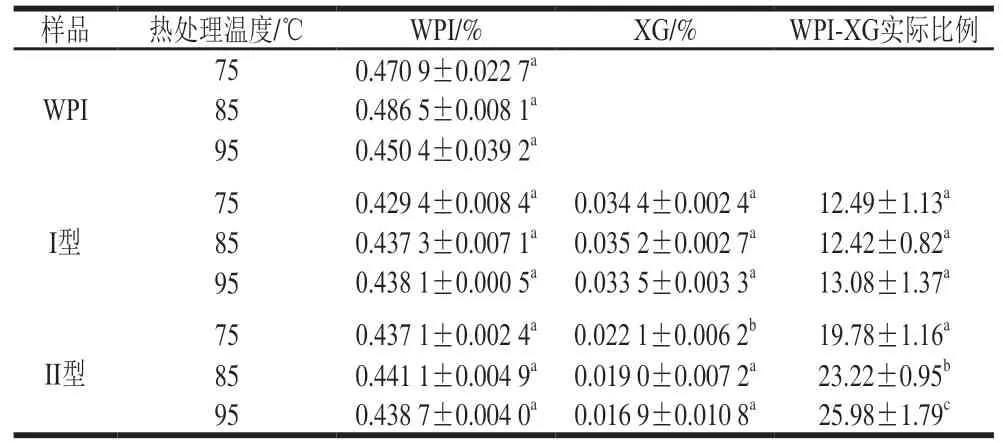
表1 WPI颗粒和WPI-XG复合颗粒的组成Table 1 Composition of WPI particles and WPI-XG composite particles
2.3 WPI-XG复合颗粒的粒径与Zeta电位
Zeta电位是表现颗粒稳定性的一个指标,电位绝对值越大,颗粒稳定性越高。表2展示了不同热处理温度和混合方式对WPI-XG复合颗粒的粒径与电位的影响,发现就WPI而言,热处理的温度越高,粒径越大,电位的绝对值越小。这是由于温度越高,WPI的解折叠越剧烈,内部的疏水基团暴露更多,表面电荷减少,WPI分子间的疏水相互作用更强,聚集程度更高,形成的颗粒粒径更大,电位绝对值更小。对于I型颗粒,75 ℃与85 ℃热处理过后的粒径及电位没有显著差异,这可能是由于XG的存在增加了WPI的稳定性;而95 ℃热处理后的粒径及电位绝对值都显著增大,这是由于WPI在95 ℃解折叠剧烈,展开了更多内部的疏水基团,分子间的疏水相互作用增强,聚集程度增加,颗粒表面积增加,WPI与XG的结合更稳定。对于II型颗粒,75 ℃与85 ℃热处理过后的粒径没有显著差异,均小于95 ℃热处理,75 ℃热处理后的电位绝对值最大,95 ℃次之,85 ℃最小。这是由于在75 ℃时WPI的解折叠程度小,在疏水相互作用和静电相互作用的驱动下XG包裹在WPI表面且结构稳定,使电位绝对值增大,85 ℃时,由于WPI解折叠程度的增加,静电相互作用减弱,WPI与XG结合的稳定性下降,电位绝对值减少。此外,II型颗粒的各组粒径比I型颗粒的小,电位绝对值比I型颗粒的大,表明方法2能形成更稳定的复合颗粒。表3展示了剪切后的各组颗粒的粒径与电位,发现与剪切前相比,各组颗粒的粒径和电位绝对值均有所减小且总体趋势不变。
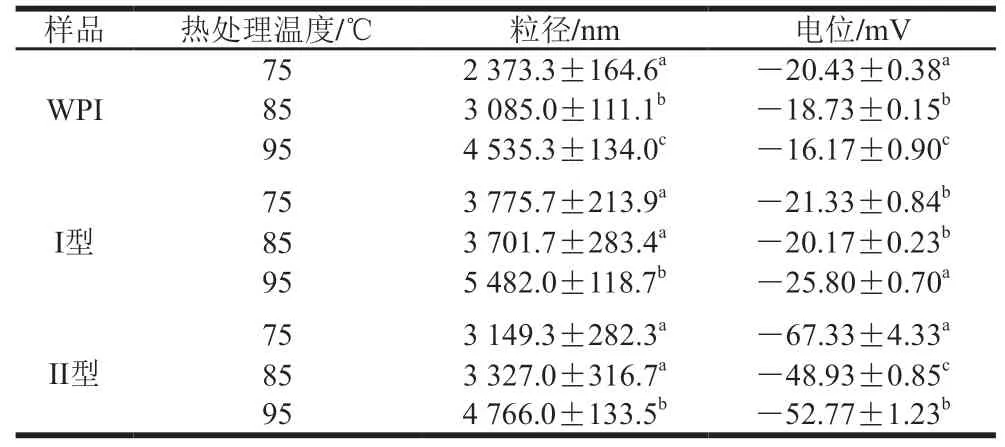
表2 WPI颗粒和WPI-XG复合颗粒的粒径与电位(剪切前)Table 2 Particle sizes and potentials of WPI particles and WPI-XG composite particles (before shearing)

表3 WPI颗粒和WPI-XG复合颗粒的粒径与电位(剪切后)Table 3 Particle sizes and potentials of WPI particles and WPI-XG composite particles (after shearing)
2.4 WPI-XG复合颗粒的微观结构
如图3所示,75 ℃热处理后的WPI以小颗粒状均匀地分布在体系中;并且75 ℃热处理后WPI解折叠,内部疏水基团展开,在疏水相互作用下发生聚集,XG在静电相互作用和疏水相互作用下包裹在聚集的WPI表面,形成以WPI为核、XG为壳的复合颗粒;由于95 ℃热处理后WPI解折叠程度较大,疏水相互作用增强,聚集程度更高,聚集体表面基团和电性变化导致XG难以完全覆盖WPI表面,最终形成粒径更大的“核壳”结构残缺的复合颗粒。激光共聚焦显微镜观察到的结果与之前粒径与电位的结果符合。

图3 WPI颗粒和WPI-XG复合颗粒的微观结构(pH 4.32)Fig.3 Microstructure of WPI particles and WPI-XG composite particles (pH 4.32)
3 结论
WPI和XG可以在静电相互作用的驱动下自发形成复合物;离子强度对WPI-XG复合凝聚的影响具有多重效应:当离子强度从0 mmol/L增加到20 mmol/L时,WPI-XG复合体系的浊度增大;当离子强度从20 mmol/L增加到200 mmol/L时,离子强度对电荷的屏蔽作用使得WPI与XG的结合减弱,复合体系的浊度减小;I型和II型WPI-XG复合颗粒的粒径与电位绝对值均大于WPI颗粒,相比于I型颗粒的粒径更小,电位绝对值更大,形成的颗粒更稳定,并且剪切后的75 ℃热处理WPI颗粒与XG复合形成更为完整的“核壳”结构。本实验结果能够丰富构建蛋白质/多糖复合颗粒的理论,作为脂肪替代物有望更广泛地应用于食品领域。
